抽象的
流行病学证据表明,儿童的SARS-COV-2感染频率低于成年人。年龄相关的ACE2受体表达,淋巴细胞计数和受过训练的免疫可能是揭示儿童秘密的基石。https://bit.ly/2qwpwxk.
介绍
2020年3月11日,一个新的人冠状病毒,名为严重的急性呼吸综合征冠状病毒2(SARS-COV-2)变得大流行[1].3月24日,372 757 SARS-COV-2确认案件和16个相关死亡在全球范围内报告[2].在意大利,报告了62844例和5542例死亡,大部分在北部地区。意大利国家卫生研究所更新了详细的数据[3.].
可用的报告表明,儿童的SARS-COV-2感染似乎是不寻常的。在44例672年确诊病例中,中国疾病治疗和预防报告中心显示416例儿科确诊病例,在0-9岁(0.9%)中(0.9%),没有死亡率,10-19岁的549例(1.2%)一种死亡(0.2%)[4.].最新的意大利报告显示出与318(0.5%)确诊的案件类似的结果表明,在0-9岁年龄组和386(0.7%)确认案件中的10-19岁组。没有孩子在重症监护病房中进行治疗,没有报告死亡[5.].
由于与成年人相比,呼吸道病毒感染通常在5岁以下的儿童中通常更常见,因此专家开始质疑孩子隐藏秘诀的人[6.那7.].最近的一项研究似乎指出,孩子们可能是成年人感染SARS-COV-2 [8.].来自Výeuganeo(意大利Veneto)镇的一份报告,据说意大利北部的两个起始爆发斑之一,表现出相反的结果。从2月22日至3月5日起,2020年3月22日,3500名居民的SARS-COV-2测试了2778人。拭子测试是在症状和无症状的居民中进行的。收集的数据显示,在14岁以下的儿童中只有316次拭子中只有两种效率[9.].不同年龄的SARS-CoV-2易感性数据相互矛盾。D.昂等.[10回顾性分析了我国2143例感染SARS-CoV-2儿童的流行病学特征,支持儿童与成人一样易感染的证据。他们发现,婴儿对SARS-CoV-2的易损性提高,该年龄组严重和危重病例的比例为10.6%(379名婴儿中有40人)。然而,该研究中的大多数严重和危重病例都没有得到SARS-CoV-2的确认,这引发了一场辩论,即是否有其他未经检测的病原体导致了这种临床观察[11].事实上,年代联合国等等。[12]表明,在八个儿童(2个月至15年)中,入院的八个儿童(2个月至15年),只有两(25%)的年龄在12个月内。
原因仍然不清楚。宿主免疫应答和病毒致病机制之间的相互作用可能是梯形石。
门口
血管紧张素转换酶2 (ACE2)是一种I型膜蛋白,在许多器官中表达,如肺(II型肺泡上皮细胞)、心脏、肠和肾,在这些器官中它在生理上参与血管紧张素II (AngII)的成熟[13那14].已被证明是ACE2是严重急性呼吸道综合征相关的冠状病毒(SARS-COV)的功能受体,最近是SARS-COV-2 [14那15].X你等.[16]发现在SARS-CoV和SARS-CoV-2刺突蛋白的受体结合域中存在几乎相同的三维结构。ACE2结构的全长阐明也表明SARS-CoV-2与ACE2更强的结合亲和力,以及更有效的受体识别,这可能具有很强的人际传播影响[16那17].至关重要的是,SARS-COV和人冠状病毒NL63感染显示下调ACE2蛋白表达[18].ACE2的一个关键作用是将AngII转化为其代谢产物血管紧张素-(1-7)(Ang1-7),特别是在肺微环境中,那里的ACE2水平本质上是升高的。Ang1-7在肾素-血管紧张素系统(RAS)的调节中具有稳态作用,具有抗高血压和促纤维化作用[19那20.].事实上,ACE的升高或ace2的低表达可导致高血压,慢性心力衰竭和肺损伤[20.].因此,由于ACE2似乎以保护性方式起作用,SARS-COV-2可以不平衡,因此血管/ Ang1-7水平不平衡,因此导致炎症和缺氧[21].
然而,RAS DANANGENTEMENT的效果尚不清楚。在患有营养慢性病症的患者中检测到低水平的ACE2,其通常不会影响儿科人群[20.-22].在X即等等。[23在大鼠模型中,ACE2随着年龄的增长而显著下降。C的报告母鸡等.[24,包括ACE2基因组学、表观基因组学和转录组学数据,支持年轻人似乎不太容易受到病毒有害影响的证据,表明ACE2表达与SARS-CoV-2严重后果之间存在负相关。此外,根据他们的分析,随着年龄的增长,雌激素和雄激素的减少已被证明会上调ACE2的表达[24那25].综上所述,这一证据可能表明,儿童肺细胞中ACE2受体浓度的增加可能对SARS-CoV-2感染的严重临床表现具有保护作用。
症结
SARS-CoV-2病毒基因组已经测序,它与SARS-CoV相同75%至80% [26].遗传和临床证据表明SARS-COV-2对SARS-COV和中东呼吸综合征相关的冠状病毒(MERS-COV)具有相似的致病机制[27那28].
先天免疫细胞通过包括可增量的受体(TLR)和其他胞质病原体传感器的图案识别受体(PRRS)识别病原体相关的分子模式(PAMP)。PRRS出现了下游信令级联的激活,导致I型和III干扰素(IFNS)和其他促炎介质的产生,该介质介质引发宿主先天和适应性免疫应答。I型IFNS激活Jak / Stat路径,在调节免疫应答方面发挥着关键作用;IFNS还可以通过树突细胞刺激直接激活免疫,并且它们也增加细胞毒性T和NK细胞活性[29].此外,NK细胞迁移到受感染的部位,并响应产生IFN-γ的病毒,杀死病毒感染的细胞并提高适应性免疫反应[29].细胞因子和IFNS促进炎症,但它们也应对急性病毒感染期间的肺损伤负责。在SARS-COV-2严重的病例中,患者具有高水平的先天性炎炎细胞因子,I型IFNS。与SARS-COV和MERS-COV感染类似,若干报告显示出患儿中的中性粒细胞和降低的SARS-COV-2患者的淋巴细胞计数,所谓的“细胞因子风暴”的发作,支持天生免疫应答的重要性的假设保护性和破坏性机制27].
儿童疾病的疾病呈现可能与“训练有素的免疫力”相关联。“训练有素的免疫”代表了先天的免疫记忆,它是通过在抗原暴露后成为“记忆细胞”的先天免疫细胞形成的[30.].mitroulis等.[31[展示了系统性抗原确定血新产物祖细胞的转录组,代谢组和功能变化,导致骨髓细胞产生更快的感染的反应性。这些修改不仅发生在骨髓中,而且在NK细胞和先天淋巴细胞组2(ILC2)中发生。如果被吸入过敏原刺激,则显示肺ILC2能够记住其激活状态[32].巨细胞病毒和甲型流感可在再感染时触发更强的NK介导的继发性先天免疫应答[33].研究表明,共同的表观遗传机制决定了记忆细胞的发育,无论是在适应性免疫系统还是先天免疫系统[34].受过培训的免疫记忆是通过血管祖的祖细胞和先天免疫细胞中的表观遗传修饰介导的介导;它代表了针对各种病原体的交叉保护,它也可以通过疫苗激活[30.].在病原体暴露后,增加抗原呈递细胞的活化导致宿主的非特异性抗性,以再灌注,为其他感染提供交叉保护。还假设疫苗可以诱导交叉反应性,训练先天免疫系统。越来越多的证据表明,麻疹接种的儿童减少了死亡率,只能通过预防麻疹相关死亡来解释[35].有几篇论文研究了流感疫苗通过诱导NK细胞毒性反应的免疫调节作用。mysliwska等.[29[研究了疫苗接种群体中NK活性与患流感病毒的特异性免疫保护和其他感染的无特异性免疫保护之间的关系。在免疫之前和之后监测NK活动,他们发现它仍然在1个月后仍然显着升高。他们得出结论,NK细胞活化可能会赋予对甲型流感和其他呼吸道病毒感染的保护。儿童常见的病毒感染和疫苗都可以诱导具有增强的激活状态的先天免疫系统,这将导致对不同病原体的更有效的防御[35].从训练有素的免疫(部分免疫状态和病毒感染的曝光不足)中相对低的益处可以解释与年龄较大的儿童相比,SARS-COV-2感染婴儿更严重的临床介绍的流行病学证据[10].此外,人新生儿抗原呈递细胞和血浆曲线树突细胞的产生类型IFNS的产生损害,并对TH1细胞因子的产生呈现偏差[36].这种两极分化允许有益的微生物定植,使新生儿更容易受到致病性感染。免疫反应的年龄依赖性成熟发生在重复的刺激和结果增强的先天功能(训练免疫),这可能保护年龄较大的儿童,如前所述。
自适应免疫反应也在SARS-COV-2感染中起着至关重要的作用;促炎介质激活Th1型免疫应答(CD4 +和CD8 + T细胞)和B淋巴细胞,导致有效的病毒特异性抗体反应[37].受SARS-COV-2感染的成年人,特别是那些具有严重疾病的人,通常具有降低的淋巴细胞计数和淋巴细胞减少[27那38那39].在SARS-COV-2的儿童中,外周血淋巴细胞大部分仍然在正常范围内,表明免疫功能障碍较少[30.那40].在健康的儿童中,这可能与淋巴细胞,尤其是NK细胞的事实有关,其在宪法中含有比在健康的成年人中更大的数量。淋巴细胞计数在生命的第一个月内非常高,并且在后期的儿童和青春期减少[41].此外,甚至由于儿童时期经常经常出现的病毒感染,淋巴细胞也可能更高,因为生命的第一年的永恒免疫系统激活,甚至是童年的病毒感染。
结论
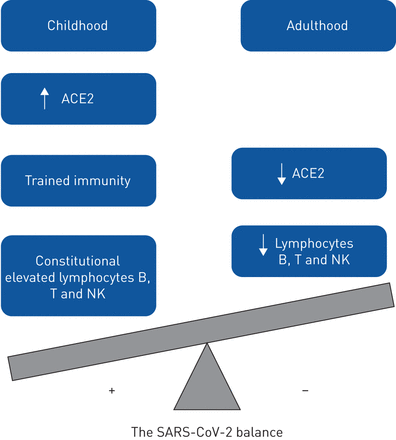
我们可以推出高αce2受体浓度,训练有素的免疫和儿童的宪法高淋巴细胞计数可能部分解释在该组患者中观察到的轻度疾病(图1).真正的原因可能仍然是个谜,幸运的是,因为受感染儿童的数量太少,不允许进行大规模的免疫学研究。
该图说明了与严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)感染相关的理论结构和假定的儿童和成人之间的免疫学和致病性差异。与成人不同,儿童的血管紧张素转换酶2 (ACE2)表达和淋巴细胞计数均有结构性升高。此外,他们经历了几次病毒感染和计划免疫,这可能会增强他们的先天和适应性免疫。
可分享的PDF.
脚注
利益冲突:L. Cristiani无需披露。
利益冲突:E.曼奇诺没有任何披露。
利益冲突:L. Matera无需披露。
利益冲突:R.南纳没有什么可披露的。
利益冲突:A. Pierangeli无需披露。
兴趣冲突:C. Scagnolari无需披露。
利益冲突:F. Midulla没有什么可披露的。
- 收到了2020年3月18日。
- 公认2020年3月25日。
- 版权©2020人队
此版本在Creative Commons归因非商业许可证4.0的条款下分发。