摘要
COVID-19相关肺曲菌病(CAPA)病例的报告越来越多,治疗COVID-19相关肺部疾病患者的医生需要积极考虑这些真菌合并感染https://bit.ly/3feuGsQ
2019冠状病毒病(COVID-19)病毒在健康人以及有常见共病的人中造成了广泛的疾病[1].重型COVID-19的特征是继发于病毒性肺炎的急性呼吸窘迫综合征(ARDS),其治疗可能需要机械通气或体外膜氧合[2].临床医生警惕细菌合并感染作为下呼吸道病毒感染并发症的可能性;例如,最近的一项综述发现,72%的COVID-19患者接受了抗菌治疗[3.].然而,真菌合并感染的风险,特别是COVID-19相关性肺曲菌病(CAPA)的风险仍未得到充分认识。
其他严重冠状病毒,如严重急性呼吸综合征-冠状病毒(SARS-CoV),已观察到与侵袭性曲菌病一致的真菌疾病[4,5]和中东呼吸综合征-冠状病毒[6].从COVID-19大流行开始,就出现了继发性侵袭性真菌感染的警告迹象。黄曲霉从中国武汉第一批详细报告的COVID-19队列中的99名患者中分离出1名患者的呼吸道[2),曲霉属真菌在该地区随后的一组危重患者队列中,52例患者中有2例(3.8%)分离出sp . [7].最近,比利时的回顾性病例系列[8,法国[9,荷兰[10和德国[11已经报告了在机械通气患者中惊人的20-35%存在CAPA的证据。
卡帕
流感相关肺曲菌病(IAPA)是流感危重患者的已知风险[12- - - - - -14]并且COVID-19的临床过程显示出许多与严重流感感染相同的特征。这包括ARDS、淋巴细胞减少、双侧肺浸润、全身促炎细胞因子反应和导致多器官衰竭的败血症[14,15].因此,我们有理由怀疑,重症COVID-19患者可能同样容易感染侵袭性曲菌病。皮质类固醇的使用是IAPA的重要获得性免疫危险因素[16]而且,在2003年sars冠状病毒流行期间,有病例报告称,患者在使用皮质类固醇后发生了sars相关的侵袭性曲菌病[5].据报告,COVID-19住院患者中使用了皮质类固醇[1],并可能进一步增加CAPA的风险。重要的是,英国RECOVERY试验的最新发现(ISRCTN50189673) [17研究发现,地塞米松可使COVID-19通气患者的死亡率降低三分之一,虽然这是一种重要的新治疗途径,但可能增加患者获得CAPA的风险,并强调了加强真菌监测的必要性。
表1总结了迄今为止已报道的33例CAPA患者的个体数据。病例的中位(四分位范围)年龄为70岁(57-75岁),其中只有2例(6%)有欧洲癌症研究与治疗组织(EORTC)宿主因子。其中16人(48%)接触过吸入或全身皮质类固醇,10人(30%)患有糖尿病,9人(27%)患有潜在慢性肺部疾病;COPD (n=5)、哮喘(n=3)、大疱性肺气肿(n=1)、肺纤维化(n=1)和非小细胞肺癌的放疗后治疗(n=1)。CAPA在重症监护病房(ICU)入院后5.5(4.3-9)天被诊断为中位数(四分位数范围),21例(63.6%)患者在发表文章时死亡。这一死亡率超过了大多数COVID-19通气患者队列,作为比较,在英国ISARIC队列中,1658名通气患者中有618人(37%)在报告发表时死亡(17%出院,46%仍在接受治疗)[23].
在没有传统宿主因素的危重病人中,侵袭性曲菌病很难诊断,因为放射学改变通常是非特异性的(如。浸润、实变或结节),罕见有晕征、气新月征或空化[24].基于这些原因chauwvlieghe等.[13]开发了改进的AspICU标准,以帮助诊断IAPA(在组织学缺失的情况下)实质上依赖于真菌学证据曲霉属真菌以阳性支气管肺泡灌洗(BAL)培养或血清/BAL中阳性半乳甘露聚糖(GM)的形式出现。应用这些改进的AspICU标准,在我国有5例CAPA表1如果是“被证实的”,11个“假定的”和17个可能被认为是假定的,但有表中描述的注意事项。例如,在许多病例中,侵袭性曲菌病的唯一真菌学证据是气管抽吸而不是BAL(在没有气管支气管炎/空化的情况下)。因此,对于从此类病例中过度估计CAPA的发生率应保持警惕,这可能包括一些只有曲霉菌定植或污染的患者。在Alanioet al。[9该研究报告了在27例接受BAL/气管抽吸的通气患者中有9例(33%)存在CAPA的证据,1例根据BAL GM为0.89(低于通常的临界值1.0)定义,2例基于气管抽吸而非BAL培养,1例基于血清GM为0.51(临界值为0.50),4例BAL培养为阳性但BAL GM为阴性,这表明缺乏组织侵犯。事实上,在没有使用抗真菌药物治疗的7个病例中,有5个存活了下来。因此,需要进行更大规模、前瞻性、多位点的研究,以完善COVID-19患者的AspICU标准,并评估发病率和CAPA对生存率的影响[25,26].
CAPA的诊断和风险
考虑到这些观察结果,我们认为,COVID-19的危重患者和进行性特征应筛查CAPA。我们承认,鉴于SARS-CoV-2病毒的危险等级为3组,以及超负荷的重症监护服务,获取和处理临床微生物样本非常具有挑战性[27].
理想情况下,CAPA筛查需要使用计算机断层扫描胸部成像和曲霉属真菌BAL和血清抗原试验,包括GM酶联免疫吸附试验或侧流试验[28],或曲霉菌PCR [29].尽管在17.6%的COVID-19重症患者中可以看到侵袭性曲菌病的特征性CT特征,如带晕征的结节,但未能确认为IPA [30.].考虑到IAPA缺乏典型的侵袭性曲菌病CT特征,如空化等经典发现的缺失不应被用来排除CAPA;然而,它们的存在有助于支持诊断,并减轻真菌学研究的证据负担。
在一项对26例经尸检确诊为(非capa /IAPA) IPA的ICU患者的研究中,血清GM对非嗜中性粒细胞减少的患者只有25%的敏感性(与70%为中性粒细胞减少症患者)[31].相比之下,BAL GM在两组中均为88-90%的敏感性。Schauwvliegheet al。[13血清GM检测在31例阳性病例中有20例(65%)表现更好,而BAL GM检测在76例阳性病例中仍有67例(88%)表现更好。在迄今报告的CAPA个案中(表1)、BAL培养和GM的敏感性分别为72.7%和66.7%,但血清GM阳性的28例中只有6例(21.4%)。此外,在迄今报告的5例已证实的CAPA病例中,4例血清GM阴性(表1) [8],提示血清GM检测在诊断CAPA方面可能较差。因此,当怀疑CAPA时,支气管镜检查,包括气管支气管检查和培养和GM的BAL取样应该是诊断的金标准,前提是这与对气溶胶产生程序的局部感染预防和控制指导相一致。BAL GM阳性(指数>1.0)可指示CAPA,而如果指数<0.5,CAPA的可能性就小得多[31].血清GM阳性结果(≥0.5)对CAPA是高度可疑的,但阴性结果不应用于排除诊断。在CL3实验室,新的侧流抗原检测可能是GM ELISA的一种可在当地实施的替代方法,但目前需要在没有EORTC宿主因子(包括COVID-19)的ICU患者中验证[28].一个曲霉属真菌-特异性PCR试验[29]可能也有帮助,如果阳性,还可以应用分子检测临床或环境衍生的唑耐药的公认标记物[32].
对血清样本进行(1-3)-β- d -葡聚糖(BDG)检测是一种很容易获得的,当怀疑IPA时,可以进行早期筛查。虽然性能可能优于血清曲霉属真菌ICU内IPA的抗原检测[33], BDG阴性不能用来排除感染,在异质性侵袭性曲菌病患者人群中测定的敏感性为77%,在CAPA中的表现尚待确定。BDG阳性可能发生在该患者队列中,原因有很多,但连续阳性检测增加了特异性,应提示诊断工作,包括计算机断层扫描和支气管镜检查曲霉属真菌上文所述的抗原[34].虽然基于BDG阳性的抗真菌治疗可能是对经验疗法的改进,但应尽一切努力利用其他更具体的诊断测试来补充BDG结果。
由于产生气溶胶的风险,目前的指南建议不要进行常规支气管镜诊断;仅建议鼻咽培养阴性和BAL取样将改变临床管理的患者使用该药物[35].在实践中,许多疑似CAPA的患者只接受气管内取样或非定向BAL取样,重要的是,任何CAPA的病例定义都应反映这一现实。为了认识到这一点,我们提出了一种CAPA的筛查和诊断算法,它有临床(呼吸)恶化和/或阳性曲霉菌痰液,或气管吸气培养作为其切入点(图1).尽管CAPA的宿主危险因素和临床特征尚不清楚,但那些符合已证实或可能的曲霉菌病标准的个体[13,14]则应按现行指南治疗[36,37].重要的是,现在地塞米松的辅助使用可能会广泛用于治疗严重的COVID-19患者[17为研究皮质类固醇使用与CAPA之间的可能联系,需要加强对侵袭性曲菌病的筛查。
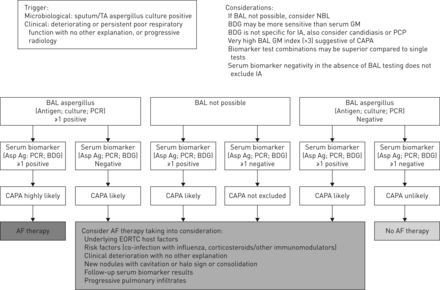
提出了2019冠状病毒病相关肺曲菌病(CAPA)的筛查和诊断算法。支气管肺泡灌洗;中心:楼(1 - 3)-β-D-glucan;TA:气管抽吸;Asp Ag:曲霉菌抗原;房颤:抗真菌;IA:侵袭性曲霉菌病;通用汽车:半乳甘露聚糖;欧洲癌症研究和治疗组织;NBL:非定向支气管肺泡灌洗; PCP: Pneumocystis pneumonia.
最后,免疫调节药物如anakinra(重组白介素- 1ra)、tocilizumab(抗白介素-6)和Janus激酶抑制剂的使用,目前正在对COVID-19进行试验,也可能使患者更易发生CAPA。也有增加的风险曲霉属真菌在医院病房或临时“医院”设施中接受治疗的患者暴露在不符合ICU适当房间通风和换气规范的环境中。值得注意的是,肺曲菌病可能在一部分患者中发展为慢性空洞疾病,可能发生在covid -19后肺纤维化的患者中。由于这些原因,随访原发性COVID-19感染后出现慢性呼吸系统问题的患者的临床医生应牢记长期真菌并发症。
结论
在疫情条件下管理COVID-19患者的艰巨任务中,真菌感染构成了额外的威胁。毫无疑问,SARS-CoV-2病毒的大流行将涉及CAPA,在大流行期间使用免疫调节疗法和超负荷的重症监护服务的影响可能会夸大其影响。关于COVID-19患者CAPA的流行病学和诊断还需要更多的研究,随着正在进行的前瞻性多位点临床研究扩展到包括该队列,这一需求得到了部分满足(如。AspiFlu) [25]或已推出(CAPA) [26,以应对2019冠状病毒病大流行。
可共享的PDF
脚注
利益冲突:D. Armstrong-James报告了Pulmocide有限公司和吉利德科学公司在提交作品之外的拨款和个人费用。
利益冲突:J. Youngs报告了来自英国和爱尔兰吉利德奖学金项目的资金。
利益冲突:T. Bicanic报告了来自吉利德科学有限公司的讲座的拨款和个人费用,以及来自辉瑞公司的讲座的个人费用,在提交的工作之外。
利益冲突:A. Abdolrasouli在提交的作品之外从吉利德科学有限公司获得了演讲酬金。
利益冲突:D.W.丹宁及其家族持有F2G Ltd的创始人股份,F2G Ltd是曼彻斯特大学的一家分拆出来的抗真菌发现公司;D.W. Denning担任或最近担任Scynexis、Pulmatrix、Pulmocide、Zambon、iCo Therapeutics、Mayne Pharma、Biosergen和Fujifilm的顾问;曾代表希克玛、吉利德、默克、迈兰和辉瑞进行谈判;D.W. Denning是美国传染病学会曲菌病指南小组、欧洲临床微生物学和传染病学会曲菌病指南小组的长期成员。
利益冲突:E.约翰逊没有什么可透露的。
利益冲突:V. Mehra报告了来自辉瑞、诺华、Incyte和吉利德科学公司的讲座的个人费用,以及来自默沙东的资助,这些都是在提交的工作之外。
利益冲突:T. Pagliuca报告了在提交的工作之外为吉利德、默沙东和辉瑞的顾问委员会工作支付的个人费用。
利益冲突:B.帕特尔没有什么可透露的。
利益冲突:j·罗兹没有什么可透露的。
利益冲突:S. Schelenz报告了来自吉利德科学公司和辉瑞公司的个人讲座费用,在提交的工作之外。
利益冲突:A. Shah报告了来自吉利德科学和Vertex制药的拨款,以及吉利德科学和辉瑞的演讲费。
利益冲突:F.L. van de Veerdonk没有什么可透露的。
利益冲突:P.E. Verweij曾获得吉利德科学、F2G有限公司、辉瑞、Thermofisher和默克的研究资助,曾担任吉利德科学、Mundipharma和F2G的顾问委员会成员,并从F2G、Mundipharma、辉瑞和吉利德科学获得演讲酬金。
利益冲突:P.L. White报告了来自吉利德、辉瑞和F2G的个人费用,来自Bruker的拨款,在提交的作品之外。
利益冲突:M.C. Fisher报告了吉利德科学有限公司在提交的工作之外的演讲经费和个人费用。
支持声明:本研究得到自然环境研究理事会(资助号NE/P001165/1)、医学研究理事会(资助号MR/R015600/1)和加拿大高等研究院的支持。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2020年5月12日。
- 接受2020年7月1日。
- 版权所有©ERS 2020
本版本按照创作共用署名非商业性许可4.0的条款发布。















