摘要
更多的证据表明肺微生物群在特发性肺纤维化中起作用。但是我们离证明因果关系有多近呢?来自Dickson, Harari和Kolb的社论ERJ。http://bit.ly/2Ps1ow4
尽管“肺微生物群”的概念,即。一个居住在下呼吸道并对其产生影响的复杂微生物群落,仅仅存在了10年[1肺是我们和我们所居住的微生物世界之间的一个重要接口,这一观点并不是什么新鲜事。路易斯·巴斯德证明了空气中存在活的微生物[2他的一个同代人计算出健康的成年人每小时吸入1500到14000个有机体[3.]。大量的放射学研究一再证明亚临床微吸入术的普遍性[4- - - - - -6,即使是健康的、无症状的受试者。肺的表面积是胃肠道的两倍[7是皮肤的30倍[8],代表人体与外界环境的最大界面。长期以来,深思熟虑的肺生物学研究者一直怀疑,我们的肺进化的机制,以应对这种持续的微生物暴露(先天和适应性免疫防御,纤维化的建立和解决),在肺部疾病的发病机制中起着核心作用。正如肺生物学家盖伦·托伊斯(Galen Toews)所常说的,早在肺微生物群系时代之前:“所有肺部疾病都是感染性疾病”(图1)。

盖伦托斯(一九四五年至2011年)。肺微生物的时代不久,陶斯博士认为,“所有的肺部疾病是传染病。”
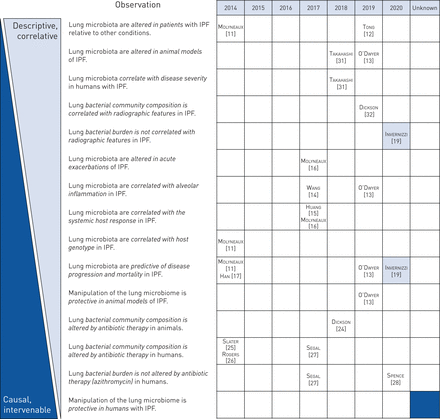
在过去的十年中,这种直觉已经平反,特别是与特发性肺纤维化(IPF)。从2014年开始,研究级联(图2)已经使用了培养独立的技术来表征和研究IPF患者肺部的细菌群落和疾病的动物模型。这一领域中不断出现的争论已经推翻了关于肺部不育症的陈旧、简单的观念。IPF患者肺部细菌群落的存在和意义现已被大量研究证实,在患者群体、实验室、测序平台和动物模型中都得到了证实。我们对呼吸微生物学在IPF中作用的思考的这种演变已经反映在我们的临床试验中:而十年前我们还在研究IPF中的免疫抑制[9,我们现在正在试验抗生素[10]。
为肺微生物群在特发性肺纤维化(IPF)中的作用建立一个因果论证。近年来,与培养无关的微生物学技术彻底改变了我们对呼吸微生物群在IPF中的重要性的认识。的关联意义IPF中肺微生物组的研究现在是无可争议的:肺细菌与疾病状态、宿主基因型、肺泡和全身宿主反应相关。本研究由Invernizzi等。[19]明确证实了肺微生物组预后意义:肺微生物群预测IPF的疾病进展,与放射学的严重程度无关。然而,因果意义其作为治疗靶点的地位仍然是目前研究的一个关键领域,需要介入性人体研究和转译动物模型。
超出了纯粹的存在在IPF肺微生物组,现场已经牢牢确立了其关联意义(图2):在IPF患者中,肺菌群的变化与疾病重要方面的变化相关:疾病状态[11,12、肺泡发炎[13,14],宿主基因型[11和系统宿主反应[15,16]。此外,一些研究已经独立地建立了预后意义在IPF肺微生物组:三个独立的分析已经表明,在肺微生物群变化预测IPF患者[之间疾病进展和死亡率11,13,17]。
无论这些发现多么具有挑战性,它们都还没有确定因果意义在IPF肺微生物。怀疑论者可能会相当问,如果在IPF肺微生物的严重程度只是一个间接指标,反映了疾病的一些内在的,不可测量的功能(如。牵引性支气管扩张导致气道粘液纤毛清除受损)。这是该领域面临的中心问题[18]:是肺微生物仅仅IPF的附带现象,一个无辜的旁观者对疾病的发病机制,或者说改变肺微生物直接参与发病?
这个核心问题是我的一项重要新研究背后的基本原理nvernizzi等。(19[steven精品五句之编辑部的故事欧洲呼吸杂志。作者研究了一大群IPF患者谁接受双方的研究支气管镜胸部计算机断层扫描(CT)扫描的定量解释。表征肺细菌,作者量化总肺部细菌DNA的负担,这已经跨越呼吸系统疾病的临床结果的最稳定的微生物预测[11,13,20.,21]。在对CT成像的分析中,他们量化了纤维化的严重程度和程度,包括牵引性支气管扩张和蜂窝化等关键特征。鉴于其已知的预后重要性,他们选择了这些影像学结果[22,23]并且,因为它们提供客观洞察IPF的解剖失真可能导致增加的肺部细菌负担。作者推断,如果肺细菌负荷在IPF预后意义仅是建筑破坏的人工产物,那么这两个预后因素(微生物学和放射学)应该被彼此相关。
相反,他们发现根本没有任何关系。虽然患者的肺部细菌负担差异很大,但与疾病的放射学严重程度无关,无论是否综合考虑(如。纤维化程度,或常见间质性肺炎模式的可能性,或其具体特征(如。牵引性支气管扩张或蜂窝状扩张)。肺细菌负担与疾病的生理严重程度(测量)也不相关通过用力肺活量)。这些关联的缺失与“无辜的旁观者”对IPF肺微生物组文献的解释相悖。如果肺细菌负担仅仅是一个间接的严重程度指标,为什么它与我们现有的最好的解剖和生理严重程度的测量没有关联呢?
然而,在同一队列中,作者再次证明了预后意义在IPF肺部细菌负担。正如先前的研究[11,13], lung bacterial burden convincingly predicted clinical outcomes, defined here as all-cause mortality or spirometric progression at 12 months. This association remained robust to multivariable adjustment for key potential confounders that represent radiographic and physiologic severity of disease. While these findings do not definitively establish a causal role for lung microbiota in IPF pathogenesis, they do provide strong evidence that the lung microbiome's prognostic significance is not merely an artefact of disease severity.
那么怎样才能证明因果关系呢?我们需要证明操纵肺微生物组(在人类身上进行治疗,在动物模型上进行实验)改变了IPF进展的生物学和临床轨迹。这一任务说起来容易做起来难,因为它依赖于几个内在的主张:1)肺微生物群可以通过干预(如。抗生素),2)这种操作影响IPF发病的轨迹,3)这些干预的效果直接归因于肺微生物组的改变,而不是治疗的脱靶效应(如。大环内酯类药物的免疫调节作用,或肠道菌群改变的全身作用)。
所示图2在这条荆棘之路上,该领域已经取得了一些进展。关于第一个嵌入的声明(肺微生物组可以被干预改变),现在确认的是社区组成肺细菌抗生素改变,无论是在动物模型中的[24]和在人类肺条件下(IPF除外)[25- - - - - -27]。然而,目前尚不确定肺细菌负担(IPF中肺微生物组最一致的预后特征[11,13,19]及其他情况[20.,21可以被抗生素改变。慢性大环内酯类药物治疗慢性阻塞性肺病患者的两项研究[27]及接受肺移植的人士[28]),慢性阿奇霉素对肺细菌负荷没有作用:社区变化,但总细菌负载为不变。如果像希望的那样,肺部细菌负担成为IPF的治疗目标,我们首先需要表明它可以被修改,无论是通过抗生素或其他干预措施(如。fundoplication)。
第二种观点认为,对肺微生物组的调控影响IPF的发病和进展,这一观点得到了早期动物和人类观察的支持。在博莱霉素肺纤维化模型中,无菌小鼠(完全没有细菌的小鼠)免于死亡[13]。在其他小鼠模型中,肺纤维化的发病机制因肺暴露而加速和增强链球菌引起的肺炎及其毒素[29,反映了肺增厚与链球菌p.和人类受试者IPF的进展[17]。一项在IPF患者中使用复方新诺明(co-trimoxazole)的随机人体试验发现,该药可降低全因死亡率(但不能降低肺功能)[30.]。正在进行的IPF抗生素试验将提供更多关于可能疗效的证据[10]。
然而,这些观察都没有涉及到第三个根深蒂固的观点:微生物组操纵IPF的好处不能归因于我们的干预的间接、脱靶效应。为了实现这一目标,我们需要在动物模型和人类介入研究的分析方法上取得进展。在动物模型中,一个主要的挑战是如何在不影响肠道菌群的情况下选择性地改变肺菌群,而肠道菌群是系统免疫反应的基础。在前瞻性人体研究中,我们应该在随机干预前和随机干预后对肺微生物组进行取样和研究:治疗前取样以评估的治疗效果的异质性(患者基线肺菌群的变化是否可以解释其治疗反应的变化?),以及治疗后的取样中介分析(患者对治疗的微生物反应的变化是否可以解释治疗反应的变化?)最后,我们目前操纵微生物组(抗生素和益生菌)的手段是广泛的和非靶向的,类似于使用系统性皮质类固醇来改变宿主免疫。一个关键的挑战将是学习如何以我们现在调节宿主反应(如。单克隆抗体)。
尽管存在这些挑战,但未来是光明的。无论是对IPF发病机制的研究人员还是对呼吸微生物学的研究人员来说,我们对IPF微生物学理解的革命都是激动人心的。生命之树的整个王国,以前在IPF研究中被忽视,现在是临床和实验研究的主要焦点。我们有很多工作要做,但目前的研究由我nvernizzi等。(19让我们有理由相信,我们正在为因果关系寻找理由。
可共享的PDF
脚注
利益冲突:R.P. Dickson没有任何需要披露的信息。
利益冲突:S. Harari没有什么要披露的。
利益冲突:m·科尔布报告赠款和个人费用咨询和讲座从罗氏公司和勃林格殷格翰的发言,赠款和个人费用咨询公司葛兰素史克,基列和Prometic,赠款从Actelion股价,Respivert, Alkermes公司Pharmaxis,个人费用咨询公司从热那亚,Indalo第三极,在提交工作。
- 收到2020年2月13日。
- 接受2020年2月14日。
- 版权©2020人队