文摘
除了主要基因BMPR2,一些新的基因诱发多环芳烃在过去十年中已确定。最近,参与的初步证据KDR基因被发现在一个大的遗传关联研究。
我们前瞻性分析KDR基因测序目标面板在一系列311 PAH患者临床分子基因诊断实验室的多环芳烃。
两个指数例严重PAH来自两个不同的家庭被发现携带功能丧失的突变KDR基因。这两个指数病例临床特点是低扩散一氧化碳血红蛋白(调整的能力DLCOc)和间质性肺疾病。在一个家庭中,隔离分析显示,变体运营商要么是有多环芳烃与低有关DLCOc,或只有减少DLCOc,而非承运人的亲戚有正常DLCOc。在第二个家庭,一个影响航母还活着。他的母亲是影响正常载体DLCOc。
我们为考虑提供了遗传学证据KDR作为一个新发现PAH-causing基因通过描述的隔离KDR在两个家庭与PAH突变。在我们的研究中,KDR变异与一个特定形式的多环芳烃含量偏低DLCOc和放射性肺实质疾病的证据包括间质性肺病和肺气肿。
文摘
KDR突变被发现在两个家庭与特定形式的多环芳烃含量偏低DLCOc和放射性肺实质疾病的证据http://bit.ly/30npPPn
介绍
肺动脉高压(PAH)是一种罕见的和毁灭性的疾病,造成逐步消灭增殖的小口径肺动脉血管细胞和内膜的纤维化,导致心脏衰竭。多环芳烃可以使确定病理条件下,或发生在上下文的家族史或基因突变导致可遗传的多环芳烃(hPAH),或被认为是特发性(iPAH)在缺乏一个确定诱发因素(1]。主要的基因与多环芳烃BMPR2、编码2型受体的骨形态发生蛋白(BMP)信号通路。在过去的十年中,一些新的基因已经被鉴定使多环芳烃异构遗传性疾病(2]。最初的发现BMPR2,利用收集的信息多路多环芳烃家庭和其他基因的含义属于BMP信号通路是基于候选基因的方法,如ACVRL1和英格在极少数情况下的遗传出血性telangiectasia-associated多环芳烃,SMAD9或BMP10(2,3]。的TBX4基因被发现由于大型基因组删除包括基因和后来被证明是一个主要的诱发基因hPAH [4- - - - - -6]。的recently identified genes were the results of whole exome or genome sequencing in families or large cohorts of sporadic cases and includedATP13A3 GDF2 (BMP9)、SOX17 AQP1 KCNK3和CAV1(6- - - - - -9]。EIF2AK4的基因遗传的肺部静脉阻塞疾病(hPVOD)也被外显子组测序10]。初始基因识别后,进一步研究这些基因在较大数量的病人给对比结果,因为没有其他案例确定了其中一些,而对另一些人来说,如GDF2,一些致病变种被发现在PAH情况下(11]。
基因关联研究过程中使用全基因组测序在一系列大型的PAH情况下和控制,G英国皇家空军et al。(6)发现的初步证据可能参与插入域受体激酶(KDR)在PAH基因通过比较protein-truncating变异基因内的病人的数量和控制。然而,这一发现并没有实现全基因组意义分析,因此被认为是不明确的。
的KDR基因编码的受体血管内皮生长因子(VEGF)——VEGFR2,能传感信号的VEGF在发展和成人对内皮细胞的影响。事实上,激活VEGFR2通过细胞外配体结合刺激几个信号通路包括signal-regulated激酶(ERK) 1/2途径提高细胞增殖,PI3 kinase-protein激酶B (PKB)途径促进细胞生存,和p38增殖蛋白激酶(MAPK)和c端Src激酶(埋头;Src)导致细胞迁移12]。此外,埋头(Src)激活和PI3K-PKB可以诱导一氧化氮(NO)的生产,因此,细胞通透性,促进血管生成(13]。VEGF高表达在肺癌和VEGF信号在胎儿肺发育中扮演着重要的角色,作为维护因素在成年生活(14]。此外,VEGFR2拮抗剂,SU5416 (Sugen),导致大鼠肺不成熟(15),并显示诱导肺动脉高压与缺氧在成年大鼠(16]。
鉴于VEGFR2重要角色的肺血管和从人类PAH基因研究获得初步证据(6),我们前瞻性分析KDR基因测序目标面板在一系列311 PAH患者临床分子基因诊断实验室的多环芳烃。我们报告两个家庭携带的基因型和表型特征KDR损失函数的变体。
患者和方法
基因分析
临床分子诊断,下一代测序(门店)的基因hPAH小组和hPVOD诱发基因和门店执行数据分析如前所述在Eyryet al。(3]。短暂,所有事件指数情况下指实验室,一个自定义面板包括九建立了多环芳烃和PVOD基因(基因BMPR2, TBX4、EIF2AK4 CAV1、KCNK3 SMAD9, ACVRL1, ENG BMP9)以及研究基因,包括KDR基因,使用。剪接变体被剪接分析预测工具,MaxEntScan, NNSplice, GeneSplicer并通过特HumanSplicingFinder积分器软件(https://blog.goldenhelix.com/splice-site-algorithms/)。因此311 PAH患者随后在法国肺动脉高压网络2017年和2019年之间进行了探讨KDR突变。所有患者进行遗传咨询和签署书面知情同意进行遗传分析。KDRDNA序列与参考序列(NM_002253.2)。可能基因干扰(乐金显示器)的变种KDR被Sanger测序证实。变体的分类遵循标准采用的美国大学医学遗传学(ACMG) [17]
临床评估
常规评估诊断PAH包括病史,体格检查,评估呼吸困难的纽约心脏协会(NYHA)功能类,6分钟步行距离(6随钻测量),超声心动图,肺功能测试,对比度增强型计算机断层扫描(CT)的胸部,肺通气/灌注扫描,腹部超声、自身免疫和艾滋病毒血清学筛查。肺功能测试包括在1 s (FEV用力呼气量1)、用力肺活量(FVC), FEV1/ FVC比率,肺活量(TLC)和扩散一氧化碳血红蛋白(调整的能力DLCOc)。血液动力学的测量获得的权利根据常规心脏catheterisation协议包括右心房压力(RAP)、平均肺动脉压(肺动脉平均),肺动脉楔压(PAWP)。由热稀释法测定心输出技术和心脏指数计算为心输出量/身体表面积。肺血管阻力(PVR)计算(肺动脉平均−PAWP) /心输出量(表达木材单位(吴))。
临床特点诊断和随访是存储在注册中心的法国肺动脉高压网络-比塞特尔(法国转诊中心医院和25个相关中心分布在法国)。这与法国生物伦理法律注册成立于协议(委员会国家de l 'Informatique et des自由)。
结果
两个指数PAH患者来自两个不同的家庭被发现携带KDR损失函数的变体。他们的家人随后探讨了(图1)。

家谱的载体KDR变异:a)家庭1;家庭2 b)。+ / +:突变非承运人。+ /−:杂合的载体KDR突变。●■:显示受影响的对象。 :显示对象怀疑PH值。
:显示对象怀疑PH值。 :表示无症状携带者的家族KDR突变。
:表示无症状携带者的家族KDR突变。
家庭1
指示病例(II.4)是一名55岁妇女诊断出患有多环芳烃。她没有病史,无烟草暴露。她的家族病史包括不明原因死亡,她的妹妹在46年(ii . 2) ii .由于心肺机能不全的上下文dexfenfluramine摄入量(图1一个)。在诊断,她是在功能类NYHA III和6随钻测量280米。肺功能测试显示轻度限制(FEV170%,FVC 74%, FEV10.8 / FVC, TLC 79%)和显著减少DLCOc预测值的29%。动脉血气显示室内空气严重低氧血动脉氧张力(PaO255毫米汞柱)。氨基端pro-brain利钠肽(中位数水平以上病人)在664 pg·毫升−1。超声心动图和心脏磁共振成像(MRI)显示严重肺动脉高压(PH)与右心室(RV)扩张(舒张压房车卷145毫升)和功能障碍(RV射血分数28%)与矛盾的隔膜。没有理由慢性心脏病和先天性心脏病。后发现右心静止catheterisation pre-capillary严重肺动脉高压与肺动脉平均为71毫米汞柱,PAWP 9毫米汞柱,心脏指数的2.23 L·分钟−1·米−2和吴PVR的15.7。急性血管扩张性测试是负面的。CT胸部显示轻微的间质性肺病的肺上叶优势(图2一个和b)。双口服联合治疗(内皮素受体拮抗剂(时代)和5型磷酸二酯酶抑制剂(PDE5i)发起。在18个月,临床和血液动力学的状态改善(NYHA功能二类,随钻测量355 m,肺动脉平均43毫米汞柱,心脏指数3.3 L·分钟−1·米−2和吴PVR 6.7)。
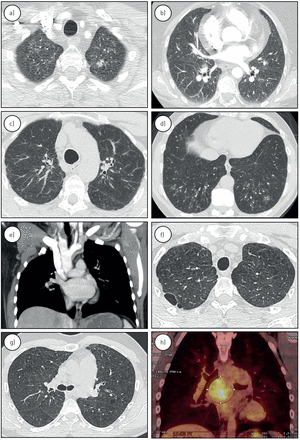
计算机断层扫描(CT)的胸部KDR突变携带者。a和b)的胸部CT肺动脉高血压(PAH)从家庭1暴露的间质性肺病患者II.4网状物上叶(a)和毛玻璃混浊主要在中低肺(b), c和d) CT胸部的PAH患者从家庭1 . 1揭示与胸膜下间质性肺病网状(c)和细支气管病变的肺(d)。e) CT胸部确定了双主动脉弓的无症状相对III.5携带KDR从家庭1突变。f-h) PAH患者III.3从家庭2,CT的胸部显示网状,轻微的肺气肿(f和g)和纵隔淋巴结肿大与温和的固定在正电子发射断层扫描CT (h)。
确定了杂合的基因分析KDR删除突变(c。3302T>G, p.Leu1101*) located in exon 24 of the gene, that induces a loss of the catalytic kinase domain of the receptor [18]。没有其他病理建立了PAH基因突变被发现。其他5个可用的家庭成员被基因分型。这KDR突变被发现在一个哥哥(. 1)抱怨呼吸困难好几年了。后KDR突变的识别,完成评估显示诊断的多环芳烃中血流动力学障碍(肺动脉平均27毫米汞柱,PAWP 4毫米汞柱,心脏指数2.3 L·分钟−1·米−2和吴PVR 5.4)。他在第三类,6-MWD 400和中位数水平以上病人是正常的。肺功能测试是正常的,除了一个显著的减少DLCOc在35%。动脉血气显示室内空气严重低氧血了PaO269毫米汞柱。CT胸部演示的间质性肺病包括胸膜下网状、小叶间隔线和细支气管异常(图2 c和d)。支气管肺泡灌洗是正常的。治疗由时代和PDE5i联合治疗开始6个月后,病人还活着的评估。
遗传分析还发现了三个无症状突变携带者(III.2完iii . 4和III.5 46岁,33岁和28年,分别)。临床评估提出了健康带菌者的亲戚。确定了低肺功能测试DLCOc所有航空公司的KDR个人III.2变异为53%、64%和50%,分别完iii . 4和III.5。DLCOc是正常的相对III.1没有携带家族突变。CT III.2胸部是正常的,和完iii . 4,确定了双主动脉弓III.5 (图2 e)。相对III.5执行正确的心catheterisation揭示无肺动脉高压(肺动脉平均17毫米汞柱),但轻度增加PVR意义不明的2.1。
家庭2
指示病例(III.3)是一个31岁的男性在30岁被诊断出患有多环芳烃。个人历史揭示了非过敏性哮喘童年和小调前烟草暴露(2久)。他的家族病史包括死亡在他外祖父60年的呼吸困难和右心衰(图1 b)。在诊断,他是在功能类NYHA III和6随钻测量210米。肺功能测试正常对照大减少DLCOc在19%。动脉血气显示室内空气严重低氧血了PaO261毫米汞柱。超声心动图和心脏MRI显示房车扩张(舒张压房车卷218毫升)和功能障碍(RV射血分数31%)与矛盾的隔膜。没有理由慢性心脏病和先天性心脏病。右心catheterisation显示严重前毛细管的肺动脉高压(肺动脉平均48毫米汞柱,PAWP 3毫米汞柱,心脏指数2 L·分钟−1·米−2和吴PVR 13.6)。急性血管舒张药测试是负面的。CT胸部的间质性肺病包括网状、小叶间隔线和磨砂玻璃的透明,轻微的肺气肿和纵隔淋巴结肿大(图2 f和g)正电子发射断层扫描(PET) - ct发现纵隔淋巴结肿大与温和的固定(最大标准化的吸收值6.8)(图2 h)。支气管肺泡灌洗进行显示haemosiderin-laden巨噬细胞(Golde得分135)。诊断为结节病最初怀疑,病人接受类固醇在3个月没有任何改善。双重口服联合治疗(时代和PDE5i)发起的。虽然是一个临床稳定性(NYHA功能II级,6随钻测量450米)为2年,最后右心catheterisation显示明显降低心输出量和增加PVR吴至11.1。清单对肺移植是目前讨论了这个病人。
建立了基因的遗传分析是负面的多环芳烃的发展,但确定了杂合的KDR突变(c.976 + 2 t > C)位于基因剪接供体基因内区7的共识。在网上这种剪接变异的分析表明,它是预测废除donor-splicing基因内区7的网站导致的跳过外显子7和截短蛋白p.His267Lysfs * 37。基因分型的父母透露,这种突变是遗传自母亲正常肺功能测试,胸部和正常的正常CTDLCOc在89%。外公已经去世,享年60岁的临床表现与PH值不一致。
讨论
我们描述了一种新的hPAH有关KDR丧失致病性变异基因的一个等位基因。我们确定了两个指数情况下携带KDR突变在311年前瞻性筛选一系列不相关的PAH基因调查病人(0.6%的患者)。在第一家庭,我们发现了一个KDR删除变体编码VEGFR2分子预测缺乏酪氨酸激酶催化部位和映射的关键催化剂残留物,比如自身磷酸化酪氨酸1175,(18,19]。隔离分析可能的两代人,表明变异运营商要么宣布多环芳烃与低DLCOc,或者只有一个下降DLCOc没有其他症状,而非承运人的亲戚是自由和有正常的症状DLCOc。在第二个家庭,影响共识的剪接变体施主能级被确认KDR并预测诱导蛋白的截断跳过的外显子7从immunoglobulin-like域3的VEGFR2证明是必不可少的VEGF绑定(20.),直到carboxy-terminal蛋白质。DLCOc还深深影响指数下降情况而这很正常在航母PAH患者的母亲的影响。有趣的是,在这个家庭,外公的病史符合PAH-induced右心衰和死亡。因此,我们找到了两个不同的变量分为致病根据ACMG标准KDR基因(17]。KDR损失函数的变体是极其罕见的一般人群(11观察变异在141 456人中可用gnomAD数据库),这个基因pLI得分为1 (o / e = 0.15(0.09 - -0.25), %你好:2.22)这意味着它非常宽容的损失函数(21,22]。这些发现强烈支持平行研究的基因研究的国际财团多环芳烃分析全基因组测序数据的13037人,包括1148名受试者招募PAH域(23]。
的DLCOc影响受试者的降低比较明显比未受感染的航空公司,是否DLCOc减少是早期发展的标志KDR相关的疾病需要进一步调查。的长期随访报道载体对象将信息如果病理过程不能被中止。除了低DLCOc,所有受影响的病人与放射性间质性肺病的证据提出了高分辨率CT可以突出,导致最初的错误诊断结节病的病人。相反,KDR突变携带者没有宣布多环芳烃有正常的高分辨率CT即使亚临床肺实质参与可能会怀疑的DLCOc减少。因此,存在轻微的间质性肺疾病可能是一个重要的辐射PAH发展的标志KDR突变携带者。在这种背景下,DLCOc减少反映出气体交换障碍可能的结果肺部远端血管床的肺实质参与和改造。三个PAH患者肺通气/灌注扫描和CT肺血管造影(表现在病人II.4家庭1和III.3家庭2)没有发现明显的肺血管畸形的证据。然而,这些考试探讨节段和subsegmental肺动脉,并不能排除肺部微脉管系统的发育异常。肺实质疾病和肺高血压协会建议可能的肺部发育障碍而不是一个特定的和独特的肺血管重塑hPAH由于观察到BMPR2突变。然而,没有可用的肺组织受影响对象KDR突变,是限制了病理生理学解释可能来自观察病变。
的表达KDR富含人类胚胎肺内皮细胞(24)和VEGFR2的绝对要求在小鼠胚胎血管的发展已经证明了KDR失活产生胚胎致死表型异常血管发展(25]。在老鼠的发展过程中,VEGF mRNA表达的远端气道上皮细胞和sub-epithelial矩阵E11.5肺,而VEGFR2-positive在间质细胞局部密切同发展中上皮细胞(26,27]。这种上皮细胞之间的空间关系产生VEGF和内皮细胞表达VEGFR2使必不可少的相声epithelium-capillary的形成影响,这对气体交换是必不可少的。VEGF信号有重要作用的适当的血管形成胚胎肺也出生后。Jakkulaet al。(15]使用VEGF-R2拮抗剂SU5416 (Sugen)表明,新生儿的老鼠,抑制VEGF信号减少alveolarisation和动脉密度下降,表明VEGFR2大大有助于血管增长出生后发生肺的快速增长。事实上,早产儿肺发育不全的远端空气空间,不能有隔膜的,导致降低了气体交换面积(28]。慢性治疗成年老鼠SU5416诱导肺泡隔细胞凋亡,导致空气空间的扩大表明肺气肿,表明VEGF信号需要肺脉管系统的维护和肺泡结构在成年期(29日,30.]。
损失一个等位基因的功能KDR预计将减少VEGFR2介导信号的haplo-insufficiency VEGF通过一种机制已被证明对多环芳烃由于mono-allelic损失函数的BMPR2(31日]。事实上,在老鼠携带的杂合的中断KDR,KDR信使rna几乎减少了50%,异常反应观察心脏缺血性预处理(32]。此外,杂合的老鼠KDR损失函数显示的缺陷在支持肿瘤生长和血管生成,清楚地展示这个基因的基因剂量效应和支持人类致病作用[33]。
虽然部分缺陷KDR基因是多环芳烃的一个原因可能出现矛盾的血浆VEGF浓度和增加VEGF和KDR表达PAH病变([34),和我们的结果补充图S1),进一步支持元素的致病作用降低VEGF信号KDR损失函数在人类PAH来自老鼠的实验模型PAH SU5416所致。多环芳烃发生在老鼠SU5416政府结合缺氧后,单侧肺切除术或在动物体内和肺部病变是接近观察人类多环芳烃(16,35,36]。这些动物模型显然支持维护的角色在成年后VEGF信号和VEGF信号引起内皮细胞凋亡,这一现象提出了参与SU5416模型。然而,这些模型是不同的KDRhaplo-insufficiency诱导人类形式的多环芳烃,因为缺乏是只有部分(约50%的表达式)和代理发展生活中肺血管限制通过降低VEGF信号可能是重要的。
由于减少了DLCOc似乎是唯一能被检测出的生理异常未受影响KDR突变携带者,需要另一个触发因素提出解释疾病的起始。影响CT胸部的话题,一起恶化DLCOc,提示有实质的肺病。实验模型记录VEGF信号的影响在博来霉素纤维化模型。的确,VEGF信号血管生成之外的其他功能,如刺激上皮细胞增殖,防止上皮细胞凋亡和血管重塑的衰减通过内皮细胞保护作用在一个上下文的实验性肺纤维化大鼠(29日,37,38]。
对于所有新发现的基因参与遗传性疾病,核心问题在于这些突变的疾病可以估算。我们确定损失的功能变体KDR基因,丧失功能变体是极其罕见的。我们也清楚地显示在一个家庭的cosegregation致病变种与特定表型结合多环芳烃和ILD和减少有关DLCOc。VEGFR2是参与肺脉管系统的发展和中起着重要的作用的结构特异性肺气体交换。此外,VEGF信号过程中起着重要作用维持上皮和内皮完整性。因此,先前的病理生理和WGS数据,结合临床和遗传元素从这项研究允许考虑KDR作为一种新的多环芳烃导致基因。是否KDR与PH值应该被视为一个纯粹的遗传多环芳烃形式或PH值发生在肺发育障碍的设置应该讨论的肺组织影响的分析主题和小鼠模型的KDR haploinsufficiency [39]。
补充材料
可共享的PDF
确认
本研究利用数据生成的破译社区。中心的完整列表的生成的数据可用http://decipher.sanger.ac.uk和通过电子邮件decipher@sanger.ac.uk。我们感谢安妮·勒罗伊和玛丽- Waill专家技术援助。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:m .巢窝没有披露。d . Montani报告赠款和个人费用从Actelion股价和拜耳,葛兰素史克的个人费用,辉瑞、默沙东公司外部提交的工作。
利益冲突:b Girerd没有披露。
利益冲突:n Favrolt没有披露。
利益冲突:m . Riou没有披露。
利益冲突:l .副检察官没有披露。
利益冲突:g . Manaud没有披露。
利益冲突:f . Perros没有披露。
利益冲突:美国伯爵没有披露。
利益冲突:M.W.莫雷尔是Morphogen-IX的一名员工。
利益冲突:m·亨伯特报告个人费用从Acceleron Actelion股价,默克和联合疗法,赠款和个人费用从拜耳和葛兰素史克在提交工作。
利益冲突:f . Soubrier没有披露。
支持声明:提供的项目经费威康信托基金会。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2019年11月7日。
- 接受2020年1月2日。
- 版权©2020人队