抽象
在阻塞性肺病负担研究中,我们研究了慢性支气管炎症状的患病率、负担和潜在危险因素。
在参与站点中选择年龄≥40岁的代表性人群样本。参与者完成了问卷调查和肺活量测定。慢性支气管炎的症状定义为每年≥3个月、≥2年、最多天数的慢性咳嗽和痰。
对来自29个国家33个地点的24 855名受试者的数据进行了分析。符合慢性支气管炎定义的自我报告症状在不同地点的患病率有显著差异,从莱克星顿(肯塔基州,美国)的10.8%,到Ile-Ife(尼日利亚)和布兰太尔(马拉维)的0%。年龄较大、教育程度较低、目前吸烟、职业暴露于烟雾、自我报告的哮喘或肺癌诊断和慢性肺病家族史都与慢性支气管炎的风险增加有关。慢性支气管炎症状与肺功能恶化、呼吸困难、呼吸系统恶化风险增加和生活质量下降有关,与其他肺部疾病的存在无关。
慢性支气管炎症状的患病率在整个研究的网站差别很大。慢性支气管炎症状与显著的负担都与慢性气流阻塞和个人与正常肺功能相关。
抽象
慢性支气管炎的症状与显著负担气流阻塞的存在,不论相关http://ow.ly/kP9P30eFELK
介绍
Chronic bronchitis is defined epidemiologically as cough and sputum production for ≥3 months in each of least two consecutive years [1]。它影响约慢性阻塞性肺疾病(COPD)的三分之一,而且还发生在肺功能正常的个体,与患病率估计在基于人口的研究(2.6-16%)变化既广泛2- - - - - -7]和之间的COPD患者(7.4-53%)[8- - - - - -10]。Presence of chronic bronchitis symptoms correlates with faster forced expiratory volume in 1 s (FEV1)下降和大多数死亡的风险增加[11- - - - - -15], 但不是所有的 [16,17]发表的研究报告。此外,它与糟糕的健康状况影响科目[相关4,9,10]。报告的慢性支气管炎的危险因素包括烟草烟雾、室内外空气污染和职业暴露[18- - - - - -21]。
虽然慢性支气管炎的症状通常报道,在受影响的个人的不同国家患病率和负担数据,特别是在那些肺功能正常的,是有限的[2- - - - - -4]。阻塞性肺疾病的负担(BOLD)的研究是一个国际性的,横断面研究在世界各地的不同部分评估COPD的患病率和负担[22]。在这篇文章中,我们报告从慢性支气管炎症状的流行,负担和潜在的风险因素的BOLD研究数据。
材料和方法
在BOLD研究中使用的方法进行了详细别处描述[22]。简而言之,在参与中心随机选择年龄≥40岁的代表性人群样本。提供书面知情同意的参与者完成了一份详细的问卷调查,并在经培训和认证的工作人员指导下进行了支气管扩张器肺量测定。问卷被翻译成当地网站使用的语言,再进行反向翻译和核实。肺量测定法进行了使用简单的肺活量计(ndd医疗技术、苏黎世、瑞士),15分钟后管理支气管扩张剂(200μg舒喘灵)。所有肺功能图的质量均进行集中评估,仅采用适当质量的测量(基于美国胸科协会/欧洲呼吸协会标准)进行分析[188bet官网地址23]。用力肺活量(FVC)和FEV1根据第三次全国健康与营养调查(NHANES III)白种人方程计算出%预测值[24]。来自33个粗体站点的数据在撰写本文时已完成数据集,这些数据用于分析。
定义
慢性支气管炎的症状定义为咳嗽和痰在大多数日子≥3个月,每年≥2年,使用肯定的回答所有的问题:“你通常咳嗽时,你不感冒吗?”、“有没有几个月你大部分时间都在咳嗽?”、“你每年有3个月的咳嗽时间吗?”以及确定咳嗽持续≥2年的问题“你患这种咳嗽有多少年了?”以及对一系列有关痰的类似问题的肯定回答。慢性气流阻塞(曹)的定义是一个后支气管扩张剂FEV1/ FVC比值小于正常年龄和性别的下限,根据NHANES III方程白种人。在那些符合此标准,我们分为疾病的严重程度基于后支气管扩张肺功能1,根据慢性阻塞性肺疾病肺功能分类FEV全球倡议(1≥80%PRED,50- <80%预解码值,30- <50%预解码值和<30%预解码值)[25]。基于问卷数据被确定的其他医疗状况的存在。Biomass fuel use was defined as self-reported ever use of coal, coke, wood, crop residues or dung for cooking or heating for >6 months. Dyspnoea was measured using the modified Medical Research Council (mMRC) dyspnoea scale [26]。mMRC 2级(“在水平上以自己的速度行走时呼吸困难”)或更高级别被用来定义临床显著的呼吸困难。根据对“呼吸问题干扰日常活动或导致参与者错过工作”的回答,以及根据导致受试者去看医生或住院的自我报告的呼吸问题对卫生保健资源的使用情况,评估了呼吸恶化情况。生活质量采用12项简式健康调查问卷(SF-12)进行测量。计算身心健康SF-12综合评分并进行分析。总分从0到100分不等,100分代表最佳生活质量[27]。
数据分析
除了位点特异性患病率估计,将其加权,以反映在每个站点的采样设计,所有其它分析中使用未加权的数据。有慢性支气管炎症状的存在相关的因素进行多元回归分析检查,用下面的协变量潜在的危险因素:年龄,性别,教育程度,吸烟状况和被动吸烟,职业接触粉尘和烟雾,生物质燃料利用(使用煤,焦炭,木,作物残余物或粪便的烹调或加热),共病症包括其他肺部疾病(哮喘,肺结核或肺癌)和心脏疾病,慢性肺部疾病的家族史和住院现有呼吸问题age of 10 years. A similar model was applied, restricted to: 1) subjects with CAO, 2) subjects without CAO and 3) current smokers.
采用线性回归模型预测FEV1在FEV改变1后给药支气管扩张剂(ΔFEV1)作为慢性支气管炎症状的函数和前面列出的协变量。此外,我们采用单独的逻辑回归模型来预测临床显著呼吸困难,呼吸加重,利用医疗资源,生活(最低四分位数)为同一组的协变量的函数的质量以及肺功能数据(CAO和FVC)。这些协变量与对生活质量的分析高血压,糖尿病和中风的医学诊断自报数据补充。这些分析中的那些具有和不CAO在所有队列进行整体和分开。所有回归模型进行了调整学习网站作为一个固定的作用,类变量。
网站使用瓦尔德卡方统计量作为衡量可变性的慢性支气管炎症状患病率在网站,我们使用了协变量减少这个统计调整后作为整体的比例的代理站点变化引起的慢性支气管炎患病率,反是。
分析均采用R统计软件(版本3.3.1进行;www.R-project.org)。统计显着性指的是p值<0.05。
结果
患病率和潜在的危险因素,慢性支气管炎的症状
Data from 23 855 males and females from 33 BOLD study sites in 29 countries were analysed. The proportion of self-reported chronic bronchitis symptoms overall was 3.1%: 3.6% for males and 2.6% for females. Chronic bronchitis symptoms were present in 10.2% of individuals with CAO and 2.2% of those without CAO (1.06% and 1.97% of the total sample, respectively). Overall, proportion of subjects reporting chronic bronchitis symptoms increased with age, worse lung function and exposure to potential risk factors (表格1)。
图1节目由性别,部位,吸烟状况和哮喘病史的慢性支气管炎症状的患病率加权。慢性支气管炎的症状患病率跨站点显著变化,与列克星敦(肯塔基州,美国),翠(吉尔吉斯斯坦)和伦敦(英国)有率最高(10.8%,分别为8.3%和7.7%)和浦那(印度),科托努(贝宁),伊费岛(尼日利亚)和布兰太尔(马拉维)每一个都具有患病<0.5%。在所有网站中的慢性支气管炎症状的患病率> 1%,它们是由与不曹俩个人的报道。在慢性支气管炎症状站点之间的患病率的方差的约18%可以通过在所测量的协变量的差异来解释。
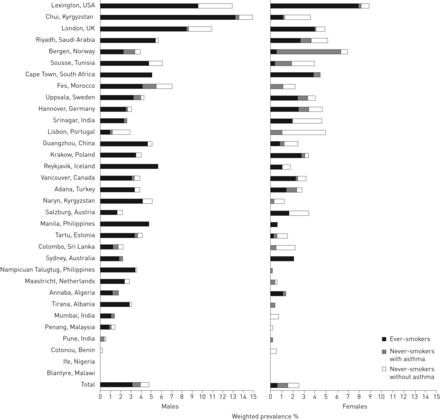
跨越研究基地慢性支气管炎的症状患病率估计。
在多变量分析,因素显著与报告慢性支气管炎症状的风险增加了年龄,教育较少,目前吸烟,职业暴露于烟雾,哮喘或肺癌和慢性肺部疾病家族史的自我报告诊断(表2)。潜在的风险因素形状以与不曹主题相似,虽然有与任何慢性肺部疾病家族史或教育那些没有CAO没有显著关联。在受限于当前吸烟者的分析,每日抽烟数量的慢性支气管炎症状的独立预测因子(为每天1.63 OR 10支增加,95%CI 1.37-2.00; P <0.001)。
负担慢性支气管炎症状
的慢性支气管炎症状的存在是有关更糟肺功能无论在CAO和哮喘基作为支气管扩张剂给药以及更显着的响应(表3)。科目与FEV改善的比例1≥12% and >200 mL after bronchodilator administration was similar in subjects with self-reported asthma and CAO (21.5%与21.8%, p=0.820),而FEV患者所占的比例1前者>改善15%,> 400ml改善较大(6.9%)与5.3%,p = 0.039)。慢性支气管炎症状与肺功能恶化(FEV)的关系1%PRED)为调整潜在的混杂因素后,二者在整个样品中的(-2.74%,P <0.001)和在那些与CAO(-4.04%,P <0.001)和不CAO(-1.92%,P亚组本<0.001)。同样,慢性支气管炎症状具有增加的关联FEV1支气管扩张剂治疗后的改善与肺功能无关(FEV)1)和其他潜在的混杂因素(ΔFEV117毫升,p = 0.011)。在logistic回归分析中,慢性支气管炎症状的存在与其他呼吸系统症状的风险增加、呼吸系统恶化和生活质量下降(表4)。调整为可能的混杂因素后,对生活质量的慢性支气管炎症状的影响比哮喘或CAO(SF-12的物理得分的显著较大-5.9与-4.9与-1.7,分别,P <0.001;SF-12心理评分-3.5与-1.4与-1.0,分别,P <0.001)。
讨论
我们观察到,慢性支气管炎的流行程度在不同的研究地点差异很大。更重要的是,我们已经证明,慢性支气管炎症状的存在与患者的显著负担相关,无论他们是否伴有气流阻塞,这与肺功能恶化、呼吸困难、呼吸系统恶化和生活质量下降有关。
慢性支气管炎症状流行数据来自大多数研究地点,但并非所有研究地点都在以前发表的基于症状评估问卷的结果范围内[2- - - - - -7]。出人意料的是,我们发现其中只有一个人(0-0.5%)报告慢性支气管炎症状的几个中心。此外,在这些中心(印度浦那;贝宁科托努,伊费岛,尼日利亚和布兰太尔,马拉维)的受试者比例谁报告咳嗽和谁报告的痰的产生,相较于其他网站均较低。这一观察是由一些支撑。4,29,三十],但并非所有来自这些国家的研究[31]。需要更多的本地数据来验证这是否是一个报告问题,或者慢性咳嗽是在这些人群中确实罕见,但观察与吸烟和哮喘在这些人群中的发病率较低一致。在跨站点慢性支气管炎的症状患病率差异幅度这里报告很大,但类似于通过在世界不同地区的标准化方法以外唯一发表的研究在年轻人群中描述2]。在站点之间的慢性支气管炎症状的患病率的方差的只有18%能够通过在所测量的协变量位点的变化进行说明。这种差异的部分原因可能是由于BOLD问卷调查,不询问一些潜在的风险因素,如慢性鼻窦炎和胃食管反流问题的局限性。在有呼吸道症状和报告他们的可能性相关联的耻辱差异也可能是重要的考虑因素。
吸烟和慢性支气管炎之间的关联是众所周知的[2,18,20],在我们的数据中,这一结论适用于目前的吸烟者,但不适用于已戒烟者(这与证明戒烟后慢性支气管炎症状消失的报告一致[32,33])。与慢性肺病家族史的相关性可能部分是由哮喘中慢性支气管炎症状的风险增加介导的,但其影响在表2是至少部分地独立哮喘的个人历史,并与慢性支气管炎相关遗传性状也有报道[34]。
我们已经描述了与慢性支气管炎症状相关的广泛的负面结果(肺功能恶化,生活质量下降,更多的症状和更多的恶化)。既往研究一致报道慢性支气管炎患者中曹和肺功能正常者的健康状况均较差[4,9,10,35,36]。类似地,在哮喘患者的慢性咳嗽和痰产生的存在已经与不受控制的哮喘风险的增加有关[37]。值得注意的是,慢性支气管炎对生活质量的不良影响可能大于哮喘或慢性阻塞性肺病,这证实了先前发表的结果[38]。尽管慢性支气管炎与气流阻塞的协会,慢性支气管炎症状的负面结果也是显而易见的个人无气道阻塞。在我们的样本,这些科目的数量几乎增加了一倍慢性支气管炎患者与CAO的那个。对于这一组,慢性支气管炎已收到流行病学研究外令人惊讶的一点关注。有一个在那些患有慢性支气管炎的症状慢性气流阻塞的高患病率,这是吸烟者和不吸烟者真实,慢性支气管炎是未来阻碍一个更好的预测比呼吸困难的存在[38]。在慢性阻塞性肺病病例研究中使用这一信息的主要限制是,这种相关性在那些有持续症状的患者中是最大的,而症状是高度可变的[39,40]。然而,对于显著慢性支气管炎负担的数据表明,慢性支气管炎症状可能戒烟后一起消失的证据表明,识别这些问题和干预措施,旨在戒烟可能是潜在的好处的。
此外,我们观察到的慢性支气管炎症状到支气管扩张剂增加响应的关联。支气管扩张试验在哮喘和COPD的鉴别诊断常用;然而,这不是一个理想的工具,因为显著改善存在于患者的一个相当大的比例与这两种疾病[的41]。当应用全球哮喘倡议(GINA)标准时,支气管扩张剂对我们人群的显著反应,特别是较低的阈值(FEV)1improvement of ≥12% and 200 mL) was of little value. Interestingly, in our sample the presence of chronic bronchitis symptoms was related to a more pronounced response to bronchodilator both in CAO and asthma groups and after the exclusion of chronic bronchitis subjects absolute improvement after bronchodilator was similar in asthma and CAO. Differential diagnosis of asthma and COPD is often troublesome, with 15–45% of subjects having the features of both of these diseases [42]。慢性支气管炎的症状有肺功能/支气管扩张剂反应,生活质量显著的影响和可能的预后,且这些症状在呼吸道阻塞性疾病的分类中包含可能导致更精确的分类。
本研究有一定的局限性。横断面调查设计排除了因果关系的评估。慢性支气管炎和其他呼吸系统症状的数据是自我报告的,因此容易出现回忆偏差或对正在评估的症状的文化定义的理解。同样,哮喘诊断的数据是自我报告的;观察到哮喘组和CAO组对支气管扩张剂的反应缺乏显著差异,这可能是由于这个问题,至少部分原因,并强调了自我报告的哮喘诊断的低准确性。以问卷为基础的慢性支气管炎患病率被过高估计,因为某些受试者的慢性咳嗽和痰的产生是由哮喘、支气管扩张、胃食管反流、心力衰竭或慢性鼻窦炎(后鼻漏)引起的[43]。在我们的研究中,哮喘报告了约三分之一患有慢性支气管炎的症状。然而,谁是慢性咳嗽困扰的科目相当大的比例可能没有正面回答界定慢性支气管炎的所有问题。在我们的样本中,受试者〜11%报告说,他们“通常是”咳嗽和痰产生“当(他们)没有冷”(用〜3%的报告慢性支气管炎相比)。如何在不同的环境了解调查问卷将通过语言和本地文化的差异[影响44,45],甚至小的变化在一个问题的措辞会影响呼吸道症状的估计[46]。使用具有严格的质量控制(包括验证后,翻译成各种当地语言),并使用训练有素的工作人员来管理最小化标准化的问卷调查表,但不能消除由于这些问题的偏见。但是,有慢性支气管炎症状的患病率和吸烟率,表明这些调查表的答复是相对一致的之间有明显的联系。Finally, a dose of 200 μg of salbutamol will not produce maximum bronchodilation in all participants, and in clinics a dose of 400 μg is commonly recommended. The BOLD programme has used 200 μg for both ethical and pragmatic reasons. Participants in the study, unlike clinic patients, have not asked for help with a specific problem, are less likely to have taken a β-agonist before and will not be used to the temporary side-effects. Standardising the dose to 200 μg provides valuable and standardised information, but interpretation of the results needs to consider that the bronchodilation may not always be maximal. Published studies have used different doses of salbutamol, and GINA guidelines mention doses in the 200–400 μg range as appropriate.
总之,慢性支气管炎症状的患病率在整个研究网站差别很大,它们的存在与显著的负面结果,不仅阻碍科目,而且在那些没有气流阻塞有关。
致谢
笔者想承认BOLD研究合作者的贡献:南山钟(首席研究员(PI)),圣明刘加春路,Pixin冉,大理王,净瓶郑和裕民周(广州呼吸疾病研究所,广州医学院学院,广州,中国);阿里Kocabaş(PI),阿提拉Hancioglu,伊斯梅尔汉坦,塞达特Kuleci,艾哈迈德思南Turkyilmaz,塞玛了Umut和图尔盖Unalan(医学库库罗瓦大学医学院,胸部疾病,阿达纳,土耳其的部门);迈克尔Studnicka(PI),Torkil道斯,贝恩德兰姆普雷希和LEA Schirhofer(帕拉塞尔苏斯医科大学,胸腔内科,萨尔茨堡,奥地利的部门);埃里克·贝特曼(PI),Anamika Jithoo(PI),西瑞·亚当斯,爱德华·巴恩斯,贾斯珀·弗里曼,安东·海耶斯,斯福Hlengwa,恭Johannisen,马里亚纳库普曼,Innocentia·洛,伊奈Ludick,阿尔塔Olckers,约翰娜Ryck和贾妮塔Storbeck(大学开普敦肺研究所,开普敦,南非);Thorarinn Gislason的(PI),Bryndis Benedikdtsdottir,克里斯汀Jörundsdottir,洛维萨Gudmundsdottir,Sigrun Gudmundsdottir和贡纳尔Gundmundsson(过敏,呼吸内科和睡眠,Landspitali大学附属医院,雷克雅未克,冰岛系);埃娃Nizankowska-Mogilnicka(PI)的Jakub弗雷,拉法尔Harat,菲利普Mejza,帕维尔Nastalek,安杰Pajak等,沃伊切赫Skucha,安德烈泽杰·斯斯卡泽克利克和玛格达Twardowska(肺疾病科,内科,雅盖隆大学医学院,克拉科夫,波兰);托比亚斯威尔特(PI),伊莎贝尔Bodemann,亨宁Geldmacher和亚历山德拉Schweda-Linow(汉诺威医学院,汉诺威,德国);Amund Gulsvik(PI),蒂娜恩德雷森和琳恩斯文森(胸腔医学,医学研究所,卑尔根,挪威卑尔根大学的系); Wan C. Tan (PI) and Wen Wang (iCapture Center for Cardiovascular and Pulmonary Research, University of British Columbia, Vancouver, BC, Canada); David M. Mannino (PI), John Cain, Rebecca Copeland, Dana Hazen and Jennifer Methvin (University of Kentucky, Lexington, KY, USA); Renato B. Dantes (PI), Lourdes Amarillo, Lakan U. Berratio, Lenora C. Fernandez, Norberto A. Francisco, Gerard S. Garcia, Teresita S. de Guia, Luisito F. Idolor, Sullian S. Naval, Thessa Reyes, Camilo C. Roa, Jr, Ma. Flordeliza Sanchez and Leander P. Simpao (Philippine College of Chest Physicians, Manila, Philippines); Christine Jenkins (PI), Guy Marks (PI), Tessa Bird, Paola Espinel, Kate Hardaker and Brett Toelle (Woolcock Institute of Medical Research, Sydney, Australia), Peter G.J. Burney (PI), Caron Amor, James Potts, Michael Tumilty and Fiona McLean (National Heart and Lung Institute, Imperial College, London, UK); Emiel F.M. Wouters and Geert-Jan Wesseling (Maastricht University Medical Center, Maastricht, the Netherlands); Cristina Bárbara (PI), Fátima Rodrigues, Hermínia Dias, João Cardoso, João Almeida, Maria João Matos, Paula Simão, Moutinho Santos and Reis Ferreira (Portuguese Society of Pneumology, Lisbon, Portugal); Christer Janson (PI), Inga Sif Olafsdottir, Katarina Nisser, Ulrike Spetz-Nyström, Gunilla Hägg and Gun-Marie Lund (Department of Medical Sciences, Respiratory Medicine and Allergology, Uppsala University, Uppsala, Sweden); Rain Jõgi (PI), Hendrik Laja, Katrin Ulst, Vappu Zobel and Toomas-Julius Lill (Lung Clinic, Tartu University Hospital, Tartu, Estonia); Parvaiz A. Koul (PI), Sajjad Malik, Nissar A. Hakim and Umar Hafiz Khan (Sher-i-Kashmir Institute of Medical Sciences, Srinagar, India); Rohini Chowgule (PI), Vasant Shetye, Jonelle Raphael, Rosel Almeda, Mahesh Tawde, Rafiq Tadvi, Sunil Katkar, Milind Kadam, Rupesh Dhanawade and Umesh Ghurup (Indian Institute of Environmental Medicine, Mumbai, India); Imed Harrabi (PI), Myriam Denguezli, Zouhair Tabka, Hager Daldoul, Zaki Boukheroufa, Firas Chouikha and Wahbi Belhaj Khalifa (Faculté de Médecine, Sousse, Tunisia); Luisito F. Idolor (PI), Teresita S. de Guia, Norberto A. Francisco, Camilo C. Roa, Fernando G. Ayuyao, Cecil Z. Tady, Daniel T. Tan, Sylvia Banal-Yang, Vincent M. Balanag Jr, Maria Teresita N. Reyes and Renato. B. Dantes (Lung Centre of the Philippines, Philippine General Hospital, Nampicuan and Talugtug, Philippines); Sanjay Juvekar (PI), Siddhi Hirve, Somnath Sambhudas, Bharat Chaidhary, Meera Tambe, Savita Pingale, Arati Umap, Archana Umap, Nitin Shelar, Sampada Devchakke, Sharda Chaudhary, Suvarna Bondre, Savita Walke, Ashleshsa Gawhane, Anil Sapkal, Rupali Argade and Vijay Gaikwad (Vadu HDSS, KEM Hospital Research Centre Pune, Pune, India); Sundeep Salvi (PI), Bill Brashier, Jyoti Londhe and Sapna Madas (Chest Research Foundation, Pune, India); Mohamed C. Benjelloun (PI), Chakib Nejjari, Mohamed Elbiaze and Karima El Rhazi (Laboratoire d'Epidémiologie, Recherche Clinique et Santé Communautaire, Fès, Morroco); Daniel Obaseki (PI), Gregory Erhabor, Olayemi Awopeju and Olufemi Adewole (Obafemi Awolowo University, Ile-Ife, Nigeria); Mohamed Al Ghobain (PI), Hassan Alorainy (PI), Esam El-Hamad, Mohamed Al Hajjaj, Ayan Hashi, Rowena Dela, Rofel Fanuncio, Elizabeth Doloriel, Imelda Marciano, Lyla Safia (Saudi Thoracic Society, Saudi Arabia); Talant M. Sooronbaev (PI), Bermet M. Estebesova, Meerim Akmatalieva, Saadat Usenbaeva, Jypara Kydyrova, Eliza Bostonova, Ulan Sheraliev, Nuridin Marajapov, Nurgul Toktogulova, Berik Emilov, Toktogul Azilova, Gulnara Beishekeeva, Nasyikat Dononbaeva and Aijamal Tabyshova (Pulmunology and Allergology Department, National Centre of Cardiology and Internal Medicine, Bishkek, Kyrgyzstan); Kevin Mortimer (PI), Wezzie Nyapigoti, Ernest Mwangoka, Mayamiko Kambwili, Martha Chipeta, Gloria Banda, Suzgo Mkandawire and Justice Banda (The Malawi Liverpool Wellcome Trust, Blantyre, Malawi); Hasan Hafizi (PI), Anila Aliko, Donika Bardhi, Holta Tafa, Natasha Thanasi, Arian Mezini, Alma Teferici, Dafina Todri, Jolanda Nikolla and Rezarta Kazasi (Tirana University Hospital Shefqet Ndroqi, Tirana, Albania); Hamid Hacene Cherkaski (PI), Amira Bengrait, Tabarek Haddad, Ibtissem Zgaoula, Maamar Ghit, Abdelhamid Roubhia, Soumaya Boudra, Feryal Atoui, Randa Yakoubi, Rachid Benali, Abdelghani Bencheikh and Nadia Ait-Khaled (Faculté de Médecine Annaba, SEMEP, El Hadjar, Algeria); Li-Cher Loh (PI), Abdul Rashid and Siti Sholehah (Penang Medical College, Penang, Malaysia); and Herve Lawin (PI), Arsene Kpangon, Karl Kpossou, Gildas Agodokpessi, Paul Ayelo and Benjamin Fayomi (Unit of Teaching and Research in Occupational and Environmental Health, Cotonou, Benin).
脚注
支持声明:BOLD研究资助机构名单可在BOLD网站(www.boldstudy.org/sponsors.html)。提案国在研究设计,数据收集,数据分析,数据解释或书面报告没有任何作用。
利益冲突:没有申报。
- 收到了2017年3月24日。
- 接受2017年8月10日。
- 版权所有©ERS 2017年
该版本采用知识共享署名4.0许可协议的条款分发。















