文摘
基质金属蛋白酶(MMPs) metzincin小组的成员分享守恒的锌结合主题的蛋白酶催化活性部位。它最初认为他们的主要功能是降解细胞外基质(ECM)的各种组件,然而,最近的研究让我们欣赏他们的意义作为细胞外信号网络组织的监管机构。由于广泛的底物特异性,基质金属蛋白酶有助于体内平衡的组织和参与多种生理过程,如骨重建、血管生成、免疫和伤口愈合。MMP的活动是在转录水平,严格控制pro-peptide激活和抑制基质金属蛋白酶组织抑制剂。特异表达MMP的活动导致病理条件下,如关节炎、炎症和癌症,因此强调基质金属蛋白酶作为有前途的治疗目标。分析MMP的突变小鼠是小说的一个重要工具识别功能和交互的单身MMP的成员。推进我们的理解组织内稳态的MMP的贡献将使我们确定因果关系失调,疾病病理学的发展,从而指导我们成功MMP-directed疗法。
matrixins或基质金属蛋白酶(MMPs)是大型的成员metzincin总科像虾红素,serralysins, reprolysins, adamalysins或disintegrin金属蛋白酶(亚当斯)。在经典视图中,基质金属蛋白酶是集体能够降解细胞外基质(ECM)的所有组件和基底膜,限制其功能组织改造和维护。然而最近的底物识别研究表明基质金属蛋白酶调节趋化因子的释放和激活,细胞因子,生长因子,抗生素肽,和其他生物活性分子从而参与生理过程如先天和适应性免疫,炎症,血管生成,骨重建和神经突生长。
高序列相似性MMP的催化领域中发现几乎所有王国的生活。至少25个不同的脊椎动物基质金属蛋白酶已经描述到目前为止,24种不同基质金属蛋白酶在人类,包括MMP-23的两个相同的形式,通过两个不同的基因编码,例如MMP23A和MMP23B。目前的哺乳动物的多样性MMP基因家族是特别来自一个广泛的基因串联重复和外显子洗牌在进化过程中在四足动物血统。考虑到这一点,一些实际的MMP的成员很可能衍生品从单个基因导致MMP基因簇,其组织保存从两栖动物到哺乳动物。集群在人类基因组中位于染色体11的时候,包含金属蛋白酶- 1、3、7、8日,-10年,-12年,-13年、-20年和-27年。相比之下,大多数的其他人类MMP基因位于不同的染色体,从而导致共有10个不同的染色体为所有人类MMP基因(241]。
尽管基质金属蛋白酶的活性已被证明是必要的在细胞生物过程和许多基本的生理事件涉及组织改造,如血管生成、骨骼发育、伤口愈合和乳房退化(2),对MMP的功能越来越浓的兴趣主要来自他们的角色在一些病理条件下,如癌症或慢性炎症性疾病3]。
本文概述的这些肽链内切酶的基本生理功能,特别关注小说的发现在他们复杂的监管和广泛的底物谱通过高通量degradomic屏幕最近显著扩大。我们进一步讨论最近的信息MMP的突变小鼠模型揭示了这些酶的功能关联到多个生理和病理过程。
调节基质金属蛋白酶
由于其广泛的底物谱,基质金属蛋白酶作为重要的监管机构整合组织内稳态和免疫网络的组织和细胞内多向交流。因为不受控制的MMP的活动可以很容易地成为体内平衡的破坏,导致崩溃,他们的活动必须严格监管。
所示图1基质金属蛋白酶的催化活性强烈控制在四个不同层次:1)基因表达与转录和转录后调控;2)细胞外的本地化和组织或细胞类型的MMP的版本,称为上;3)通过切除pro-domain pro-enzyme激活;和4)抑制特定抑制剂,即。基质金属蛋白酶组织抑制剂(TIMPs),由非特异性蛋白酶抑制剂,如。α2巨球蛋白。一旦活跃,基质金属蛋白酶可以调节全球蛋白水解的潜力通过发酵菌细胞外环境(MMP pro-form)激活和抑制退化或其他蛋白酶失活4,5]。
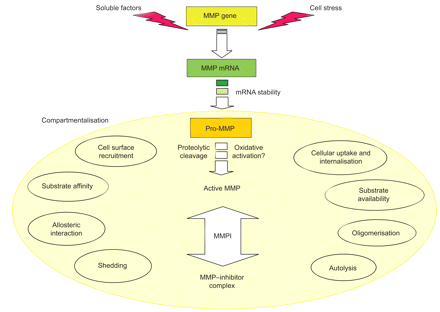
基质金属蛋白酶(MMP)活动严格监管四个不同层次:1)基因表达,主要是通过调节转录和mRNA稳定,2)上(如淡黄色填充eclipse),负责监管效率通过细胞表面蛋白质水解的招聘、衬底可用性和蛋白质相互作用,但也会影响3)pro-enzyme激活和抑制蛋白水解作用。
调制的MMP基因表达
尽管MMP基因表达主要是在转录水平调节,细胞因子mRNA转录后控制稳定,一氧化氮或微核糖核酸(microrna)最近被描述为一个重要的贡献机制。
尽管大多数的低表达基质金属蛋白酶在静止的条件下,他们的转录紧密和单独监管。没有单一的细胞因子,趋化因子,致癌基因或生长因子已被确认,专门负责基质金属蛋白酶在肿瘤的过度表达,尽管肿瘤坏死因子(TNF) -α和白介素1 (IL)往往牵连。的信号转导通路调节MMP的启动子活动也多种多样。几个MMP的推动者分享几个cis-elements在基因的启动子区域,与观测一致,一些基质金属蛋白酶被各种感应刺激粘住,生长因子和细胞因子等,也可以由糖皮质激素荷尔蒙和co-repressed类维生素a (6]。
显著,启动子功能相关的基质金属蛋白酶如MMP-2 / MMP-9(白明胶酶)或金属蛋白酶- 1 / MMP-8(胶原酶)显然是不同的,指向不同的激活方式。根据cis-element组成、MMP的启动子可分为三组(7]。第一组代表大多数MMP的推动者和包括一个TATA盒和一个AP-1-binding网站经常接近他们的转录启动和加上一个上游PEA3-binding网站,MMP的转录控制由几个细胞因子和生长因子,如表皮生长因子、角质细胞生长因子,血管内皮生长因子(VEGF)、血小板源生长因子,TNF-α,转化生长因子(TGF) -β[8]。在第二组MMP的推动者(MMP-8, -11年和-21年)也包含一个TATA盒,但缺乏一个近端AP-1网站。这些启动子的调控是相对简单的从第一组和不同的促进剂。最后一批的发起人(包括MMP-2, -14年和-28年)没有港口TATA盒,从这些启动子的转录和后面,开始在多个网站。此外,基质金属蛋白酶的表达在这后者主要取决于无处不在的sp 1的转录因子家族,绑定到一个近端GC盒。这些基质金属蛋白酶的表达主要部分是本构,只有适度的敏感性诱导生长因子或细胞因子(9]。
另外的转录控制基质金属蛋白酶是最有可能受到表观遗传机制(如DNA甲基化和组蛋白乙酰化和/或染色质重塑。DNA甲基化的胞核嘧啶在CpG岛在启动子区域通常是与压制性染色质状态和抑制相关基因的表达。因此,hypomethylation MMP的发起人可以导致癌症,增加酶的表达作为MMP-3观察MMP-9淋巴瘤细胞和结肠癌细胞(7)或其他炎症性疾病如关节炎,软骨细胞表达水平的提高MMP-3, MMP-9和MMP-1310]。染色质重塑是与可逆的乙酰化组蛋白(主要是H3和H4)通过染色质的组蛋白乙酰转移酶和树叶更放松的状态,通常与基因活化有关。表观遗传染色质重塑已经证明了IL-1β-induced金属蛋白酶- 1和MMP-13表达与组蛋白乙酰化状态的变化和增加绑定的AP-1蛋白质。相反,镇压的金属蛋白酶- 1和MMP-13表达核激素受体类维生素a X受体(RXR)包括脱乙酰作用在这个网站,也许伴随着减少AP-1绑定(11]。然而,进一步的研究是必要的理解底层控制MMP基因表达的表观遗传机制。
可以由胞质mRNA转录后基因调控稳定,介导通过trans-acting rna结合蛋白与多个AU-rich交互元素(是)主要位于3′未翻译区(utr)。mRNA的稳定性可以通过增加增强约束力胡蛋白质家族的因素(如。户珥)元素或可以减少增加绑定不稳定蛋白质的因素,像AUF1元素,促进mRNA招募外来体机械降解。的确,至少MMP-2的表达,MMP-9 MMP-13监管已被证明是通过信使rna的稳定性。为例,IL-1β-induced MMP-9鼠肾系膜细胞中基因表达被ATPγS增强通过绑定的增加户珥的战神3′utr MMP-9信使rna。相比之下,孵化与一氧化氮的系膜细胞诱导表达户珥的抑制反过来增加了MMP-9 mRNA衰变(7,12]。
此外,有证据表明,microrna有助于翻译后调节MMP的表达。短的microrna是一个丰富的类(21 - 25日核苷酸),非编码RNA干扰转录后基因表达,导致转化抑制或信使RNA降解。由于确认microrna的数量近年来发展迅速,许多基因的人类基因组可能以这种方式受到监管。生物信息学分析显示,几个MMP的和TIMP包含microrna的结合位点的基因3′-UTRs,包括MMP-2 (miR-29) MMP-14 (miR-24 miR-26和mir - 181), TIMP-2 (miR-30)和TIMP-3 (miR-21 miR-1/206, mir - 181) [12]。到目前为止,一些最近的研究已经证明,成绩单的基质金属蛋白酶或TIMPs确实是microrna的直接目标,像MMP-2抑制通过miR-29b MBP-1刺激前列腺癌细胞(13),MMP-13监管通过miR-27b人类骨关节炎软骨细胞(14),通过mir - 181 b TIMP-3抑制TGF-β-mediated hepatocarcinogenesis [15]。
MMP活动监管从上开始
调节MMP的蛋白质水解特异性开始已经在早期分泌。细胞外环境和基质金属蛋白酶的本地化pericellular空间通常对他们的活动有强烈影响pro-form激活和蛋白水解效率和特异性(5]。
分泌基质金属蛋白酶通常关联到细胞膜,pericellular集中他们的活动到特定的底物的空间。例子对细胞表面基质金属蛋白酶- 1的招聘具有约束力α2β1整合素,这取决于交互α2整合素与链接器+ haemopexin-like域的金属蛋白酶- 1 (16),MMP-9绑定CD44 (17),和绑定MMP-7 (matrilysin-1)胆固醇硫酸改变其衬底的偏好,促进退化pericellular层粘连蛋白- 332和纤连蛋白(18]。
整合蛋白等细胞表面受体,告诉自己什么蛋白在细胞外围已经遇到,因此,需要哪种类型的酶,它必须被释放。这种机制已经得到证实在活的有机体内金属蛋白酶- 1在人类皮肤的伤口,这种酶是诱导细胞在基底角质细胞的时候从基底膜分离和联系类型我底层真皮中的胶原蛋白(19]。此外,它已被证明,这种机制取决于整合蛋白之间的相互作用α2β1与I型胶原蛋白,也触发分泌的酶cell-matrix接触的点(20.]。
几种pro-MMP激活
基质金属蛋白酶是最初合成活性pro-forms(发酵菌),pro-domain已被激活。pro-domain港口守恒的“半胱氨酸开关”序列图案接近催化域的边界地带,其免费的半胱氨酸残基与酶催化锌离子保持交互延迟和防止绑定和乳沟的衬底21]。激活MMP的发酵菌取决于构象变化pro-domain拿出半胱氨酸残基,使水与锌离子在活性部位。这个事件可以由三个机制:1)切除pro-domain直接劈理的另一个endoproteinase;2)变构reconformation pro-domain;和3)化学改性的免费的半胱氨酸通过活性氧或nonphysiological代理。后者的事件,别构调节和自由半胱氨酸的减少也会使酶去除其pro-domain自溶(5]。
11日的24人基质金属蛋白酶,包括所有膜结合基质金属蛋白酶,被激活的细胞内过程特征通过pro-protein转化酶或furins守恒furin表示的裂解位点(R-x-R / K-R)的氨基酸序列在催化领域。Furin是transmembranous subtilisin-like丝氨酸蛋白酶反式高尔基体网络,负责分拣蛋白分泌途径最终目的地,包括细胞表面和分泌颗粒。作为结果,这些基质金属蛋白酶成员可以立即开始他们的催化作用出现在细胞表面或被分泌pericellular环境。
剩下的MMP的表达和分泌活性pro-forms成员,需要激活。在体外,可以激活孵化基质金属蛋白酶与单个成员的丝氨酸蛋白酶,如血纤维蛋白溶酶和chymase或其他基质金属蛋白酶,如MMP-3和MMP-14。然而,在活的有机体内pro-MMPs相关激活机制尚不清楚,因为分析突变小鼠并没有发现任何变化pro-MMP激活的淘汰赛MMP-3 [22),没有或小pro-MMP-2激活减弱MMP-14淘汰赛(23),不改变激活pro-MMP-2和pro-MMP-9纤溶酶原基因敲除(物24,部分减少激活pro-MMP-2和pro-MMP-9 chymase淘汰赛(25]。因此,发酵菌激活可能是引发的替代机制与多个参与者。
Pro-MMP激活被认为是一个逐步的过程,发生在眼前的pericellular空间。第一步包括pro-peptide内的初始构象改变,从而导致中断的半胱氨酸switch-zinc交互。随后,pro-domain被内部或分子间的处理部分激活MMP的中间体或其他活性基质金属蛋白酶(21]。有据可查的例子为激活更多的参与者已被证明pro-MMP-2激活的合作行动TIMP-2和MMP-14内建立一个细胞表面活化络合物比化学计量比(26]。
另一种发酵菌激活机制可能是由内在的变构效应MMP的分子。因此,域模域组织MMP的灵活性可以贡献通过促进远程构象转变引起的蛋白质绑定通过exosites [27]。这种交互的证据已被证明的孵化pro-MMP-9β-hematin,疟色素的核心成分或疟色素,这导致催化裂解的pro-domain最有可能通过别构与haemopexin域(28]。pro-MMP-7的另一个例子是pericellular激活tetraspanin CD151,在骨关节炎软骨细胞中过表达,最有可能导致软骨破坏增加过度MMP-7激活(29日]。
在体外,孵化的重组pro-MMPs thiol-modifying化学药剂,如汞化合物、SDS、氧化谷胱甘肽和活性氧(ROS),导致几个基质金属蛋白酶的激活。在人类中,活性氧是由专门的酶免疫细胞吞噬,如中性粒细胞和巨噬细胞。MMP激活通过活性氧是优惠thiol-zinc交互和催化裂解的氧化,紧随其后的是酶失活与延长曝光修饰的氨基酸催化活性的关键,如图所示在体外MMP-7 [30.]。因此,通过吞噬细胞ROS生产可能调节基质金属蛋白酶的激活和失活在炎症情况下,如图所示在活的有机体内的巨噬细胞抑制MMP-12活动期间组织损伤(31日]。然而,它还没有证实活性氧可以作为MMP的催化剂/钝化剂在活的有机体内。
基质金属蛋白酶的抑制:找到合适的平衡
它是一个建立视图之间的平衡活动及其抑制酶的生产是至关重要的,以避免不受控制的ECM营业额的条件,炎症、细胞生长和迁移特异表达,会导致疾病。两个主要的体液和组织中基质金属蛋白酶抑制剂α2巨球蛋白和TIMPs分别。
人类α2巨球蛋白是一种广谱蛋白酶抑制剂的组织体液和血液。这homotetrameric高分子725 kDa抑制几乎所有类诱骗整个肽链内切酶的酶,虽然这些复合物迅速通过低密度脂蛋白受体相关蛋白1介导的内吞作用[32]。
人类MMP活性的天然抑制剂四TIMPs的成员。每个TIMP分子由约190个氨基酸组成的两个截然不同的领域,一个更大的氨基端和一个更小的c端域,每一个稳定三个守恒的二硫键。n端结构域单独独立可以折叠,全功能抑制基质金属蛋白酶通过螯合锌原子催化1:1摩尔比。c端域的功能并不完全理解,但它已被证明能紧密结合的haemopexin领域潜在的基质金属蛋白酶。TIMP-2被描述,或者TIMP-3 TIMP-4可以与pro-MMP-2, TIMP-1或TIMP-3 pro-MMP-9 [33]。然而,除了与pro-MMP-2 TIMP-2之间的相互作用,这是pro-MMP-2的激活机制的一部分,这些复合物的生物相关性是未知的。
TIMPs一般都是广谱基质金属蛋白酶抑制剂,但有特异性的差异。例如TIMP-1已被证明对MMP-19抑制活性较低和膜结合MMP-14, -16年和-24年,而它更强有力的MMP-3和比TIMP-2 MMP-7 TIMP-3 [33]。TIMP-2抑制基质金属蛋白酶的活性,其表现为本构,相比其他TIMP成员诱导。
TIMP-3有能力抑制MMP的所有成员(如TIMP-2),但其抑制形象进一步延伸到disintegrin成员和金属蛋白酶(亚当斯)。动力学研究表明,TIMP-3更好的TNF-α转换酶抑制剂(TACE或ADAM17)和aggrecanases ADAMTS-4比基质金属蛋白酶和5。此外,TIMP-3 TIMP的家庭中是独一无二的,因为它将紧密地绑定到ECM的N -和c端领域促进MMP的抑制(34),与其他TIMPs可溶性分子自由。TIMP-3似乎是一个更相关在活的有机体内比TIMP-2和1抑制剂,因为亏损TIMP-3老鼠与肺肺泡扩张和增强细胞凋亡在乳腺导管上皮细胞(35),而淘汰赛TIMP-1或TIMP-2老鼠不显示任何挑战异常。TIMP-4,最近发现家庭成员显示最高TIMP-2相似,能够抑制基质金属蛋白酶的大部分。
其他几个分子已被证明抑制单个或一些基质金属蛋白酶,如胶原蛋白酶C C端片段的增强剂,它可以抑制MMP-2 [36]或glycosylphosphatidylinositol (GPI)固定血管生成抑制糖蛋白顾虑,块MMP-2的活动、9和-1437]。
此外,如前所述,高浓度的活性氧来源于吞噬免疫细胞在炎症场景可用阻断剂被认为是非常有效的和快速的大规模增加MMP的活动(5]。
模块化域组织基质金属蛋白酶
酶的基质金属蛋白酶构成一个高度多样化的家庭,都有个共同的属性和域结构。根据他们的域结构和衬底的偏好,他们传统上分为:1)胶原酶,包括金属蛋白酶- 1 / -8/-13;2)stromelysins MMP-3, -10;3)明胶酶,MMP-2和9;4)matrilysins MMP-7, -26;5)膜式基质金属蛋白酶(MT-MMPs);和6)其他人。最近执行系统分组,包括整个基因组的海鞘类Ciona intestinalis作为最亲密的相对的脊椎动物和无脊椎动物斑马鱼鲐鱼类提供新的见解,在脊椎动物进化的早期阶段金属蛋白酶和建议六个进化子组(38]。
所有基质金属蛋白酶合成是不活跃的pro-enzymes,除了膜结合MT-MMPs,分泌到细胞外的环境中。所示图2,所有基质金属蛋白酶分享至少三个守恒的域结构,包括一个氨基端信号肽,它是裂解在运输通过分泌途径,其次是pro-domain约80氨基酸和催化领域。这两个matrilysins MMP-7和-26只由这三个域,从而代表minimal-domain家庭成员。pro-domain拥有一个“半胱氨酸开关”PRCGxPD共识序列。这个保守的半胱氨酸残基与锌离子催化域原本被用于催化。催化域(约160 - 170个氨基酸)有高度的相似性所有基质金属蛋白酶和包括一个守恒HExxHxxGxxH催化锌约束力的主题。
域结构的基质金属蛋白酶(MMP)组。人类所有的基质金属蛋白酶分享至少信号肽,pro-domain和催化领域。pro-domain包含复合物催化锌的半胱氨酸开关序列2 +发酵菌的形式。催化域港口守恒的催化序列。明胶酶MMP-2和MMP-9独特包含三个纤连蛋白重复在催化领域。一些基质金属蛋白酶furin识别网站在催化领域之前,它允许通过furin胞内酶原的激活。除了MMP-7和-26年,所有基质金属蛋白酶有灵活的脯氨酸铰链区和haemopexin-like c端域,在底物识别功能。膜结合MMP-14, -15、-16和-24年包含另外一个跨膜和胞质域,而MMP-17和-25在质膜集成glycosylphosphatidylinositol (GPI)锚。搞笑:免疫球蛋白。
明胶酶MMP-2和9港口三个独特的整合纤连蛋白II型催化域的模块。这些作为一个紧凑的collagen-binding域高亲和力的α1-chain胶原蛋白我和诱发大量胶原蛋白三螺旋的解除。相反,胶原酶的底物识别和特异性金属蛋白酶- 1、8、-13和MT-1 MMP提供的c端haemopexin域。然而,haemopexin域的约束力并不引起构象改变纤维胶原蛋白分子,但会导致特定的裂解位点的识别α链的生成氨基端四分之三的c端四分之一片段,迅速变性胶在体温。除了底物识别,haemopexin域也被证明与TIMPs互动是很重要的。灵活的链接器区域局部的催化和haemopexin域和可以参与酶裂解过程定位底物的催化域(39]。
一旦分泌,可以激活pro-MMPs pro-peptide的乳沟。超过三分之一的所有发现人类可以激活基质金属蛋白酶pro-protein转化酶或furins。这些基质金属蛋白酶包含furin共识序列之间的赞成和催化域(图2),这是在他们分开反式高尔基体通道。与分泌蛋白酶,四膜式基质金属蛋白酶(MMP-14、-15、-16和-24年)被插入到质膜通过跨膜域和基质金属蛋白酶的-17年和-25年是插在质膜GPI锚。跨膜型基质金属蛋白酶(MMP-14、-15、-16和-24年)包含一个额外的胞质域。因为大部分的注意力都集中在了MT-MMPs酶学性质的,这个领域的功能没有被详细调查;然而,它似乎发挥重要作用的过程中MT-MMPs clathrin-dependent掩饰,可能与网格蛋白的笼子里(40]。
MMP的基质
基质金属蛋白酶是多功能蛋白酶
基质金属蛋白酶已经改建和ECM的降解相关的传统,但出现了新的基质类和基质金属蛋白酶现在视为多功能蛋白酶。MMP的基质和乳沟网站的全面列表可以在网上找到资源,比如MEROPS [41]。在这里,我们将介绍主要的衬底类和提供选择的例子。
ECM和动态成分十分复杂。集体,基质金属蛋白酶能够粘住每一个ECM组件(42]。然而,不同的ECM组件容易被不同的基质金属蛋白酶和蛋白质水解并不是所有ECM组件由每个MMP的裂解。纤维胶原蛋白如胶原蛋白I, II和III是主要由胶原酶裂解(金属蛋白酶- 1,MMP-8 MMP-13) MMP-2和MT1-MMP2,43]。蛋白质水解发生在一个特定的网站从n端四分之三。乳沟碎片迅速变性和形成凝胶,可以通过许多其他蛋白酶降解,如明胶酶MMP-2 MMP-9。基底膜组件胶原IV容易蛋白质水解明胶酶,stromelysins, matrilysins和其他基质金属蛋白酶,如巨噬细胞metalloelastase [44),而hemidesmosomal胶原十七是由明胶酶降解[45]。ECM组件如层粘连蛋白、纤连蛋白、弹性蛋白或aggrecan最能被裂解,如果不是全部,基质金属蛋白酶。细胞粘附分子也MMP的基板,包括钙粘蛋白乳沟matrilysin和stromelysin-1 MT-1 MMP CD44和pro-α调解处理v整合素(46]。
MMP ECM组件可以产生生物活性片段的处理。例如,MMP-2和MMP-9公开神秘的抗原决定基内胶原IV,促进血管生成而抗血管生成因子如血管内皮抑制素胶原蛋白可以形成于十八。生物活性乳沟产品也从ECM蛋白质,如perlecan、层粘连蛋白、纤连蛋白(47]。
除了“塑造”生物活性乳沟产品,ECM降解释放非共价结合生长因子和细胞因子,从而提高其生物利用度。例子包括VEGF和TGF-β的释放。VEGF与非共价结合与释放硫酸乙酰肝素蛋白聚糖在ECM蛋白水解作用[2,48]。TGF-β维护处于潜伏状态通过绑定到latency-associated肽(圈)。圈依次是蛋白质共价绑定到fibrillin潜伏TGF-β结合蛋白(LTBP)。ECM降解释放潜在的复合物和离解TGF-β-LAP复合物增加TGF-β可用性。此外,圈是MMP-2的衬底,9日,-13年和-14年,可以裂解LTBP MMP-7 (42]。同样,基质金属蛋白酶有助于细胞因子和生长因子生物利用度的蛋白质水解可溶性蛋白质绑定,如胰岛素样生长因子结合蛋白(49,50)和pleiotrophin VEGF掩蔽蛋白(51]。
基质金属蛋白酶参与劈理域释放细胞表面和membrane-spanning蛋白质。流是由膜式基质金属蛋白酶,基质金属蛋白酶,注定要膜受体(如分组人口MMP-2 MMP-9) (43)和可溶性基质金属蛋白酶。脱落的重要功能包括释放生物活性蛋白质域和受体处理,因此改变细胞生长因子和细胞因子的响应能力。MT1-MMP“sheddome”一直在异形细胞蛋白质组学(52,53]。验证实验证实MT1-MMP脱落的蛋白质如纤连蛋白、死亡receptor-6, cysteine-rich运动神经元1蛋白质。进一步MT1-MMP脱落事件包括syndecan的乳沟,CD44, semaphorin 4 d和betaglycan [46]。
蛋白质基质分析MMP-2透露脱落的基板(49,51]fractalkine趋化因子等领域。对可溶性MMP-7脱落基质包括膜结合Fas配体(54]。有些膜蛋白容易乳沟了基质金属蛋白酶,如脱落尿激酶纤溶酶原激活物受体MMP-3, -12年、-19年和-25年(46]。
基质金属蛋白酶是突出重要的生长因子和细胞因子的特有的乳沟。通过处理这些信号分子,基质金属蛋白酶干扰细胞通讯。例如,MMP-2转换单核细胞化学引诱物蛋白(MCP) 3成receptor-blocking拮抗剂切除四氨基残基55]。同样的,各种MCP-type趋化因子容易MMP的处理(56]。重要的是,通过基质金属蛋白酶是选择性趋化因子处理:基质金属蛋白酶在处理不同的趋化因子和趋化因子在乳沟易感性不同56,57]。在某些情况下,趋化因子乳沟网站不同MMP-specific地(57]。signalling-related MMP的乳沟事件的列表不断生长和细胞因子处理已被认为是关键的MMP的函数在活的有机体内(46]。进一步的例子包括处理基质细胞衍生因子1,引发,IL-1β、结缔组织生长因子和肿瘤坏死因子(46]。
蛋白酶和蛋白酶抑制剂的重要类MMP的基质。通过发酵菌激活和抑制退化,基质金属蛋白酶加强全球蛋白水解的潜在细胞外环境。与此同时,基质金属蛋白酶proteolytically灭活其他蛋白酶。功能性相声不同蛋白酶之间已经建立了作为一个关键管理组件的微调细胞蛋白水解作用[46]。这是说明了MMP-2 MT1-MMP介导激活(26]。MMP-2反过来被发现分裂半胱氨酸蛋白酶抑制物C和分泌白细胞蛋白酶抑制剂以及各种组织蛋白酶蛋白酶和骨形态形成蛋白1 (49- - - - - -51]。
总之,基质金属蛋白酶是多功能蛋白酶:1)proteolyse ECM组件与后续释放生物活性和蛋白质片段;2)参与膜脱落;3)趋化因子处理中发挥着重要的作用;和4)改变其他蛋白酶的活性状态。新颖的蛋白质组学技术现在开始提供全面刻画MMP衬底degradomes(见下文)。由于蛋白酶底物的知识是理解的关键蛋白酶生物,这种发展是至关重要的,以便更好地理解MMP的参与(patho)生理学。MMP的基质的全面分类根据其生理意义是由罗德里格斯(patho)et al。(46],包括乳沟事件涉及骨骼和ECM重塑、血管生成、细胞迁移、细胞浸润和转移,细胞增殖,肿瘤生长,细胞凋亡和炎症,以及先天免疫和伤口愈合。
基质金属蛋白酶在底物特异性的细微差别
蛋白酶特异性根本上是由es互动引导在一个细长的活性部位间隙。Schechter和伯杰术语指定底物结合口袋的氨基端易裂开的肽键S1、S2、S3,等。和相应的底物残留,P1, P2, P3,等。绑定的口袋和底物残留c端易裂开的肽键命名S1′, S2′, S3′,等。P2′, P1′分别P3′。很少有无偏分析的主要方法和非优质特异性58]。大多数MMP的特异性信息源于肽库的方法(59- - - - - -61年]proteome-derived肽库有了> 1200 peptidic乳沟MMP-2序列。
基质金属蛋白酶共享一个通用特异性概要文件只有细微的差别。MMP的特异性因素从P3-P3′和由子站的偏好,而不是严格的裂解位点图案。混合特异性观察到在某些子站。MMP的特异性主要是由偏爱脂肪族氨基酸,特别是亮氨酸,P1′。基质金属蛋白酶2、3、9和-14年还显示一个P1′偏爱芳香残留物和被认为有一个更深的S1′口袋(61年,62年]。偏爱脯氨酸在P3构成二级MMP的特异性行列式。然而,基质金属蛋白酶也喜欢中型脂肪残留物(P3(缬氨酸、异亮氨酸)60,61年]。进一步子偏好包括轻微的偏爱小丙氨酸等残留物,在P2 MMP-2时基质金属蛋白酶1、3、7、9和-14年据报道喜欢脂肪族和芳香族残留在P2。在P1,基质金属蛋白酶喜欢小残留如丙氨酸、甘氨酸和丝氨酸。在P2′,基质金属蛋白酶混合偏好基本和大脂肪残留物。在P3′,基质金属蛋白酶1、2和9喜欢小残留。
这些基于寡肽底物特异性概要文件和不一定转化为生理基质。折叠的蛋白质是最有潜力的乳沟网站结构的屏蔽和选择在活的有机体内基板的基板包括识别exosites外活性部位间隙(更多关于exosites下文)。因此,预测蛋白质基质完全基于序列相似性MMP特异性概要文件可以误导60]。然而,MMP基于蛋白质底物特异性概要文件共享功能的肽链型特异性概要文件,因此验证MMP的特异性测定(50]。
Exosite识别蛋白质基质
虽然基质金属蛋白酶分享全球活性位点特异性概要,蛋白质基质体验有显著区别。例如,无偏的蛋白质组学测定MMP-2和9衬底degradomes显示有限的重叠63年]。这一观点强调了底物识别的重要性之外的活性部位间隙通过蛋白质和域称为exosites领域。许多基质金属蛋白酶多畴的蛋白质和整个领域exosites MMP的很重要因素在活的有机体内蛋白质水解。Exosite交互调解乳沟的原生胶原纤维。Collagenolysis是一个三步过程涉及胶原蛋白绑定,解除和乳沟。胶原酶1 - 3和MT1-MMP haemopexin域结合原生胶原蛋白(53,64年]。然而,这不是MMP-2。这里,三纤连蛋白II型重复的催化域形成另一种胶原蛋白结合域(64年]。胶原蛋白还参与胶原解除绑定域。除了促进collagenolysis,胶原蛋白绑定将基质金属蛋白酶ECM,从而影响基质金属蛋白酶的空间分布。这是一个对MMP的间接贡献在活的有机体内衬底体验(64年]。的MMP-2 haemopexin参与进一步的识别,non-collageneous基质如某些趋化因子(55]。事实上,使用MMP-2 haemopexin域作为诱饵分子识别潜在的扶少团团员在酵母两个屏幕混合导致了开创性的趋化因子的识别MCP-3作为MMP-2衬底(55]。
系统范围的MMP的底物的识别
蛋白酶底物测定一直是一个串行的过程中,个别蛋白质为解理敏感性测试。而迷人的见解蛋白酶生物是基于这种方法,它缺乏吞吐量完全理解在活的有机体内蛋白质水解。蛋白质组学策略现在已经出现了能够描述cell-contextual蛋白水解作用在全系统范围内。一般来说,这些方法在两类:全球定量蛋白质组学和蛋白酶乳沟的直接识别网站。全球定量蛋白质组学决定改变蛋白质丰度与不同的蛋白水解活性生物系统。在细胞或动物性的系统中,这通常包括过度,消耗或抑制蛋白酶进行调查和比较本地,未经处理的控制样本。分泌蛋白酶,基质金属蛋白酶在很多方面可以改变蛋白质的丰度。降解减少蛋白质丰度。脱落增加细胞表面蛋白质丰富但减少ectodomain浓度在细胞微环境。最后,有限的处理,如删除一些终端氨基酸,可能不会反映的量变,因此仍然忽视全球定量蛋白质组学。串联质谱分析的方法建立了选择蛋白质识别这些方法由于其出色的分析能力,敏感性和吞吐量。 Proteome separation and relative quantification has been historically realised with two-dimensional gel electrophoresis. These are now increasingly replaced by liquid chromatography–tandem mass spectrometry (LC–MS/MS)-based shotgun proteomics with greatly increased proteome coverage. Here, relative quantification is typically achieved by stable isotope labelling, although label-free quantification is increasingly gaining attention [58]。MMP-2基质如半胱氨酸蛋白酶抑制物C和fractalkine已确定在cell-conditioned媒介质/ MS-based蛋白质组学屏幕采用商用ICAT或iTRAQ标签(49,51]。巴特勒和整体(65年]目前proteomically发现MMP的基质的概述。
全球定量蛋白质组学无法识别蛋白酶乳沟网站和不能描述微妙的蛋白质组变化引起的蛋白水解作用有限。完全在系统层面上描述蛋白质水解,蛋白质组学策略已经发明,选择性地分析蛋白质N -或c终端(58,66年]。结合定量的比较系统缺乏或overexpressing蛋白酶在调查中,衬底候选人可以被识别和区别背景蛋白水解作用(图3)。“终端”蛋白质组学策略要么依赖于内部的积极选择的蛋白质末端或损耗肽(消极的选择),与消极的选择策略也确定修改(如。cyclised或乙酰化)N-termini [50,67年]。终端胺基质的同位素标签(反面)是一种新型的集成平台系统识别蛋白酶底物的定量N-terminome分析(50]。尾巴依赖于高效的聚合物-选择策略。迄今为止,MMP cell-contextual乳沟事件已经专门分析用尾巴和众多小说基质和乳沟网站已经显示(50,63年,67年]。等MMP-2包括蛋白质基质的细胞外基质蛋白1,实验,巨噬细胞迁移抑制因子。如前所述,基质金属蛋白酶具有广泛的活性位点特异性。蛋白酶相比还存在诸如,MMP的乳沟网站主题无法认可的共识。已经建立了一个统计数据平台仔细辨别MMP-2乳沟网站从反面背景蛋白质水解实验(67年]。Proteome-wide识别蛋白质c终端最近才建立的66年]。
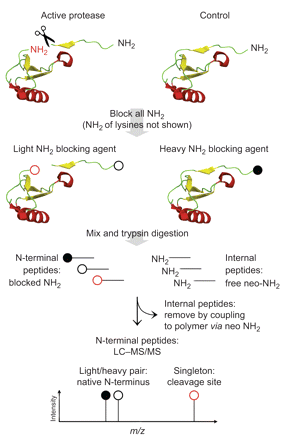
的识别在活的有机体内乳沟网站终端胺同位素标签的基质。这种基质degradomic策略侧重于蛋白质N-termini和比较控制样本与protease-treated样本为了区分从背景蛋白水解作用和诱导乳沟事件本机蛋白质末端。收获和初级胺样品,包括蛋白质N-termini和赖氨酸侧链化学保护,如。通过还原甲基化。介绍了稳定同位素在这一步中,允许相对量子化的液体chromatography-tandem质谱(质/ MS)分析。样品然后混合,胰蛋白酶消化。内部和c端肽具有自由neo N-termini而氨基肽化学N-termini保护。内部和c端肽是耦合的高分子量聚合物通过他们的自由NH2组。氨基肽仍非耦合,由超滤分离polymer-peptide共轭。在以下质/ MS分析,N-termini出现独立的蛋白酶活性在调查中发生轻/重同位素对。N-termini从乳沟网站基于蛋白酶活性在调查中发生的单件同位素形式用于标签“积极蛋白酶”样品状态。米/z:质量/电荷比率。
Proteome-wide衬底和裂解位点识别将打开新航线我们对蛋白酶的理解生物学综合映射蛋白酶底物以公正的方式。然而,候选人基质需要进一步验证,特别是对于基质金属蛋白酶。因为这些多功能蛋白酶,改变MMP的活动可能导致各种各样的继发效应。衬底的候选人通常验证了在体外乳沟化验和检测时间和空间colocalisation蛋白酶与底物在细胞或动物模型系统/产品(55]。同时,越来越多的degradomic分析多种蛋白酶和模型系统很快就会为一个强大的荟萃分析奠定基础,歧视下游效应和区分protease-specific基质配置文件。
基质金属蛋白酶的生理功能
学习MMP基因敲除小鼠
分析基因敲除突变体提供了机会识别基本MMP的功能和到目前为止16 MMP基因敲除突变体进行了分析。然而,单一的分析MMP零突变体显示惊人的良性表型与所有MMP-knockout小鼠存活至少前三个产后周(表1冗余),表明蛋白水解、酶的补偿和自适应发展。因此,大多数基因敲除模型描述的到目前为止只显示明显的缺陷在调节组织应对环境挑战,如受伤、感染和炎症。
相比其他MMP基因敲除小鼠,MMP-20基因敲除小鼠有显著的表型,即使没有一个环境的挑战。MMP-20是表示通过中间阶段的早期牙釉质发展组织,零老鼠确实显示严重和深远的牙齿表型,在他们无法处理正常amelogenin开发一个改变搪瓷矩阵和杆模式(92年]。
MMP-19缺陷小鼠,相反,是一个代表性的例子MMP-driven提供应对环境挑战。尽管他们区别野生型小鼠建立食源性肥胖由于脂肪细胞肥大和展览减少对化学致癌物引起的皮肤肿瘤(91年]。
由于基质金属蛋白酶共享许多基质在体外最有可能是遗传冗余也存在在活的有机体内。这一事实MMP的双基因敲除突变体显示严重的表型支持了这一观点。冗余的一个突出的例子是由MMP-2/MT1-MMP双零小鼠出生后立即死亡由于呼吸衰竭和发育异常血管缺陷导致血管形成和不成熟的肌肉纤维(96年]。这些缺陷导致添加剂病理学相比单淘汰赛,因此提供一个证明遗传发育冗余。
类似的现象被观察到MMP-2/MMP-9双零老鼠不表现出明显的表型。然而,使用激光损伤,兰伯特et al。(97年)展示了一个放大血管相比,单一零缺陷突变体。这个观察独立消息来源的证实了肿瘤入侵和vascularisation研究[95年]。
基质金属蛋白酶引发骨骼生长和建模
导致人或老鼠骨骼的形成取决于两个主要骨化过程需要大量的矩阵改造。虽然endochondrial骨化最需要身体的骨头,膜内的骨化等平的骨头是至关重要的头骨和下颚。到目前为止,5个基因敲除模型描述显示骨骼生长表型,即:MMP-2, MMP-9, MMP-13, MT1-MMP MT3-MMP。即使所有5个基因敲除模型显示骨表型的机制影响骨骼发育显著不同是因为他们在小鼠骨骼细胞特定类型表达式(35]。
老鼠缺乏白明胶酶(MMP-2显示生长延迟和颅骨畸形,由于膜内的骨化缺陷(70年),与其他MMP基因敲除小鼠,发达endochondrial骨化的缺陷。
白明胶酶B (MMP-9)空突变体的特点是延迟长骨增长和发展由于受损的血管侵犯骨骼生长板。在野生型小鼠,MMP-9血管生成信号的生成一个梯度最有可能通过从ECM的释放,从而指导新成立的船只chemokine-dependent机制。虽然这种表型标记在他们的成长阶段,成年老鼠只显示大约10%的缩短长骨头,再次表明其他基质金属蛋白酶可能补偿。
如前所述,两种蛋白酶的表达MMP-9 MMP-13由RUNX-2,建议类似骨表型MMP-13基因敲除小鼠。事实上,MMP-13在老鼠的失活导致异常的骨骼生长板软骨细胞的发展和推迟退出生长板(86年]。因此,删除MMP-9和MMP-13导致严重受损的软骨内骨形成,减少ECM重塑,软骨细胞存活时间延长,延迟血管招聘和有缺陷的骨小梁形成,从而导致大幅缩短骨(86年]。
在所有单MMP基因敲除模型中,只有MT1-MMP空的老鼠表现出严重的自发的表型。这些老鼠表现出骨骼缺陷包括颅面先天性畸形、关节炎、骨量减少,侏儒症,由于烧蚀和软组织纤维化溶胶原的活动对建模至关重要的骨骼和extraskeletal结缔组织。这些发现揭示MT1-MMP在结缔组织代谢的一个重要功能的发展。此外,它说明造型软结缔组织基质的维护是至关重要的骨架的硬组织(87年]。
的分析MT3-MMP(MMP-16)缺乏小鼠揭示小说ECM重塑的机制的先决条件适当的间充质细胞的功能。在缺乏MT3-MMP,老鼠显示增长抑制由于间充质细胞在骨骼组织的生存能力下降。间充质细胞增殖和迁移的抑制是由于缺乏乳沟的高密度纤维胶原蛋白(89年]。的生理意义MT3-MMP (MMP-16)进一步验证双MT1-MMP和MT3-MMP不足的老鼠。双缺乏超越了个别单一的缺陷,导致严重的胚胎palatogenesis缺陷和骨形成,这与生活是不相容的。这些缺陷所需的必不可少的溶胶原的活动直接与损失在collagen-rich ECM重塑和间叶组织在胚胎发生细胞增殖(89年]。
基质金属蛋白酶在血管生成和血管的发展
除了前面提到的血管生成的表型MMP-9空鼠长骨生长期间,MMP-2和MT1-MMP在血管生成基因敲除小鼠也显示修改,特别是在病理条件下,如。tumour-induced血管生成发芽(68年,88年]。这个观察意味着缺乏单一基质金属蛋白酶基本上不干扰胚胎血管网络的形成。然而,没有两个基质金属蛋白酶MMP-2 / MT1-MMP双基因敲除小鼠导致严重发育血管缺陷并导致产后死亡。
MT1-MMP的机制导致的发芽neovessels只是通过降解I型胶原蛋白。因此MT1-MMP零突变体不能入侵胶原蛋白类型我富裕产后矩阵(98年]。相比之下,胚胎ECM只有胶原蛋白I型含量低,这或许可以解释这一事实没有看到血管系统的缺陷。除了它的角色在胶原蛋白降解,MT1-MMP还参与pro-MMP-2激活的过程(26]。活跃MMP-2本身可以调节萌芽新形成的血管的细胞因子和生长因子的释放。
除了它的结构功能ECM作为“海绵”,结合细胞因子和生长因子。这些因素的控制乳沟不同的基质金属蛋白酶可以从而调节细胞信号在细胞内事件。ECM-tethered VEGF的情况就是这样,这是不活跃的在复杂与结缔组织生长因子(CTGF),但变得活跃MT1-MMP CTGF蛋白水解分裂后,金属蛋白酶- 1,3 - -1399年]。此外,特定的绑定模式VEGF ECM组件创建一个“地毯”指导入侵的内皮细胞,从而支持neo-angiogenesis的过程。然而,VEGF的乳沟MMP-3和9生成一个短,non-heparin绑定活动形式的VEGF,随后引起不规则的船。
进一步例子为积极分子的释放蛋白酶的催化释放胰岛素样生长因子通过MMP-19或释放TNF-α明胶酶(99年]。还重要的是,基质金属蛋白酶不仅促进血管生成,产生抗血管生成肽:MMP-3, 7日,9日,-13年和-20年,例如,已被证明产生的抗血管生成血管内皮抑制素处理十八型胶原蛋白(47]。这个观察符合基因敲除小鼠的表型观察,因为他们在vascularisation显示缺陷。
基质金属蛋白酶的主要功能的免疫反应和先天免疫
在肺气道上皮细胞只有MMP-7表达。在老鼠中,受伤的气管完全压制的re-epithelialisation MMP-7缺失的情况下,展示MMP-7在正常伤口修复的要求。此外,MMP-7突变小鼠则不愿肠道细菌感染,部分因为他们无法释放的内源性抗菌肽α-defensin肠道上皮细胞,表明MMP-7在先天免疫中的作用[75年]。
在最近的一项研究中,陈et al。(One hundred.]表明肺部MMP-7 chemotatic招募中性粒细胞是至关重要的。随着syndecan-1能储备大量的细胞因子,其proteolytical释放MMP-7形成化学引诱物梯度中性粒细胞指导受损的肺上皮细胞所必需的。相比之下,中性粒细胞迁移是废除MMP-7零突变体。
在协议与基质金属蛋白酶的表达模式,2和9在先天免疫细胞,如单核细胞、激活巨噬细胞,肺泡巨噬细胞和中性粒细胞,这些酶与病态与先天免疫失调有关,正如我们最近显示巨噬细胞衍生MMP-2和MMP-9 monocyte-driven肾脏自身免疫性炎症模型(101年]。MMP-2和9参与免疫细胞招聘通过提供一种趋化因子梯度的CC - (如。CCL7)和CXC-motif (如。CXCL12, CXCL6 CXCL8)配体64年,102年),从而支持和抗炎作用。的截断macrophage-derived CCL7明胶酶,例如,结果形成的肽,作为受体拮抗剂(55),而MMP-9介导乳沟激活处于受控和4 (CXCL6 CXCL8和灭活102年]。这些观测结果符合MMP-9缺陷小鼠的抗自身免疫性疾病大疱类天疱疮(表1),这是由于中性粒细胞减少招聘97年]。
基质金属蛋白酶在伤口愈合有重要作用和细胞迁移
在活的有机体内以及在体外数据已经证明了许多分泌和膜结合基质金属蛋白酶的重要性都直接或间接地有助于伤口愈合和neovascularisation的过程。伤害大多数,如果不是全部,基质金属蛋白酶诱导,并表示在几乎所有的细胞类型,包括间叶细胞、上皮细胞和免疫细胞。因此定义的时间和空间模式MMP的表达已经成为研究的主要目标伤口愈合和细胞迁移(图4)。
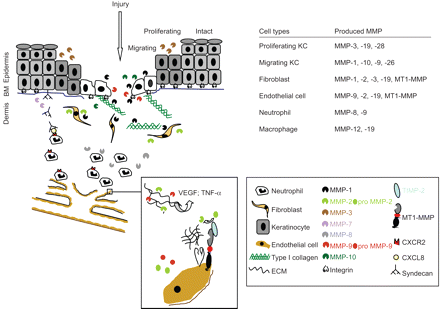
不同功能的基质金属蛋白酶(MMPs)有助于伤口愈合和血管生成。在健康的皮肤,基底基质金属蛋白酶的表达很低,但受伤后,许多分泌和膜结合基质金属蛋白酶的相互作用直接或间接有助于伤口愈合。例如,金属蛋白酶- 1强烈影响角化细胞迁移在伤口边缘,而MMP-7调节中性粒细胞招募(见右下网站)上的传奇。伤口诱导neoangiogenesis,内皮细胞的迁移和增殖的结果,是由血管内皮生长因子(VEGF)和肿瘤坏死因子(TNF)通过明胶酶MMP-2 -α释放和9(见框炸毁的迁移内皮细胞(EC))。BM:基底膜;KC:角化细胞;TIMP:基质金属蛋白酶组织抑制剂;ECM:细胞外基质。
金属蛋白酶- 1表达的诱导角质细胞在伤口边缘,例如,是由绑定α2β1整合素真皮胶原蛋白类型。这种高亲和力附件会使皮肤角质细胞,使它们无法迁移。活跃的金属蛋白酶- 1的增加会导致随后的真皮胶原蛋白I型胶原降解,我退化的亲和力降低integrin-collagen绑定,从而允许角化细胞迁移,减少金属蛋白酶- 1的表达(20.]。这种监管机制表明,细胞不需要MMP的活动只是为了消除矩阵壁垒。
另一个最近发现MMP的活动在伤口愈合中的作用是免疫细胞自嗜中性粒细胞的招聘招聘需要的存在和活动MMP-7(参见:主要功能的基质金属蛋白酶免疫反应和先天免疫)和MMP-876年]。
neoangiogenesis伤口愈合的重要过程,包括内皮细胞的迁移和增殖,刺激纤维蛋白、纤连蛋白来自伤口肉芽组织。基质金属蛋白酶诱导释放ECM绑定pro-angiogenic因素,包括释放VEGF和TNF-αMMP-2和9 (图4];与内皮细胞增大盒)。Pro-MMP-2由特征明显激活MT1-MMP / TIMP-2复杂表示激活内皮细胞表面。MT1-MMP的co-localisationανβ3整合素在内皮细胞的细胞间连接显示额外的监管作用,细胞迁移和附着力。
见一个简化的卡通MMP的功能和相互作用的图4披露单一MMP的),基板不能充分解释在活的有机体内MMP的函数,没有复杂的相互作用的知识。必须投入更多的工作为了揭示复杂的MMP交互上下文依赖的方式,来促进我们对基质金属蛋白酶的作用的理解组织内稳态的调节。
MMP的表达的组织特异性
本构生理MMP的表达通常是低,即使是暂时性的更高的利率由于体内平衡矩阵改造或者特定的发育事件有关。然而,强烈的结构相似性在MMP的发起人(7)提出的问题是否和如何不同的基质金属蛋白酶在特定的细胞或组织差异表达。
到目前为止,MMP-7 8 -13年、-20年和-28年被发现被表达在不同的组织或细胞类型。它们中的大多数都是表示由于不同细胞类型表达的转录因子。原型为真实的组织特定的表达式由MMP-20表示,这已被证明是局限于牙齿组织,最有可能由tooth-specific转录因子(103年]。此外,MMP-28表情似乎仅限于发展中生殖细胞的转录是由转录因子介导的Sox-5 [104年]。
蛋白酶的表达在肥厚性软骨细胞和发展中软骨受矮子域因子2 (RUNX-2),结合RUNX-2网站,例如,MMP-13启动子,从而限制合成的MMP骨成骨细胞(11]。此外,MMP-9表达式也受RUNX-2,这符合成骨细胞的表达模式,非常适合于骨骼生长表型观察到MMP-9零老鼠。然而,生物信息学分析显示RUNX-2绑定网站越来越多的MMP的推动者,包括金属蛋白酶- 1的推动者,7、8和-13年,表明大多数基质金属蛋白酶都没有真正的组织特异性。例如,明胶酶MMP-2和9主要与基底膜降解在病理条件下因为它们表达的反应性上皮和间充质细胞在皮肤内。然而几个观察明显支持的作用扩大这些基质金属蛋白酶表达的大量不同的细胞类型,包括内皮细胞、骨相关细胞和免疫细胞(69年,105年,106年]。
特异性表达的另一个明显的例子是两间质胶原酶所代表的金属蛋白酶- 1和8。这两个酶的底物特异性相近,都降解胶原蛋白I, II和III。然而,它们的表达模式有很大的不同(表2)。金属蛋白酶- 1表达的几种类型的细胞,例如成纤维细胞、内皮细胞、软骨细胞和成骨细胞(44),而MMP-8主要由中性粒细胞分泌(108年]。这种差异可以解释的成分中不同cis-elements推动者,因为MMP-8推动者缺乏近端AP-1结合位点。
人类MMP-7启动子包括两个上游Tcf / Lef-1β-catenin调解transactivation的结合位点。因此,matrilysin (MMP-7)表示只在细胞上皮来源,包括一些外分泌腺体,如乳腺上皮细胞,腮腺、前列腺癌、胰腺、肝脏和支气管旁腺[107年]。
总之,似乎只有少数MMP的表达仅限于特定的细胞或组织成员在生理条件下,虽然大多数是广泛表达,参与许多重要的生理作用。未来的研究在小鼠模型可以揭示特定疾病某些成员MMP的表达模式。
选择性MMP瞄准的新策略
由于基质金属蛋白酶是强烈的调节在癌症和炎症相关的疾病,他们一直被视为有吸引力的治疗靶点。因此有效的MMP抑制剂的设计已经成为一个强烈的兴趣领域在过去的25年。然而,选择性抑制剂的设计已被证明是非常困难的,因为所有MMP的成员有着惊人相似的结构,在其活跃的网站(119年]。因此,大多数的临床试验使用这些小分子与负面结果MMP抑制剂已经结束,主要是由于其广泛的抑制活性。选择性抑制不同的MMP的成员在疾病早期阶段很可能比使用更有效的广谱抑制剂阻止大多数基质金属蛋白酶和亚当斯的活动,包括任何antitargets考虑成员(4]。
选择性MMP一个有趣的战略目标关注的目标函数专用酶抑制exosite域的MMP的分子,它们参与大分子底物识别整合蛋白或细胞表面绑定。这一代已成功实现的阻断肽或单克隆抗体(mAb)目标exosite大分子底物结合位点被基质金属蛋白酶切断的,如图所示,有效抑制MMP-2 collagenolysis通过堵塞它的胶原蛋白绑定域或特定高度MMP-9马伯REGA-3G12,选择性地抑制MMP-9的生物活性,而不是MMP-2 [27]。
选择性MMP的另一个方法针对具有相当大的潜力在于RNA干扰技术,在目标基因的表达减少短双链RNA数量具体绑定目标mRNA和干扰蛋白质翻译和/或促进信使RNA降解。干扰RNA可以引入了瞬时转染(短干扰(si) RNA)或通过稳定整合到细胞的基因组(短发卡RNA)。该技术已成功应用在实验小鼠模型与MMP-9 siRNAs,导致抑制肿瘤起始和进展120年),或与MMP-7目标siRNA导致抑制转移的胃癌和结肠癌(121年),似乎是一个有前途的未来治疗选择性抑制MMP的策略。然而,问题和困难与核稳定、功效的组织目标和非目标效应挑战他们的潜在治疗药物。
结论和未来的角度
基质金属蛋白酶是集成在多向交流的网络组织和细胞内细胞增殖和分化的重要监管机构,组织内稳态,免疫反应和其他几个过程。因为不受控制的MMP的活动可以很容易地成为体内平衡的破坏,导致崩溃,它已经意识到,他们的活动需要各级严格监管,通过表观遗传,转录和转录后基因表达的控制,激活他们的pro-enzymes,抑制他们的活动。许多研究表明,每个级别的控制结合几种不同的调节单元;其中一些非常具体的针对单一基质金属蛋白酶。此外,有证据表明,不同监管模式的单身或小群体的基质金属蛋白酶与癌症和炎症性疾病的不同阶段相关,可用于选择性MMP的目标通过RNA干扰技术表达水平或选择性抑制剂和阻止抗体的蛋白质水平。然而,需要进一步调查动物模型来验证这些相关性在活的有机体内。
在过去的几年中它已经建立,基质金属蛋白酶是多功能蛋白酶具有广泛的底物曲目。除了他们的经典角色与后续ECM降解释放生物活性因子,他们参与膜脱落,趋化因子或生长因子处理中扮演很重要的角色,并改变其他蛋白酶的活性状态。事实上,大多数的MMP的基质non-matrix分子,从而表明释放生长因子和细胞因子是基质金属蛋白酶的主要功能。新颖的蛋白质组学技术现在开始提供全面刻画MMP衬底degradomes和很快就会为一个强大的荟萃分析奠定基础,歧视下游效应和区分protease-specific基质配置文件。自蛋白酶底物的知识是理解的关键蛋白酶生物之一,这种发展的先决条件是一个更好的理解MMP参与生理和病理学。
16 MMP的分析,到目前为止,基因敲除突变体显示惊人的良性自发的表型在产后骨骼,循环和乳房发育,表明蛋白水解冗余和酶的补偿。唯一的例外是淘汰赛MMP-14导致一些异常在骨骼和结缔组织改造和血管生成,导致过早死亡。此外,大多数的MMP的淘汰赛中功能表型,缺陷的形式应对环境挑战,如急性伤害或细菌感染。然而,酶的突变小鼠的解释与损失与基质金属蛋白酶等广泛的底物谱是复杂的。由于他们的活动,基质金属蛋白酶可以参与许多不同的信号网络仅仅通过调节其他蛋白酶,直接或间接地通过解理和失活的蛋白酶抑制剂。因此,MMP基因敲除小鼠演示整个有机体的反应是一个复杂的系统损失的一个组件,而不仅仅是其特定的分子缺陷的影响。在这方面,未来的挑战将是评价MMP的突变体以及详细转基因小鼠模型。
大部分的MMP的成员都是广泛表达,参与许多重要的生理活动,而只有其中一些细胞类型特异性或组织的限制,像MMP-20牙科组织。与瞬变本构生理表达式通常是低,更高的利率由于体内平衡矩阵改造或特定发育事件。这些简短的表达高峰强调严格的监管在生理条件下,强调组织内稳态和发展的重要作用。
MMP的活动的失调,尤其是早期癌症阶段,仍然引发了极大的兴趣对基质金属蛋白酶治疗目标,尽管早期临床试验的失败使用广谱MMP抑制剂。未来研究的重点努力将躺在设计不同的选择性抑制MMP的成员的疗法。
确认
这项工作是德国研究基金会赠款支持DFG北京市。850 - tb6 Franzke (SFB)和o .先令(SCHI 871/2-1)。
脚注
社论评论看第12页。
感兴趣的语句
没有宣布。
- 收到了2010年9月15日。
- 接受2010年12月5日。
- ©2011人队