摘要
有证据表明,肺损伤,炎症和细胞外基质中的间质性肺病(ILD)重塑上一页肺纤维化。我们检查了计算机断层扫描(CT),增加肺衰减的定量测量是否检测肺损伤,炎症反应和细胞外基质,而不考虑呼吸道症状或吸烟采样社区居住的成年人重塑。
我们测量了高衰减区(HAA;在入选动脉粥样硬化多种族研究的成年人的心脏CT扫描中,肺体素在- 600到- 250 Hounsfield单位之间的百分比。
HAA与高血清矩阵metalloproteinase-7(平均调整差异6.3% HAA翻倍,95%可信区间1.3 - -11.5),更高的白细胞介素- 6(意味着调整差异8.8%,95%可信区间4.8 - -13.0),较低的用力肺活量(FVC)(意思是调整不同−82毫升,95% CI 119 -−−44),较低的6分钟步行距离(−40米,意味着调整差异95% CI - 1 - - - 80), 9.5年间质性肺异常的几率更高(校正OR 1.95, 95% CI 1.43-2.65), 12.2年全因死亡率更高(HR 1.58, 95% CI 1.39-1.79)。
高衰减区与炎症和细胞外基质重塑、肺功能降低、肺间质异常和社区居住成人的较高死亡风险的生物标志物有关。
摘要
CT上肺衰减增加可识别社区居住成人的亚临床肺损伤和炎症http://ow.ly/97k3300tvKX
介绍
复发性肺泡上皮细胞损伤,肺炎和呼吸困难的细胞外基质重塑被认为是关键前体事件,导致间质肺病(ILD)中的肺纤维化[1那2].患有ILD的成年人通常在初始侮辱后患者发生症状,使得肺纤维化的前一种难以识别。具有亚临床疾病的人类的研究可以为肺损伤的早期机制提供新的见解;然而,直到最近,在发育症状之前,很少有研究看过间质性肺部变化[3.-5.].
最近对大型人口群体的胸部CT扫描的胸部CT扫描的最新识别已经推进了我们对早期间质性肺病的理解[6.-9.].ilas已被证明与吸烟有关[6.],减少肺量[6.,减低运动能力[7., MUC5b多态性[8.,以及全因死亡率[9.]在基于人口的队伍中。然而,ILA评估是劳动密集型,需要受训练读者的视觉评分,并且有时,可能释放可能具有临床意义的临床意义。自动化方法可以提供卓越的再现性和对人眼无法检测到的早期异常的更大敏感性,包括可能先对ILA视觉识别的变化。
我们之前提出,在计算机断层扫描(CT)上定量测量肺衰减,称为高衰减区(HAA),可能是一种适合的测量肺发生ILD之前早期病理过程的方法[10].我们报道,HAA在肺更大的体积与吸烟有关[10].其他人报道,横断面分析显示,HAA累及10%以上肺的成年人总肺容量降低,ILA发生的几率增加[11].然而,缺乏缺乏早期肺损伤,炎症或纤维化的定量测量,缺乏缺乏炎症或纤维化的定量衡量,并且不知道少量HAA的意义。
因此,我们寻求确定Haa是否与亚临床肺损伤,炎症和纤维化的特征有关,包括炎症的血清生物标志物(白细胞介素-6(IL-6)和C反应蛋白(CRP)。)和肺重塑(表面活性剂蛋白-A(SP-A)和基质金属蛋白酶-7(MMP-7)),降低FVC,减少运动能力,视觉鉴定的ILA的几率增加,以及社区住宅成年人的所有导致死亡率。我们选择了IL-6和CRP,因为它们在全身炎症中具有良好的作用作用[12那13],以及MMP-7和SP-A,这些研究表明这些生物标志物与ILD中肺损伤和细胞外基质重塑相关[14-20.].
方法
补充附录中有完整方法。
学习参与者
动脉粥样硬化多种族研究(MESA)是一项由美国国家心肺血液研究所(NHLBI)赞助的多中心前瞻性队列研究,旨在调查亚临床心血管疾病。报名条件已详列[21].简单地说,这项研究招募了6814名年龄在45岁到84岁之间、在2000年到2002年间没有临床心血管疾病的美国6个社区的成年人。没有基于肺部疾病、呼吸道症状或吸烟史的选择标准。MESA参与者进行了随访,最近一次随访时间为2010年至2012年(图S1) [21].通过每9-12个月联系每个参与者或家庭成员来确定至关重要的地位。这通过审查国家死亡指数(NDI)进行补充,以确保通过最近的NDI更新(2015年3月13日)确保彻底的死亡后达。
MESA担任我们研究的采样框架。我们采样三个蛋白酶参与者:生物标志物,肺功能和ILA测量,以及运动测试。我们在补充材料和图S2中详细描述了每个替换的采样策略。报告每个替换的样品尺寸与每个替换的结果一起报告。
我们还将48名成人的比较剂组包括在临床诊断的ILD(具有特发性肺纤维化(IPF)的75%),这些中心(哥伦比亚省,PENN或DUKE)之一被纳入NHLBI资助的肺部移植机身组成(LTBC)研究。
MESA、LTBC和所有辅助研究均由所有合作中心的机构审查委员会批准,所有参与者均提供知情同意。
CT扫描的高衰减区域
在使用先前描述的标准化协议的2000-2002在2000-2002上的MESA基线访问,在2000-2002上的MESA基线访问中执行的非对比性心脏CT扫描上测量了HAA。使用先前描述的标准化协议,在电子束断层扫描仪(三个站点)上进行了[22].每位参与者在完全启发中接受了两个顺序扫描在单独的呼吸上持续,在完全启发中,具有横坐的视野,捕捉到肺部到肺部的整个肺部。使用较高空气量的扫描用于分析,除非是不间断的扫描质量控制评分,在这种情况下,使用更高的质量扫描[23].CT协议的细节显示在补充附录中的表S1中。使用MESA全肺扫描的先前验证研究表明,这些心脏CT扫描约65%的总肺体积,不包括大部分上叶,而是捕获大部分下叶片[23].Haa被定义为在-600和-250 hounsfield单元(hu)之间具有CT衰减的成像肺体积的百分比,如前所述[10].百分比肺气肿定义为-950胡以下的体素的百分比[24].根据临床方案,LTBC参与者在每个部位接受全肺吸气CT成像。定量图像衰减是由爱荷华大学成像实验室(爱荷华市,IA,美国)训练过的阅读者使用改良版的肺分析软件测量的。
生物标志物的测量
使用来自R&D系统(MMP-7和IL-6)和Biovendor (SP-A)的酶联免疫吸附试验(ELISA),测定银行基线血清样本中的MMP-7、SP-A和白介素-6 (IL-6)。使用BNII浊度计测定基线血清c反应蛋白(CRP)。所有测量均由佛蒙特大学临床生物化学研究实验室(Burlington, VT, USA)的MESA核心实验室进行。附加的分析特性在附录中提供。
肺活量测定和运动测试
肺活量测定是根据美国胸科学会(ATS)/欧洲呼吸学会指南进行的[188bet官网地址25],如前所述[26].6分钟步行检测(6MWT)按照ATS指南进行,无补充氧气[27].CPET在VMAX ENCORE 29代谢运动系统上进行,VIASPRINT 150P(VIASYS呼吸护理,Yorba Linda,CA,USA),带有电动制动的循环测力计。
间质肺异常
2010 - 12年度全肺MESA CT扫描在64片扫描仪(GE和SIEMENS)上暂停的全部启发,使用MESA肺/螺旋议定书(见补充附录)[28].图像重建使用0.625 mm的切片厚度,如前所述[29].ILA被定义为磨玻璃,网状异常,弥漫性循环结节,蜂窝状,牵引支气管扩张,非催眠性囊肿或至少5%的肺部的肺部,使用前面描述的方法[6.那8.那30.].
分析方法
我们将HAA视为连续独立的以2为底的对数(二进制)变换变量。对于大多数分析,我们使用广义线性模型校正年龄、性别、种族/民族、教育程度、身高、体重指数(BMI)、腰围、吸烟状况、烟盒年、肾小球滤过率(GFR)、研究地点、mA剂量、成像肺总体积和肺气肿百分比。由于肺活量和肺活量呈共线关系(Pearson相关系数为0.7),我们在分析HAA和肺活量之间的关系时排除了肺活量。我们使用logistic回归估计ILA的调整优势比。鉴于运动子研究的样本量小,我们选择了病例对照设计。我们将HAA病例定义为HAA的十分位数最高(>占总影像学肺的7.5%),我们给出了年龄和性别校正的最小二乘平均值。MMP-7和SP-A分析的采样细节在补充附录中提供。
我们使用Cox比例风险模型和添加剂Cox模型研究HAA和生存时间之间的关联,如前所述[31].生存时间以死亡时的年龄、最后一次随访或最近的国家死亡指数更新(以较晚发生的为准)计算。对上述协变量进行了调整。继发性分析进一步调整了饮酒、运动、癌症史、冠状动脉钙化和脚注中列出的心血管危险因素表3。
我们检查了通过吸烟状态,年龄,性别,种族/种族和BMI分层的模型。我们进行了敏感性分析,分析除了哈哈(> 7.5%的总成像肺部)和调整心脏收缩和舒张功能的测量。我们将社区住宅的平均HAA值与使用Wilcoxon等级试验临床诊断为ILD的48名成年人中的Haa值。
所有统计测试均在SAS version 9.3 (SAS Institute)和R version 3.2.0 (R Foundation for statistical Computing)中进行。
结果
由于缺乏有效的基线HAA评估,从分析中排除了一个参与者(图S2)。剩余的MESA参与者的基线特征在补充附录中的表S2和S3中示出。Mesa参与者的平均年龄为62岁;53%是男性;38%是白色的,28%是非洲裔美国人,22%是西班牙裔和12%的亚洲人。55%的MESA参与者是前者或目前吸烟的吸烟者,吸烟了15个卷烟组的中位数。48 LTBC参与者的平均年龄为63岁(范围34-75岁),31%是妇女,75%有IPF。
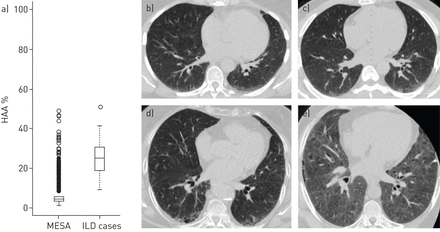
MESA参与者的平均±SD(范围)的5.1±3.1%HAA值(1.2%-48.9%)。LTBC参加临床诊断ILD有一个平均值(sd的25.4%(8.8%)与一系列的9.3%-50.8%(Wilcoxon秩和p值的<0.001)HAA值与MESA参与者;图1一个).与HAA值较低的MESA参与者相比,HAA值较高的MESA参与者更有可能是女性、西班牙裔或华裔、从不吸烟的人,且bmi较高(表S2)。那些在较高的HAA四分位数也倾向于有较低的肺成像体积和较低的肺气肿百分比。
a)高衰减区域(HAA)的盒子值为6813种多种族研究的动脉粥样硬化(MESA)参与者和48名成人,患有临床诊断的间质性肺病,注册肺移植体组成研究。实心水平线表示HAA值的中值。盒子由上下四分位数限定。晶须延伸到狭窄范围的1.5倍。异常值由开放圈表示。Wilcoxon等级和测试p值<0.001。b-e)从哈哈高架的四个台面参与者中选择了计算机断层扫描扫描图像。b)与Haa = 8.8%的成像肺的外周基底玻璃异常。c)HAA的液体玻璃不透明度= 10.0%的成像肺。d)早期外周网和囊性变化与HAA = 10.2%的成像肺。 e) Diffuse ground glass abnormality and an area of peripheral reticular changes with HAA=27.7% of imaged lung. All participants had interstitial lung abnormalities on follow-up computed tomography scans at MESA exam 5 (median follow-up time 9.5 years). None of the participants was clinically diagnosed with interstitial lung disease.
CT上HAA的视觉表现
HAA升高(任意定义为大于7.5%)的MESA参与者在CT图像视觉检查中出现一系列异常[10].常见的异常包括毛玻璃和网状改变。图1在基线上显示来自四个MESA参与者的选定CT图像,在线,在10年的随访中也有ILA。
血清生物标志物
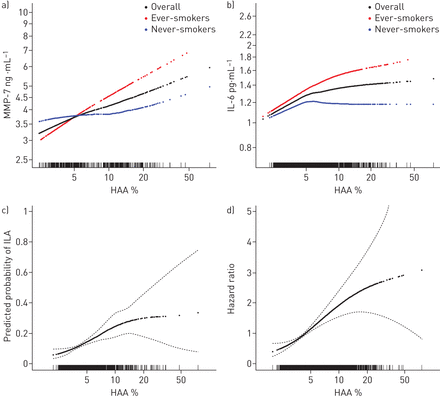
有908名MESA参与者测量了MMP-7和SP-A(见补充附录)。6621名受试者测量了IL-6, 6671名受试者测量了CRP。HAA越大,血清MMP-7和IL-6水平越高(表1和表S4)。对于HAA的每加倍,MMP-7中有6.26%(95%CI 1.29-11.47; P = 0.01)(图3一)中并在8.78%的IL-6(95%CI 4.77-12.95; P <0.001)(图3 b).HAA和MMP-7之间的关联被吸烟状态改变(交互作用p<0.001)。HAA每增加一倍,MMP-7增加15.45% (95% CI 7.91-23.53;p<0.001), MMP-7增加1.39% (95% CI - 5.36至8.62;p = 0.69;表1不吸烟者之间)。HAA和IL-6之间的相关性在经常吸烟的人群中更强,尽管只有少量的证据表明效果改变(交互作用的p=0.11;表1).我们发现HAA与CRP或SP-A水平之间没有显著相关性(表1).
肺量测定法
有3834名MESA参与者完成肺活量测定法,并在1 S中有有效的强制呼气量措施(FEV1)和FVC(见补充附录)。在完全调整的模型中,每增加一倍HAA, FVC就减少82 mL (95% CI 119-44;p<0.001),预测FVC百分比绝对下降2.8% (95% CI 3.9-1.7;p < 0.001;表S5)。吸烟状况改变了这种关联(交互作用的p=0.002)。在完全调整的模型中,每增加一倍的HAA与FVC减少157 mL相关(95% CI 216-97;p<0.001)(表S5),并且减少了15 mL (95% CI 60 -−31;p=0.53)(表S5)。我们在FEV中也发现了类似的关联1和百分比预测的fev1但不为FEV的比率1到FVC(表S6)。
运动能力
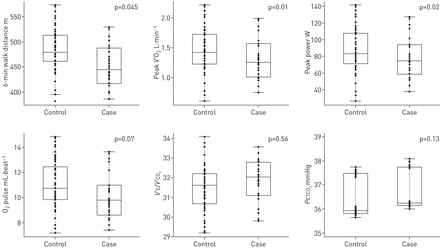
有89名MESA参与者完成了运动测试;其中30例为病例(HAA高于90百分位(7.5%)),59例为对照(HAA低于90百分位)。HAA高的患者与对照组相比,6-MWT和CPET的运动能力均降低(图2).校正年龄和性别后,最小二乘平均差为40 m (95% CI 1-80;p = 0.045;表S7)。HAA患者调整后的峰值摄氧量也较低(V'O.2) (1.28与1.47 L·min-1;P =0.01),百分比预测峰值V'O.2(72%与83%;p = 0.01)和峰值瓦特(76与88 w;p = 0.02;图2和表S7)。呼吸储备在案件中低于控制(53与61%;P = 0.04),表明锻炼的通风限制。心率和心率的控制之间没有显着差异,o2脉冲,微小通风/ CO2生产,终端潮2在峰值运动。
运动能力在10万例随访30例,高衰减区域(HAA)(> 7.5%)和59个对照组而没有升高的动脉粥样硬化(MESA)基线计算断层扫描扫描。O.2脉冲,微小通风/ CO2生产(V'E./V'CO.2)和最终的CO2张力(P.Etco.2)在运动高峰期进行测量。点表示根据年龄和性别调整的个体预测值。实心水平线表示HAA值的中值。盒子由上下四分位数限定。晶须延伸到狭窄范围的1.5倍。V'O.2:耗氧量。
间质肺异常
有2907名MESA参与者进行了有效的ILA定性评估。HAA测量和ILA评估之间的中位时间为9.5年(范围为8.0-11.4年)。在2907次扫描中,477例(16.5%)ILA被认为是模棱两可的,并被排除在进一步的ILA分析之外。在剩余的2430名参与者中,306名(占总样本的10.5%)有ILA: 285名(9.8%)扫描显示ILD可疑,21名(0.7%)扫描显示多叶双侧纤维化伴胸膜下分布的蜂窝和牵引性支气管扩张(明确的ILD)。162例(53%)ILA患者的变化主要发生在胸膜下分布。异常类型分布情况见附录表S8。
在四分之一HAA组中,ILA患者人数增加(p<0.001趋势;表2).在完全校正模型,这些与基线HAA值大于5.3%(第四四分位数)具有ILA与那些在最低四分位数(OR 3.07比较的三倍高几率,95%CI 1.77-5.33; P <0.001;表2和图3 c),Haa的每加倍与ILA的含量增加95%(或1.95,95%CI 1.43-2.65,P <0.001)相关。曾经吸烟者和从未吸烟者的这些结果相似(表2).分析,其中含有抗体ILA发现的参与者作为“No ILA”产生类似的结果(表S9)。
死亡率
由于发现前基线心血管事件的发现,从MESA活动委员会的后续行动中排除了五名参与者,并且这些参与者没有死亡数据。剩余的6808 MESA参与者在12.2年的中间随访中,有1093名死亡人员中的剩余6808个梅萨参与者(范围0-14.2)。大Haa与较高的全因死亡率有关(图3 d).在完全调整模型中,HAA最高四分之一的MESA参与者的死亡率大约是HAA最低四分之一的参与者的两倍(HR 1.94, 95% CI 1.53-2.46;趋势p < 0.001;表3)HAA的每一倍,任何原因的死亡率增加了55%(HR 1.55,95%CI 1.37-1.77; P <0.001),没有通过吸烟状态修改的证据。
a) 908名MESA参与者中基质金属蛋白酶(MMP)-7(总体和按吸烟状态分层)基线水平之间的高密度区(HAA)和b) 6621名多种族动脉粥样硬化研究(MESA)参与者中白细胞介素(IL)-6(总体和按吸烟状态分层)基线水平之间的持续关联。c)间质性肺异常(ILA)) 2430名MESA参与者在HAA测量后的9.5年和d) 6808名MESA参与者在12.2年随访后的死亡率。所有模型根据年龄、性别、种族/民族、教育程度、身高、体重指数、腰围、肾小球滤过率、研究地点、mA剂量、肺总容积成像和肺气肿百分比进行校正;整体模型还根据吸烟状况和烟盒年份进行了调整。a)关联的总体p值为0.01,非线性的p值为0.37;在吸烟者中,相关性的p值<0.001,非线性的p值为0.70;在不吸烟者中,关联的p值为0.69,非线性的p值为0.18;吸烟交互作用的p值<0.001。b)总体关联p值<0.001,非线性p值0.005;在曾经吸烟的人群中,p <0.001; p-value for non-linearity 0.17; among never-smokers p-value for association 0.28; p-value for non-linearity 0.02; p-value for smoking interaction 0.11. c) p-value for association <0.001; p-value for non-linearity 0.05. d) p-value for association <0.001. Black points are the overall effect estimate; thin dashed lines are the 95% confidence bands; red points are the effect estimate among ever-smokers; blue points are the effect estimate among never-smokers. Each point in the graphs and each vertical mark in the rug plot along the x-axis represent one study participant.
额外的分析
分层和敏感性分析,包括调整左心室功能和限制那些HAA小于7.5%的参与者,如表S10-S12所示。这些分析并没有实质性地改变我们的发现。
讨论
我们发现,居住在社区的中老年患者肺部CT高衰减区域与血清MMP-7和IL-6水平升高、肺活量减低、运动能力降低、10年随访时ILA发生几率增大和死亡率升高有关。与从不吸烟的人相比,经常吸烟的人更容易产生这些联想。这些发现支持了HAA作为亚临床肺损伤和炎症的一种新的定量表型的构建有效性,它具有生物学和生理学上的重要性,可能是亚临床ILD的前体。
HAA与IL-6和MMP-7之间的关系表明,在某些情况下,HAA可以识别间质炎症、细胞外基质重塑和纤维化的区域。IL-6是一种促炎细胞因子,急性肺损伤时其血清水平升高[32那33].IL-6已牵涉于慢性阻塞性肺病[34],急性呼吸窘迫综合症[35]和某些类型的ILD [36].在以人群为基础的队列中,IL-6水平也与FVC百分比的降低有关[37那38].IL-6诱导CRP和其他下游炎症介质的肝脏生产[12].虽然IL-6水平通常与CRP相关,但有许多条件的条件,其中两个生物标志物的水平不互相跟踪[39-41],暗示还有额外的途径来调节这些生物标志物,这可以解释为什么我们在我们的研究中没有看到Haa和CRP之间的关联。MMP-7被认为在对上皮损伤的正常反应中发挥重要作用[42].MMP-7的上皮表达在损伤后以及在肺炎症和纤维化的环境中增加[18-20.那43那44].我们发现,哈哈和血清MMP-7之间的关联(以及在较小程度上,IL-6)在有效的吸烟者中更强大,为HAA提供支持,作为香烟烟雾诱导的肺泡重塑的衡量标准。
虽然,在一些人中,Haa可能代表静水肺水肿,肺部感染,恶性或恶性损伤,或由于肥胖或不完整的灵感而言,我们的研究结果的总体表明,Haa识别肺部结构的异常,生理和生理亚临床ILD的特征。我们发现没有通过心功能,BMI,腰部周长或成像肺总量强烈混淆的证据。MESA参与者在注册时通常很好,如果它们分别进行急性传染性过程或临床诊断的心力衰竭,则重新安排或排除。MESA参与者的整体良好健康降低了HAA反映参与者无法执行全面吸气机动的可能性。我们研究的特定优势在于,在许多放射生物和生理学测量中的预期变化的一致性以及通过吸烟的效果改性的证据,如果哈哈代表左心室填充压力或肥胖,则不会预期。
其他人使用了HAA的替代定义(−700至0 HU,−700至−500 HU) [45-47]、直方图特征等自动化方法[48-51],包括基于纹理的方法[52],识别和表征临床显而易见的ILD,但不是亚临床的变化。最近的研究已经审查了视觉上鉴定的ILA和死亡率之间的协会[9.],但我们的研究是首个将HAA作为肺损伤和炎症的定量测量方法的研究,在不考虑肺部疾病、症状或吸烟状况的社区居住成人样本中,HAA与较高的死亡率相关。我们的结果在HAA的整个谱系中都是一致的,特别是在排除了HAA的90%以上的个体(可能有临床可识别的ILD)之后。大多数参与者的HAA涉及不到10%的成像肺,这表明即使是少量的肺衰减增加,可能很难被人眼检测到,也可能识别出有ILD风险的个体。如果验证有效,研究者可以使用HAA来研究早期损伤、炎症和肺细胞外基质重塑的原因,甚至在放射科医生发现肺间质异常之前。这些研究可能有助于识别人类ILD的新危险因素和生物途径,为未来旨在ILD一级和二级预防的临床试验奠定基础[53].
我们的研究有几个局限性。首先,我们缺乏可验证Haa疾病的病理相关性。这是对任何呼吸道症状未选择的社区住宅成年人的亚临床疾病的研究,因此没有可用的病理样本。然而,我们还在临床诊断的ILD中衡量了Haa,其中大多数人诊断为ATS标准,我们向Haa值报告明显高于Mesa参与者的价值观。其次,Haa被评估在心脏CTS上,其不会将整个肺图像图像,但已被证明可用于检查肺气肿[31那54那55].我们之前已经表明,心脏CT上的Haa在全肺CT扫描上与Haa相同意[10].第三,我们报告HAA和生物标志物,这限制了任何因果关系推论之间的横断面分析。然而,先前的研究已牢固确立MMP-7作为肺损伤和ILD的生物标志物,IL-6已在文献中描述为炎症的标志物,我们的ILA和死亡率分析在很位随访时间of 10–12 years. Fourth, we lacked baseline assessment of ILA and therefore can only report the period cross-sectional associations between HAA and ILA. Given the long follow-up period in our study and the 10-year difference between assessment of HAA and ILA, we believe that at least in some cases, HAA precedes the development of ILA. However, the odds ratios we report should not be interpreted as incidence rate ratios.
总之,使用定量CT密度测量增加的肺衰减的更大体积与较高的血清IL-6和MMP-7的水平,在FVC减少,ILA的增加的可能性,并独立潜在混杂的全因死亡率的增加的速率相关联的社区居住的成年人因素。我们的数据表明,HAA是亚临床肺损伤,炎症,并可能早期细胞外基质重塑可能对肺间质异常和疾病发展的CT-基于风险因素的新定量测量。今后的研究应集中在因素的高危人群,如吸烟者或老年人和影响HAA应努力包括HAA在事件ILD临床预测模型。这样的研究将导致干预措施,防止ILD的临床试验。
致谢
作者感谢其他调查人员,员工和MESA学习的参与者的宝贵贡献。可以找到参与的MESA调查员和机构的全部列表http://www.mesa-nhlbi.org。
Anna J. Podolanczuk、Elizabeth C. Oelsner、David J. Lederer、R. Graham Barr和Steven M. Kawut构思和设计了这项研究。Anna J. Podolanczuk, Elizabeth C. Oelsner, R. Graham Barr, Hilary F. Armstrong, Robert C. Basner, Matthew N. Bartels, Jason D. Christie, Karen Hinckley Stukovsky, Joel D. Kaufman, Scott M. Palmer, Russell P. Tracy, Kayleen Williams和David J. Lederer获得了数据。安娜·j·Podolanczuk伊丽莎白·c·Oelsner r·格雷厄姆•巴尔埃里克·a·霍夫曼约翰•莫莱森奥斯汀罗伯特·c·Basner马修·n·巴特尔斯凯伦·欣克利Stukovsky p . Hrudaya纳,约翰·d·纽厄尔,Dan Rabinowitz杰西卡·l .出售Jered Sieren, Sushil k . Sonavane罗素·特雷西犹八r·瓦Kayleen威廉姆斯,和大卫·j·莱德尔分析数据。所有作者都对数据的解释做出了贡献。安娜·j·波多兰祖克(Anna J. Podolanczuk)起草了初稿。所有作者对手稿中重要的知识内容进行了修改,并批准了手稿的最终版本。所有作者同意对工作的所有方面负责
脚注
编辑评论欧元和J2016;48: 1271 - 1273。
本文提供了补充材料www.qdcxjkg.com
支持声明:本研究由国家心肺血液研究所R01 HL103676、R01 HL077612、R01 HL114626、R01- 100543、R01- hl093081、N01-HC-95159、N01-HC-95160、N01-HC-95161、N01-HC-95162、N01-HC-95163、N01-HC-95164、N01-HC-95165、N01-HC-95166、N01-HC-95167、N01-HC-95168、N01-HC-95169、T32 HL105323资助。并由NCRR/NCATS授予UL1-TR-000040和UL1-RR-025005。该项目部分由肺纤维化基金会资助。本手稿的资金信息已存入FundRef。
利益冲突:可以在本文的在线版本旁找到披露www.qdcxjkg.com
- 收到了2016年1月16日。
- 接受2016年5月7日。
- 版权所有©2016