抽象的
嗜酸性肉芽肿病伴多血管炎(EGPA)的呼吸系统表现尚未得到详细研究。
在这项回顾性多中心研究中,EGPA被定义为哮喘、嗜酸性粒细胞增多和至少一种新发的支气管外肺器官疾病表现。
研究人群包括157名患者(平均值±sdage 49.4±14.1 years), with a mean±sd血液咽芯计数为7.4±6.4×109. L-1诊断。有一个平均值±sd从哮喘发作到EGPA的诊断,从外周嗜酸性粒细胞症的第一次发作到EGPA的诊断,从EGPA诊断到最后一次访问,从EGPA诊断为1.4±8.4岁。尽管吸入和口服皮质类固醇治疗,但哮喘的严重程度在全身表现前3-6个月增加了3-6个月。哮喘患者在57%,48%和56%的诊断中,3年和最后一次访问。持续气流阻塞分别在38%,30%和46%的诊断下,3年,最后一次和最终访问。
在EGPA中,哮喘严重,通过12年的平均抗体进行系统性表现,并且尽管在大部分患者的皮质类固醇中,对长期持续气流阻塞进行了进展,这影响了长期管理和发病率。
抽象的
在EGPA中,尽管许多患者皮质类固醇,但哮喘严重并进行了持续气流阻塞http://ow.ly/8uf8301KSoT
介绍
嗜酸性粒细胞芽孢杆菌(EGPA)(以前称为Churg-Strauss综合征)定义为富含嗜酸性粒细胞和坏死性肉芽肿的炎症,通常涉及呼吸道,其正常影响中小血管的坏死性血管炎,以及与哮喘和嗜酸性粒细胞有关的病例[1].系统血管炎的命名在2012年国际教堂山共识会议上进行了修订[1],和Churg-Strauss综合征的术语替换为EGPA [2].EGPA的经典描述遵循三个阶段[3.那4.]:1)哮喘和鼻炎;2)组织嗜酸性粒细胞(包括嗜酸细胞性肺炎);3)肺外嗜酸性疾病与血管炎。
虽然哮喘是定义的一个关键组成部分和用于EGPA [分类标准1那5.],很少有研究具体评价EGPA的呼吸道表现,特别是相应的年表和系统性血管炎的哮喘和严重程度,以及与治疗的血管炎和哮喘肺功能方面的结果。哮喘EGPA是经典严重[6.]和皮质类固醇依赖性[7.],比全身性疾病发作早数年[8.].哮喘的严重程度被认为减弱了血管炎的发作[7.].大多数患者可能需要用低剂量口服皮质类固醇进行长期维持治疗,以控制哮喘一旦获得了全身嗜酸性疾病的缓解[8.].我们在一个单一的中心一系列连续24名患者以前曾表明,持久性气流阻塞引起不受控制的哮喘存在尽管在许多患者口服皮质类固醇在诊断,在EGPA的和随访期间临床缓解,具有部分可逆性中的可能性在口服糖皮质激素剂量的短暂升高某些情况下[9.].
在此,我们描述了157例EGPA患者的回顾性多期分析中的支气管肺组合,并阐明了哮喘的严重程度和治疗方面的变化。
患者和方法
研究设计和数据收集
这项回顾性研究是由肺孤儿疾病研究小组(GERM“O”P)和欧洲呼吸学会EGPA工作组成员进行的,该小组致力于包括EGPA在内的罕见(所谓孤儿)肺部疾病的研究。188bet官网地址一份详细的调查问卷被发送给先前预先向GERM“O”P登记处报告过EGPA病例的医生和预先在自己的数据库中收集过数据的工作组成员。问卷通过查阅病历进行填写。使用标准表格系统地收集医学档案中的数据,包括流行病学特征、吸烟史、特应性状态、临床表现、影像学和用药情况,包括诊断时和转归时的数据,特别是呼吸道表现。这项研究得到了美国国立卫生研究院机构审查委员会的批准Société de Pneumologie de Langue Française(法国巴黎)。数据库是匿名的,符合要求的要求国家信息委员会等。患者收到证明其不受限制权利的信息,要求从数据库中删除其数据。
患者选择
EGPA的诊断是由调查人员重新评估,并列入情况下,如果他们符合以下两个条件,从那些兰哈姆提出派生等。[7.]并修改如下:1)哮喘;2)由血液嗜酸性粒细胞定义> 1.5×10定义的嗜酸性粒细胞9. L-1在至少一种测量和/或血液嗜酸性粒细胞> 10%的白细胞,和/或标记活组织检查验证的组织嗜酸性粒细胞和血液咽喉> 0.75×109. L-1;3)至少一种新的发病患者疾病的表现(鼻窦炎或其他耳,鼻子和喉咙)表现)。来自整个随访期的数据被考虑在内[10.,最终被诊断为患有其他嗜酸性肺疾病的患者被排除在外。有单一全身表现的患者被纳入考虑到疾病早期诊断的可能性(”形式吓坏了“EGPA)。
治疗
治疗由医生自行决定,并遵循标准的护理指南。除了皮质类固醇治疗,口服或静脉注射环磷酰胺作为诱导治疗的因素与不良预后[11.[后者在完整的临床缓解后使用免疫抑制治疗的维持治疗获得了全身疾病。副唑唑或甲氨蝶呤用于皮质类固醇不能逐渐变细2毫克的患者-1泼尼松。
器官表现的分类
系统器官表现认为血管炎的直接明确表现包括任何器官的活检证明的坏死性血管炎,坏死性肾小球肾炎(活组织检查证明),肺泡出血(定义为胸部射频和/或高分辨率兼容不透明度的血腥支气管血清灌洗液由于经过验证的冠状动脉炎(与全身疾病有关,可触及的断层扫描(CT)),可触及的紫癜或心肌梗塞,例如在没有冠状动脉动脉粥样硬化的冠状摄影或心肌梗塞的非血液冠状动脉狭窄)。
此外,系统性血管炎的强代谢物包括:1)血尿伴有红细胞铸型或>10%畸形红细胞,或尿液分析中出现血尿和2+蛋白尿(与系统性疾病相关,无活检)[12.];和2)比ENT或与相关联的活检支气管肺表现表明白细胞分裂毛细血管和/或动脉壁的嗜酸性细胞浸润[其他任何器官表现2].血管炎或强烈血管炎的患者被认为是具有全身血管炎的患者。
当按年表和缺乏另一种合理的原因建议时,考虑了其他新的发病系统表现与EGPA有关;然而,它们不被认为是血管炎的直接表现,并且这些包括尤其是单一的单一炎或单一的多重(用于第一步分析),或者心肌炎自信地归因于嗜酸性疾病,仇心膜炎除了无症状的轻度心包积液之外,肾病除外以上,以及任何其他器官/系统表现在活组织检查或与嗜酸性疾病(没有活组织检查)的令人信服相关的嗜酸性嗜嗜酸性渗透性。
评估
发烧定义为体温>38°C。体重减轻定义为诊断前3个月>为体重的5%或>为体重的3kg。根据临床表现结合超声和心电图结果诊断心脏表现[11.].心肌炎被定义为具有心力衰竭的临床表现的患者,减少了收缩射血分数,增加了N-末端促脑利钠肽或脑利钠肽,和/或增加血清肌钙蛋白水平。明确的呼吸道过敏由过敏症状的存在定义,增加了特定的IgE和阳性刺的试验与暴露和症状的季节一致。慢性鼻窦炎被定义为存在鼻排放,头痛,鼻塞和/或低咽部,超过12周,没有完全解决症状[13.].
当通过免疫荧光和血清在疾病过程中血清中的血清中的血清中的血清检测时,抗癫痫培养酚细胞质抗体(ANCA)被认为是阳性的。活检发现被记录为正常或显示坏尺寸血管炎,嗜酸性组织浸润,肉芽肿或特定器官特征(坏死性肾小球肾炎或新月形肾小球炎)。
用标准协议进行肺功能测试,并在国际指南下进行[14].值表示为预测值的百分比,除了1 s中的强制呼气量(FEV1)/强迫肺活量(FVC),以绝对值表示。FEV1和FEV1/ FVC在支气管扩张剂之前评估,然后在给予短作用吸入β-2激动剂后10-15分钟。持续气流阻塞由后支气管扩张器FEV定义1/ FVC比率<0.70带FEV1<预期的80% [9.].
哮喘严重程度定义如下。温和:需要低剂量吸入皮质类固醇或其他低强度治疗(例如血红素或白三烯受体拮抗剂);中度:需要低至中剂量吸入性皮质激素和长效β -2激动剂(或其他额外治疗);严重:需要高强度治疗(大剂量吸入皮质类固醇和长效β -2激动剂伴或不伴口服皮质类固醇和/或其他额外治疗)[15那16].
学术放射科医生和肺科医生对每个机构的胸部CT进行审查,并使用标准表格收集经共识获得的数据。支气管肺影像学特征分为:1)由小叶中心小结节、V型或y型混浊、树芽征、支气管扩张及支气管壁增厚、花叶灌注型组成的气道模式;2)由毛玻璃样混浊、实变和界限不清的结节组成的空域模式[17].
如所描述的预后因子5个得分和订正5因子得分进行评价[11.那18].临床缓解定义为缺乏全身疾病的临床表现和外周嗜酸性粒细胞计数<1×109. L-1至少连续三个月。EGPA的复发[10.那19那20.]被定义为在缓解至少3个月后的EGPA的临床表现的复发或恶化,和/或恢复皮质类固醇治疗,增加每日剂量的口腔或静脉内皮质类固醇或引起免疫抑制治疗除哮喘或鼻窦炎外,EGPA的临床表现也会发生恶化。呼吸表现的复发(Exacterbation)被定义为哮喘,鼻窦炎或鼻炎症状的增加或复发,有或没有增加嗜酸性粒细胞血细胞计数并需要治疗调整。
统计分析
所有结果表示为平均值±sd对于分类变量的连续变量和数字(百分比),除非另有说明。使用非参数Mann-Whitney测试进行比较连续变量。使用Fisher的确切测试进行比较分类变量。使用Kaplan-Meier方法计算随访时间,从EGPA诊断到死亡或最后一次随访访问时计算。GraphPad Prism(GraphPad Software,Inc.,La Jolla,CA,USA)和SPSS 13.0(SPSS Inc.,Spss Inc.,Chicago,IL,USA)软件。结果被认为是P <0.05的重要结果。
结果
患者特征,诊断标准和系统性表现
在168例案例报告中收到的报告表格,11种被排除在外,由于在10例中没有呼吸道器官表现,并且在一个案例中没有嗜酸性粒细胞凋亡。共有157例(表格1)中,用平均值±sd年龄49.4±14.1岁(范围:17.2-80.9岁),其中51%是女性。
根据纳入标准,所有患者患有哮喘,嗜酸性粒细胞症和至少一种全身体式表现(除哮喘,肺部或腹部)直接归因于EGPA的历史。所有患者均满足以前的临时诊断标准[21];148(94%)符合美国风湿病学会建立的分类标准[22];其他9例患者均至少有两种可归因于该疾病的胸外器官表现。
在157例患有至少一个全身表现的患者中,42例(27%)患者具有除哮喘或肺部或肺部或抗体之外的一个系统性表现,46例(29%)有两种表现,34例(22%)有三种表现,14(9%)有四种表现,21例(13%)有五个或更多的全身表现。
共有63例(40%)患者具有明确的血管炎特征,活检证实坏死性血管炎(28例(18%)患者),活检证实坏死性肾小球肾炎或新月体肾小球肾炎(9例(6%)患者),白细胞碎屑性毛细血管炎(21例(13%)患者),肺泡出血(6例(4%)患者)。可触及紫癜(26例(17%)患者)或血尿(14例(9%)患者),冠状动脉炎引起的心肌梗死(8例(5%)患者),或活检证实的其他器官血管炎(10例(6%)患者)。在明确血管炎患者中,1个器官受累30例,2个器官受累21例,3个器官受累8例,4个器官受累3例,6个器官受累1例。
一种活组织检查导致89例(57%)患者EGPA的诊断,证明了小于中等大小血管(18%),白细胞痉挛性毛细胞炎(13%),动脉壁的嗜酸性渗透性(8%)或相邻的组织(18%),血管外肉芽肿(6%)和/或巨细胞(4%)。
平均值sd外周血嗜酸性粒细胞计数最大值为7.4±6.4×109. L-1,平均从外周嗜酸性粒细胞症的第一个发病到EGPA的诊断。均为1.4±8.4岁。41(26%)患者在诊断时服用白三烯受体拮抗剂(所有病例中的蒙特利亚斯特)。抗白三烯拮抗剂的起始之间的中位延迟为0.67岁(从21天至8.1岁),并用抗白酮拮抗剂治疗中值持续时间,直至EGPA的诊断为0.50岁(从7天至2.58岁)。在诊断EGPA时通常停止抗白硫治疗。
104名患者的五个因子评分为0,4例患者1例,2例患者2例。修订后的五个因子评分为90例患者,4例患者1例,20名患者2例,两名患者3例。
ANCAs和生物学
在48名(31%)患者的诊断时发现了ANCAS,其中46(29%),抗髓氧化酶特异性和2(1%)在ELISA的抗蛋白酶3抗体。免疫荧光的ANCA模式在23例(15%)患者中,10(6%)和15(10%)未知的细胞质。总血清IGE水平为981±1571 mg·l-1。C反应蛋白血清水平为53±48 mg·L.-1。
在所有情况下,诊断过敏性支气管瓣曲霉病,特发性过嗜合体综合征,寄生虫感染和药物有关的嗜酸性嗜酸性嗜酸性嗜酸虫病。但是,阳性IgG血清学aspergillus fumigatus.6例(4%);4例(3%)患者外周血t细胞克隆水平低,8例(5%)患者有意义不明的单克隆γ病。
哮喘和肺功能检查诊断
哮喘是目前所有患者和平均先于全身表现的发病±sd11.8±18.2岁;它伴随着单身患者的血管炎。平均值sd从首次发生外周血嗜酸性粒细胞增多症到出现全身表现的时间为1.4±8.4年。
在EGPA的诊断下,144名(92%)患者患有呼吸困难;102(65%)咳嗽,其中40(25%),痰液生产;25(16%)患者报告胸痛;11(7%)有血液术。
45(29%)患者患有烟草吸烟的历史,其中10(6%)在诊断时活跃吸烟,平均值±sd20.8±22.0(范围1-100)包年。
142名患者的诊断肺功能试验(90%)显示了一款支气管扩张剂FEV1的69.7±24.9%的预测,后支气管扩张FEV1/FVC为68.9±15.3%,支气管扩张剂后FVC为82.8±23.1%。Post-bronchodilator FEV1/ FVC为54%的测试患者的<0.7。哮喘严重程度在17%的患者中轻度,26%的患者中度和57%的患者严重。
仁表现
四分之三的患者患有慢性鼻窦炎的临床表现,其中72%的非过敏型(表2.), 66%的CT表现为上颌鼻-鼻窦炎。约一半的患者有鼻息肉病病史;55%的患者病程复杂,需要手术治疗,28%的患者复发鼻息肉病。慢性中耳炎较少;然而,它导致6%的患者听力损失。
过敏
43例(27%)患者有明确的呼吸道过敏史(表3),21(13%)他们也有过敏的家族史。确定的最常见的过敏症是Dermatophagoides pteronyssimus和D. Farina(16%的患者),草(8%),曲霉属真菌(6%),猫(5%)、狗(3%)、short-ragweed(3%)、桦木(2%)和alternaria.(2%)。只有3%的患者已脱敏Dermatophagoides。
哮喘和鼻炎症状分别为10%和15%的病例,并且在其余情况下常年。四(3%)患者在EGPA诊断前2个月内患有疫苗接种历史。有趣的是,33名(21%)患者患有食物和药物伪能反应的历史,涉及阿司匹林和非甾体抗炎剂(8%),食品添加剂(3%)或醇(10%)的反应。没有患者对昆虫毒液过敏。
肺影像学表现
91例(58%)患者诊断时出现胸片异常,其中磨玻璃衰减46例(29%),实变45例(29%),结节或肿块14例(9%),胸腔积液15例(10%)。58%的病例的异常分布为双侧。
报告CT上的成像功能表4.。在30%的病例中分析了特征,以30%的气道模式,15%的病例和混合模式的10%的病例;在45%的病例中被认为是不确定的。
支气管肺泡灌洗
在92例中进行纤维 - 光支气管镜检查,并在27例(29%)患者中,在27例(29%)患者中展示了支气管粘膜的弥漫性炎症,14例(15%)患者中的粘液分泌物,以及八个(9%)患者的白粒颗粒。支气管肺泡灌洗调查结果显示在表5.包括平均33%的嗜酸性粒细胞中的差异细胞计数。
胸腔积液
胸腔积液在10例中,调查员直接与EGPA相关,两种情况下心力衰竭(在五种情况下不确定原因)。在15例中有九种情况,对应于探讨的五种病例中的五种情况(三种情况下有20%的嗜酸性粒细胞或更多的嗜酸性粒细胞或两种情况)的渗出物。
哮喘严重程度和结果
虽然所有患者在每个时间点的哮喘严重程度的评估无法获得,但在全身性疾病发病前3-6个月,哮喘严重程度有增加的趋势(图1).
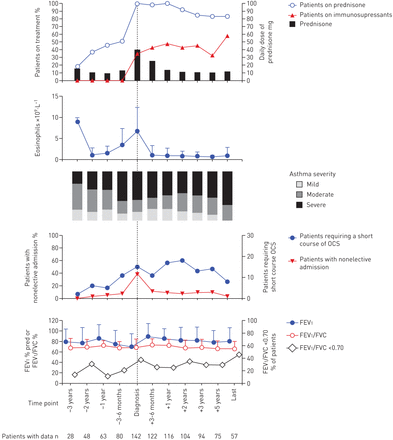
嗜酸性肉芽肿伴多血管炎患者在诊断前后口服皮质激素(OCS)和免疫抑制治疗时外周血嗜酸性粒细胞计数、哮喘严重程度和肺功能的时间程。FEV1: 1秒内用力呼气量;FVC:强迫肺活量。
所有患者均接受EGPA全身皮质类固醇治疗和/或同时接受免疫抑制治疗(表6.).6例(4%)患者也接受了奥玛珠单抗治疗。此外,所有慢性哮喘患者均接受大剂量吸入糖皮质激素和支气管扩张剂治疗。
从EGPA的诊断,157名患者的整体后续随访时间为7.4±6.4岁。三名患者死于(心室颤动在一个情况下;两种情况下未知的原因)。201日复发事件发生在71例(46%)患者中,相当于三分之二的病例中,复发哮喘症状通常伴随着外周嗜酸性粒细胞的增加> 1×109. L-1,其余病例为全身性疾病复发。复发的数量与基线时全身特征的数量、基线时血管炎特征的数量或修订的五因素评分(数据未显示)无关。5因素评分为1或1以上的患者(2.20±2.25)和评分为0的患者(2.86±1.70)的复发次数没有差异;p = 0.163)。27%的患者有长期后遗症,其中8%的患者有衰弱性持续性慢性哮喘。大多数患者有类固醇副作用(未量化)。
尽管接受了治疗,但在诊断为EGPA后的几个月和几年里,哮喘的严重程度保持不变。所示图1,超过80%的患者接受了口腔皮质类固醇的几年,平均每日剂量> 10 mg·日-1控制哮喘所需的泼尼松。治疗与嗜酸性粒细胞减少有关,并且平均外周嗜酸性粒细胞细胞计数剩余低于1.0×109. L-1在长期的。然而,FEV1/ 25-35%的患者FVC仍然<0.7(取决于时间点)。此外,每年有11-18%的患者需要短期的全身皮质类固醇治疗,每年有~ 10%的哮喘患者需要非选择性住院治疗,在开始全身治疗后没有显著下降(图1).
讨论
在这项关于EGPA患者呼吸系统表现的研究中,我们发现所有患者中都存在哮喘,其发病时间比全身性表现早一个±sdof 11.81±18.18 years. The severity of asthma increased 3–6 months before the onset of the systemic manifestations, with one-third of patients having long-term airflow obstruction and severe asthma despite continuation of high-dose inhaled corticosteroids in all patients and oral corticosteroid treatment in more than 80% of patients. Only a quarter of the patients had a definite history of respiratory allergy. ENT manifestations predominantly consisted of non-allergic chronic rhinosinusitis, with nasal polyposis in half of the patients. CT features were variegated, with an indeterminate airspace/airway pattern in nearly half of cases.
以前关于EGPA的研究要么没有关注呼吸表现[7.那8.那10.那23-26],或者在样本大小是有限的[6.那9.那27].本研究是一个大型,协作,多期的研究,平均值±sd诊断EGPA后随访7.4±6.4年。由于研究人员大多来自呼吸内科,肺部特征可能被过分强调。我们发现,与之前研究发现的3-6年(至9年)的哮喘病史相比,患者在血管炎发病前有更长的哮喘病史[7.].我们的数据证实,在血管炎发病前的几个月,哮喘经常迅速变得严重依赖糖皮质激素[6.].当血管炎恶化和血管炎消退时,哮喘总体上仍然严重,这与之前的一份报告所描述的在较短的2年随访期内哮喘的良好病程形成了对比[27].在连续24例患者先前的研究与EGPA [9.[我们观察到70%的患者在诊断中有气流梗阻,13名患者中有超过3年的后续行动的患者有持久的气流阻塞。有趣的是,日常剂量的口腔皮质类固醇的瞬态持续增加经常改善气流阻塞,并部分恢复对立即吸入的β-2激动剂的反应[9.].在另一系列21例成人发病哮喘和EGPA患者中,68%的患者哮喘严重;然而,在启动血管炎的治疗后,哮喘严重程度/对照和肺功能测试改善,并实现了稳定的呼吸表现物缓解[27].在本研究中,平均FEV1在诊断EGPA前1年的预测率为86.1±25.7%,而诊断时的预测率为69.7±24.9%(142例)。在诊断EGPA时开始口服皮质激素(同时43%的患者继续吸入皮质激素、支气管扩张剂和免疫抑制剂),FEV1在诊断后3-6个月预测到89.1±24.9%,75例仍然遵循呼吸系统的75名患者患者78.1±22.8%。此外,46%的患者有FEV1/ FVC <0.7和FEV1<80%在最后一次随访时预测。尽管可用数据可能受到症状持续存在的影响,但由于长期呼吸道部门的持续气流阻塞的患者更容易遵循我们的调查结果,确认持续气流阻塞在长期内存在大部分患者,有助于EGPA的发病率。我们的数据与S的研究相比amson等。[20.],其中83%的EGPA患者在最后一次访问时仍患有慢性哮喘。由于研究设计,无法准确地评估其他发病率,特别是治疗诱导的不良事件的贡献者。
这项研究证实了EGPA患者耳鼻喉科表现的高频率,四分之三的患者患有慢性鼻窦炎,一半的患者患有鼻息肉病。此外,耳鼻喉科的表现对发病率有重要影响,因为超过一半的鼻息肉病病例有复杂的病程,需要手术治疗,28%的病例复发,以及慢性中耳炎导致的听力损失。这与之前几个系列的结果相当[6.那10.那27-29].
egpa患者的过敏率较低,如bottero.et al。[30.].慢性鼻-鼻窦炎多为非变态反应型,表现为慢性上颌鼻-鼻窦炎或富含嗜酸性粒细胞的鼻息肉病。只有四分之一的患者有明确的呼吸道过敏史。当出现哮喘和鼻炎症状时,大多数病例是常年的。
最近,EGPA的CT支气管扩漏特征已经暂时分为气道模式(大多数患者具有阻塞性或混合阻塞性和限制性通气缺陷)和空域模式[17].我们研究中的成像特征不能分类为大约一半的病例,从而限制放射性功能相关性,并且说明在较大的患者的较大群体中可能难以实施细异的放射学研究的细分析。支气管炎的直接特征不常见,含有中心结节,分支不断,芽芽型图案和马赛克衰减分别在14%,12%,10%和4%的病例中发现,表明有些人可能适合该定义最近描述了过稳定性的支气管炎的实体,具有定义EGPA的系统性表现的显着例外[31].肺纤维化32在这个系列中没有观察到。
由于目前没有确定EGPA的诊断标准,所以纳入标准反映了专门中心的常见实践,实际选择分享常见疾病特征和结果的患者。所有患有哮喘,嗜酸性粒细胞和至少一种全身体式表现(除哮喘,肺部或患者)直接归因于EGPA的历史。L.anhamet al。[7.]提出了三种诊断标准,包括:1)哮喘,2)嗜酸性粒细胞率超过1.5×109.L, 3)两个或多个肺外器官的系统性血管炎。然而,这些标准不包括ANCAs(当时没有),当ANCAs存在时,有助于诊断。美国风湿病学会建议的分类准则[22只有在怀疑EGPA和系统性血管炎患者中才有助于诊断。然而,在EGPA的特征性患者中,血管炎的病理诊断是很少的。最近提出临时诊断标准,包括ANCA [2]目前正在评估。
EGPA新定义的一个缺陷[1并不是所有EGPA患者都有明确的多血管炎诊断标准;因此对EGPA术语的有效性提出了质疑[2].我们系列中只有64名患者具有明确的血管炎特征。此外,该系列中的42名患者具有单一的脱果表现,其中包括30个具有明确血管炎的特征。这一发现支持L的概念anhamet al。[7.], EGPA术语不适用于呼吸内科的病人[2那27].
本研究的局限性包括其回顾性设计;然而,这不太可能影响结果,特别是最小估计的频率和类型的呼吸和全身表现。参与这项研究的医生对EGPA有浓厚的兴趣,并常规记录了大量的患者档案,大多数病例在机构数据库中进行了前瞻性收集。包括所有参与组在研究期间的所有连续评估的患者。对严重哮喘或持续性气流阻塞患者比例的估计与我们之前较小的研究一致[9.].严重程度和哮喘控制的评估可能会缺乏准确性,因为没有正式的评估是前瞻性进行;然而,该标准使用(包括住院nonelective和要求的频率为短期口服皮质类固醇)是鲁棒的。影像学特征不集中审查,这可能有疾病的有限归类气道和空域模式。并非所有的患者之前EGPA诊断肺功能数据。虽然不是所有的患者都长期随访肺功能检查供审查,呈现的数据清楚地表明,在患者显著比例与EGPA是持续的气流阻塞有利于发病。用抗白介素5单克隆抗体可以改善肺功能遗体是否治疗进行评估。
总之,这项关于EGPA呼吸系统表现的大型研究表明,哮喘比全身性表现的出现平均早12年,在全身性表现出现前3-6个月,哮喘的严重程度增加,并显示三分之一的患者出现长期固定气流阻塞,尽管吸入和经常口服皮质类固醇治疗。这些发现与EGPA患者的长期治疗有关。
致谢
我们感谢安妮比尔,Raphaele Guelminger,Marion Durand,Chantal Silarakis,Sabrina Zeghmar(全国参考中心,罕见的肺病,法国)贡献,他们为数据收购和入境做出了贡献。
Groupe d'Etudes et de Recherche Sur Les Mathadies Orphelines肺(Germ“O”P)促成该研究的成员如下:Guillaume Beltramo(第戎,法国),Pascal Beynel(Bourg En Bresse,France),伊莎贝尔苑 -财富(圣埃蒂安,法国),伊曼纽尔·戈麦斯(南希,法国),Lize Kiakouama(里昂,法国),Christophe Leroyer(法国),Marianne Levesque(Montréal,加拿大),Anita Mollard(法国斯特拉斯堡,法国),克里斯托夫Rogé(Morlaix,法国)。核心小组的其他成员:Wolfgang总,彼得A. Merkel,Ulrich斑点,让·鲍特,Eric Marchand,Ian Pavord,Johan-Christian Virchow。
欧洲呼吸学会嗜酸性肉芽肿伴多血188bet官网地址管炎工作组成员如下。主席:Loïc Guillevin(法国巴黎),J.F. Cordier(法国里昂),David Jayne(英国剑桥)。秘书:Christian Pagnoux(加拿大多伦多)。副秘书:Vincent Cottin(法国里昂)负责呼吸系统小组,Matthieu Groh(法国巴黎)负责血管炎小组。核心小组:Wolfgang L. Gross (Lübeck and Bad Bramstedt, Germany), Peter A. Merkel (Philadelphia, USA), Renato A. Sinico (Milan, Italy), Ulrich Specks (Rochester, MN, USA)以及主席、秘书和助理秘书。血管炎面板:Chiara Baldini(意大利Pisa), Paolo Bottero(意大利米兰),Bertrand Dunogué(法国巴黎),Matthieu Groh(法国巴黎)(血管炎工作组主席),Wolfgang Gross (Lübeck和Bad Bramstedt,德国),Loïc Guillevin(法国巴黎)(血管炎工作组主席),Julia Holle (Lübeck和Bad Bramstedt,德国),David Jayne(英国剑桥),Charles Jennette(美国北卡罗来纳州教堂山),Alfred Mahr(法国巴黎),Peter A. Merkel(美国宾夕法尼亚州费城),Luc Mouthon(法国巴黎),Christian Pagnoux(加拿大多伦多),Renato A. Sinico(意大利米兰),Ulrich Specks(美国明尼苏达州罗切斯特),Augusto Vaglio(意大利帕尔马)。呼吸顾问小组:Elisabeth Bel(荷兰阿姆斯特丹),Jean Bousquet(法国蒙彼利埃),Jean-François Cordier(法国里昂)(ERS工作组主席),Vincent Cottin(法国里昂)(ERS工作组秘书),Klaus Dalhoff (Lübeck,德国),Marc Humbert(法国巴黎),Romain Lazor(瑞士洛桑),Eric Marchand (Yvoir,比利时), Pasupathy Sivasothy (Cambridge, UK), Ulrich Specks (Rochester, USA) (Core panel ERS task force), Johan-Christian Virchow (Rostock, Germany), Michael E. Wechsler (Denver, USA).
脚注
利益冲突:可以在本文中找到披露www.qdcxjkg.com.
- 已收到2016年1月13日。
- 公认2016年6月1日。
- 版权所有©2016















