文摘
pbi - 4050是一种新型口服活性小分子化合物与anti-fibrotic示威活动在几个纤维化的模型,包括肺纤维化。我们提出我们的第一个临床研究的结果pbi - 4050患者的特发性肺纤维化(IPF)。
这12周的开放研究探索安全、疗效和药物动力学的每日口服剂量800毫克pbi独自- 4050,结合nintedanib或pirfenidone主要是轻度或中度IPF患者。9名患者仅接受pbi - 4050, 16个病人接受pbi - 4050 nintedanib和16个病人收到pbi pirfenidone - 4050。
pbi - 4050单独或结合nintedanib或pirfenidone耐受性良好。药代动力学资料pbi - 4050相似仅pbi - 4050和pbi - 4050 + nintedanib组但pbi - 4050 + pirfenidone组降低,表明药物之间的相互作用。没有明显变化,用力肺活量(FVC), %预测或mL,从基线到第12周pbi - 4050单独或pbi - 4050 + nintedanib。相比之下,显著减少(p < 0.024), FVC % pred被pbi - 4050 + pirfenidone后12周。
没有安全隐患pbi - 4050单独或结合nintedanib或pirfenidone IPF患者。FVC的稳定性之间的基线,第12周看起来鼓励pbi - 4050,结合nintedanib。
文摘
独自pbi - 4050,结合nintedanib证明没有安全隐患,对IPF患者肺功能显示出令人鼓舞的结果http://ow.ly/olQD30myD0E
介绍
特发性肺纤维化(IPF)是一种慢性的、不可逆转的,进步的,通常致命的肺病的原因不明1,2]。它的特点是肺实质的疤痕,肺功能的逐步丧失,呼吸困难和咳嗽,最终导致呼吸衰竭(1]。IPF主要发生在老年人,平均年龄在66年的诊断。在欧洲和北美,IPF的发生率范围从3到9例/ 100 000人每年3),似乎在上升。患病率已报道高达45 - 199每100人000年个人60 - 79岁(4]。生存中值是3 - 4年后诊断(1,5,6]。
当前临床实践指南推荐使用pirfenidone或者nintedanib治疗IPF (1,7]。然而,这两种药物疗效和耐受性方面的局限性。因此,需要额外的治疗方法来治疗这种渐进和致命的疾病8]。
尽管炎症可能发挥作用在IPF初始损伤肺,主要过程是一个epithelial-dependent fibroblast-activated进行性纤维化的过程(2]。引发IPF的能力被认为是肺泡II型细胞自我更新和修复,导致纤维化因子的释放(2,9- - - - - -11]。这种损伤导致成纤维细胞招聘、增殖和分化成myofibroblasts,躺下胶原蛋白和细胞外基质蛋白,导致疤痕形成(10,12,13]。
pbi - 4050, 3-pentylbenzeneacetic酸钠盐,是first-in-class,口服有效,低分子量化合物在临床治疗纤维化疾病的发展。它是一种合成的碳链脂肪酸的模拟显示受体激动剂和拮抗剂受体配体的亲和力对g蛋白耦合GPR40 GPR84,分别导致的减少或逆转纤维化通过调节巨噬细胞,成纤维细胞/ myofibroblasts和上皮细胞(14]。通过绑定GPR40和GPR84 pbi - 4050减少纤维化通过多个anti-fibrotic通路的调节与IPF的发病机制(14]。pbi myofibroblasts - 4050抑制成纤维细胞的分化,废除了的α-smooth肌肉肌动蛋白表达成纤维细胞和随后的细胞外基质蛋白沉积的积累和纤维化。pbi - 4050减少炎性标记物的表达(单核细胞化学引诱物蛋白1,白介素8 (IL)和IL - 6)和pro-fibrotic标记(结缔组织生长因子和白介素)。pbi - 4050也明显变弱在肾脏纤维化,肝、肺、心脏、胰腺和皮肤纤维化模型,包括bleomycin-induced肺纤维化小鼠模型(14]。在后者的模型中,pbi - 4050导致减少了47%的组织学病变描绘成破坏肺架构,肺泡壁厚度和纤维化14]。这些发现表明,pbi - 4050可能是临床上有效的纤维化疾病,包括IPF。
一系列的第二阶段的探索性研究pbi - 4050已经完成或正在进行患者的纤维化疾病,包括IPF、2型糖尿病和代谢综合征和Alstrom综合症。本文报导的数据,第二阶段开放研究评估安全、疗效和药物动力学(PK) pbi - 4050 IPF患者接受nintedanib pirfenidone或没有。
方法
研究设计
这是一个为期12周的单组开放研究(第二阶段NCT02538536)在成人IPF在加拿大的6个地点进行的。它的主要目的是评估的安全性和耐受性pbi - 4050人口这个病人。本研究还探讨了pbi - 4050对肺功能的影响。患者自愿参加的一个子集PK∶评估pbi的PK - 4050。非盲设计选择由于探索性研究的性质。
协议是审查和批准的机构审查委员会的每个参与中心和研究符合赫尔辛基宣言和良好的临床实践指南。所有患者进入研究前提供书面知情同意。
研究人群
患者合格如果他们≥40岁,被诊断出患有IPF由研究者根据指导方针从美国胸科学会(ATS),欧洲呼吸学会(人),日本呼吸协会(青年队)和拉丁美洲胸协会(ALAT) [188bet官网地址1]。高分辨率ct (HRCT)扫描的胸腔进行筛选或在12个月内获得药物治疗的研究开始之前。执行HRCT扫描现场标准化之后体积收购协议,它提供了切面改革(冠状及矢状)的整个肺部,改善异常分布的评估和疾病的程度。尽管所有扫描被送往中央读者(de路易斯塔里夫大学医疗中心,魁北克,加拿大)进行审核,确认IPF由中央读者没有考虑到病人的资格。没有根据肺功能测试合格标准。HRCT也被用来评估任何并发感染。
关键的排除标准包括一个已知的IPF以外的呼吸障碍的诊断;肺气肿的程度大于纤维化的程度变化(蜂窝网状变化)在HRCT上;和一个活跃的吸烟者在3个月前检查,因为吸烟可能恶化IPF的恶化和减少背景anti-fibrotic疗法的疗效[15- - - - - -17]。
治疗
所有患者接受了pbi - 4050在每日剂量为800毫克一次计划治疗12周期间,口服药物4×200毫克凝胶胶囊≥1 h前或饭后> 2 h。这个剂量是根据pbi的PK - 4050从第一阶段的研究18)提供曲线下的面积相同的有效剂量pbi - 4050 (200 mg·公斤−1)bleomycin-induced肺纤维化小鼠模型的14]。这一剂量也在健康志愿者和患者耐受性良好稳定肾功能损害(18]。Nintedanib和pirfenidone获准在研究过程中,就像使用糖皮质激素。硫唑嘌呤和防治禁止基于at /人/青年队ALAT建议对这些药物对大多数IPF患者(1]。
分析
本研究的主要目的是检查的安全性和耐受性pbi - 4050,以下端点:patient-reported不良事件,临床实验室检测、生命体征、ecg和物理考试。不良事件定义为新的事件后新兴研究药品监督管理局或先前的事件严重程度增加研究药品监督管理局后,监控整个治疗期间,直到后续访问(定义为后28天的最后一剂研究药物)。临床实验室检测和测量生命体征在周1、2、6 - 12,在随访;物理检查和记录ecg周1和12和随访。安全端点都是描述性的分析。
二级目标是临床疗效的评估,这意味着从基线测量的肺功能测试(用力肺活量(FVC)和haemoglobin-corrected扩散能力的肺一氧化碳(DLCO))。FVC测量在周1、2、6和12DLCO测量在周1和12;FVC和DLCO测量由当地实验室使用标准程序,按照ATS /人标准(19,20.]。有效性的测量都是描述性的分析。
pbi的PK - 4050也是一个次要的目标,由个人和血浆浓度与在第12周的时间曲线作为单独的亚组的一部分。亚,在禁食条件下收集血液样本在以下时间点:pre-dose和0.5,1,2,3,4,5 - 6 h post-dose。描述性统计是用来描述pbi的PK - 4050。pirfenidone PK概要和nintedanib没有检查在这项研究。
本研究探索性在自然界的主要目标测试pbi的安全- 4050;因此,任何力量或治疗组进行比较分析。
本研究设计为单组试验,所有患者作为一个组来分析主要分析。一个事后分析也是根据其背景IPF患者分组进行药物治疗(pbi - 4050, pbi - 4050 + nintedanib pbi - 4050 + pirfenidone)。作为分析的一部分,探索性进行假设检验在每个治疗组评估从基线到第12周FVC和差异DLCO。探索性的假定值(t)和95% CIs。有最小的缺失数据和归责并不是必要的。多重性测试没有应用疗效端点。
结果
2015年10月至2017年1月,52岁患者筛选和41名患者登记(图1)。除了一个病人完成了研究计划(图1)。剩下的病人(pbi - 4050 + pirfenidone)撤回了早期的研究由于IPF恶化,发生在2周内开始研究药物。9名患者接受pbi - 4050没有背景IPF药物治疗(pbi - 4050年),16个患者接受了pbi - 4050 nintedanib (pbi - 4050 + nintedanib)和16个患者接受了pbi - 4050 pirfenidone (pbi - 4050 + pirfenidone)。9名患者(分别为2、4和3例患者)包含在PK亚组。
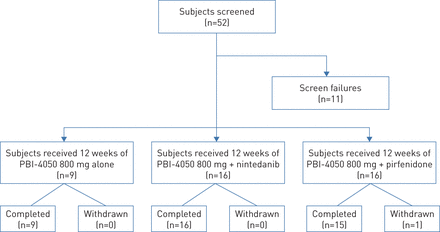
耐心的性格。
基线患者人口统计学和疾病特征
人口和基线特征数据总结表1。总的来说,整个研究人口特征符合IPF的潜在疾病,除了两个病人(95%)有一个明确的通常的间质性肺炎(摘要)模式在HRCT(其余的患者可能摘要模式)。患者年龄从46到83年,大多数患者是男性和白人。其他基线特征被更多的变量在整个治疗组。/平均重量是pbi - 4050 + pirfenidone组高于其他两个治疗组,但这些差异没有达到统计学意义,似乎与一些异常值。pbi - 4050 + pirfenidone组患者通常是最近诊断和有中度或严重疾病的比例高于其他两个治疗组。意味着/ FVC %预测中值两组组合之间的相似但最高仅pbi - 4050组。
安全性和耐受性
所有患者接受至少一个剂量的pbi - 4050是包括在安全分析。大多数病人(∼83%)至少有一个不良事件的总结表2。大多数事件是轻度或中度严重程度和不严重。三个病人经历了严重不良事件,包括腹泻(pbi - 4050 + nintedanib)、呼吸困难和IPF恶化(pbi - 4050 + pirfenidone)和肠胃失调(pbi - 4050 + pirfenidone);这些事件相关pbi - 4050。没有患者死亡,一个病人在pbi - 4050 + nintedanib组严重不良事件(肺炎)与pbi - 4050。此外,一个病人在pbi - 4050 + pirfenidone组停止治疗由于不良事件(IPF恶化)相关的潜在疾病。最常见的不良事件是腹泻、恶心和头痛。没有临床显著变化在临床实验室测试结果,生命体征,体检结果或ecg。
药物动力学
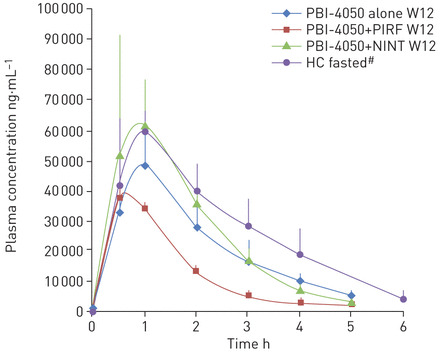
的平均PK概要pbi独自- 4050和pbi - 4050 + nintedanib组相似(图2)。pbi的PK概要- 4050 + pirfenidone集团,然而,演示了一个减少吸收速度或降低最大血浆浓度和更快的新陈代谢(短半衰期)与其他治疗组相比,表明pbi - 4050和pirfenidone之间的药物之间的相互作用。
pbi的药动学特征- 4050 (n = 2)单独或结合nintedanib学院(NINT)举办(n = 4)或pirfenidone (PIRF) (n = 3)在第12周(W12)。数据意味着±sd。HC:健康对照组。#:这些数据从不同的研究。
功效
肺功能测试结果所示表3。只有病人治疗12周都包括在疗效分析。没有观察到显著变化在意味着FVC (% pred或mL)从基线到第12周pbi - 4050 + nintedanib组(0.06%,p = 0.9513;1.87毫升,p = 0.9539)或仅在pbi - 4050组(−1.11%,p = 0.4759;−12.2毫升,p = 0.7959) (表3)。pbi - 4050 + pirfenidone组,有统计学意义的意思是减少FVC (% pred和mL)从基线到第12周(−2.69%,p = 0.0240;−102毫升,p = 0.0124)。这不是影响基线差异的重量,因为没有相关性FVC减少(% pred和mL)及个人体重:62公斤:7%和220毫升;69公斤:10%和280毫升;78公斤:6%和250毫升;84公斤:6%和250毫升;88公斤:5%和200毫升;113公斤:5%,220毫升。
均值变化的意思DLCO% pred从基线到第12周未达到统计上的显著水平在任何治疗组(pbi - 4050单:−4.00%,p = 0.1427;pbi - 4050 + nintedanib:−1.50%, p = 0.1073;pbi - 4050 + pirfenidone:−2.54%, p = 0.1390;表3和图3)。
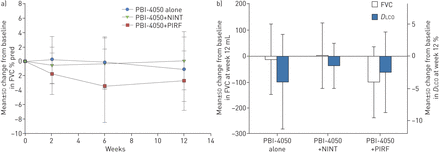
从基线)绝对意味着改变用力肺活量(FVC) %预测与pbi - 4050治疗12周后单独或结合nintedanib学院(NINT)举办或pirfenidone (PIRF)。b)绝对意味着改变基线FVC (mL)及肺一氧化碳(的扩散能力DLCO)(%)治疗12周后pbi - 4050学院单独或结合NINT或PIRF举办。
讨论
积极的结果从bleomycin-induced肺纤维化小鼠模型14第一临床研究)提供了动力pbi - 4050在IPF患者。本研究的目的是评估的安全性和耐受性pbi - 4050治疗12周后,评估其PK在这个患者人群和有效性。这研究是探索性的,不是关键。非盲设计选择最大化接触pbi - 4050和伴随的疗法与nintedanib或pirfenidone被允许。
每日口服pbi - 4050在一天800毫克的剂量·−1在12周内IPF患者耐受性良好,当被单独或结合nintedanib或pirfenidone。没有病人死亡,唯一的严重不良事件(肺炎)被认为是由于潜在的疾病。不良事件通常是轻度或中度严重程度,治疗并没有停止对任何pbi - 4050相关的不良事件。最常见的不良事件是腹泻、恶心和头痛。PK的概要文件之间的相似患者接受pbi - 4050单独或结合结合pirfenidone nintedanib但是是不同的。pbi的PK - 4050年加入pirfenidone显示减少吸收和降低最大pbi观察血浆浓度- 4050和更快的新陈代谢(短半衰期)与其他治疗组相比,表明pbi - 4050和pirfenidone之间的药物之间的相互作用。
肺功能下降的FVC一直在IPF用于监测疾病进展,已被确定为一个独立的预测死亡率IPF (22- - - - - -25]。减少FVC % pred年增长率下降,由肺量测定法,因此适合IPF治疗研究的主要终点。当前临床实践指南推荐使用两个可用anti-fibrotic药物之一,pirfenidone或nintedanib IPF的治疗(1,7]。这两种药物的发展放缓肺功能下降大约50%相比安慰剂在大型3期临床研究26,27]。尽管pirfenidone和nintedanib代表显著提高IPF的治疗,他们并不代表一个治疗药物有显著的和有时无法忍受副作用。因此,临床研究继续关注新疗法治疗的进步,常常是致命的疾病。
一个事后分析的三个治疗组无显著变化,FVC (% pred或mL)在患者接受治疗12周后pbi - 4050单独或结合nintedanib (p > 0.40)。相比之下,FVC显著下降的患者被发现在同一时期pbi - 4050 + pirfenidone集团(% pred p = 0.024;毫升p = 0.0124)。后者发现不影响基线体重的差异。相反,支持的FVC发现PK数据,减少吸收速度或降低最大观察到等离子体浓度和更快的新陈代谢(短半衰期)pbi - 4050 pirfenidone集团。
药物之间的相互作用与pirfenidone已报告在临床IPF研究[28,29日),类似于这pbi - 4050 IPF的研究中观察到的结果。减少疗效观察pirfenidone结合防治作用的24周的随机双盲安慰剂对照研究IPF患者(全景研究)28]。这种组合的调整率显著降低FVC下降与安慰剂相比,pirfenidone(125.6毫升超过6个月与分别为34.3毫升超过6个月;与安全基本未变(p = 0.031),28]。减少暴露也观察到与nintedanib和pirfenidone 28天随机双盲剂量研究日本IPF患者(29日]。曲线下的面积和最大血浆浓度nintedanib及其代谢物在病人接受pirfenidone减少,但是没有变化为pirfenidone PK概要文件(29日]。
总之,没有安全隐患与pbi - 4050单独或结合nintedanib或pirfenidone经过12周的治疗主要是轻度或中度IPF患者。PK pbi概要——仅4050年,结合nintedanib相似但与pirfenidone减少,表明药物之间的相互作用。FVC结果鼓励单独pbi - 4050及结合nintedanib,尽管样本量的限制和研究设计。
确认
医疗援助,写作形式的手稿准备和修改,是莎莉尼·Kanekar (Prometic生命科学Inc .)作者的概念方向,基于作者的反馈。
脚注
本研究注册临床试验(NCT02538536)。研究协议和个人参与者数据,构成结果报道在这篇文章中,后de-identification(文本、表格、数据和附录),将提供给研究人员提供了方法论上的声音建议直接在Prometic.com的首席医疗官。发表文章后的数据将提供9 - 12个月,直到文章出版后36个月。获取、数据请求者将需要签署一份数据访问协议。数据将提供第三方网站。
利益冲突:n·哈利勒没有披露。
利益冲突:h . Manganas报告收到Prometic赠款,在进行这项研究的。
利益冲突:C.J.瑞尔森报告Prometic参与临床试验,在进行研究;和接收赠款和个人费用从勃林格殷格翰集团和罗氏公司,在提交工作。
利益冲突:美国Shapera报告接收:个人费用从阿斯利康演讲;赠款和个人费用参与临床试验站点π,顾问委员会的成员,授予知识的翻译研究从勃林格殷格翰集团加拿大和演讲酬金;赠款和个人费用参与临床试验站点π,顾问委员会的成员,资助临床流行病学研究和演讲从霍夫曼-罗氏公司加拿大谢礼,外提交的工作。美国Shapera参与临床试验作为落实网站πPrometic加拿大和赛诺菲-安万特(sanofi - aventis)外提交的工作。
利益冲突:上午Cantin报告收到Prometic赠款和咨询费用,在进行这项研究的。
利益冲突:p·埃尔南德斯报告接收:拨款支付给他从Prometic机构进行的研究,在研究的行为;个人费用咨询委员会工作从Actelion股价,个人费用咨询委员会工作,从阿斯利康CME会谈,拨款支付给他的机构行为的研究和个人费用从勃林格殷格翰集团顾问委员会工作,授予支付给他的机构进行的研究从CSL贝林,Grifols Cyclomedica,个人费用咨询委员会在葛兰素史克公司诺华工作,Teva, Trudell和赠款和个人费用咨询委员会工作,从拜耳CME会谈,在提交工作。
利益冲突:一些Turcotte没有披露。
利益冲突:J.M.帕克是受雇于Prometic生命科学公司,在进行这项研究的。
利益冲突:J.E.莫兰报告接收个人费用,现金和股票的考虑作为一个员工和股东的Prometic生命科学公司,在提交工作。
利益冲突:广义相对论艾伯特是Prometic生命科学公司的员工。
利益冲突:r . Sawtell受雇于Prometic生命科学公司,在进行这项研究的。
利益冲突:a . Hagerimana受雇于Prometic生命科学公司,在进行这项研究的。
利益冲突:p .三月桂酸甘油酯报告接收个人费用,现金和股票的考虑作为一个员工和股东的Prometic生命科学公司,在提交工作;此外,EP 2427417发布的专利,专利EP 2427416发表和专利EP 2427416悬而未决。
利益冲突:l . Gagnon报告接收个人费用,现金和股票的考虑员工和股东Prometic生命科学公司,在提交工作;专利,专利EP 2427417发布,EP 2427416发表和专利EP 2427416悬而未决。
利益冲突:f·塞萨里报告接收个人费用,现金和股票的考虑作为一个员工和股东的Prometic生命科学公司,在提交工作。
利益冲突:m·科尔布报告接收:从Prometic赠款,在进行研究;赠款和个人费用从罗氏,勃林格殷格翰的发言和葛兰素史克公司,个人费用从基列和热那亚,从Actelion股价和赠款,Respivert, Alkermes公司和Pharmaxis外提交工作。
支持声明:本研究是由Prometic生命科学有限公司融资信息本文已沉积的Crossref资助者注册表。
- 收到了2018年4月6日。
- 接受2018年的10月28日。
- 版权©2019人队。
本文是开放和分布式根据创作共用署188滚球软件名非商业性4.0许可证。