摘要
所有现有的证据表明,慢性血栓栓塞性肺动脉高压(CTEPH)主要是由静脉血栓栓塞引起的,而不是原发性肺血管栓塞原位血栓形成。最初的血栓大小和肺栓塞(PE)复发都可能导致慢性肺栓塞的发展。只有少数特定的亲凝因子,如磷脂抗体、狼疮抗凝剂和ⅷ因子升高,与CTEPH有统计学上的相关性。
将CTEPH视为肺动脉中央动脉栓塞所致的疾病的机制观点过于简单化。根据现有的数据,人们可以推测PE之后可能会发生由感染、免疫现象、炎症、循环和血管滞留祖细胞、甲状腺激素替代或恶性肿瘤所修饰的肺血管重构过程。血浆因素(高凝血、“粘性”红细胞、高血小板计数和不可裂解的纤维蛋白原)和错误的血管重塑过程都导致大血管和小血管的闭塞。内皮功能障碍和内皮-间充质转化可能是重要的,但它们的确切作用仍不清楚。CTEPH尚无动物模型;因此,未来的实验必须同时包括人体组织和临床数据。
慢性血栓栓塞性肺动脉高压(CTEPH)是由有组织的血凝块阻塞主要的(中央或近端大的)肺血管造成的。CTEPH是一种常见的肺动脉高压(PH)变异[1].目前从登记处获得的数据表明,在一般人口中,CTEPH的发病率为百万分之3-30。虽然CTEPH没有表现出静脉血栓栓塞(VTE)的典型风险特征,但该疾病已被证明是症状性肺栓塞(PE)的长期并发症,在事件发生后2年内累计发生率为0.1-9.1% [2- - - - - -11].尽管如此,仍有相当数量的病例可能起源于无症状静脉血栓栓塞[1,12].
定义
CTEPH的定义是在有效抗凝≥3个月后的观察[13]: 1)平均肺动脉压>25 mmHg,肺毛细血管楔形压≤15 mmHg;2)通过肺扫描、多探头ct血管造影或肺血管造影检测到至少一个(节段)灌注缺陷。
血栓栓塞的概念
虽然CTEPH被认为是一种静脉血栓栓塞性疾病,但缺乏典型的血栓栓塞性血浆危险因素。在过去几年中,就更好地了解这种疾病进行了几项重要的观察和澄清[1].在以前的病理系列中,<50%的患者有可识别的凝血、自身免疫或血液学异常[14,15].然而,欧洲CTEPH登记处最近显示,74.8%的CTEPH患者曾检出PE,而56.1%的患者曾检出深静脉血栓(DVT) [16].根据这些数据,将CTEPH视为CTEPH作为经典血栓栓塞的后遗症,其被误导血栓分辨率改性,导致闭塞血管重塑(如图。1)在近端和远端血管。此外,一些(但不是全部)复发静脉血栓栓塞的危险因素存在,如因子VIII (FVIII)升高[17]和狼疮抗凝血(LAC)/抗磷脂抗体(APAs) [18].与肺动脉高压(PAH)累及血管直径<300 μm不同,慢性肺动脉高压通常累及主要血管[13],因此可以通过外科手术清除障碍物[19],即。肺部动脉内膜切除术(豌豆)。图2显示由CTEPH患者手术中除去的典型标本,代表肺血管床的施放,由内皮细胞,平滑肌细胞,成纤维细胞和新鲜血栓组成的组织学检查[1].而大血管疾病的概念(即。CTEPH)和小血管疾病(即。肺动脉高压(PAH)听起来很有趣,CTEPH与PAH重叠的病例,其特征是远端血栓栓塞病变和典型的肺动脉病变。根据手术团队的评估,这些病例被归类为不可手术的CTEPH。
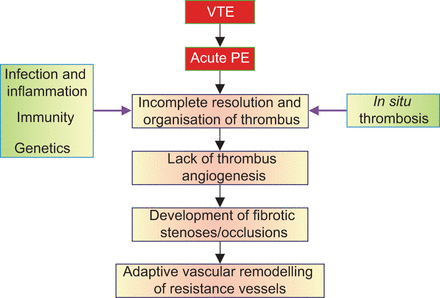
慢性血栓栓塞性肺动脉高压的病理生理学概念方案。静脉血栓栓塞:静脉血栓栓塞;体育:肺栓塞。
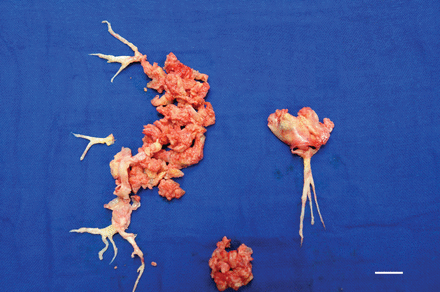
右、左肺动脉的主要血管阻塞(“急慢性血块”)经肺内膜切除术清除。比例尺= 1厘米。
凝固和纤维蛋白溶解
PE后CTEPH发生率低,≥25%的CTEPH患者缺乏症状性PE,以及没有经典的血栓栓塞危险因素,挑战了PE和CTEPH之间的联系[1,20.,21].例如,抗凝血酶、蛋白C和蛋白S的缺乏、凝血酶原G20210A突变和高同型半胱氨酸血症与CTEPH无关。V R506Q因子突变(V Leiden因子)在CTEPH中并不常见[18].然而,在最近的一项回顾性研究中,V莱顿因子在CTEPH中出现的频率高于其他PH (29%)与7.8%;p=0.001), CTEPH中凝血酶原突变更为常见,但差异无统计学意义[22].因子V变异的流行程度取决于被研究的人群。复合缺陷和CTEPH之间的联系是轶事式的[23].已发现LACs/APAs和凝血因子FVIII与VTE和CTEPH有关[13,18,21,22,24,25].
在不同PH值的患者中检测到APAs,但通常是低滴度。在CTEPH患者中发现高的APA滴度,高滴度与LAC相关[18].在CTEPH患者中,LAC的检测表明普癌态;非网络栓塞pH值的患者可能并非如此,其中其他免疫学和炎症机制可能涉及[26,27].CTEPH患者中多重阳性试验的发现引起了人们的兴趣,因为最近的一份出版物表明,三阳性试验中静脉血栓栓塞(VTE)复发的风险更高[28,29].
在122例CTEPH患者、88例非血栓栓塞性PAH患者和82例年龄和性别匹配的健康对照者中测定FVIII和血管性血友病因子抗原(VWF:Ag)的血浆浓度[17].VWF升高:Ag和FVIII (>230 IU·dL−1)在CTEPH患者中比肺动脉高压患者和对照组更常见(41%)与分别为5%和22%)。PEA成功后,FVIII血药浓度没有下降;相比之下,前列腺素治疗缓解PH后血浆FVIII下降[30.].这些数据提示CTEPH患者FVIII值升高可能是疾病进程的原因。
静脉血栓栓塞的急性发作可能与发生CTEPH的风险有关。在一项前瞻性队列研究中,共招募了305例有症状的静脉血栓栓塞患者,其中223例为首次PE, 58例既往DVT, 24例既往PE [8].在前两年后,第一组中CTEPH的发病率为3.8%。在另外两组中,CTEP的累积发血分别为5.2%和33.3%。在多变量逻辑回归模型中,较小的年龄(或1.79,95%CI 1.23-2.56),PE(或19,95%CI 4.5-79.8),PE的特发性临床介绍(或5.70,95%CI 1.41-22.97)和PE诊断时间(或2.22,95%CI 1.49-31)的较大灌注缺陷与CTeph的风险增加有关的相关缺陷[8].在最近一项针对110例急性PE患者的小型前瞻性队列研究中,CTEPH在2年内的发病率为9.1%;6例(5.4%)在可变临床随访中确诊,其余病例是根据超声心动图和指标事件后2年的临床表现确诊的[11].在多元回归模型中(每年的相对风险(RR)1.2,95%CI 1.0-1.3)和先前和复发性PE的组合与CTEPH(RR 5.7,95%CI 1.5-22.0)相关.在一个大的回顾性队列研究中,687名连续pH值患者参加了四个大型欧洲数据库[25].433个患者被诊断出患有CTEPH和254年nonthromboembolic博士进行逻辑回归分析在585例显示之前和复发性静脉血栓栓塞的风险明显增加CTEPH(或4.52,95%可信区间2.35 - -9.12或14.49,95%可信区间5.40 - -43.08,分别)。慢性静脉溃疡(可视为DVT的晚期后遗症)在CTEPH患者中更为常见(OR 2.84, 95% CI 0.99-9.00)。
在一项对254名受试者进行的前瞻性队列研究中,首次急性PE发作后平均观察3.8年,0.8%发生了CTEPH [3.].有趣的是,如果只考虑有特发性临床表现的PE患者,该发病率上升到1.5%,这与P观察到的相似engo等.[8]但是虽然在被诊断患有CTEPH的患者中没有观察到VTE复发。然而,排除癌症患者和具有主要血栓性疾病的人,急性PE发作的相对较低的严重程度和对抗凝血治疗的非常仔细的管理可能影响了CTEPH的真正发病率。在另一种潜在的疑似PE患者的前瞻性队列研究,320名客观确诊的诊断患者被出现了22.1 YRS [6].这项研究的独特之处在于,它对所有患者进行了连续的肺扫描。CTEPH发生率为1.3%;CTEPH患者肺血管阻塞的中位范围约为60%。在连续的肺部扫描中没有发现复发性PE的证据。然而,PE复发和CTEPH之间的关联可能被低估:1年死亡率很高,4例CTEPH患者中有3例在研究之前记录过DVT发作,没有任何PE的客观影像学检查。P奥利等.[31对239例首次出现PE的患者进行了前瞻性观察,经3年的中位随访,发现CTEPH发生率为0.4%。静脉血栓栓塞复发和停用抗凝治疗后d -二聚体水平高与CTEPH风险增加无关。值得注意的是,静脉血栓栓塞复发患者中没有一例出现高收缩期肺动脉压。然而,缺乏有关指标事件严重程度的数据和排除癌症患者引入了选择偏倚。高达14%的受试者采用了基于d -二聚体检测的治疗策略,以减少静脉血栓栓塞的复发,这可能影响了CTEPH的发生率。K洛克等.[5]调查了866例未被选中的连续诊断为PE的患者CTEPH的发生情况。如果没有诊断出CTEPH, 588名幸存者在指数事件发生后的中位时间为3.7年进行了超声心动图研究;在疑似慢性teph的情况下,为确认目的进行了诊断程序。CTEPH的累计发生率在总体人群中为0.57%,在无因PE患者中为1.5%。复发性PE与发生CTEPH的风险不相关。然而,缺乏与急性指数事件相关的数据,随访时间可变,以及将约30%的合格受试者排除在外,显著限制了检测CTEPH的能力。
Riedel等.[20.]对76例急性PE后≥2个月的血流动力学进行了评估。随后对第一次检查后存活1-15年的受试者进行了血流动力学研究[32].基线时平均肺动脉压>30 mmHg与随访期间进一步升高相关(从47.1±14.6到55.3±10.1 mmHg, p<0.05),而正常的平均肺动脉压后期没有升高。
在一个小的前瞻性队列研究RIbeiro等.[7]在急性事件发生后1年内对78例患者进行了连续超声心动图检查,随后随访5年以上。在最初诊断PE时检测到收缩期肺动脉压>50 mmHg与1年后PH风险增加3倍相关[7].值得注意的是,四分之三的持续性PH患者接受了PEA治疗。在301例首次急性PE患者的队列中,在PE急性期检测到右心室功能障碍与3年随访后静脉血栓栓塞(VTE)复发的近4倍风险相关(风险比3.79,95% CI 1.8-7.8) [33].然而,早期发现肺动脉压明显升高是否与真正的急性PE伴有右心室劳损有关,还是与CTEPH的早期表现有关仍是一个问题。
综上所述,目前可获得的证据证实,至少一些急性和复发静脉血栓栓塞的血栓前危险因素在CTEPH患者中普遍存在,而纤溶因子已被证明是旁观者而不是疾病的介质[34].一般来说,急性PE发作的临床表现,以及可能的静脉血栓栓塞的复发,增加了发生CTEPH的风险。最近的研究表明,深静脉系统中持续残留的血栓物质与VTE复发的高风险相关,并确定了一组延长抗凝治疗是有益的患者[35].
目前的证据存在几个局限性:患者队列异质性大,死亡率也不相同;研究通常是回顾性的,没有充分的控制;最初栓塞发作的严重程度通常是未知的;,然而,很难排除既存博士最近欧洲病人群体的描述表明以前的体育证实了以往的四分之三的病人和静脉血栓栓塞在其中一半提供有力的证据来证明的血栓栓塞性疾病,尽管持续争论这个问题(36].
其他风险因素
非血浆性危险因素如脾切除术、脑积水治疗的心室-心房(VA)分流术、炎症性肠病和慢性骨髓炎与CTEPH的高发生率和较差预后相关[21,25,37].在最近一个涉及3个欧洲PEA中心的回顾性数据库中,来自687名CTEPH患者的数据与参与机构的非血栓栓塞的毛细血管前PAH队列进行了比较。VA分流和感染的起搏器(OR 76.40, 95% CI 7.67-10351;p<0.001),脾切除(OR 17.87, 95% CI 1.56-2438;p=0.017)和非o型血(OR 2.09, 95% CI 1.12-3.94;p=0.019)多与CTEPH相关。甲状腺替代治疗(OR 6.10, 95% CI 2.73-15.05;p<0.001)和恶性肿瘤史(OR 3.76, 95% CI 1.47-10.43;p=0.005)成为新的CTEPH危险因素。法国PH项目最近的数据报告了17例Port-A-Cath®(Smiths Medical, Grasbrunn, Germany)中心静脉通路系统,包括CTEPH [3830%的细菌培养呈阳性葡萄球菌epidermidis这支持了静脉注射管感染是慢性荨麻疹的病理诱因的概念。
病理生理学概念和动物模型
“炎性血栓形成”概念
在大多数受试者中,静脉血栓通过复杂的降解和组织过程去除,包括血管壁的适应性(大部分是积极的)重塑和再通。这一过程与伤口愈合过程中肉芽组织的形成非常相似。白细胞招募和血管生成在血栓溶解过程中起重要作用。最初是中性粒细胞,随后是单核细胞被招募成有组织的血栓。当单核细胞招募减少时,血栓溶解严重受损。单核细胞能够表达和分泌大量的化学引诱剂(例如单核细胞趋化蛋白(MCP)-1)、生长因子(例如血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)、转化生长因子(TGF)-α和-β1)和蛋白酶(例如尿激酶型纤溶酶原激活剂和基质金属蛋白酶)。炎症标记物,例如c反应蛋白(CRP) [26,肿瘤坏死因子-α [39]和MCP-1 [40)在CTEPH患者的血浆和血栓组织中均有升高,与血流动力学相关。
“血管生成不足”的概念
在CTEPH中,血管生成依赖于来自全身支气管动脉的血管导管。在肺动脉闭塞后,这些血管通常会扩散到肺动脉内,原有的支脉会被打开。在愈合或血栓形成的过程中,血管生成的正调节因子占主导地位,内皮被激活,穿透闭塞的血栓[41].先前的动物研究表明,静脉壁再通可能发生在血栓形成的24小时内。在溶解的早期阶段,血栓开始从静脉壁收缩和收缩,导致血栓体和静脉壁内膜之间形成细胞内衬袋。血管通道的出现与VEGF和bFGF的表达有关,它们被认为是血栓内新生血管形成的驱动因素[42].在PEA材料中检测到胶原分泌细胞[43],参与导致不支持血管生成过程的内皮细胞功能失调的微环境的形成[44].先前的动物研究表明,给VEGF可以增强动物模型中的血栓溶解[45,46].然而,某些实验装置拒绝了这个观察结果[47].最近的实验数据表明,刺激静脉壁的缺氧诱导因子-1α水平会导致血管生成驱动力增加,促进静脉再通和血栓溶解[48].这些观察结果,以及通过差异显示分析和RT-PCR检测到的CTEPH障碍中血管生成基因表达的不足,表明肺血管阻塞的解决失败可能与血管生成的不足有关。
血管病理学
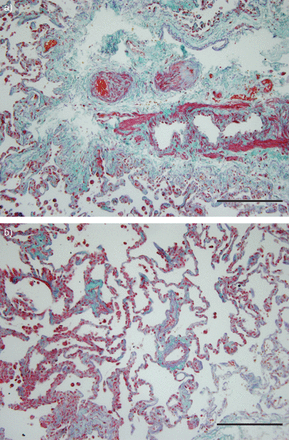
根据目前的知识,CTEPH是一种“双”肺血管疾病,合并血栓诱导的大血管血管重构,并伴有一种小血管疾病(肺动脉病)[1,58].血管病变包括远端肌肉扩张、同心层状内膜纤维弹性增生和偏心内膜纤维化、内侧肥大和偶尔的丛状病变。后者似乎在有专用饲料容器的地区占主导地位(图3),而在血管狭窄或闭塞的远端,观察到血管稀少(图3 b).CTEPH患者的肺动脉病变目前被解释为内皮功能障碍合并不对称二甲基精氨酸异常积累的后遗症[59],平滑肌和内皮细胞的异常增殖,成纤维细胞和平滑肌细胞迁移,抑制血管平滑肌细胞的凋亡原位血栓形成(60,61].这种紊乱的关键因素是前列环素和前列环素合成酶,这已被发现在PAH中缺乏,并在生理上抑制RhoA/ RhoA激酶的作用,RhoA/ RhoA激酶是一种小的细胞内鸟苷三磷酸酶,在组织因子表达、核因子-κB诱导和细胞周期素D转录方面具有重要的信号传导功能。目前尚不清楚小血管疾病的程度是否与患者在诊断为慢性血管栓塞性脑炎之前出现PH的时间长短有关[62].最近的数据表明,在有相关疾病的患者中,小血管疾病的发病率可能更高[37],例如应用VA分流术治疗脑积水、脾切除术、炎症性肠病、低度恶性肿瘤和甲状腺替代治疗。此外,肺血管反应性被认为反映了阻力血管的功能反应性,与预后平行[63].更详细地说,诊断性右心导管吸入一氧化氮后平均肺动脉压降低≥10%是较好的预后预测因子。最近,葡萄球菌感染的观察证实了这两种在活的有机体内[38,57)和一项涉及滞流静脉血栓小鼠模型的详细分析[57].金黄色葡萄球菌或葡萄球菌epidermidis是导致多达一半设备感染的原因,细菌病原体促进纤维性伤口愈合[64].在小鼠模型中,葡萄球菌感染延迟血栓溶解,同时TGF-β和结缔组织生长因子上调,这为血栓感染可能与血栓不溶解相关的假设奠定了基础。基于这些数据,我们可以推测,对主要静脉血栓栓塞及时进行抗生素治疗可能会防止CTEPH的发展。
慢性血栓栓塞性肺动脉高压的“继发性血管疾病”在一项临床研究过程中在肺内膜切除术中获得的肺活检中观察到。a)肺动脉小动脉三色染色,直径<200 μm,内膜纤维化,平滑肌肥大;B)来自完全闭塞的肺动脉瓣的肺标本。注意血管的缺乏。现有血管不显示平滑肌细胞肥大和内膜病变。两个肺标本来自同一患者(不同于如图。2).比例尺条= 200μm。
CTEPH患者的肺血管壁增厚可能是由于外膜成纤维细胞、循环的前体细胞/前体细胞和/或肌成纤维细胞的增殖,形成有血管新生的纤维斑块和含胆固醇的动脉粥样硬化斑块[65].加州大学圣地亚哥分校(San Diego, CA, USA)对一系列的血栓栓塞性阻塞进行了分析,血栓在不同阶段的重塑,肉芽肿伴结节病,以及一个表现为炎性肌纤维母细胞瘤、原发性或转移性恶性肿瘤特征的罕见病例。并观察到孤立性肺动脉炎[58].15%的病例有明显的炎症[14].CTEPH发病机制中炎症的作用已被研究强调,说明了CTEPH中从肺主要血管分离出来的细胞上CRP受体LOX-1的表达[27].从CTEPH患者的动脉内膜切除组织中分离的细胞表现出不同的形态表型。平滑肌细胞(SMC)标记物平滑肌α-actin免疫荧光染色在大多数细胞中检测到;然而,一些细胞显示明确的肌动蛋白丝结构,一些细胞质染色更普遍,还有一些染色很弱。除了更原始的间充质前体细胞/祖细胞的典型标记外,纤维母细胞标记波形蛋白染色非常强烈,其中一些具有过度增殖、锚定不依赖、侵袭性和血清不依赖的特征[66].此外,RT-PCR确认存在指示原始细胞类型的mRNA转录物。在体外,研究表明,从PEA标本中收获的肌成纤维细胞样细胞诱导了内皮细胞向间充质细胞的转化,雷帕霉素有效地抑制了这种转化[44].在PEA期间从近端肺动脉分离培养的细胞中也观察到类似的增殖特征[67].这些数据表明,在闭塞血管中,除了外膜成纤维细胞的转徙或转分化外,还可能发生前体细胞向SMC类型的增强或不受控制的分化。这些机制表征了CTEPH中观察到的血管重构过程[43,68].
结论和展望
CTEPH是PH的一个独特子集,因为它具有可治愈性。因此,它也可以作为研究右心室功能和肺血管组织的一个优雅的模型。在欧洲,CTEPH研究协会已经建立了一个独特的数据库和平台,以推动研究和教育这一重要的肺血管医学分部。
脚注
本系列之前的文章。1号:Delcroix M, Vonk Nordegraaf A, Fadel E,等.慢性血栓栓塞性肺动脉高压的血管和右心室重构。欧元和J2013;41: 224 - 232。
感兴趣的语句
im Lang的兴趣声明可以在www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2012年3月22日。
- 接受2012年5月10日。
- ©2013人队