摘要
背景
慢性血栓栓塞性肺动脉高压(CTEPH)与近端肺动脉阻塞和血管重构有关。我们推测肺动脉平滑肌(PASMC)和内皮细胞(PAEC)可能积极参与CTEPH患者近端肺血管壁重构。我们目前的目的是对CTEPH患者大动脉的PASMC和PAEC进行表征,并研究它们在血管重构中的潜在参与作用。
方法
来自CTEPH、非血栓栓塞性肺动脉高压(PH)和肺供体的近端PAEC和PASMC的原代培养已经建立。PAEC和PASMC使用特异性标记进行免疫荧光表征。用免疫荧光和免疫印迹法研究了平滑肌特异性标记物在肺血管壁内的表达。研究了PASMC和PAEC的有丝分裂活性和迁移能力在体外.
结果
PAEC在其表面表达CD31,在Weibel-Palade体中表达von Willebrand因子,并吸收乙酰化LDL。PASMC表达多种分化标记,包括α-平滑肌肌动蛋白(α-SMA)、desmin和平滑肌肌球蛋白重链(SMMHC)。在CTEPH和非血栓栓塞性PH患者的血管组织中,α-SMA和desmin的表达较肺供体下调;与非血栓栓塞性PH患者相比,CTEPH患者血管组织中desmin表达也下调。低比例的α-SMA阳性细胞在CTEPH患者近端肺动脉内膜中表达desmin和SMMHC。血清诱导的PAEC和PASMC的有丝分裂活性以及PASMC的迁移能力仅在CTEPH中增加。
结论
修改PASMC和PAEC的增殖和/或迁移反应在体外与PASMC增殖表型相关,提示PASMC和PAEC可能有助于CTEPH的近端血管重构。
背景
慢性血栓栓塞性肺动脉高压(CTEPH)是肺动脉高压的主要原因之一。CTEPH的特征是存在与肺动脉近端纤维性狭窄相关的未解决的血栓栓子。这导致近端肺动脉阻塞,肺血管阻力增加,肺动脉高压和进行性右心衰。它可能是由单次或复发性肺栓塞和/或局部血栓形成引起的。近端肺动脉闭塞,经肺内膜切除(PEA)可切除,是CTEPH的主要特征[1].
造成永久性血管阻塞的机制仍然知之甚少。近端病变与动脉粥样硬化斑块有相似之处,包括中质增厚和新生内膜形成[2].血栓形成和/或溶栓的调节失调已被描述[3.- - - - - -5]以及炎症疾病的发病率上升[6]及轻度全身炎症[7].尽管在近端血管病变中观察到血管重塑和细胞增多[8],细胞的主角尚未被确定,内皮细胞(PAEC)和平滑肌细胞(PASMC)各自的参与仍未被探索。
CD31或PECAM-1(血小板内皮细胞粘附分子-1)是免疫球蛋白超家族的成员,是一种跨膜糖蛋白,在所有人肺EC中均有表达[9].血管性血友病因子(vWF)是一种介导血小板粘附于内皮下的糖蛋白,主要由内皮细胞产生,储存在Weibel-Palade小体中[9].内皮细胞表达的清清剂受体可与荧光dii标记的乙酰化低密度脂蛋白(ac-LDL)结合,目前被用于表征EC [10].α-平滑肌肌动蛋白(α-SMA)、desmin和平滑肌肌球蛋白重链(SMMHC)是参与平滑肌收缩功能的细胞骨架组成蛋白,在平滑肌分化过程中存在差异表达[11].
强化血栓形成似乎不是肺动脉近端永久阻塞的主要原因。因此,我们假设来自CTEPH患者肺动脉壁的PAEC和PASMC可能是CTEPH生理病理的积极贡献者。我们目前的目标是i)从CTEPH患者的近端和(亚)节段肺动脉壁分离EC和SMC, ii)使用特异性标记进一步表征它们,iii)研究它们的增殖和迁移能力在体外.
方法
研究人群
近端肺血管材料来自i) 16例CTEPH患者,ii) 12例非血栓栓塞性肺动脉高压(PH)患者(4例特发性肺动脉高压(PAH), 1例与先天性心脏病相关的PAH, 7例由肺部疾病引起的PH)和15例肺供体。肺移植或PEA时右心导管检查血流动力学参数。研究方案由鲁汶大学医院伦理委员会批准,参与者给予书面知情同意。
组织收集
在肺移植或PEA时,采集了一块2cm的近端肺动脉(图1&1 b).用于分离细胞的材料不含任何血栓性物质,包括基质(仅是PEA样本的一部分)和新生内膜(见图)1).在PEA时也采集了一段段或亚段状肺动脉(直径5 ~ 10mm)。
Neointima厚度
用4%多聚甲醛固定动脉,石蜡包埋,7 μm切片。切片进行脱蜡和复水处理。细胞核和细胞质分别用苏木精和伊红染色。用Verhoeff's van Gieson法对弹性蛋白进行染色。新生内膜厚度以管腔到内弹性层的最大距离为测量值。
PAEC和PASMC的分离
通过胶原酶消化,然后使用抗cd31单克隆抗体标记的小球进行免疫磁分离(Miltenyi Biotec, Utrecht, The Netherlands)获得近端PAEC。使用外植体-生长法分离近端PASMC [12].所有实验都是用传代次数少于7次的细胞进行的。
细胞培养基
EC在M199培养基(Life Technologies, Gent, Belgium)中培养,添加20%胎牛血清(FBS), 100 U.mL-1青霉素,100 μg.mL-1链霉素,1.25 μg.mL-1fungizone(生命科技),10 U.mL-1肝素(Aventis,布鲁塞尔,比利时)和5 ng.mL-1α-FGF (R&D Systems, Abington, UK)。SMC在DMEM培养基(Life Technologies)中添加10%胎牛血清、青霉素、链霉素和真菌素。
肺动脉组织的细胞特性和免疫荧光
PAEC表型的特征是用diI-Ac-LDL标记细胞(Tebu, Le Perray en Yvelines,法国)和使用抗CD31和抗vWF抗体的免疫荧光(Dako, Heverlee,比利时)。使用抗α-SMA、desmin (Dako)和人类SMMHC抗体(生物医学技术,Stoughton, MA)对PASMC表型进行免疫荧光表征。在10 μm组织冷冻切片上用免疫荧光法定位了α-SMA、desmin和SMMHC。
西方墨点法
利用针对α-SMA或desmin的特异性一抗,通过Western blotting对肺血管组织中的α-SMA和desmin进行鉴定。β-肌动蛋白(Abcam, Cambridge, UK)被用作内部对照。用辣根过氧化物酶标记的驴抗兔抗desmin IgG和抗小鼠抗-αSMA和抗-β-actin IgG (Jackson, Suffolk, UK)作为二抗。过氧化物酶染色用化学发光试剂盒(GE Healthcare,白金汉郡,英国)进行,并在室温下曝光。使用photopprint成像系统和BIO-1D软件(Vilber Lourmat, Marne-la-Vallée, France)量化蛋白表达。
PASMC和PAEC增殖
未汇合的PASMC和PAEC在添加0.2%胎牛血清的培养基中饥饿24 h。分别在5%和10% FBS外加0.5 μCi.mL条件下测定PAEC和PASMC的有丝分裂活性-1(3.胸腺嘧啶(74 GBq.mmol .-1;(GE医疗保健公司),持续48小时。放射性掺入按先前描述的方法进行量化[13].[3.H]-胸苷激酶结合试验已通过PASMC和PAEC的细胞计数进行验证。
PASMC迁移
未融合的PASMC在DMEM中添加0.2%胎牛血清后饥饿24 h。如前所述,在10%胎牛血清存在下,使用划伤试验评估PASMC迁移,持续36小时[12].
统计分析
使用SAS Enterprise Guide 4.1 (SAS Inc., Cary, North Carolina)和GraphPad Prism 4.01 (GraphPad Software Inc., La Jolla, California)进行数据库管理和统计分析。数据以平均值±标准差表示。2组或3组之间的差异采用学生t检验或双向方差分析检验,然后进行事后检验。p≤0.05为有统计学意义。所有p值均为2侧检验。
详细的“方法”部分可以在附加文件中找到1.
结果
收集肺血管材料的患者特征显示在表格中1.附加文件中有一个包含患者个人特征的表格2.
mPAP:平均肺动脉压;RAP:右心房压;TPR:肺总血管阻力;CO,心输出量。在PEA或肺移植时测量了血流动力学参数。
CTEPH患者和非血栓栓塞性PH患者的平均肺动脉压(mPAP)相似,而与非血栓栓塞性PH患者相比,CTEPH患者表现出明显更高的总肺阻力(p = 0.04)和较低的心排血量(p < 0.0001)。收集到的肺血管物质包括新生内膜和中膜(图1 c而且1 d).然而,CTEPH和非血栓栓塞患者的内膜厚度有很大差异,中位数(范围)为1.54 mm(0.46-2.08)。vs.0.26 mm(0.04-1.34),分别(Mann-Withney, p < 0.0001)。
PAEC和PASMC表征
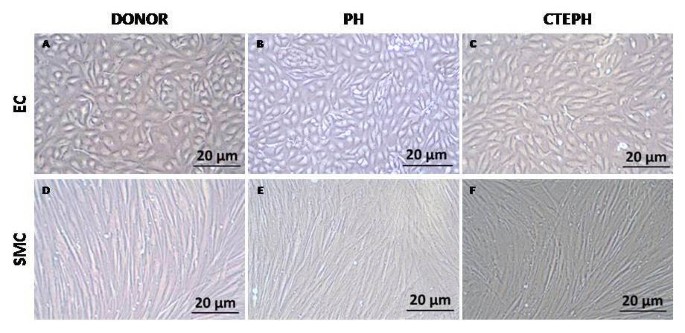
从肺供体肺动脉近端分离出的近端PAEC,非血栓栓塞性PH和CTEPH患者具有典型的“鹅卵石”形态,而PASMC显示“丘陵和山谷”组织(图)2).
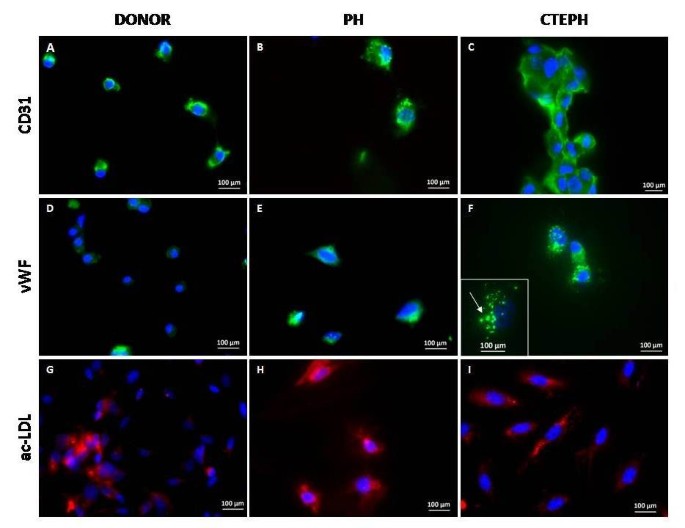
PAEC来源于肺供体,非血栓栓塞性PH和CTEPH患者在其表面表达CD31,在Weibel-Palade体中含有vWF,并能够吸收乙酰化的LDL(图3.).
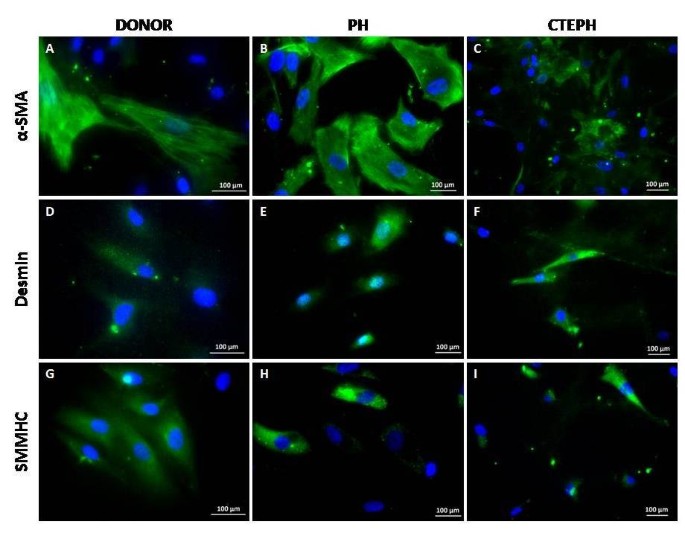
来自肺供体、非血栓栓塞性PH和CTEPH患者的PASMC人群显示α-SMA纤维并表达desmin和SMMHC(图4).
分化标志物在肺动脉组织中的表达和分布
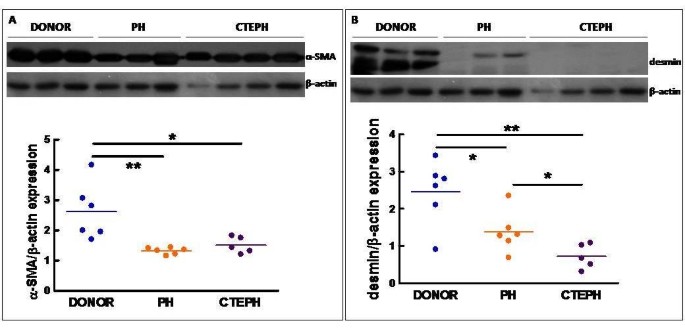
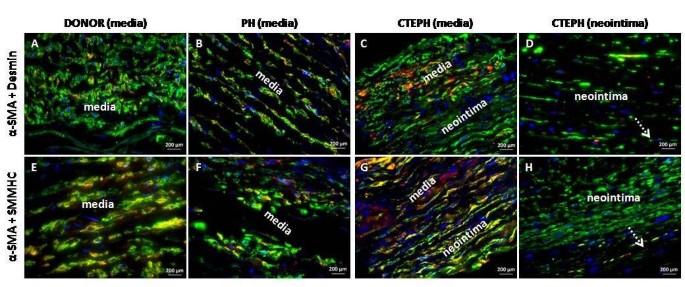
与肺供体相比,非血栓栓塞性PH和CTEPH患者的肺动脉组织中α-SMA的表达分别显著降低50%和42%(图5).同样,与肺供体相比,非血栓栓塞性PH和CTEPH患者的肺动脉组织中desmin的表达分别低44%和71%(图5 b).肺供体、非血栓栓塞性PH和CTEPH患者培养液中的大多数α-SMA阳性细胞表达desmin(图a, b, c)和SMMHC(图6e, f, g),而CTEPH患者新生内膜中只有较低比例的SMC被α-SMA和desmin联合染色(图6 d)或α-SMA和SMMHC(图6小时).
肺动脉中SMC分化标志物的表达.冰冻后的肺动脉均质裂解,取100 μg蛋白样品进行SDS-PAGE电印迹分析。α-SMA的免疫检测(一),肌间线蛋白(B)和β肌动蛋白(A, B)使用特异性抗体进行了Western blotting。用标准标记物以kDa估算蛋白质分子质量。蛋白表达用Western blotting密度法定量。结果用α-SMA或desmin的带体积与β-actin的带体积之比表示。供体(n = 6), CTEPH (n = 5)和PH (n = 6)。PH组:圆,多环芳烃;不含PAH-PH。(一)方差分析,p = 0.003;*p < 0.05;**p < 0.01。(B)方差分析,p = 0.002;*p < 0.05;**p < 0.01。
PAEC和PASMC的增殖和迁移
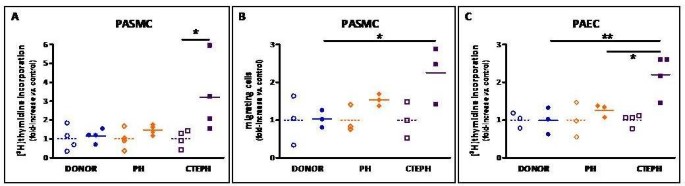
在10% FBS存在的情况下,与PH-PASMC(48%)和供体- pasmc(16%)相比,CTEPH-PASMC的有丝分裂活性显著增加220%(图)7一个).与PH-PASMC(54%)和供体- pasmc(3%)相比,在存在10% FBS的情况下,CTEPH-PASMC的迁移能力显著增加了126%(图)7 b).在5%胎牛血清的存在下,与PH-PAEC(26%)和供体paec相比,CTEPH-PAEC的有丝分裂活性显著增加(增加120%)(图)7 c).
肺近端血管细胞增殖和迁移能力.(一)从肺供体(n = 4)、非血栓栓塞性PH (n = 4)和CTEPH患者(n = 4)中分离的近端PASMC的有丝分裂活性。在0.2%(对照)或10% FBS + 0.5 μCi.mL时测定有丝分裂活性-1(3.H]-胸腺嘧啶36 H。方差分析,p = 0.02;*p < 0.05。(B)从肺供体(n = 3)、非血栓栓塞性PH (n = 3)和CTEPH患者(n = 3)分离的近端PASMC迁移能力。在0.2% FBS培养基中饥饿亚融合细胞24小时。在0.2%(对照)或10%胎牛血清存在36小时的情况下,使用划伤试验评估PASMC迁移。方差分析,p = 0.02;*p < 0.02。(C)从肺供体(n = 1)、非血栓栓塞PH (n = 3)和CTEPH患者(n = 4)中分离的近端PAEC有丝分裂活性。如前所述,在0.2%(对照)或5%胎牛血清中测定有丝分裂活性。方差分析,p = 0.0002, *p < 0.02, **p < 0.002。开放的符号, 0.2% fbs;简单的符号, 10%。PH值组:圆多环芳烃;三角形,不含PAH-PH。(A, B)或5%(C)的边后卫。对每个患者进行1 ~ 3个独立实验,共3个重复。对于肺供体EC,进行3次独立实验,每次重复3次。
cteh患者(亚)节段肺动脉的细胞组成
α-SMA染色肺亚节段动脉(图8)和CD31(图8 b)抗体显示轻度新生内膜(图8)和完整的内皮(图8 b).在5%和10%胎牛血清存在的情况下,从CTEPH患者节段或亚节段肺动脉分离出的PAEC和PASMC的有丝分裂活性分别增加了184%和156%(图8 c而且8 d).
讨论
本研究的目的是从CTEPH患者的大动脉中分离出PASMC和PAEC,并研究PASMC和PAEC在导致CTEPH患者大动脉永久阻塞的血管重构中的潜在作用。我们的结果显示,在CTEPH患者中,肺近端血管组织中平滑肌分化标志物下调,肺血管细胞增殖和迁移能力增强在体外提示PASMC和PAEC对CTEPH患者近端肺动脉血管重构的潜在贡献。
使用原代细胞培养意味着选择具有增强生长潜力的细胞。然而,CTEPH和PH细胞都是按照相同的方法分离出来的,所有的实验都是用传代次数较少的细胞进行的。PEA材料通常由阻塞肺动脉的血栓性和纤维性物质组成,我们收集的40%的PEA材料中没有任何可见的血栓性物质。然而,用于建立原代细胞培养的材料不含任何血栓性物质,包括部分培养基和增厚的新生内膜。从非通栓性PH患者和肺供体分离出的肺动脉近端包括整个中膜和中度增厚内膜。因此,在所有组患者中,PAEC和PASMC都是从血管壁分离出来的,而不是从血栓分离出来的。此外,尽管在CTEPH和非血栓栓塞性PH中暴露在类似的高压下,来自非血栓栓塞性PH患者的肺血管细胞与来自无血栓栓塞性PH肺供体的肺血管细胞具有类似的增殖和迁移特性。最后,与近端动脉相比,来自CTEPH患者的亚节段肺动脉仅表现出轻微的内膜增厚和完整的内皮。PASMC和PAEC均具有增强的增殖能力,与近端肺动脉相似。
肺血管细胞特征
部分CTEPH患者的血栓和溶栓调节异常[5]不足以解释腔内血栓组织和纤维血管闭塞。此外,近端肺血管重构甚至可能在没有血栓形成的情况下发生[14].在近端血管病变中观察到细胞增多[8,但是细胞中的主角还没有被清楚地识别出来。很少有研究集中于肺动脉细胞在疾病发病机制中的意义。Lang和同事研究了CTEPH患者主要肺动脉来源的EC分泌的组织纤溶酶原[15].Firth和Yao强调了CTEPH患者肺血管组织中内皮细胞和多功能间充质祖细胞的存在[16,17].考虑到CTEPH的生理病理仍不完全清楚,从CTEPH患者中建立特征良好的肺近端血管细胞原代培养,应该是揭示导致CTEPH中未解决血栓持续存在的机制的一项资产。PAEC在其表面表达CD31,在Weibel-Palade体中表达vWF,并能够吸收ac-LDL,证实了我们的PAEC原代培养物的同质性,如别处所述[18].因此,温和的酶解结合纯化CD31抗体偶联磁珠可以建立均匀的PAEC原代培养。尽管CTEPH和非血栓栓塞患者的内膜材料存在差异,但两种原代培养的PASMC都有SM分化标志物的表达,包括α-SMA、desmin和SMMHC。
PASMC增生性表型
在平滑肌分化标志物的肺动脉组织含量方面,CTEPH中晚期平滑肌分化标志物desmin的表达明显低于ph。相比之下,两组患者中早期平滑肌分化标志物α-SMA的表达相似,提示CTEPH- pasmc可能向增殖表型转变。此外,内侧和PH-PASMC同时表达α-SMA和desmin或SMMHC,而内膜CTEPH-PASMC大多表达α-SMA标记。此外,CTEPH患者近端肺动脉内膜厚度明显高于非血栓栓塞患者。综上所述,这些发现可能表明CTEPH-SMC可能来源于增殖表型切换的PASMC簇。因此,SMC的去分化或表型调节已被广泛描述为各种血管壁疾病,包括动脉粥样硬化[19].这一过程伴随着肌球蛋白重链、α-actin、desmin、smooththelin、caldesmon等平滑肌分化标志物的下调,以及它们增殖和迁移能力的增强在体外[19].在目前的研究中,我们已经证明了来自CTEPH患者的近端肺动脉内膜内膜表达较少的晚期SM分化标志物,并包含具有增殖表型的SMC,显示出增强的增殖和迁移能力在体外.然而,我们不能排除CTEPH- smc也可能来源于祖细胞,因为Firth等人在从CTEPH患者分离的多功能祖细胞群中发现了一种肌成纤维细胞表型[16].
肺血管功能障碍
我们的结果表明,血管壁在CTEPH的病理生理过程中有潜在的参与在体外增加近端CTEPH-PASMC的增殖和迁移能力,增强近端CTEPH-PAEC的有丝分裂活性。相比之下,增强的在体外PAH中已描述了远端毛细血管前PASMC和PAEC的增殖能力[20.,21].抗高增殖细胞凋亡的EC [22]和PAEC的细胞生物能学改变已在特发性多环芳烃中得到证实[23].以内膜和中膜肥大为特征的肺血管壁重塑是PAH中远端肺血管丛状病变形成的关键过程[24- - - - - -26].内皮功能障碍,由高增殖的CTEPH-PAEC引起,可能分别通过PAEC蛋白酶诱导的基质损伤和PAEC衍生的生长因子促进PASMC迁移和增殖。如上所述,近端和亚节段肺血管细胞的高增殖表型也表明,这些变化不仅归因于血栓衍生化合物的作用,还与细胞内的修饰有关。
研究的相关性
到目前为止,很少有研究关注CTEPH的病理生理学。通过建立来自CTEPH患者的PAEC和PASMC的原代培养,我们的目的是揭示大规模或复发性肺栓塞后近端肺动脉持续阻塞的潜在机制。PAEC和PASMC的增殖和/或迁移增强可能与疾病的进展有关。尽管我们的研究结果主要基于原代细胞培养绕过细胞间通讯、剪切应力和血流的动态效应,但它仍然是进一步了解CTEPH病理生理学的有趣工具。
结论
改良的原代PASMC和PAEC增殖和/或迁移反应在体外,与CTEPH- pasmc的增殖表型相关,提示CTEPH中的肺血管细胞功能障碍,可能与血管重构有关。
缩写
- αsma:
-
α-平滑肌动蛋白
- ac-LDL:
-
acetylated-LDL
- CTEPH:
-
慢性血栓栓塞性肺动脉高压
- 的边后卫:
-
胎牛血清
- PAEC:
-
肺动脉内皮细胞
- 多环芳烃:
-
肺动脉高压
- PASMC:
-
肺动脉平滑肌细胞
- 豌豆:
-
肺部动脉内膜切除术
- SMMHC:
-
平滑肌肌球蛋白重链
- sPAP:
-
收缩压
- vWF:
-
冯·维勒布兰德因子。
参考文献
Hoeper MM, Mayer E, Simonneau G, Rubin LJ:慢性血栓栓塞性肺动脉高压。流通,2006,113:2011-2020。10.1161 / CIRCULATIONAHA.105.602565。
Arbustini E, Morbini P, D'Armini AM, Repetto A, Minzioni G, Piovella F, Vigano M, Tavazzi L:多源性和血栓栓塞性肺动脉高压中的斑块组成:血栓物质在脉冲质核形成中的关键作用。中华心脏杂志,2002,32(5):557 - 557。10.1136 / heart.88.2.177。
Bonderman D, Turecek PL, Jakowitsch J, Weltermann A, Adlbrecht C, Schneider B, Kneussl M, Rubin LJ, Kyrle PA, Klepetko W, Maurer G, Lang IM:慢性血栓栓塞性肺动脉高压中凝血因子VIII升高的发生率较高。中华血液学杂志,2003,32(4):376 -376。
Bonderman D, Wilkens H, Wakounig S, Schafers HJ, Jansa P, Lindner J, Simkova I, Martischnig AM, Dudczak J, Sadushi R, Skoro-Sajer N, Klepetko W, Lang IM:慢性血栓栓塞性肺动脉高压的危险因素。中国科学(d辑:自然科学版),2009,38(4):369 - 371。
Lang I, Kerr K:慢性血栓栓塞性肺动脉高压的危险因素。中华医学会胸外科杂志,2006,3:568-570。10.1513 / pats.200605 - 108 lr。
Bonderman D, Jakowitsch J, Adlbrecht C, Schemper M, Kyrle PA, Schonauer V, Exner M, Klepetko W, Kneussl MP, Maurer G, Lang I:医疗条件增加慢性血栓栓塞性肺动脉高压的风险。中华血液学杂志,2005,32(5):516 -516。
Quarck R, Nawrot T, Meyns B, Delcroix M: c反应蛋白:肺动脉高压不良结局的新预测因子。中华心血管病杂志,2009,53:1211-1218。10.1016 / j.jacc.2008.12.038。
肺血栓内膜切除术:一项连续200例肺血栓内膜切除术的临床病理研究。中华病理学杂志,2007,38:871-877。10.1016 / j.humpath.2006.11.017。
Pusztaszeri MP, Seelentag W, Bosman FT:内皮标志物CD31, CD34, von Willebrand因子和Fli-1在正常人体组织中的免疫组织化学表达。中国组织化学杂志,2006,54:385-395。10.1369 / jhc.4A6514.2005。
田村Y、大菅吉、安达H、户泽里、高泽Y、大桥K、Yahagi N、Sekiya M、冈崎H、富田S、Iizuka Y、Koizumi H、Inaba T、Yagyu H、Kamada N、Suzuki H、Shimano H、Kadowaki T、Tsujimoto M、Arai H、Yamada N、Ishibashi S:内皮细胞表达的清除率受体I (sreci)介导脂多糖刺激巨噬细胞摄取乙酰化低密度脂蛋白。中国生物医学工程学报,2004,29(4):394 - 394。10.1074 / jbc.M313088200。
调节血管平滑肌细胞分化。物理学报,1995,15:487-517。
Theilmeier G, Quarck R, Verhamme P, Bochaton-Piallat ML, Lox M, Bernar H, Janssens S, Kockx M, Gabbiani G, Collen D, Holvoet P:猪冠状动脉成形术后高胆固醇血症损害血管重构。心血管杂志,2002,55:385-395。10.1016 / s0008 - 6363(02) 00409 - 1。
Quarck R、Berrou E、Magnier C、Bobe R、Bredoux R、Tobelem G、Enouf J、Bryckaert M:平滑肌细胞周期中Rap1a和Rap1b蛋白的差异上调。中国生物医学工程学报,1997,19(4):369 - 371。
Sacks RS, Remillard CV, Agange N, Auger WR, Thistlethwaite PA,袁建新:慢性血栓栓塞性肺动脉高压的分子生物学研究。中华心血管外科杂志,2006,18:265-276。10.1053 / j.semtcvs.2006.09.004。
Lang IM, Marsh JJ, Olman MA, Moser KM, Schleef RR:慢性肺血栓栓塞患者血浆和内皮细胞中组织型纤溶酶原激活物和1型纤溶酶原激活物抑制剂的平行分析。流通,1994,90:706-712。
Firth AL, Yao W, Ogawa A, Madani MM, Lin GY,袁建新:慢性血栓栓塞性肺动脉高压患者动脉内膜切除组织中存在多能间充质祖细胞。中国生物医学工程学报,2010,29(4):369 - 369。10.1152 / ajpcell.00416.2009。
姚伟,Firth AL, Sacks RS, Ogawa A, Auger WR, Fedullo PF, Madani MM, Lin GY, Sakakibara N, Thistlethwaite PA, Jamieson SW, Rubin LJ,袁建新j:慢性血栓栓塞性肺动脉高压患者去内膜组织中内皮祖细胞(CD34 + CD133 + Flk-1+)的鉴定。中国生物医学杂志,2009,29(4):394 - 394。10.1152 / ajplung.90413.2008。
Yan Q, Vernon RB, Hendrickson AE, Sage EH:猕猴视网膜微血管内皮细胞的原代培养及特性研究。中华眼科杂志,1996,37:2185-2194。
Owens GK, Kumar MS, Wamhoff BR:血管平滑肌细胞分化在发育和疾病中的分子调控。物理学报,2004,44:767-801。10.1152 / physrev.00041.2003。
Dewachter L, Adnot S, Fadel E, Humbert M, Maitre B, Barlier-Mur AM, Simonneau G, Hamon M, Naeije R, Eddahibi S:血管生成素/Tie2通路对特发性肺动脉高压平滑肌增生的影响。中华急救医学杂志,2006,32(4):394 - 394。10.1164 / rccm.200602 - 304摄氏度。
Eddahibi S, Guignabert C, Barlier-Mur AM, Dewachter L, Fadel E, Dartevelle P, Humbert M, Simonneau G, Hanoun N, Saurini F, Hamon M, Adnot S:内皮细胞与平滑肌细胞之间的交叉作用:血清素诱导平滑肌增生的关键作用。《流通》,2006,113:1857-1864。10.1161 / CIRCULATIONAHA.105.591321。
马思丽,徐伟,徐文华,吴晓燕,吴晓燕,吴晓燕,吴晓燕。特发性肺动脉高压中内皮细胞高增殖凋亡抵抗的研究。中国生物医学杂志,2007,29(3):394 - 394。10.1152 / ajplung.00428.2006。
Xu W, Koeck T, Lara AR, Neumann D, DiFilippo FP, Koo M, Janocha AJ, Masri FA, Arroliga AC, Jennings C, Dweik RA, Tuder RM, Stuehr DJ, Erzurum SC:肺动脉内皮细胞生物能量学的改变。美国国家科学研究院。2007, 36(4): 447 - 449。10.1073 / pnas.0605080104。
Blauwet LA, Edwards WD, Tazelaar HD, McGregor CG:肺血栓动脉内膜切除术的外科病理:对1990 - 2001年54例病例的研究。中华病理学杂志,2003,34:1290-1298。10.1016 / j.humpath.2003.07.003。
Jamieson SW, Kapelanski DP, Sakakibara N, Manecke GR, Thistlethwaite PA, Kerr KM, Channick RN, Fedullo PF, Auger WR:肺动脉内膜切除术1500例的经验和教训。中华外科杂志,2003,23(4):557 - 562。10.1016 / s0003 - 4975(03) 00828 - 2。
Yi ES, Kim H, Ahn H, Strother J, Morris T, Masliah E, Hansen LA, Park K, Friedman PJ:慢性肺动脉高压阻塞性内膜病变的分布及其细胞表型。形态计量学和免疫组化研究。中华呼吸与危重护理杂志,2000,162:1577-1586。
确认
这项工作得到了辉瑞公司和比利时心脏外科基金的研究资助。医学博士是鲁汶大学肺动脉高压Actelion主席和肺血管病理学研究与教育GSK主席的持有者。作者感谢W. Coosemans、W. Daenen、P. De Leyn、T. Lerut、P. Nafteux和F. Rega在收集患者样本方面的帮助和合作,并感谢L. revenge thasamy提供的技术援助。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
作者声明他们没有竞争利益。
作者的贡献
MW对数据进行了采集、分析和解释,进行了统计分析并起草了手稿。RQ对研究进行了构思和设计,对数据进行了获取、分析和解释,进行了统计、监督和对稿件进行了严格的修改。AR已经获得了数据。MRS和FW对手稿进行了严格的修改。DVR和BM收集了人体组织标本,并对手稿进行了严格的修改。MD构思和设计了研究,处理了资金和监督,并对手稿进行了严格的修改。所有作者阅读并批准了最终稿件。
Rozenn夸克,Marijke Wynants对这项工作也做出了同样的贡献。
权利与权限
188滚球软件本文由BioMed Central Ltd.授权发布。这是一篇开放获取文章,188滚球软件根据创作共用授权协议(https://creativecommons.org/licenses/by/2.0),它允许在任何媒体上不受限制地使用、分发和复制,只要原著被恰当地引用。
关于本文
引用本文
夸克,R,怀南斯,M,罗尼兹,A。et al。慢性血栓栓塞性肺动脉高压患者近端肺动脉细胞的特征。和物13日,27(2012)。https://doi.org/10.1186/1465-9921-13-27
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1465-9921-13-27
关键字
- 慢性血栓栓塞性肺动脉高压
- 平滑肌细胞
- 内皮细胞
- 血管重建