摘要
哮喘是一种复杂的呼吸系统疾病,其严重程度和治疗反应各不相同。几种具有独特临床和炎症特征的哮喘表型已经被确定。基于不同分子谱的内型有助于进一步阐明哮喘的异质性。2型炎症,包括先天(2型先天淋巴样细胞)和适应性(t辅助2型细胞)免疫系统,支撑哮喘慢性炎症的复杂病理生理学,以及共病的存在(如。慢性鼻窦炎与鼻息肉,过敏性鼻炎和特应性皮炎)。2型炎症的特征在于,表征2型细胞因子白细胞介素(IL)-4,IL-5和IL-13,IgE介导的免疫介质的释放和上皮或表皮屏障的功能障碍。靶向这些关键的近端2型细胞因子在最近的研究中表明了采用靶向生物学治疗的个性化方法的疗效。2型细胞因子下游的升高的生物标志物水平,包括分数呼出的一氧化氮,血清IgE和血液和痰液粒细胞已与参与2型炎症的机制有关。他们有潜力可以帮助诊断,并预测和监测治疗的反应。本综述的目的是总结目前对哮喘中2型炎症生物学的理解,检查其对2型炎症性炎症性的影响,并讨论2型炎症生物标志物如何利用生物药物时代进一步个性化治疗方法.
摘要
这篇综述涵盖了哮喘中的2型炎症的病理生理学,它对2型共病的影响,以及在生物药物时代利用2型生物标志物来改善诊断和进一步个性化治疗的方法https://bit.ly/2MSOI2O
介绍
哮喘与显着的异质性有关。现在已经确定了具有独特临床和炎症型材的几种不同的哮喘表型。2020年的哮喘(GINA)的全球倡议(GINA)指导方针建议评估严重哮喘患者的炎症表型,因为这些型材可以帮助描述气道炎症的物理表现,也可能有助于预测对定制治疗的反应性[1,2].表1呈现当前哮喘表型的一个例子,因为它们涉及在FL盐态(2-高或2-低)和表型特征中。2型途径激活的标志包括IgE产生,嗜酸性粒细胞和升高的2型生物标志物,如呼出的一氧化氮的一部分(Feno.).通过基于不同的功能或病理生理学特征来鉴定条件的亚型,内容物有助于进一步阐明哮喘内的异质性[12.- - - - - -14.].与表型可能随时间变化或响应于治疗而言,因素亚组保持相对稳定,因为它们由固有的遗传和分子机制定义[15.].
在50-70%的哮喘患者中观察到哮喘和相关的2型炎症,并由先天型(2型先天淋巴(ILC2)细胞)和适应性(T-辅助细胞类型2(TH2)细胞)驱动免疫体系,其特征在于释放细胞因子,例如白细胞介素(IL)-4,IL-5和IL-13,哮喘的关键病理学特征[3.,13.].IL-4和IL-13参与粘液生成和杯状细胞增生、气道平滑肌收缩和增殖、纤维化、基底膜增厚、屏障功能障碍、嗜酸性粒细胞运输到肺和IgE生成[16.].IL-5促进嗜酸性粒细胞成熟,激活和贩运[16.].然后促进肥大细胞和嗜碱性粒细胞的升级以及哮喘中过敏反应的发展。炎症细胞和2型细胞因子下游的生物标志物的升高,包括Feno.血清IgE、血液和痰中的嗜酸性粒细胞与2型炎症有关[17.].
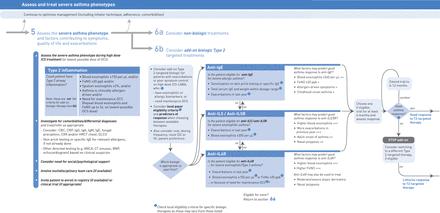
靶向2型炎性途径内的特异性细胞因子降低了哮喘和其他2型炎症性炎症性的病理生理学[13.].已经评估了许多有针对性的生物制剂作为潜在治疗,包括IL-4,IL-5,IgE和IL-13的单克隆抗体;在该过程中,已经提供了这些特征性疾病的分子机制的见解[18.- - - - - -20.].当前吉娜指南建议封锁的il - 4受体(IL-4R)(因此抑制信号的il - 4和IL-13)患者2型/嗜酸性哮喘,严重抑制IgE患者严重的过敏哮喘,和抑制IL-5 /封锁IL-5受体(IL-5R)严重嗜酸性哮喘患者(图1)[2,21.].反映2型细胞因子受累的生物标志物目前用于许多这些靶向生物制剂的临床试验中的个性化治疗或患者选择[13.].
吉娜关于评估成人和青少年患者难以治疗的哮喘,包括生物治疗方案。©2020哮喘的全球倡议,转载许可(www.ginasthma.org).ANCA:抗替托罗氏菌细胞质抗体;BNP:B型利钠肽;CBC:完全血统;CRP:C-反应蛋白;CT:计算机断层扫描;CXR:胸部X射线;DLCO:用于一氧化碳的肺部的延伸能力;FENO:分数呼出一氧化氮;HRCT:高分辨率计算机断层扫描; ICS: inhaled corticosteroids; Ig: immunoglobulin; IL: interleukin; IV: intravenous; LABA: long-acting β2-agonist; OCS: oral corticosteroids; SC: subcutaneous.
本综述讨论了我们目前对哮喘2型炎症生物学的理解,其对2型炎症性炎症性的影响以及2型炎症生物标志物如何利用生物学药物时代进一步个性化治疗。
2型细胞因子对哮喘病理生理学特征的影响
2型炎性气道疾病可以与衰弱的症状有关,对皮质类固醇药物的更大要求,次优疾病控制和生活质量差。如上所述,2型哮喘的特征病理特征包括细胞因子诱导的嗜酸性嗜酸性气道炎症,粘液堵塞,戈尔特细胞增生,上皮屏障变化和气道平滑肌肉功能,以及气道墙的重塑(表2)[16.,23.].在本节中,我们依次讨论每个功能,突出显示关键的驱动器和细胞因子。
炎症反应
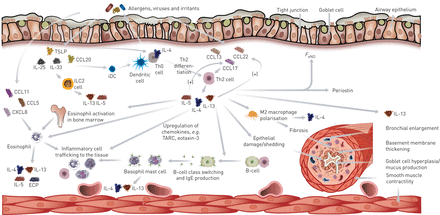
在2型炎症中的先天和自适应细胞和介质之间的相互作用是哮喘病理生理学(图2.)[3.,16.,24.].气道中的2型免疫应答主要由嗜酸性粒细胞,肥大细胞,嗜碱性粒细胞,TH2细胞,ILC2和产生B细胞介导。气道上游的上游事件涉及分泌母导管机构或诸如IL-33,IL-25或胸腺基质淋巴泛菌素(TSLP)的母版调节型CD4的成熟+T细胞诱导Th2自适应免疫应答。Th2细胞迁移到气道上皮,其中,与ILC2细胞一起产生各种类型的2型细胞因子(IL-4,IL-5和IL-13),其有助于嗜酸性粒细胞募集和B细胞类切换[13.,24.].这些细胞因子在疾病病理生理学中发挥关键作用,并驱动各种下游事件,包括激活呼吸道上皮细胞,效应细胞的化学,气道平滑肌肉调节和上皮基质的重塑。反过来,这些反应倾向于高反应性,气流阻塞和恶化。除了对外部刺激的适应性响应外,IL-25,IL-33和TSLP可以直接激活ILC2,分泌IL-5,IL-13和IL-9,后者有助于ILC2S的进一步活化和存活[25.,26.].体外研究表明,IL-4和IL-13可诱导B细胞转换和IgE产生,导致肥大细胞和嗜碱性粒细胞致敏,从而释放促炎症介质,如2型细胞因子(IL-4、IL-5和IL-13)、组胺、白三烯和前列腺素D2过敏原暴露[16.].IL-4和IL-13的重叠功能可以是由于受体和细胞因子表达模式,因为两种细胞因子信号通过两个潜在的异二聚体受体,其具有共用受体部分,IL-4Rα链[27.].
2型炎症中先天性和适应性细胞及介质之间的相互作用是哮喘病理生理学的基础。上皮细胞的破坏允许过敏原、病毒或细菌穿透,激活先天性和适应性免疫反应。树突状细胞表达抗原可激活幼稚的T辅助细胞(T辅助细胞0型(Th0)细胞)分化为T辅助细胞2型(Th2)细胞,进而产生白细胞介素(IL)-4,导致Th0细胞进一步分化。Th2细胞释放的细胞因子导致嗜酸性粒细胞活化和炎性细胞运输,B细胞类转换和气道改变,包括基底膜增厚、支气管扩张、杯状细胞增生和纤维化。CCL:趋化因子(C-C基序)配体;趋化因子(C-X-C基序)配体;ECP:嗜酸性阳离子蛋白;Feno.:呼出一氧化氮的级分;IDC:间隙树突状细胞;ILC2:2型先天淋巴细胞;TARC:胸腺和激活调节的趋化因子;TSLP:胸腺基质淋巴二蛋白。
IL-4和IL-13在2型炎症中的中枢神经临床作用在目前的GINA指南中认识到IL-4Rα的阻断,IL-4和IL-13的共同受体组分,治疗患者具有严重的2型哮喘(以及特应性皮炎(AD)或慢性鼻窦炎,具有鼻息肉(CRSWNP)。相比之下,抗IgE和抗IL-5 /抗IL-5R抗体用作针对组分的靶向疗法2型炎症,它们仅限于分别用于严重过敏性哮喘和嗜酸性哮喘的患者(图1)[2,21.].
上皮屏障功能和上皮源性细胞因子
响应慢性气道损伤的上皮屏障功能障碍是跨2型炎症气道疾病共享的病理生理学特征。上皮屏障的破坏允许环境代理(如。气道病毒,过敏原,细菌和真菌)渗透上皮并激活先天生先生和适应性免疫反应,导致气道粘膜上皮的组织学变化和功能异常。从支气管和鼻上皮细胞的上皮衍生的细胞因子如Tslp,IL-25和IL-33的释放有助于哮喘的总体病理学生理学,并且对屏障函数的损害将粘膜渗透率增加对外来物质的粘膜渗透性[28.].上皮衍生的细胞因子募集树突细胞并促进其成熟;它们反过来激活T细胞通过抗原提呈与共刺激[29.].它们还充当嗜酸性粒细胞和中性粒细胞的化学特征,而TSLP,IL-25和IL-33的分泌可以进一步刺激关键2型细胞因子的产生(IE。IL-4,IL-5和IL-13)在INNINATE(ILC2S)的炎性细胞和免疫系统的适应性(TH2细胞)臂[3.,30.].这些细胞因子有助于上皮阻隔破坏,增加上皮渗透性[31.,32.].此外,ILC2s释放IL-13刺激上皮细胞增加IL-33的产生,形成正前馈循环[33.]. 人支气管上皮细胞暴露于IL-4和IL-13体外以Janus激酶依赖的方式严重损害气道上皮细胞连接复合物的结构和功能。这表明,th2细胞因子依赖性屏障破坏可能是过敏性哮喘屏障功能缺陷的基础[31.].IL-13对支气管上皮紧密连接屏障蛋白的破坏在活的有机体内研究强调了哮喘发病机制的另一个重要机制[32.].
类似的结果也在其他促炎细胞因子(包括肿瘤坏死因子-α和干扰素-γ)中观察到,它们破坏了人类气道上皮的紧密连接,促进炎症细胞因子的释放[34.].由于气道上皮细胞,树突细胞和ILC2s的激活,上皮细胞因子,TSLP,IL-25和IL-33的上皮细胞因子,TSLP,IL-25和IL-33的释放也强烈关联。28.].
粘液分泌
呼吸道粘液堵塞在哮喘病理生理学中的作用早已被认识[35.].来自哮喘死亡的主要原因是来自深刻气流阻塞的窒息,这可能包括广泛的粘液塞的腔内气道阻塞[36.].过量的粘液生产有助于气流阻塞[37.[随后形成粘液塞与肺功量降低有关。这种病程中通常观察到严重气流阻塞的患者。
粘液化生(IE。表面上皮粘蛋白生成增加)和支气管微血管数量增加是哮喘气道重塑的组成部分,是粘液功能障碍的易感性[38.].气道炎症患者的这些变化发生,其特征在于气道墙和腔粘液的渗透和CD4+分泌Th2细胞因子的T细胞,嗜酸性粒细胞和ILC2s [39.].
在小鼠模型中,IL-13信号在过敏刺激后影响杯状细胞计数,并在气道炎症、重塑和功能障碍的产生和持续中发挥重要作用[40].IL-13还增加了糖蛋白粘蛋白5Ac(MUC5Ac)的产生,其与更粘附的粘液相关的粘液相关。粘液组成和组织的变化可能是哮喘呼吸道阻塞,发病率和死亡率的主要贡献者[36.].
平滑肌功能与气道重塑
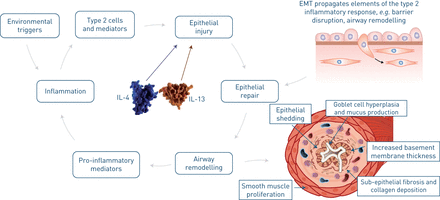
气道重塑是一个集合术语,它代表发生在气道上皮和粘膜下层的多种病理变化,导致哮喘患者气道的永久性结构改变[3.].IL-4和IL-13引起气道粘膜的变化,可以通过缩小基线气道口径和改变夸大吸入触发的反应的结构元素来促使患有哮喘的患者加剧哮喘的患者(图3.)[3.,16.,41.]. IL-5也与上皮脱落和气道重塑有关[42.].哮喘中持续的炎症和气道重塑也有助于加重表型中自我持续的加重周期[43.].
白细胞介素(IL)-4和IL-13是气道重塑的核心。环境触发器开始刺激2型炎症细胞和介质,包括IL-4和IL-13的刺激,该炎症在气道中刺激,这损坏了上皮。修复从上皮 - 间充质转换(EMT)传播,导致气道的屏障破坏和重塑。这种重塑导致上皮脱落,增加厚度的基底膜厚度,纤维化和胶原沉积,平滑肌增殖,脚耳细胞增生和粘液生产。另外,重塑导致增加的促炎介质,进一步增加炎症和上皮损伤。
气道平滑肌细胞表达来自CD4的细胞因子的受体+T细胞。这些细胞因子,特别是IL-13可以直接在气道平滑肌细胞上起作用,导致收缩和弛豫响应,增殖和平滑肌细胞产生趋化因子等趋化因子的变化,例如Eotaxin和胸腺和激活调节的趋化因子(TARC),因此增强了促致泌胞效应[44.,45.].
IL-13促进钙内流(一种介导气道平滑肌收缩的机制)对人体气道平滑肌细胞组织胺收缩的反应[44.].IL-13信号传导还影响组织学反应,是由2型炎症引起的组织纤维化的关键介质[46.,47.].IL-13的纤维原效应可以通过转化生长因子-β(TGF-β)来介导,IL-13选择性地刺激Clara细胞10-KDA(CC10)-13转基因小鼠的TGF-β产生。TGF-β拮抗剂(可溶性TGFβR-FC)降低小鼠IL-13诱导的肺胶原蛋白产生[46.].还有证据表明IL-13通过直接对成纤维细胞增殖和胶原蛋白产生的影响诱导亚上皮纤维化,这两者都取决于[48.]独立于[49.] TGF-β。IL-13还增加了哮喘患者的人气道成纤维细胞中的成纤维细胞侵袭性[47.,50].
嗜酸性粒细胞也被认为在气道重塑过程中也发挥着重要作用。上皮衍生的细胞因子,包括趋化因子配体CXCL8,CXCL5和CCL11,促进嗜酸性粒细胞渗透到气道组织中[29.].嗜酸性细胞分泌大量促纤维化分子,如嗜酸性细胞阳离子蛋白和TGF-β1,它们是气道重塑和促炎细胞因子的关键驱动因素(如。IL-5)延续组织炎症。体外研究还证明了嗜酸性粒细胞与肥大细胞和上皮细胞相互作用,诱导炎性细胞因子的上皮细胞分泌和刺激肥大细胞,以产生纤维纤维因子以及肿瘤坏死因子-α,其进一步刺激来自嗜酸性粒细胞的TGF-β1释放[51,52].
2型炎症共病的常见病理生理特征
共病可与2型炎症相互作用,增强组织损伤的现有免疫过程。2型炎症是未控制、持续性哮喘和多种共病炎症疾病的统一特征,包括CRSwNP、过敏性鼻炎(AR)、嗜酸性食管炎(EoE)和AD,可表现为与哮喘不同或共病的疾病[16.].常见同种植的患病率在炎性疾病中变化,患有高达50%的慢性鼻窦炎或CRSWNP患者,高达60%的eoE,患者也具有可混合哮喘的广告,高达26%的患者增加了26%[53- - - - - -55].同样,> 80%的哮喘患者患有AR,高达40%的AR患者具有共用哮喘[56,57].
类似于哮喘中所见的发病机制,CRSWNP,AR,EOE和AD的特征在于2型细胞因子的上调,IgE介导的免疫介质释放和上皮或表皮屏障的功能障碍[58- - - - - -63].
最近的哮喘和CRSWNP指南更新识别2型炎症和关键2型细胞因子IL-4,IL-5和IL-13在这些疾病的病理生理学中的重要性[2,21.,64].靶向这些关键的临床类型2细胞因子代表了有希望的策略,以实现多种疾病的治疗益处。功效导致最近采用个性化的治疗方法的研究表明,如果关键上游司机被有效地阻止,则2型炎症在严重的哮喘群体中广泛相关;这些结果支持靶向中央途径可以使多种过敏性疾病有益的假设[16.].吉娜(哮喘)建议的2型生物治疗和过敏和呼吸道病的欧洲研究和教育论坛(CRSWNP)通过靶向IgE,IL-5 / IL-5R和IL反映了该途径中的关键2型细胞和介质-4r(图2.)[21.,64].
慢性鼻窦炎与鼻息肉
上皮屏障功能障碍和粘膜缺陷导致金黄色葡萄球菌鼻息肉定植,进而促进CRSwNP慢性炎症的发展。S.金黄色葡萄球菌肠毒素倾斜朝向2型表型的细胞因子反应,其具有增加的IL-4,IL-5和IL-13表达,其引起并使炎症反应延伸。这些因素组合以驱动各种免疫细胞的涌入,包括嗜酸性粒细胞,肥大细胞,ILC2和淋巴细胞,所有这些都将其参与鼻息肉中的慢性炎症反应[16.,38.,65].
关于潜在的2型炎症来自生物标志物的炎症可以了解什么?
哮喘的准确诊断和治疗,同时通过疾病的异质病理生理学复杂,鉴于可用于特定患者亚组的靶向疗法的可用性尤其重要。与参与2型气道炎症的机制相关的生物标志物也有可能有助于诊断和预测和监测对治疗的反应[13.,16.,72,73].已经显示出型2型炎症的生物标志物在区分型2高中具有潜在的效用相对型2低表型并预测对2型细胞因子靶向治疗的响应性[3.].这些类型相关的生物标志物包括Feno.,血清总和过敏原特异性的IgE和血液或痰嗜酸性粒细胞水平[17.].
一氧化氮(NO)是从氨基酸L-精氨酸中内源性衍生出来的,可在呼出的呼吸中测量为Feno.通过一种简单的非侵入性程序,在严重的空气流动障碍患者中使用相对容易使用[74].IL-4和IL-13从气道上皮诱导没有生产[73].Feno.正日益被认为是2型炎症的可行生物标志物,反映有症状患者的糖皮质激素应答性气道炎症和尽管使用吸入糖皮质激素,但气道炎症持续存在[2,21.,74- - - - - -78].
IL-4和IL-13的表达显着增加了气道上皮的生产没有生产[75].哮喘患者高高Feno.表型(≥35ppb)代表哮喘群的大量比例,并且该子表型是通过增加的精氨酸代谢而典型的,并且通过更大的气流阻塞和气道反应性临床表征[79].
高的Feno.严重哮喘的水平已被证明可以识别出气流限制和可逆性更强的患者,痰中嗜酸性粒细胞更多,急诊和重症监护病房入院最多,提示严重哮喘患者按以下因素分组Feno.识别最具侵略性的哮喘表型[80].
血清IgE升高是b淋巴细胞中il -4驱动的免疫球蛋白类转换的结果,是特应性疾病的一个特征[16.].特异性IgE抗体也有助于哮喘炎症过程。目前,该生物标志物的主要临床应用是估计抗IgE抗体omalizumab的最佳剂量[81]对于严重过敏性哮喘的加入治疗,并支持过敏性支气管瓣曲柄的筛选,一种通常伴有非常高的血清总IgE的病症[82].
如前所述,嗜酸性粒细胞是2型炎症的关键细胞效应因子,在维持哮喘的长期炎症中发挥重要作用。嗜酸性粒细胞可在外周血、肺组织和气道腔(痰)中使用各种技术测量;然而,除极少数学术中心外,常规的临床实践中并没有浸润性程序,如组织活检和诱导痰评估。因此,外周血嗜酸性粒细胞的测量在临床应用中更为广泛[83].临床研究表明血液梭粒水平与哮喘相关结果之间的相关性,例如严重恶化和哮喘控制水平的风险[84].此外,对哮喘生物治疗的临床试验经常表明,在基线的高水平血液粒细胞患者中,治疗反应较高,因此至少部分预测治疗反应[85].研究表明,当使用> 3%痰嗜酸性粒细胞的截止时,痰嗜酸性嗜酸性粒细胞引导的哮喘管理可以减少加剧的频率,并表明该措施是引导治疗的敏感和可靠的生物标志物[13.].嗜酸性粒细胞有助于免疫应答调制,气道高反应性和重塑,以及与IL-4,IL-5,IL-13和其他炎症介质的协同相互作用,以促进它们在肺部的积累[86.].
治疗的影响
2型细胞因子在哮喘发病机制中具有整体作用,并且许多靶向生物学已被评估为潜在的处理,包括靶向IL-4,IL-5和IL-13途径的潜在治疗。目前可用的单克隆抗体包括omalizumab(抗IgE);Mepolizumab,Reslizumab和Benralizumab(抗IL-5途径);和Dupilumab(抗IL-4 / IL-13)(表3).这些新的生物制剂的主要好处是实现疾病控制,临床研究中观察到的病情恶化的显著减少证明了这一点[18.].这些药剂的相对疗效与靶选择和抑制剂的分子特征相关。靶向2型途径下游介质的抗IgE和抗IL-5剂是有效治疗哮喘,虽然目前没有批准,但不是AD。IL-4和IL-13的双阻断表现出跨多种过敏性疾病(哮喘,AD,CRSWNP,EOE)的显着效果,确认了这些特应疾病中IL-4 / IL-13途径的共平[16.,94].
根据GINA的研究,在严重哮喘患者中,基于2型炎症生物标志物(血液和/或痰中嗜酸性粒细胞和/或)的升高,可能会识别出潜在的2型气道炎症Feno.(临床过敏原驱动和/或需要维持口服皮质类固醇的哮喘)(图1)[2,21.,78].
目前用于反映潜在炎症过程特征和2型炎症的存在的生物标志物目前用于分析患者的临床试验中的一些这些药剂。2型高哮喘表型的准确分类需要临床参数的组合,例如对皮质类固醇的过敏表型或反应性,以及单独或组合的2型生物标志物[13.].
鉴于哮喘中炎性途径的复杂性,在每种哮喘表型中可能在这些生物标志物中具有相当大的重叠;因此,可能存在多于一个主要的生物标志物。2型生物标志物的面板可以更准确地反映哮喘的风险,最终帮助医生选择最合适的治疗方法。两个单独的研究表明,两者的水平升高Feno.血液化粒细胞与更大的支气管高反应性和加剧增加相关[95,96].
结论
2型炎症包含多种哮喘表型,并驱动哮喘和共病条件的关键病理生理特征。提高对疾病认识的综合努力标志着一种更以疾病生物学为基础的方法的趋势,其中疾病的临床、细胞和分子方面被一起检查,以更好地确定临床特征和特定疾病机制之间的相关性。与2型炎症机制相关的生物标志物的使用有可能改善诊断和治疗选择,并为针对特定的2型炎症通路细胞因子的新的和个性化治疗提供合理基础。
可共享的PDF
确认
作者谨此感谢Dianne Barry,Colin Mitchell和Ledia Goga of Sanofi和Nora Crikelair of Regeneron Pharmaceuticals,Inc。在手稿开发期间的批判性反馈。作者在编写来自Jennifer L.F.的jennifer L.F. of Excerpta Medica港,由Sanofi Genzyme和Regeneron Pharmaceuticals,Inc。提供的书面/编辑支持。
脚注
利益冲突:W.W.巴士在研究期间向Novartis,Regeneron Pharmaceuticals,Inc.和Sanofi的个人费用向Glaxosmithkline和个人费用报告个人费用。
兴趣冲突:M. Kraft报告美国肺协会,Astrazeneca,Chiesi,国家卫生学院,Regeneron Pharmaceuticals,Inc。和Sanofi以及来自Astrazeneca,Regeneron Pharmaceuticals,Inc。和Sanofi的其他(咨询)的奖金研究;和其他(特许权使用费)从elsevier外,在提交的工作之外。
利益冲突:K.F.Rabe在研究期间向Astrazeneca,Boehringer Ingelheim,Novartis,Sanofi和Teva报告了顾问和讲座的个人费用。
利益冲突:Y. Deniz是Regeneron Pharmaceuticals, Inc.的雇员和股东。
利益冲突:P.J.Rowe是一名员工,可能持有赛诺菲的股票/期权。
利益冲突:M. Ruddy是Regeneron Pharmaceuticals,Inc。的员工和股东
利益冲突:M. Castro报告了来自美国肺脏协会、阿斯利康、勃林格殷格翰、Chiesi、美国国立卫生研究院、诺华、PCORI和赛诺菲、其他(咨询)来自4D Pharma、Aviragen Therapeutics、Boston Scientific、Genentech、Nuvaira、Sanofi、Teva、Therabron Therapeutics、Theravance Biopharma、Vectura和Vida Pharma、在研究期间,AstraZeneca、Boehringer Ingelheim、Boston Scientific、Genentech、Sanofi、Regeneron Pharmaceuticals, Inc.和Teva的讲座费用和爱思唯尔的其他费用(版税)。
支持声明:这项工作得到了Sanofi和Regeneron Pharmaceuticals,Inc。本文的资助信息已存入Crossref资助者注册表.
- 收到2020年9月4日。
- 接受2020年12月21日。
- 版权所有©作者2021。
这个版本是在知识共享署名非商业许可4.0的条款下发布的。有关商业复制权利和许可,请联系权限{exernet.org