抽象的
部分纤维化间质性肺病(ILDs)患者发展为进行性表型,其特征为肺功能下降、生活质量下降和早期死亡。除了特发性肺纤维化(IPF),目前还没有批准的治疗纤维化型ild的药物,目前的治疗方法缺乏证据支持。具有进行性表型的纤维化型ILDs在临床行为和导致疾病恶化的致病机制方面具有共性。Nintedanib是一种酪氨酸激酶胞内抑制剂,已被批准用于IPF的治疗,最近已被证明可降低伴有系统性硬化(SSc-ILD)的ILD患者的肺功能下降率。在体外数据表明,nintedanib可抑制肺纤维化起始和进展中的几个步骤,包括促炎症和促纤维化介质的释放,纤维细胞和成纤维细胞的迁移和分化,以及细胞外基质的沉积。Nintedanib还能抑制血管细胞的增殖。在纤维化型ILDs(如IPF、SSc-ILD、类风湿关节炎- ild、超敏性肺炎和矽肺)动物模型的研究表明,nintedanib具有抗纤维化活性,与肺病理的触发无关。这表明nintedanib抑制了纤维化发病机制中的基本过程。nintedanib在除IPF (INBUILD)外的进展性纤维化ILDs (INBUILD)患者中的试验将于2019年报告结果。
抽象的
非临床研究表明,nintedanib,一种已获批准的特发性肺纤维化治疗药物,可能对其他具有进行性纤维化表型的间质性肺疾病具有抗纤维化作用http://bit.ly/2NiCAYx
介绍
间质性肺病(ILDs)包括一大类不同类型的疾病,通常影响间质,即分隔肺部上皮和内皮屏障的结缔组织间质。ILDs可能有一个已知的原因,如。它们可能是自身免疫性疾病的表现或对吸入抗原敏感的结果。然而,ild也包括一些原因不明的疾病[1].特发性肺纤维化(IPF)是最常见的ILD类型之一。虽然IPF的过程是可变的,但是,根据定义,IPF是一种最终导致呼吸衰竭的渐进纤维疾病[2].部分其他类型的ILD患者也发展为进行性纤维化表型,与肺功能下降、症状恶化和生活质量恶化以及早期死亡率相关[3.].这些包括特异性非特异性间质性肺炎[4]、类风湿性关节炎(RA-ILD)等自身免疫性疾病相关的ild [5]和系统性硬化(SSc-ILD) [6]、慢性超敏性肺炎[7]、慢性结节病[8],曝光相关的ILD等矽肺病[9]和不可分类的特发性间质性肺炎[10].目前,治疗具有进行性表型的纤维化型ILDs的目标是减缓肺功能的下降。然而,IPF是唯一一种已获批准的药物治疗的纤维化间质性肺病的形式。其他类型的渐进性纤维化ILD患者的治疗主要基于免疫抑制,而除了SSc-ILD,免疫抑制没有强有力的证据支持,这使得患者对有效治疗方案的需求很高[11,12].
进展型纤维化ILDs的发病机制
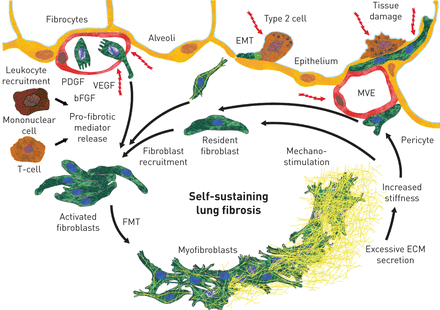
已知几种机制参与了所有纤维化ILD的发病机制和进展(图1).所有的ild都被认为是由重复的慢性上皮或血管损伤或肉芽肿性炎症引发的,这些炎症导致细胞破坏,在纤维性疾病的情况下,导致不受控制的修复[13- - - - - -15].成纤维细胞,纤维化ild的主要效应细胞,从不同来源到损伤部位。常驻间质成纤维细胞增殖和迁移[16循环入侵的纤维细胞[17和上皮细胞[18]和周细胞[19获得通常与成纤维细胞有关的特征。最终,这些成纤维细胞被激活成为肌成纤维细胞,它分泌过量的细胞外基质,导致组织僵硬度增加,肺泡组织功能丧失[20.].此外,癌细胞和淋巴细胞被募集到损伤部位和释放亲纤维化介质的部位,进一步促进成纤维细胞活化[16].在前馈回路中,肺组织僵硬程度的增加进一步激活并刺激成纤维细胞,这一过程被称为机械刺激,从而驱动自我维持和进行性肺纤维化[21].
已知涉及思生间质性肺病的发病机制和进展的机制。EMT:上皮 - 间充质转换;PDGF:血小板衍生的生长因子;VEGF:血管内皮生长因子;BFGF:基本成纤维细胞生长因子;MVE:微血管上皮;FMT:成纤维细胞 - 肌纤维细胞过渡;ECM:细胞外基质。肺泡上皮和/或微血管内皮部位可能发生组织损伤。成纤维细胞从驻留成纤维细胞,循环纤维细胞和上皮细胞和正在进行EMT的上皮细胞和纤维细胞募集。 Growth factors are released by the damaged epithelium and endothelium, and leukocytes are recruited. Mononuclear cells and T-cells release pro-fibrotic mediators. Activated fibroblasts transition to myofibroblasts (FMT), which release excessive amounts of ECM. This results in increased tissue stiffness, which further stimulates fibroblast activation, leading to self-sustaining fibrosis.
nintedanib.
Nintedanib已经被许多国家批准用于IPF的治疗,包括欧洲和美国。成人的标准剂量是每天两次150mg。IPF患者在标准口服给药后稳定状态下的最大血药浓度为约59-74 nmol·L−1[22,23].
Nintedanib是一种小分子酪氨酸激酶抑制剂,靶向血小板源性生长因子(PDGF)受体-α和-β,成纤维细胞生长因子(FGF)受体-1 - 3和血管内皮生长因子(VEGF)受体-1 - 3 [24].Nintedanib竞争性地与这些受体的atp结合袋结合,从而阻断细胞内信号[24].Nintedanib还能抑制Src家族激酶淋巴细胞特异性酪氨酸蛋白激酶(Lck)、集落刺激因子(CSF)-1受体(CSF1R)和其他20种激酶,具有中位抑制浓度(IC)50)值<100 nM [24,25].大多数这些激酶的酶抑制对细胞功能的影响尚未被探索。
尼尼达尼在肺纤维化中的作用机制
在体外数据表明,nintedanib抑制了肺纤维化开始和进展中的多个步骤,这些步骤可能与进行性纤维化型ild患者的治疗有关。
Nintedanib具有抗炎活性,减轻纤维化的起始和进展
激活时,t细胞释放促炎症和促纤维化介质,据信这些介质会启动并促进自身免疫性疾病纤维化的进展[26,27].Lck在t细胞刺激后被激活,它是t细胞增殖和白细胞介素(IL)-2产生所必需的[28- - - - - -31].在酶水平上,nintedanib以IC抑制Lck的活性5016 nm [24].此外,nintedanib可抑制人外周血单个核细胞或t细胞中IL-2、IL-4、IL-5、IL-10、IL-12p70、IL-13和干扰素-γ的释放[32].nintedanib的效力在IPF患者接受标准剂量150mg每日两次治疗时观察到的暴露范围内,这表明使用nintedanib治疗将在临床使用药物期间调节这些介质是可行的。
CCL18是M2巨噬细胞极化的标记,已与抗纤维ILD患者的疾病进展相关,包括IPF,SSC和RA [33- - - - - -36].已经证明nintedanib可以防止前纤维化巨噬细胞的极化。当从人THP-1细胞分化出来的巨噬细胞暴露在IL-4/IL-13或IL-4/IL-13和IL-6的鸡尾酒中,nintedanib以100 nM的浓度处理时,CCL18的释放明显减少[37].假设尼丁尼对CSF1R的抑制活性已经用IC酶促水平证明505nm [25,至少对这种减少负有部分责任。最近的一项研究表明,nintedanib (0.01-1 μM)可抑制csf1诱导的CSF1R磷酸化,显著减少CCL2的产生、巨噬细胞的粘附和巨噬细胞对M2a替代品巨噬细胞的极化[38].Nintedanib也被证明可以抑制单核细胞的替代活化。在100 nM的浓度下,nintedanib显著降低了与巨噬细胞CSF、IL-4和IL-13孵培养的人巨噬细胞M2的极化,从CD163和CD206的平均荧光强度的变化可以看到,而M1标记物的表达没有变化[39].
Nintedanib抑制进行性肺纤维化的基本过程
纤维细胞是纤维化型ild中肺成纤维细胞的来源,并被认为促进纤维化[40].Nintedanib已被证明可以减弱纤维细胞的迁移,它们向成纤维细胞的分化,以及通过培养的纤维细胞触发成纤维细胞的增殖[41].激活的间质成纤维细胞是纤维化性ild发病机制中的关键效应细胞。Nintedanib抑制PDGF、FGF、VEGF等刺激诱导的成纤维细胞增殖[42,43]和血清[44].Nintedanib也被证明可以减少特发性肺纤维化患者肺成纤维细胞的运动[45]并抑制PDGF刺激的胶原凝胶中人肺成纤维细胞的收缩[46].这些效果不限于肺部:在SSC患者的皮肤成纤维细胞上进行的研究表明,尼丁胺降低了它们的PDGF和转化生长因子(TGF)-β-诱导的增殖和迁移[47].
Nintedanib抑制TGF-β诱导成纤维细胞向肌成纤维细胞转化[48]和TGF-β刺激的肺成纤维细胞释放胶原蛋白[37].在TGF-β刺激下,周细胞,间充质来源的微血管壁细胞,可以实现肌成纤维细胞的特征,形成成纤维细胞灶。Nintedanib被证明在脱细胞肺基质上培养具有肌成纤维细胞特征的周细胞可以抑制纤维连接蛋白和胶原1的沉积[49].此外,nintedanib降低IPF患者原发性肺成纤维细胞基质金属蛋白酶(MMP)-2和MMP组织抑制剂(TIMP)-2的酶活性和分泌[42],增加了TGF-β1激活的周细胞中MMP-8、MMP-9和MMP-13的表达,以及MMP-2和MMP-9的活性[49].在肺外,nintedanib减少了SSc患者皮肤成纤维细胞的肌成纤维细胞分化和胶原释放[47].
nintedanib在肺纤维化动物模型中的研究
Nintedanib已经在一些具有纤维化ILDs特征的动物模型中进行了探索,如IPF、SSc-ILD、RA-ILD、慢性超敏性肺炎和矽肺。在这些动物模型中,nintedanib被用于治疗,即。在实质性纤维化发作之后。Nintedanib表现出抗纤维化活性,而不考虑引起纤维化肺病理的触发因素,这支持了Nintedanib抑制纤维化发病机制中基本过程的假说。除了抗纤维化疗效外,nintedanib还显示了抗炎活性和对血管腔室的影响。在一些动物模型中,nintedanib还显示了对纤维化ILD以外疾病的影响,如在sc -ILD模型中对心脏纤维化的影响,在显示慢性超敏性肺炎特征的模型中对气道高反应性和炎症的影响。文中概述了不同的模型表1。
化学触发:博莱霉素诱导的肺纤维化
在啮齿动物中,脑内脑内菌霉素引发严重的上皮损伤,肺炎,肺部巨大纤维化反应和不规则的血管激发。在博莱霉素诱导的肺纤维化的三种动物模型中,Nintedanib显示出抗纤维化,抗炎和血管改造活性[43,48,53].通过微CT (micro computed tomography, CT)、Ashcroft评分、TIMP-1蛋白表达、TGF-β1和前胶原蛋白1 mRNA表达、肺组织胶原含量的显著降低,以及肺功能的改善,显示了抗纤维化活性。由压力-容积回路计算的静态顺应性决定。此外,nintedanib显示了抗炎活性,包括减少支气管肺泡灌洗液(BALF)中淋巴细胞的积累,减少IL-1β和趋化因子CXCL1/KC。在博莱霉素诱导的肺纤维化小鼠模型中,nintedanib使扭曲的血管结构正常化,并抑制肺泡巨噬细胞和肺泡上皮II型细胞的增殖[53].
环境触发:硅晶体诱导肺纤维化
在小鼠的气管内应用硅晶体导致持续的肺部炎症和类似矽肺特征的进行性纤维化反应。在这个模型中,nintedanib减少了肺炎症和肉芽肿的形成,减少了BALF中的中性粒细胞和淋巴细胞数量,以及肺组织匀质的IL-1β、CXCL1/KC和IL-6水平。nintedanib的抗纤维化活性被证明是减少肺组织纤维化和降低肺组织胶原水平[48].
过敏触发:卵蛋白诱导的纤维化肺重塑
在小鼠中,卵清蛋白对肺的慢性过敏刺激会导致气道高反应性、肺部炎症和杯状细胞增生等特征,最终还会导致气道纤维化重塑,不仅类似哮喘,还类似慢性超敏性肺炎。在这个模型中,nintedanib治疗导致气道高反应性的显著降低和肺部羟脯氨酸含量的降低,表明抗纤维化活性[54].
免疫触发:酶聚糖诱导的SKG小鼠关节炎和肺纤维化
在SKG小鼠(含有ZAP70突变导致自动反应性T细胞)中,唑氮施用诱导关节炎病理学。关节炎评分在唑氮给药后6周增加,仍然高达第10周,然后慢慢减少。至少有20%的唑氮经过肺纤维化治疗的SKG小鼠,反映在第10周的10周内肺胶原(羟脯氨酸)含量增加,这将进一步增加,直到第16周。在Zymosan施用后的第5-11周内用尼丁胺治疗SKG小鼠已被证明可以衰减关节炎病理学对肺纤维化没有影响,而尼丁胺治疗在10-16周内导致肺部胶原沉积的降低。尼林尼布似乎在肺中引发轻微但有选择性炎症;这对纤维化的影响是未知的[55].
血管触发:FRA-2的血管病变,皮肤,肺和心肌纤维化+ / -老鼠
转基因fos相关抗原-2 (fra2)在小鼠中的过表达导致微血管疾病和肺动脉高压的发展。fra2转基因小鼠发展进行性暴发性皮肤纤维化,真皮增厚,羟脯氨酸含量增加和肌成纤维细胞增加。这些动物的纤维化也会影响肺。在这个模型中,从9到16周使用nintedanib有效地减轻了皮肤和肺的纤维化,真皮厚度接近正常化,皮肤和肺中的羟脯氨酸含量减少,两个器官中的肌成纤维细胞数量减少。nintedanib能显著抑制肺动脉高压样变化,降低肺动脉平滑肌细胞增殖、肺动脉血管壁增厚及闭塞血管数量。在皮肤中,nintedanib减少了真皮微血管内皮细胞的凋亡,增加了内皮细胞的数量(血管化的标志),并阻止了前纤维化M2极化巨噬细胞的增加[39].
nintedanib治疗进展性纤维化型ild的临床研究
基于上述来自非临床研究的证据,nintedanib抑制进展性纤维化的基本过程,不管触发因素如何,以及nintedanib在减慢IPF患者疾病进展中的既定疗效[61,62), nintedanib已被研究为具有进行性表型的其他纤维化型ild的潜在治疗方法。SENSCIS试验(ClinicalTrials.gov标识符NCT02597933)对尼替尼的疗效和安全性进行了研究与高分辨率CT (HRCT)显示纤维化程度≥10%,筛查前7年出现SSc [63].在52周(主要终点)评估中,Nintedanib显著降低了强迫肺活量(FVC)的年下降率(−52.4)与−93.3毫升·−1).SENSCIS试验中SSc-ILD患者的FVC下降率低于INPULSIS试验中IPF患者的FVC下降率[62],但nintedanib的植被覆盖度下降率相对降低与安慰剂相似(分别为44%和49%)。“内联的试验”(ClinicalTrials.gov标识符NCT02999178)每天两次评估尼丁尼布150毫克的疗效和安全性与Plationbo在患者患者诊断的IPF诊断的患者中,他在HRCT上具有扩散纤维肺病> 10%范围的特征[64].为了符合进入INBUILD试验的资格,患者必须在筛查前2年达到疾病进展的标准,这是基于FVC下降、呼吸症状恶化或HRCT上纤维化改变程度增加。在SENSCIS试验中,主要终点是植被覆盖度的年下降率(mL·年−1)进行了52周的评估。有两个共同初级分析人群:所有患者和HRCT上常见间质性肺炎(UIP)样纤维化的患者;一些研究显示,在HRCT上有ILD和uip样模式的患者比其他模式的患者有更大的FVC下降风险[5,10,65].INBUILD试验的结果将于2019年报告。
结论
具有进行性表型的纤维化型ILDs在临床行为和驱动其进展的致病机制上都表现出共性。Nintedanib是一种已获批准的IPF治疗药物,最近已被证明可降低SSc-ILD患者的ILD进展速率。数据从在体外和在活的有机体内研究表明,尼丁尼抑制了肺纤维化的开始和进展中的许多步骤。此外,Nintedanib在几种动物模型中表现出抗纤维化效应,其具有纤维化ILD的特征,而不管导致纤维化肺病理学的触发。除IPF以外的渐进纤维血液患者患者中,初级临床试验很快就会报告结果。
可共享的PDF
致谢
编写本文期间,由Wendy Morris (FleishmanHillard Fishburn, London, UK)提供的写作援助由勃林格殷格翰(Boehringer Ingelheim)资助。作者完全负责所有内容和编辑决策,参与稿件开发的所有阶段,并批准最终版本。
脚注
L. Wollin是Boehringer Ingelheim Pharma GmbH & Co. KG的员工。
利益冲突:迪斯勒没有什么可透露的。
利益冲突:E.F. reente没有什么可透露的。
利益冲突:D.W.H. Riches没有什么可透露的。
利益冲突:S. Stowasser是勃林格殷格翰国际有限公司的雇员。
利益冲突:R. Schlenker-Herceg是Boehringer Ingelheim Pharmaceuticals, Inc.的雇员。
利益冲突:下午马赫有,通过他的研究机构获得了葛兰素史克研发和UCB的产业-学术资助;曾获得Apellis、AstraZeneca、Bayer、Biogen Idec、Boehringer Ingelheim、Galapagos、GlaxoSmithKline R&D、Indalo、Pliant、ProMetic、Roche、Samumed和UCB的咨询或演讲费用;并收到了Galecto的咨询费。
利益冲突:M. Kolb报告了来自罗氏(Roche)和勃林格殷格翰(Boehringer Ingelheim)的咨询和演讲资助和个人费用,来自葛兰素史克(GSK)、吉利德(Gilead)和Prometic的咨询资助和个人费用,来自Actelion、Respivert、Alkermes和Pharmaxis的资助,来自热那亚(Genoa)、Indalo和Third Pole的咨询个人费用。
- 已收到2019年1月23日。
- 接受2019年6月20日。
- 版权所有©ers 2019
本版本在知识共享署名非商业性许可4.0条款下发布。