抽象的
总体而言,由于诊断和更好的治疗,哮喘死亡率在过去30年中急剧下降,特别是在20世纪90年代,遵循吸入的皮质类固醇(ICS)更广泛地使用。IC对其他长期结果的影响,例如肺功能下降,部分是部分原因是与这些结果相关的因素不完全理解。本综述的目的是评估药理学干预,特别是ICS对哮喘进展和死亡率的影响。此外,我们审查了药物治疗对哮喘进展和死亡率的潜在作用机制,IC对肺功能的长期变化的影响,以及IC在各种哮喘表型中的作用。
总体而言,通过改善症状,肺功能和降低的恶化来测量,存在令人兴奋的ICS值为改善哮喘控制的证据。然而,令人信服的证据表明,ICS阻止了一些患者患有肺功能下降的证据,虽然不是全部,哮喘患者。严重的恶化与肺功能的更快下降相关,并且通过降低严重加剧的风险,可能至少部分地防止这种下降。使用行政数据库的研究也支持IC在降低哮喘死亡率方面的重要作用,但幸运的是,令人难以置信的事件令人难以置信的事实使得这将在前瞻性试验中表现出来。
抽象的
在改善哮喘控制和间接证据时,IC的价值有令人信服的证据,即IC通过防止严重加剧来阻止肺功能下降。基于登记的研究支持IC在降低哮喘死亡率方面的作用。http://bit.ly/2vcnjaz.
介绍
从古代描述了哮喘死亡[1].亨利·海德索尔特(自己患有哮喘)写道,在1860年,哮喘的自然历史,虽然非常年轻的患者恢复和死亡的风险较低,在那些年龄超过45岁有一个逐步恶化的疾病,死亡的风险增加(2].
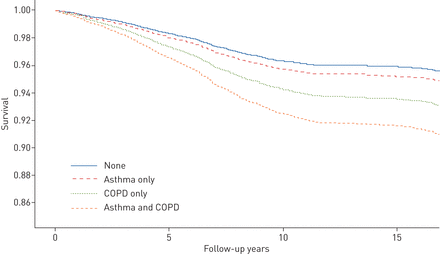
吸烟(3.]和慢性阻塞性肺病(COPD)[4.]已知与死亡率增加有关,主要是由于非呼吸性原因。毫无疑问,从20世纪50年代到80年代,一些国家出现了哮喘死亡和哮喘死亡流行的报道,可能是由于过量使用吸入性β2受体激动剂(5.,一个悬而未决的问题是,在生命早期出现哮喘的患者是否会由于哮喘本身或其他疾病而增加死亡风险。造成这种不确定性的原因包括哮喘的异质性、它与其他疾病的频繁关联以及经证实的死亡原因的准确性较差[6.].一些在哮喘诊断后的患者中进行的长期研究得出结论,与年龄匹配的对照组相比,没有吸烟或肺功能下降等伴随风险因素的哮喘本身与生存率降低无关[7.-14].相比之下,晚发型哮喘患者和老年哮喘患者[15]似乎增加了死亡风险,特别是与其他疾病,主要是慢性阻塞性肺病(图1)或肺功能减低[8.-11那13].
Cox比例风险模型的结果。曲线根据基线检查时的性别、年龄、体重指数、教育程度、种族/民族和吸烟状况进行调整。慢性阻塞性肺病:慢性阻塞性肺病。复制自[8.经允许)。
总的来说,哮喘死亡率在过去30年有所下降[16],部分原因是改善诊断和更准确的死亡认证,而且由于更好的治疗,特别是引入吸入皮质类固醇(ICSS)[6.].然而,没有随机对照试验(RCT)证明,ICS治疗哮喘患者的主要或次要结局是生存改善;唯一的证据来自基于登记的研究[17那18].本综述的目的是评估药理学干预措施,特别是ICS对哮喘进展和死亡率影响的证据。
哮喘自然史
描述哮喘的自然历史与定义哮喘的挑战造成相同的挑战。这是由于气道疾病在“哮喘”标签下统一的异质性[19].因此,自然史可能遵循疾病进展的不同路径,包括肺功能下降、缓解、复发、发病率和死亡率。
有关哮喘的自然历史的信息主要来自三种研究:1)在专业医院诊所进行的主要严重或难以治疗的哮喘患者的研究;2)患有哮喘,儿童和成人的个体的群体,与健康的个人一起注册潜在人口研究;3)基于注册表的研究,使用从医院,处方和死亡率记录中检索的数据。介入研究的数据也可以有助于了解自然历史的知识,尽管这种研究通常太短暂,无法推断到寿命的观点。虽然来自专业部门的研究通常包括良好的患者,但它们选择具有最严重的哮喘的个体亚组,代表哮喘群的10%,他们可能对大多数人具有更差的预后,具有较高的哮喘,谁使用间歇性治疗,谁具有罕见的恶化[20].一般人群队列研究(尤其是基于注册的研究)可能因诊断不确定和参与者特征不佳而受到批评,因为它们并不总是包括临床重要变量,如肺功能、日常症状和生物标志物,例如嗜酸性粒细胞或呼出的一氧化氮(Feno.).然而,近年来,一些精心设计的儿童哮喘队列为哮喘从儿童到青少年甚至成年的进展提供了新的线索,其中一些队列包括50多岁的人[21].
儿童哮喘肺功能的自然史
儿童研究表明,在诊断时,作为一个群体,哮喘的儿童已经在1 s中已经减少了强制呼气量(FEV1)和fev.1/强制生命能力(FVC)比率。纵向观察已经确定了几种不同于正常的轨迹,就最大fev而言1,fev的持续时间1成年早期高原和FEV发病年龄1衰退。在一项研究中,只有25%的儿童具有正常的肺功能发展模式,而26%的增长率降低和早期下降,23%仅降低增长,26%的生长率下降和早期下降[22].
在另一个队列中,患有最严重的症状的儿童在10年龄和达到50年代的时候减少了肺功能。但是,肺功能下降(FEV1和FEV1/FVC比率)介于20和50之间 年龄不比无哮喘对照组快,且与初始哮喘严重程度无关[23].在另一个队列中也观察到了类似的模式,在该队列中随访的儿童年龄为10-15岁至60-65岁[24].因此,似乎儿童哮喘大多数在生长期期间大多施加对肺功能的有害影响[25].预测成年期导致较差的肺功能导致的因素包括低基线FEV1早期过敏、低支气管扩张剂反应、气道高反应性(AHR)、男性。
活性吸烟对儿童哮喘和早期哮喘的个体肺功能的影响一直是辩论的主题[26-28].有些研究表明,在这一组中,吸烟的作用在驾驶肺功能障碍方面很小[29].其他研究表明,吸烟只在非特应性哮喘患者中起重要作用[30],然而仍有其他研究表明特应性和吸烟的协同作用导致慢性气流受限[31].
成人发病哮喘肺功能自然史
大多数针对成人的研究表明,作为一个群体,哮喘患者的FEV较低1和FEV1/ fvc比率比健康的个体。降低肺功能的预测因素包括成人发作,长期疾病,严重的症状,频繁的恶化,吸烟,持续暴露于过敏原和职业药物,慢性粘液的过度术和高水平的AHR,IgE和嗜酸性粒细胞[26].其中一些预测因子已在纵向研究中转载,结果已被肺功能下降。这些分析的初始焦点是肺功能在哮喘的哮喘上的速度比健康的个人更快,包括吸烟的作用[32那33].近期纵向研究确定了与更快的FEV相关的可修改特性1下降,包括高频率和严重程度的恶化[34那35),和高Feno.嗜酸性粒细胞[36-38].
早期的研究没有区分童年发病与成人哮喘(39]. 这是相关的,因为成人发作的哮喘除了对治疗反应较差外,似乎还与疾病进展的更高风险相关,包括更快的FEV1衰退 [40-42].此外,在具有哮喘的个体中的基线上存在气流限制,有时标记的哮喘 - COPD重叠(ACO)的条件也与更快的FEV相关联1下降,特别是在40岁后哮喘病发作者[13].相比之下,基线时无气流限制的早发哮喘和伴有早发哮喘的ACO均与随后的正常FEV相关1衰退 [13].
哮喘死亡率
大多数哮喘死亡是可以预防的。虽然在过去几十年中,大多数国家的哮喘死亡率大幅下降,但即使在发达国家,哮喘死亡仍在发生,并与社会贫困密切相关[43那44].这表明对医疗保健/药物的差额良好,并且对IC的低粘附是重要的可修改因素。此外,在IC的引入之前和之后的研究表明,过度吸入β2-激动剂增加哮喘死亡率[5.].
哮喘死亡风险增加相关的患者特征包括与快速肺功能下降相关的因素。因此,严重且难以治疗的哮喘,晚期哮喘,目前吸烟,慢性气流的存在,嗜酸性粒细胞,支气管性高度,AHR,阿司匹林敏感性,先前的重症监护单位录取以及心脏病的存在已经相关贫穷的生存[7.那45-48].最近明确表示具有哮喘和COPD(ACO)的特征的个体减少存活率。在哥本哈根市心脏研究中,与健康从不吸烟者相比的预期寿命减少了~9岁,患有ACO和早期发病哮喘,并在患有ACO和晚期哮喘的人中〜13岁,而它只是减少3年的哮喘,保存肺功能和低烟草暴露(图2) [13].在一项丹麦队列研究中,患有ACO的女性死亡率高于单独患有哮喘或COPD的女性[49].
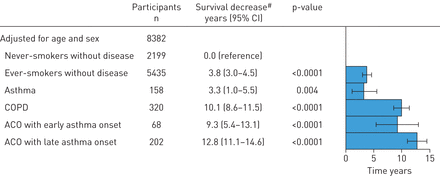
在哥本哈根城市心脏研究的六个亚组中,由吸烟和存在气道疾病定义的生存率降低。COPD:慢性阻塞性肺疾病;华:asthma-COPD重叠。#:基于Makuch-Ghali曲线的偏置纠正盗法估计。再现和修改[13经允许)。
早期的流行病学研究,基于纵向跟踪队列或健康登记,一直表明普通社区的哮喘患者作为一个群体,死亡风险高于健康人群(风险比1.5)[46那50].风险增加的原因是包括慢性阻塞性肺病和肺炎在内的呼吸道疾病的死亡率升高。人们还在争论,哮喘是否像慢性阻塞性肺病一样,也会使个人更容易患缺血性心脏病和肺癌。然而,一项针对吸烟者和从不吸烟者哮喘的长期预后的研究表明,这些关联可能是由于对吸烟、社会地位和心脏病的情况下的心血管危险因素的不适应造成的[14那51].
在哮喘诊断,严重程度评估和治疗中改变概念,以及它们对哮喘进展和死亡率的影响
第一个哮喘诊断和治疗指南发表于20世纪80年代末[52-55]. 一些国家(特别是新西兰)哮喘相关死亡率的增加刺激了这些文件的编制[5.]),20世纪70年代和1980年代的许多国家哮喘患病率显着增加[56].这些是共识陈述,而不是正式的循证临床实践指导方针,但所有这些指南都确定了使用目标标准来确定哮喘的诊断,并根据感知的情况下没有改变,并基于所感知的推荐治疗选择疾病的严重程度。治疗的目标是改善症状控制和肺功能。已经确定了气道炎症在哮喘发病机制中的重要性[57]但早期的文件并没有强调抗炎治疗的益处,并且由于迅速改善症状和肺功能,特别吸入β的药物2-激动剂是治疗的重点,特别是轻至中度哮喘患者。
过度依赖吸入β的影响2一名主义者是深刻的[58].最常用的是吸入短效β2目前似乎已知为唯一用作哮喘的唯一治疗方法,以促进嗜酸性气道炎症[59],导致哮喘控制恶化[60]在某些情况下,还会增加哮喘死亡的风险[61].吸入长效β也会增加哮喘死亡风险2-激动剂(LABAs)是唯一的治疗方法[62].
发生了哮喘管理的范式变革,在该管理中,现在专注于整体哮喘控制,由两个域组成:1)实现当前的哮喘控制和2)最大限度地减少未来风险,特别是严重的恶化,肺功能丧失和副作用的药物。现在由控制疾病所需的治疗水平定义哮喘严重程度[63],而不是像以前那样,对症状、肺功能和缓解药的使用进行复杂的算法计算,该算法没有考虑治疗要求。此外,人们对气道炎症在引起哮喘表现中的作用有了更好的理解,包括症状、可变气流阻塞和严重恶化。事实上,严重恶化不仅被认为是至关重要的治疗目标,而且还与哮喘的进展和肺功能的更快下降有关[35].
这些变化导致了对ICS在哮喘管理中的关键作用的进一步认识。ICS治疗已知可以改善哮喘的所有表现,并降低哮喘死亡率[17],在过去十年中,对于所有需要缓解症状的患者,建议每周使用2次或更多的维持性ICS治疗。最近,由于越来越多的人认识到轻度哮喘患者的发病率比以前认识到的要高[64],ICS现在推荐作为所有患者的治疗选择[6.].此外,ICS/快速发作β的使用2作为所有哮喘患者的患者的救助药物,优先于SABA,对治疗建议(图3) [65].
全球哮喘倡议:针对12岁以上成人和青少年的逐步哮喘治疗策略。ICS:吸入激素;萨巴:短效β2- 一方;LTra:白酮受体激动剂;Laba:长效β2- 一方;IL:白细胞介素;R:受体;OCS:口腔皮质类固醇。#:超说明书(仅与布地奈德-福莫特罗有关);¶: off-label(单独或联合ICS和SABA吸入器);+:考虑增加屋尘螨舌下免疫治疗致敏患者变应性鼻炎和强迫呼气量在1 s >70%预测;§:低剂量ICS-Formoterol是针对患者规定的患者蛋白质蛋白质或BECLOFORAONE甲酰胺 - 蛋白质维持和缓解疗法的救济。从[65经允许)。
这种关注于ICS使用的结果,作为轻度哮喘的单一疗法或在单一吸入器中与吸入患者的患者一起用于中度至严重的疾病的患者,是严重哮喘恶化和相关的急诊部门访问或住院的风险均下降,都在研究这些治疗方案的临床试验中[66-68]和现实世界的环境中。加拿大安大略省的一项研究报告,在2003年至2013年期间哮喘急诊部门访问近50%69],整体哮喘死亡率在测量的国家下降[43那70].
目前药物对严重哮喘进展和死亡率的影响
大多数患者可以从有或没有LABA的ICS实现对哮喘的令人满意的控制。然而,5-10%的疾病有严重的疾病,需要进行广泛的治疗,以实现控制或仍然不受控制,尽管这种治疗方法71那72].这一亚组占哮喘发病率和死亡率的大多数,占哮喘总保健费用的60%。此外,近期有哮喘加重史的患者每年的医疗费用尤其高,估计为无哮喘加重史的严重哮喘患者的3倍[73].
重度哮喘在临床问题、肺功能损害的性质和潜在病理方面具有异质性[74].正常复杂,因为许多患者主要存在临床严重的病症,主要是因为诊断是不正确的,或者由于吸入器技术或治疗依赖性的问题。其他患者具有主要由合并因子驱动的持续性哮喘症状。国际欧洲呼吸协会/美国胸部社会(ER188bet官网地址S / ATS)严重哮喘的指导方针承认这些困难并产生了最广泛接受的定义[71].这是“哮喘需要治疗(与guideline-suggested药物为全球倡议哮喘阶段4 - 5哮喘(大剂量ICS和腊八或白三烯修饰符/茶碱)前一年或系统性皮质类固醇≥50%的前一年),防止它成为“不受控制”或仍“不受控制”尽管这种疗法”。在做出严重哮喘的诊断之前,应确认哮喘的诊断和解决共病。
ERS/ATS定义的一个重要方面是确定了不受控制的哮喘的不同标准,并且没有对病理生理途径的参与做出假设。这很重要,因为越来越清楚的是,不同的机制驱动临床问题的不同方面[74].例如,症状可能反映了与潜在的2型高气道炎症的气道功能障碍,合并症和心理因素更紧密地密切相关,而严重的加剧则更加紧密地反映了由于嗜酸性嗜纤过,2型高气道炎症引起的支气管扩张剂无响应气流限制。推动肺功能丧失丧失的机制不太清楚,但中性粒细胞和2型高气道炎症可能是有贡献的[36那75].治疗干预对临床问题的影响也不同,LABAs对症状和肺功能的影响比例大于恶化(特别是更严重的事件),而ICS或增加ICS剂量则相反[76].
严重哮喘的发病率高,医疗成本和治疗相关的副作用意味着对替代疗法有大的未满足需求。治疗应靶向负责临床问题的病理生理机制,应适用于每个患者。一个特别富有成效的发展领域一直在使用靶向2型细胞因子的单克隆抗体参与2型高气道炎症的发育[72].这些治疗对发作频率有很大的影响,但对症状和肺功能的影响不那么显著。其中第一个是抗ige (omalizumab),目前已知对有2型气道炎症证据的患者特别有效[77].许多较新的方法,包括抗白细胞介素(IL)-5(Mepolizumab,Reslizumab),抗IL-5受体(Benralizumab)和抗IL-4受体α(杜帕里卢比,其中阻断IL-4和IL-13),已被监管机构批准用于治疗严重嗜酸性哮喘。
最近的一项大型流行病学研究表明,大多数严重哮喘患者随着时间的推移会转变为较轻的疾病[78].低社会经济阶层、合并症和高药物使用率都被认为是病情严重的预测因素。生物制剂治疗严重哮喘的临床试验显示,安慰剂治疗后的第一个月左右症状明显改善,但此后几乎没有改善(表1) [79-86].生物学处理对这一的影响是适度的,这意味着与炎症无关的因素,例如可用性,正在推动许多残留的症状。肥胖症的存在和高医院焦虑和抑郁症和抑郁症评分之间的高度相关性以及严重哮喘的症状也是一致的[87].
人们对肺功能随时间变化的了解较少,而肺功能在哮喘中的固有变异性、许多研究中的大量安慰剂效应和有限的随访时间使分析复杂化。因此,关于严重哮喘患者肺功能下降率和治疗影响的明确结论是不可能的。尽管如此,对大量人群的研究和评估气道结构的新方法的使用允许一些初步结论。H阿尔达et al。[88]报道了在使用美泊珠单抗治疗1年后,经ct评估支气管壁增厚减少,提示对气道重塑有一定影响。与此一致,C阿斯特罗et al。[86]发现了支气管扩张剂FEV的下降率的统计上显着差异11年后患有中重度哮喘的患者 使用杜匹单抗治疗的年份。
需要口服皮质类固醇(OCS)治疗或导致急诊部门访问和/或住院治疗的加剧,严重哮喘更频繁地发生,并且通常对与生物药物的治疗比其他结果措施(表1).这些事件的危险因素包括治疗依从性差、肺功能低下,特别是既往有加重史[72].此外,临床试验表明,恶化风险的增加与血液嗜酸性粒细胞计数或Feno.[89].这些生物标志物还可以预测生物治疗的功效,血液化粒细胞最接近抗IL-5的反应[90]及Feno.对抗il -4/13的反应[86]和奥玛珠单抗[77].
其发病率与正常饮食有关[91]或频繁使用急救OCS,如体重增加、糖尿病、高血压、骨质疏松和白内障形成[92],对严重哮喘患者影响最大。生物制剂具有显著的OCS保护作用[93-95因此,这很可能是严重哮喘长期自然史的另一个方面,在未来将得到改善。
目前药物对死亡率的影响
如前所述,过去30年哮喘死亡率的下降是社会经济条件和药物治疗改善的结果[6.那96].后者可以简单概括为过度使用救援SABA和无控制性药物(ICS)作为哮喘死亡的风险因素[61],以及越来越多地使用ICS [17],ICS /支气管扩张剂组合的优越性控制中度和严重哮喘[76那97],引入综合分子和快速作用β2受体激动剂(IE。Formoterol)作为释放和控制器药物[68那98],Tiotropium的额外效果[99],并在严重哮喘中引入单克隆抗体[100].
在评估随机对照试验(rct)提供的证据(包括严重不良事件、住院和死亡)时,必须考虑到在将患者纳入对照临床试验时进行的护理优化。显然,在这些环境中坚持护理与现实生活中是截然不同的。
英国医师学会发表的一份关于哮喘死亡的报告强调,哮喘死亡的最大危险因素是β-受体的过度使用2-激动剂,无持续抗炎治疗,既往住院和指南推荐依从性差[101]. 预防哮喘死亡的建议可以概括为:每家医院和初级保健机构都应指定专门标记的临床服务,负责在识别有哮喘死亡风险的患者和正确管理急性哮喘方面进行正式培训[101].考虑到>95%的哮喘死亡发生在具有可识别危险因素的成人中,而>85%的哮喘死亡发生的不是急性,而是进行性恶化,这尤其相关。芬兰哮喘规划的数据证实,采用抗炎治疗(主要是ICS)与哮喘发病率下降有关,从而减少了紧急服务、住院和死亡的使用[102].在这种背景下,很难探索目前可用的药物在预防哮喘死亡率方面的作用机制。此外,由于此类事件的数量极少,不可能进行随机对照试验来测试治疗效果或机制。
目前可用的生物治疗可有效地减少加剧,住院治疗和近乎致命的不良事件,并且可以防止急性致命事件。现实生活观察将来将在未来提供这些信息。然而,所有目前可用的药剂包括批准的生物学和新的制定的新化学实体,据信主要在2型高疾病患者中工作[100].不幸的是,对于严重的2型低哮喘患者,似乎没有新的治疗方法[71那96那100].
IC对肺功能长期变化的影响
在大多数哮喘患者中,ICS治疗可改善症状和肺功能,减少加重频率,并减少气道炎症[6.].此外,对哮喘ICS的功效的最早研究证明了它们减少或消除OCSS作为维护治疗的需要的能力[103那104]. 此外,登记研究表明,即使是低剂量的ICS也能降低严重哮喘恶化和哮喘死亡的风险[17那105].当ICSS和快速发射吸入β时,甚至可以看到IC以降低严重恶化风险的能力2-激动剂,由同一吸入器提供,只用于缓解治疗[66那106].
证明长期ICS治疗是否导致肺功能的保存更好的结果是更困难的。如前所述,大量少数患有哮喘经验的患者加速了FEV的下降1和FEV1/ FVC比率,可能导致不可逆转的气流限制[107].这可能是由气道壁增厚,所谓的气道重塑引起的,而不是像慢性阻塞性肺病那样的肺气肿[108].研究表明,ICS可能会降低气道重塑的某些成分[109那110]. 因为ICS,特别是与LABA联合使用,可以降低可能加速FEV的严重哮喘恶化的风险1下降,早期开始长期治疗可能会改变FEV的自然历史1患者的亚组下降,易于肺功能快速丧失[111].
哮喘诊所的儿童和成年人的观察性,非andomisienced研究[112那113],以及对普通人群中患有哮喘的成年人的研究[114[已表明ICS治疗可能对肺功能的疗程有益。然而,这一直很难在RCT中证明,因为需要3年的观察,以得出关于FEV的长期变化的结论1,由于相当大的测量误差和一个非常适度的年龄相关的年度FEV的组合1衰退 [115].此外,由于症状不充分的症状和恶化的发生,在这种研究中可能导致甚至温和哮喘的个体随机化可能导致在这种研究中产生大量戒断。
然而,具有足够长的观察时间的两个RCT评估了IC对纵向肺功能变化的影响。营地(童年哮喘管理计划)研究5-12岁的随机儿童,患有轻度至中度的哮喘,对布达尼顿,Nedocromil或安慰剂,并遵循6年[116].该研究发现,IC在Nedocromil或安慰剂上没有任何关于核心偶联剂FEV的生长速度的损益1.START(吸入类固醇治疗作为早期哮喘的常规治疗)研究将持续时间小于2年的轻度持续性哮喘儿童和成人随机分为布地奈德或安慰剂作为维持药物[117]. 使用支气管扩张剂后FEV的平均下降量较基线检查时有所降低1在成人吸烟者和不发器中的安慰剂和安慰剂中,在培养蛋白酶组的1和3年间[118].3年后,所有患者均给予布地奈德治疗;在包括FEV在内的多个临床变量方面,在整个研究中,从安慰剂转换为布地奈德的患者赶上了接受布地奈德的患者1[119].肺功能的这一结果与CAMP研究中看到的结果相似。
与ICS的早期干预的另一项研究表明,与初始服用SABA的群体,在早期发起ICS的良好益处,包括更好地改善肺功能[120].两年后,最初使用SABA的参与者被切换到ICS。研究结束后,参与者在现实生活中调整了ICS剂量。经过13年的随访,研究人员不再能观察到早期启动ICS治疗的患者肺功能的差异与那些在2年后开始IC的人[121].
ICS单独或联合在不同哮喘表型中的作用
随着许多不同表型的鉴定,对哮喘生物学和病理生理学的理解已经取得了进展[87那122那123].然而,目前的国际指南建议对几乎所有患者启动ICS治疗[6.].ICSS通过阳性基因调节和基因抑制作用,结果这种双重作用在航空公司中有效的抗炎作用[124].
ICS在某些临床参数(如肺活量测定)方面的改善是可变的[125].结果,使用不同的生物标志物,单独或组合,用于增加ICS响应的可预测性[126].例如,已显示痰嗜酸性粒细胞水平来预测对IC的响应[127那128]并预测ICS提款的恶化风险[129].在一个单独的研究中,根据痰嗜酸性粒细胞计数滴定IC治疗导致与指南驱动治疗相比的严重恶化较少[130].然而,诱导痰分析仍未广泛应用于常规应用。此外,通过使用多种炎症标志物(Feno.(包括血清嗜酸性阳离子蛋白浓度和血液嗜酸性粒细胞计数),持续哮喘患者ICS剂量的增加与症状和肺功能的平稳相关,但与炎症结局和AHR的进行性改善相关[131].遗憾的是,在治疗失败的时间内,使用基于生物标志物或基于症状的IC的调整不优于医师评估的ICS调整[132].
对IC的可变响应归因于潜水道炎症的不同机制[133].使用旨在鉴定特应炎症和氧化应激的存在,用于预测类固醇的临床反应的临床反应的研究表明高Feno.价值和高尿溴旋蛋白水平(氧化应激的指标)预测了对ICS治疗的有利临床反应(在哮喘控制问卷评分方面,FEV1和AHR),尽管缺乏安慰剂控制限制了研究的有效性[126].用复合生物标志物算法进行严重哮喘急性哮喘优化的随机务语试验(Feno.(血嗜酸性粒细胞和血清骨膜蛋白)来调节ICS剂量与最近提出了标准护理[134].U-BIOPRED(预测呼吸系统疾病结果的无偏性生物标记物)项目是一个为期5年的全欧洲项目,旨在确定严重哮喘的生物标记物[135].目前可用的几种生物标志物,U-Biopred将有助于进一步澄清常规实践中这些和其他生物标志物的潜在使用,并为新潜在的生物标志物的临床效用提供证据。
超过20年前的1997年发表的具有里程碑意义的研究显示,持续哮喘症状的患者尽管ICS治疗,增加formoterol布地奈德治疗能够减少轻微和严重恶化的速度,和改善症状和肺功能没有减轻哮喘控制(76].随后,一系列其他IC / Laba组合对哮喘患者的维护治疗表现出有益效果[6.]. 例如,GOAL(获得最佳哮喘控制)研究表明,ICS/LABA组合(氟替卡松/沙美特罗)比ICS单独使用更有效地控制1年以上的哮喘 年[136],且受益持续至少6个月,在稳定的剂量下几乎没有失去控制的迹象[137].与维护ICS / Laba组合实现更好的疾病控制的概念与中度至严重的哮喘的倍增ICS单药治疗相比,使用IC / Laba组合作为维护和救济,因为此类使用确保了及时管理疾病恶化的抗炎剂[68那98那138].在症状恶化时给予ICS同时给予快速支气管扩张剂的好处也应用于轻度哮喘与倍氯米松-沙丁胺醇联合用药[106]以及最近的布地奈德-福莫特罗联合用药[66那67].
最后,ICS治疗与下呼吸道微生物组中相对丰度的变化有关,特别是ICS和OCSS的组合影响不同细菌物种的α-和β-多样性[139]. 即使是轻度激素性哮喘患者,支气管微生物组的差异也与疾病的不同免疫学和临床特征以及对ICS的反应有关[140].
结论
有令人信服的证据表明ICS在改善哮喘控制方面的价值,通过改善症状、肺功能和减少恶化来衡量。然而,有不太令人信服的证据表明ICS可以防止某些(尽管不是所有)哮喘患者的肺功能下降。严重恶化与肺功能更快下降相关,通过降低严重恶化的风险,ICS可能至少部分地阻止这种下降。使用管理数据库的研究也支持ICS在降低哮喘死亡率方面的重要作用,但幸运的是,哮喘死亡率是一个罕见的事件,这使得在前瞻性试验中证明这一点的可能性极低。
致谢
编辑支持(以编辑语法,一致性,格式化参考文献和绘图人物编辑的形式)由大卫杨(Young医疗通讯和咨询有限公司,英国Horsham)提供。此支持由Chiesi Farmaceutici Spa提供资金。
脚注
支持声明:Chiesi Farmaceutici Spa支持这项工作。本文的资金信息已存入交叉参考基金登记处.
利益冲突:L.M. Fabbri报告了来自Chiesi的拨款、个人费用和非金融支持,来自AstraZeneca、GSK、诺华、Menarini、Boehringer Ingelheim、Zambon、Pearl Therapeutics的个人费用和非金融支持,以及来自Dompe的非金融支持。
利益冲突:I.D.Pavord报道了发言者的酬金,旅行费用和酬金从Astrazeneca,GSK,Boehringer Ingelheim和Teva,Grants and Speaker费用,咨询委员会的费用以及参加Chiesi的国际会议,咨询委员会工作的个人费用/ regeneron,梅克,诺华,Knopp和Roche / Genentech,从Circassia和Mundipharma发表讲话的个人费用,咨询委员会的咨询委员会的咨询和个人费用在提交的工作之外。
利益冲突:A. Papi报告了Chiesi、阿斯利康、葛兰素史克、Boehringer Ingelheim、Mundipharma和Teva的董事会成员、咨询顾问、讲座费用、研究拨款和差旅费用报销、Menarini、诺华和赞邦的讲座费用和差旅费用报销、赛诺菲的拨款,以及提交工作之外的费用。
利益冲突:S. Petruzzelli受雇于该研究的赞助商Chiesi Farmaceutici SpA。
利益冲突:P. Lange报告了阿斯利康、勃林格殷格翰和葛兰素史克的教学和顾问委员会工作的拨款和个人费用,Chiesi的教学和顾问委员会工作的个人费用,在提交的工作之外。
利益冲突:P. O'Byrne报告称,他接受了阿斯利康、Chiesi、葛兰素史克、Medimmune和诺华的演讲费;担任阿斯利康、Medimmune、诺华、GSK和Chiesi的顾问委员会成员;以及来自阿斯利康、Medimmune、Genentech和诺华的资助。
- 收到了2019年3月8日。
- 公认2019年4月24日。
- 版权©2019人队
本文是开放获取的,并根据知识共享188滚球软件署名非商业许可4.0的条款分发。