文摘
组织蛋白酶S(猫)是调节患者的肺囊性纤维化(CF)。然而,它的作用在CF肺部疾病发病机理尚不清楚。
在这项研究中,β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg), CF-like肺病的典范,与猫零交叉(猫−−/v)小鼠或对待猫抑制剂- 999。
活跃的猫是水平升高的肺βENaC-Tg小鼠与野生型相比(WT)同窝出生的。猫−−/βENaC-Tg老鼠表现出肺部炎症,减少粘液阻塞和结构相比βENaC-Tg小鼠肺损伤。药物抑制猫在肺部炎症,导致明显降低肺的肺损伤和粘液堵塞βENaC-Tg老鼠。此外,滴注法WT老鼠的猫进入肺部导致炎症,肺改造和upregulation粘蛋白的表达。猫的目标,抑制protease-activated受体2 (PAR2),βENaC-Tg老鼠导致减少气道炎症和粘蛋白表达,表明这种受体的作用CatS-induced肺部病理。
我们的数据表明猫的一个重要的角色在CF-like肺部疾病的发病机制介导的PAR2和突出猫作为治疗目标。
文摘
组织蛋白酶S参与炎症,粘液生产和肺组织损伤的模型CF-like肺病http://ow.ly/tHcm30nhlcX
介绍
组织蛋白酶S(猫)是表示由专业和非专业的抗原递呈细胞,并在主要组织相容性复合体是一个至关重要的组件类II抗原处理和表示(1]。猫是一个强有力的elastinolytic和溶胶原的半胱氨酸蛋白酶能够保持其酶活性在更中性pH值的环境中(2,3]。先前的工作已经证明,猫的升高患者的肺囊性纤维化(CF)肺部疾病(4- - - - - -7)和慢性阻塞性肺疾病(COPD) (8),猫与肺功能的下降和增加显著相关肺肺中性粒细胞浸润到CF (7]。此外,猫具有分裂能力和灭活宿主防御蛋白质如乳铁蛋白、β-defensins, LL-37、分泌leukoprotease抑制剂和表面活性剂的蛋白质(4,9- - - - - -12),可能会增加对感染的易感性这些muco-obstructive肺疾病患者。
然而,猫的角色在CF肺部疾病病理学尚未完全阐明。在本研究中我们使用CF-like肺部疾病的小鼠模型研究猫的功能在活的有机体内。超表达的β亚基上皮Na+通道(βENaC)导致气道表面脱水和粘液清除受损,产生慢性肺疾病的特点是气道粘液阻塞,炎症和结构性肺损伤小鼠(13]。因此,βENaC-overexpressing转基因小鼠模型(βENaC-Tg)分享了很多特征与人类CF,和是一个有用的在活的有机体内模型来研究中的作用和治疗潜在的猫CF-like肺部疾病(14]。
示范后,猫水平升高和活动的一个特征βENaC-Tg肺,我们走过βENaC-Tg老鼠在猫空(猫−−/)背景和评估气道炎症,粘液阻塞,肺损伤。验证的观察在这个模型中我们也调查了猫的治疗目标的影响通过一种小分子抑制剂在病变的肺。此外,我们灌输猫直接进入肺部的野生型小鼠(WT)调查影响炎症细胞招聘、粘蛋白生产和肺改造。为了进一步了解猫在肺功能,我们评估的角色protease-activated受体2 (PAR2),猫的目标(15- - - - - -20.),在调解猫βENaC-Tg小鼠的影响。
方法
全部细节是可用的补充的方法。
缩写的方法
所有实验是按照动物(科学程序)法案1986和当前的指导方针批准贝尔法斯特女王大学的伦理审查委员会(英国贝尔法斯特)。
本研究中使用的所有小鼠C57BL / 6的背景。这育种计划生成的四个基因型的老鼠进行调查:WT,猫−−/,βENaC-Tg和猫−−/βENaC-Tg老鼠。后代经聚合酶链反应(如前所述)基因分型(13,21,22从新生儿阶段使用)和老鼠。新生儿βENaC-Tg老鼠和WT同窝出生14天每天服用一次通过猫的皮下注射抑制剂v - 999 (100 mg·公斤−1;美国Virobay,门洛帕克,CA),选择性PAR2肽FSLLRY-NH2(4毫克公斤−1;研发系统,阿宾顿、英国)或各自的车辆控制,即。葡萄糖溶液和无菌水。WT小鼠气管内的灌输与重组人类猫(rhCatS 5µg;默克密理博,英国诺丁汉)。支气管肺泡灌洗(BAL)流体收集分析炎症标记物和细胞招聘如前所述13,23]。组织学染色和地貌形态示量评估领空的扩大,肺泡壁破坏和气道粘液含量进行了如前所述[24- - - - - -26]。
结果
UpregulationβENaC-Tg老鼠的猫在肺部
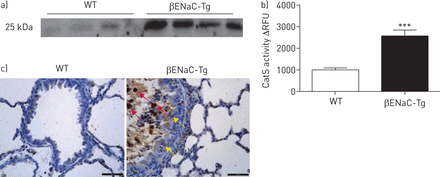
为了验证βENaC-Tg小鼠模型作为一个合适的模型来测试的影响针对猫,我们确定的状态猫βENaC-Tg老鼠和活动水平。我们观察到猫的蛋白质含量增加(图1一个猫)和活动(图1 b)BAL流体从βENaC-Tg老鼠WT与健康同行。另外,我们观察到猫染色增加βENaC-Tg鼠肺,主要是局部的巨噬细胞,与一些上皮染色也呈现(图1 c)。这些发现表明,就像人类CF,水平的提高活动βENaC-Tg老鼠的猫是一个特征模型。
组织蛋白酶S的水平和活动(猫)调节肺的β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。WT:野生型;RFU:相对荧光单位;拜尔港:支气管肺泡灌洗。猫的)免疫印迹BAL流体从βENaC-Tg和WT老鼠。n = 4 /组。b)猫活动落下帷幕流体从WTβENaC-Tg老鼠决心使用Z盐酸-Phe-Arg-7-amido-4-methylcoumarin,衬底(pH值7.5)。结果提出了随着时间的推移ΔRFU。n = 10组。* * *:p < 0.001。c)免疫组织化学染色对猫肺部分从WTβENaC-Tg老鼠。红色箭头:猫巨噬细胞染色;黄色箭头:上皮猫染色。
猫的基因消融导致降低βENaC-Tg小鼠肺部炎症
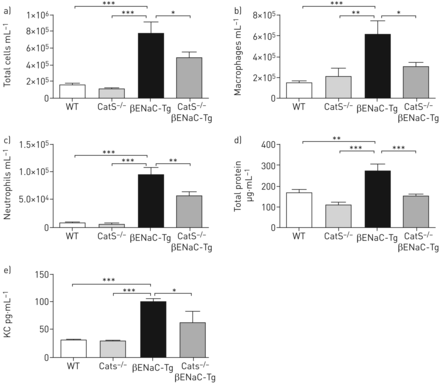
为了研究猫的角色CF-like肺部疾病的发病机制,我们首先评估肺部炎症的猫−−/βENaC-TgβENaC-Tg和控制老鼠(猫−−/和WT同窝出生的)。没有显著改变BAL流体细胞总数的猫−−/相比之下,WT控制老鼠(图2一个)。正如所料,βENaC-Tg老鼠表现出显著增加细胞的渗透与WT和猫相比−−/老鼠(图2一个)。猫−−/βENaC-Tg老鼠BAL总细胞数明显减少而βENaC-Tg老鼠(图2一个减少巨噬细胞(),证明了这一点图2 b)和中性粒细胞(图2 c)细胞群。平衡液总蛋白浓度显著高于在βENaC-Tg老鼠相比,控制老鼠(图2 d)。然而,在猫总蛋白质含量显著降低−−/βENaC-Tg老鼠与βENaC-Tg老鼠相比,建议减少肺损伤和炎症的严重程度(图2 d)。另外,我们观察到的趋化因子水平显著降低KC (图2 e)BAL流体的猫−−/βENaC-Tg老鼠而βENaC-Tg老鼠。
的基因消融组织蛋白酶S(猫)减少气道炎症β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。WT:野生型;拜尔港:支气管肺泡灌洗。βENaC-Tg老鼠与猫了−−/老鼠生产猫−−/βENaC-Tg老鼠。从WT BAL液体收集,猫−−/,βENaC-Tg和猫−−/βENaC-Tg老鼠。矿山总细胞,b)巨噬细胞和c)中性粒细胞计数,d)总蛋白浓度被量化。n =每组7 - 10。e) BAL流体的趋化因子水平KC评估ELISA。n = 5 - 7每组。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
猫的基因消融导致结构减少肺损伤和肺部的粘液阻塞βENaC-Tg老鼠
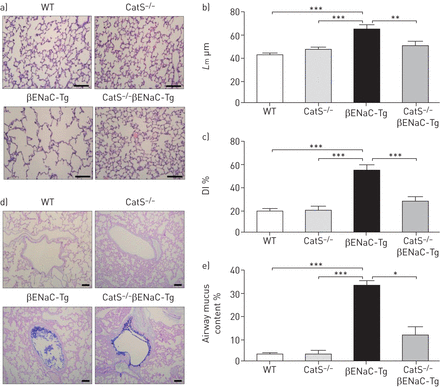
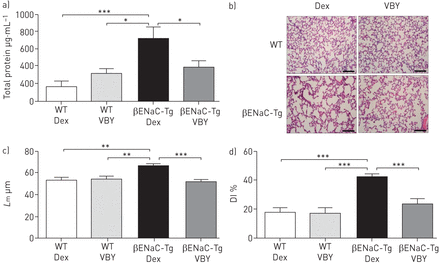
意思是线性拦截长度(l米)是一种测量远端领空扩大。气道部分与苏木精和伊红染色(代表图片所示图3一证明没有区别l米之间的猫−−/和WT老鼠(图3 b)。正如预期的那样,一个显著增加l米很明显的肺βENaC-Tg老鼠相比,控制老鼠(图3 b)。与βENaC-Tg老鼠相比,l米显著降低在猫−−/βENaC-Tg老鼠(图3 b),建议增加βENaC-Tg老鼠的猫在肺部可能发挥作用在远端领空扩大。此外,肺泡间隔破坏的程度,评估测量的破坏性指数(DI),显著降低了猫−−/βENaC-Tg老鼠与βENaC-Tg老鼠相比,没有区别的DI WT和猫之间的测量观察−−/控制老鼠(图3 c)。领空的情况下扩大和损伤观察,这些发现表明,增强猫水平βENaC-Tg中可能起着重要的作用在调节肺组织损伤和重塑CF-like肺病。组织学染色和量化的气道粘液含量表现出显著减少气道粘液阻塞的猫−−/βENaC-Tg老鼠而βENaC-Tg老鼠(图3 d和e)。总的来说,这些发现表明,猫与慢性炎症的发病机制,肺组织损伤和粘液插入CF-like肺部疾病的发展。
缺乏组织蛋白酶S(猫)β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)减少气道粘液阻塞,肺组织损伤。WT:野生型;他:苏木精和伊红;l米:意思是线性拦截长度;迪:破坏性的指数。WT)代表肺部分的图像,猫−−/,βENaC-Tg和猫−−/βENaC-Tg老鼠沾他用来评估气道损伤。酒吧规模:100µm。b)l米和c)迪测量评估HE-stained肺部分。d)代表图像的肺部分沾阿尔新Blue-Periodic acid-Schiff。酒吧规模:100µm。e)气道粘液量化表示为总数的百分比气道粘液。n =每组7 - 10。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
药物抑制βENaC-Tg老鼠的猫减少气道炎症
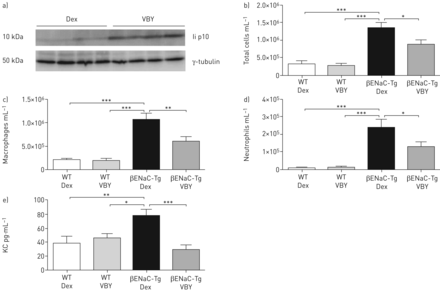
猫是有针对性的使用小分子抑制剂,v - 999 (27),在βENaC-Tg老鼠。抑制猫改变不变的链(2)处理和结果的积累10 kDa中间(p10) [1,22]。确定v - 999成功针对猫肺,我们评估的积累Ii p10片段通过免疫印迹。βENaC-Tg老鼠的肺治疗v - 999表现出二世p10水平的积累与车辆(葡萄糖)治疗βENaC-Tg老鼠(图4一)。最初,我们观察到βENaC-Tg老鼠用v - 999治疗14天从出生一段表现出显著增加生存而dextrose-treated老鼠(补充图S1)。βENaC-Tg老鼠与v - 999治疗显著降低矿山总炎症细胞浸润而vehicle-treatedβENaC-Tg老鼠(图4 b)。没有影响细胞总数在控制老鼠不管治疗。v - 999治疗显著降低BAL巨噬细胞的数量(图4 c)和中性粒细胞(图4 d)βENaC-Tg老鼠。另外,我们观察到KC(水平显著下降图4 e)BAL液体治疗的v - 999βENaC-Tg老鼠相比vehicle-treatedβENaC-Tg老鼠。这些数据表明,抑制猫抑制肺部炎症的小鼠模型CF-like肺病。
药理的目标组织蛋白酶S(猫)导致减少肺部炎症β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。敏捷:葡萄糖;v: v - 999;2:不变的链;WT:野生型;拜尔港:支气管肺泡灌洗。WT与猫βENaC-Tg小鼠每日治疗v抑制剂(100 mg·公斤−1)或车辆控制(敏捷)为14天。二世p10)免疫印迹的肺匀浆从敏捷,VBY-treatedβENaC-Tg老鼠。n = 4 /组。总细胞BAL b), c)巨噬细胞和d)中性粒细胞计数量化。n = 10 - 15每组。e) BAL流体的趋化因子水平KC评估ELISA。n = 15 /组。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
抑制肺猫减少肺损伤和肺结构蛋白质含量水平βENaC-Tg老鼠
蛋白质含量是评估BCA (bicinchoninic酸)测定和v - 999治疗βENaC-Tg老鼠BAL流体的总蛋白水平较低而vehicle-treatedβENaC-Tg老鼠(图5一个)。l米和迪用苏木精和eosin-stained肺部分从每组(图5 b空域扩大和肺泡杀伤性)作为标记,分别。有一个显著的减少l米βENaC-Tg小鼠治疗v - 999与车辆(图5 c)。此外,观察肺泡壁的破坏能显著降低v - 999治疗βENaC-Tg老鼠相比vehicle-treatedβENaC-Tg老鼠(图5 d)。这些数据表明,抑制猫导致的减少气道损伤CF-like肺病。
组织蛋白酶S(猫)抑制减少气道组织损伤β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。WT:野生型;敏捷:葡萄糖;v: v - 999;拜尔港:支气管肺泡灌洗;BCA: bicinchoninic酸;他:苏木精和伊红;l米:意思是线性拦截长度;迪:破坏性的指数。WT与猫βENaC-Tg小鼠每日治疗v抑制剂(100 mg·公斤−1)或车辆控制(敏捷)为14天。)BAL液蛋白质含量由BCA量化分析。n = 7 - 8每组。b)代表图像的肺部分沾他用来评估气道损伤。酒吧规模:100µm。c)l米DI和d)测量从HE-stained评估肺部分。n = 6 - 7每组。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
猫的抑制导致βENaC-Tg小鼠气道粘液含量减少
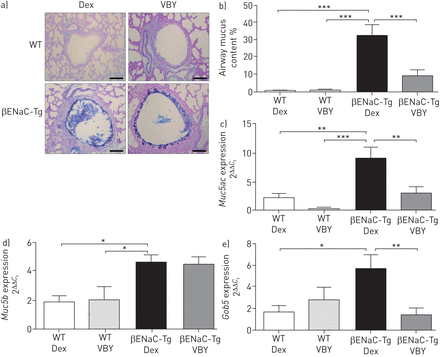
组织学分析表明,v - 999治疗βENaC-Tg小鼠出现明显降低气道粘液含量与dextrose-treatedβENaC-Tg老鼠(图6和b)。鉴于我们之前的结果改变粘液含量的猫−−/βENaC-Tg老鼠(图3 d和e),我们调查的表达黏蛋白Muc5ac Muc5b和杯状细胞标记Gob5 (图6 c- e)。治疗βENaC-Tg老鼠的v - 999出生的表达水平显著降低Muc5ac(图6 c),Gob5(图6 e)与dextrose-treatedβENaC-Tg老鼠。相比之下,抑制猫的表达水平没有影响Muc5b(图6 d)。
药理的目标组织蛋白酶S(猫)减少气道粘液堵塞和粘蛋白基因表达在β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。敏捷:葡萄糖;v: v - 999;WT:野生型。WT与猫βENaC-Tg小鼠每日治疗v抑制剂(100 mg·公斤−1)或车辆控制(敏捷)为14天。从WT)代表肺部分的图像,βENaC-Tg小鼠接受敏捷或v沾阿尔新Blue-Periodic acid-Schiff评估气道粘液的内容。酒吧规模:100µm。b)气道粘液量化WT和βENaC-Tg小鼠接受敏捷或v。结果给出了含有粘液气道总面积的百分比。n =每组卖地。表达水平的c)Muc5acd)Muc5b和e)Gob5在肺组织被定量PCR分析。每组n = 6日至14日。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
猫肺滴剂对肺部炎症和粘蛋白的影响生产
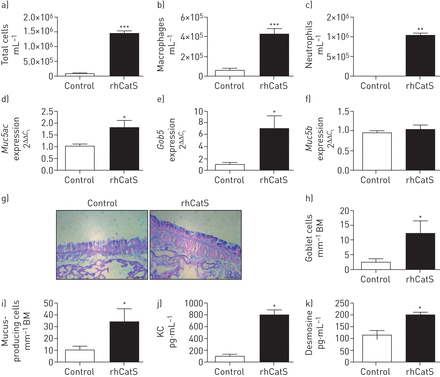
直接滴注法rhCatS WT诱发小鼠的肺部炎症细胞的重要的招聘(图7),很大程度上归因于大量巨噬细胞(图7 b)和中性粒细胞(图7 c)。尽管有显著的表达水平增加Muc5ac(图7 d),Gob5(图7 e)小鼠的肺中,收到了猫,的表达水平Muc5b是不变的(图7 f)。此外,rhCatS政府与杯状细胞增生(图7 g我)。KC水平平衡液(图7 j)后显著增加rhCatS滴注法和肺损伤的证据也观察到弹性蛋白分解产物的水平显著增加,锁链素,可检测CatS-treated小鼠的肺(图7 k)。
组织蛋白酶S(猫)滴剂诱发炎症和肺部的粘液。rhCatS:重组体人猫;BM:基底膜;WT:野生型;拜尔港:支气管肺泡灌洗;AB-PAS:阿尔新Blue-Periodic acid-Schiff。rhCatS WT老鼠收到一个气管内的滴剂(5µg)或醋酸钠缓冲控制。24小时后,BAL液体收集,和总细胞,b)巨噬细胞和c)中性粒细胞计数量化。d)的表达水平Muc5ac,e)Gob5和f)Muc5b在肺组织被定量PCR分析。g)代表沾AB-PAS肺的图像部分。酒吧规模:50µm。h)酒杯和我)食用从AB-PAS-stained肺部分细胞被量化。结果表现为细胞·毫米1BM。BAL流体j)趋化因子KC ELISA和k)锁链素水平进行评估。第4 - 9 n =每组。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
CatS-induced肺部炎症和粘蛋白表达部分介导的通过PAR2
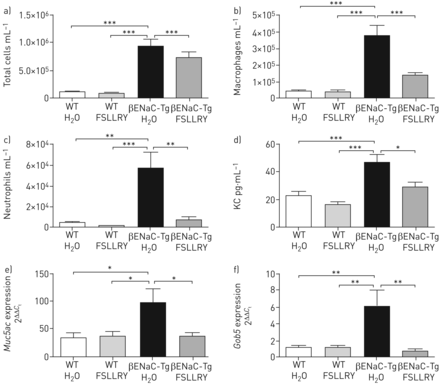
猫曾PAR2激活受体,导致炎症的症状,瘙痒和疼痛,和与环境有关,如特应性皮炎和结肠炎以及内皮功能障碍与狼疮肾炎和糖尿病(15- - - - - -20.]。然而,一个角色在CatS-mediated PAR2肺部炎症或粘蛋白的表达在活的有机体内迄今为止还没有被描述。治疗与PAR2拮抗剂(FSLLRY-NH WT老鼠2)减少炎症细胞的渗透到肺部rhCatS-treated老鼠(补充图S2)。因此,PAR2拮抗剂的影响在βENaC-Tg鼠肺评估。类似于基因和药物抑制猫,封锁的PAR2βENaC-Tg导致肺部炎症,显著降低小鼠肺渗透总共减少炎性细胞(图8)、巨噬细胞(图8 b)和中性粒细胞(图8 c)在肺部βENaC-Tg老鼠相比,车辆(无菌水)治疗βENaC-Tg老鼠。此外,BAL流体KC水平显著降低PAR2 antagonist-treatedβENaC-Tg老鼠相比vehicle-treatedβENaC-Tg老鼠(图8 d)。的表达水平Muc5ac和Gob5(图8 e和f)减少肺部PAR2 antagonist-treatedβENaC-Tg老鼠相比vehicle-treatedβENaC-Tg老鼠。然而,没有级别的领空扩大或减少肺泡的毁灭l米分别和DI(数据没有显示)。总的来说,这些数据表明一个重要的角色在CatS-mediated PAR2肺部炎症和肺部的粘液生产βENaC-Tg老鼠。
Protease-activated受体2 (PAR2)抑制减少气道炎症在β-epithelial Na+channel-overexpressing转基因小鼠(βENaC-Tg)。WT:野生型;H2O:无菌水;FSLLRY: FSLLRY-NH2。WT和βENaC-Tg小鼠每日治疗PAR2肽FSLLRY·(4毫克公斤−1)或车辆控制(H2O)为14天。支气管肺泡灌洗)总细胞,b)巨噬细胞和c)中性粒细胞计数,d)趋化因子KC水平量化。n = 6尺11寸每组。表达水平的e)Muc5ac和f)Gob5在肺组织被定量PCR分析。每组n = 9。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
讨论
猫是升高的CF肺部疾病和慢性阻塞性肺病muco-inflammatory条件,并被视为一个潜在的治疗各种疾病的目标(最近了28,29日])。我们曾表明,猫活动增加CF肺癌与肺功能的下降(7]。此外,肺猫与中性粒细胞浸润和活动显著相关水平CF肺(7猫,充实的假设可能发挥作用在肺中性粒细胞招募30.),这是与CF肺部疾病有关。在目前的研究中,我们表明,升高的猫也是一个关键特性βENaC-Tg小鼠的肺部疾病,CF-like肺病的典范。βENaC-Tg鼠标提供了一个相关模型为研究CF肺部疾病发病机理,特别是离子运输之间的交互,气道表面液体和黏膜纤毛的清除(13,14]。然而,由于CF跨膜电导调节器(雌性生殖道函数是βENaC-Tg正常小鼠肺(13),这个模型不允许直接与CFTR突变检测研究相关的病理生理变化,如细胞功能障碍和粘液成分。可拆卸的猫的药理抑制剂(v - 999)或基因方法(猫−−/)在βENaC-Tg模型导致肺巨噬细胞和中性粒细胞细胞数量大幅下降,为猫提供一个角色的进一步证据在调停肺部炎症30.- - - - - -32]。
βENaC-Tg老鼠的以前的工作表明,中性粒细胞弹性蛋白酶的基因击倒,基质金属蛋白酶12显著降低结构肺损伤,但没有影响粘液阻塞,肺死亡率(33,34]。在这项研究中,药物抑制和基因消融的猫不仅导致气道结构损伤和减少肺部炎症,而且改善气道粘液堵塞和提高了新生儿小鼠的存活率。这些数据表明猫在炎症细胞的参与招聘、肺组织损伤和粘液堵塞的发展。在协议,我们也表明猫的直接管理WT诱发小鼠的肺中性粒细胞增加招聘和KC水平这些小鼠的肺。肺猫滴剂导致显著增加粘蛋白Muc5ac的表达和Gob5标记与杯状细胞增生(35,36),杯状细胞的数量以及食用细胞,尽管没有影响观察Muc5b表达式。这些结果表明CF肺CatS-mediated肺部炎症的作用,并表明,猫可能导致气道粘液堵塞通过杯状细胞增生,粘液增加生产。
这些影响可能是由于部分激活PAR2的猫,曾被证明在其他肺外的器官系统(15- - - - - -20.]。迄今为止的研究表明,PAR2激活与炎症有关,白细胞招募和粘蛋白表达(37- - - - - -40]。在这项研究中,我们已经表明,拮抗PAR2导致肺部炎症细胞浸润减少小鼠暴露于猫以及βENaC-Tg肺。此外,减少BAL流体KC水平和Muc5ac的表达水平和Gob5也观察到PAR2 antagonist-treatedβENaC-Tg老鼠。与之前的报道相一致,我们的数据表明,猫可能施加其影响肺部炎症和粘液堵塞,至少在某种程度上,通过PAR2。相比之下,虽然击倒或抑制猫减少βENaC-Tg小鼠的肺组织破坏,我们没有观察到减少肺损伤(l米或DI) PAR2 antagonist-treatedβENaC-Tg老鼠,这表明猫可能是表演通过其他途径引起肺损伤。例如,我们已经表明,直接滴注法的猫WT老鼠肺部可迅速诱导(24小时内)BAL流体的锁链素水平,表明猫的影响也可能是直接在肺组织以及介导的通过PAR2。
总之,我们的调查显示,猫是升高的在活的有机体内模型CF-like肺部疾病,并可能促进肺细胞渗透,粘液阻塞和结构性肺损伤与慢性肺部疾病,如CF有关。这些结果表明,猫可能CF-like肺部疾病发病机制中发挥重要作用,最终导致组织结构完整性和肺功能的丧失。正如前面提到的,猫具有分裂能力和灭活抗菌蛋白主机(4,9- - - - - -12),可能会增加对感染的易感性muco-obstructive患者肺部疾病如CF和慢性阻塞性肺病。然而,进一步的工作是需要调查的影响高猫活动和肺猫抑制的影响假单胞菌感染的慢性肺部疾病。我们的研究结果表明,猫可能是一个有前途的治疗目标停止气道炎症的恶化,粘液阻塞和肺损伤与CF肺部疾病有关。
补充材料
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:D.M.小没有披露。
利益冲突:水银血压计布朗没有披露。
利益冲突:测向多尔蒂没有披露。
利益冲突:a . Abladey没有披露。
利益冲突:z Zhou-Suckow没有披露。
利益冲突:r德莱尼没有披露。
利益冲突:l . Kerrigan没有披露。
利益冲突:蔡玫杜德恒没有披露。
利益冲突:K.S. Borensztajn没有披露。
利益冲突:l . Holsinger Virobay的员工。
利益冲突:r·布斯7547701年美国专利。
利益冲突:C.J.斯科特是融合抗体的顾问公司,在提交工作;和对各种专利发明者命名组织蛋白酶S抗体用于治疗癌症,其中许多已经失效,不是目前的研究方向为公司(融合抗体PLC)。
利益冲突:g . Lopez-Campos没有披露。
利益冲突:j.s Elborn报告个人费用咨询委员会在拜耳工作,赠款和个人费用从Horizion顾问委员会的工作,在进行研究;个人费用咨询委员会工作从基耶西和Polyphor外提交的工作。
利益冲突:硕士商场赠款从德国联邦教育和研究报告(合同编号82 dzl00401和82 dzl004a1),在进行研究;个人费用从Spyryx生物科学顾问委员会和咨询工作,勃林格殷格翰集团和Polyphor从ProQR个人费用咨询委员会工作,PTC制药、箭头和Pro轴,个人费用从拜耳咨询和讲课,个人费用咨询企业疗法和胸骨生物制剂,个人费用咨询委员会工作,从顶点医药咨询和讲课,在提交工作;并在这项技术上拥有专利Scnn1b转基因小鼠与支付的版权费。
利益冲突:s·韦尔登报告英国赠款从草毒死和辉瑞在提交工作。
利益冲突:林祖嘉Taggart报告个人费用从Albumedix咨询公司,从草毒死和英国辉瑞和赠款,在提交工作。
支持的支持声明:囊性纤维化基金会(TAGGAR12I0、WELDON15G0 WELDON18G0),欧盟FP7(之下CFMATTERS;格兰特603038)、工程和物理科学研究委员会(a . Abladey和l·克里根助学金),QUB启动资金(s·韦尔登),医学研究理事会的信心概念规划(s . Weldon林祖嘉Taggart),经济部门(林祖嘉Taggart)和德国联邦教育和研究(82 dzl004a1硕士商场)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年8月10日。
- 接受2018年12月27日。
- 版权©2019人队