摘要
比较不同海拔地区慢性阻塞性肺疾病(COPD)患病率的研究报告了相互矛盾的结果。然而,家庭空气污染(HAP)是COPD的主要危险因素,在以往的分析中大多未被考虑,也从未被客观测量。我们的目的是比较低资源高原和低地地区COPD患病率及其危险因素,特别关注客观测量的HAP。
在农村吉尔吉斯斯坦,我们在高地(海平面〜2050米)和低地(海平面上方)环境中进行了一项基于人口的观察研究。我们在随机选择的家庭中进行了肺活量测定法,测量室内颗粒物质,空气动力学直径<2.5μm(PM2.5),并对其他COPD危险因素进行问卷调查。使用描述性统计和多变量logistic回归进行分析。
我们包括392名参与者:199名高地人和193名低地人。慢性阻塞性肺病在高地人群中更为普遍(36.7%)相对10.4%;p < 0.001)。他们的平均点2.5暴露也更高(290.0相对72.0µg·m-3;p<0.001)。除高PM外2.5暴露(OR 3.174, 95% CI 1.061-9.493)、海拔环境(OR 3.406, 95% CI 1.483-7.825)、吸烟包年(OR 1.037, 95% CI 1.005-1.070)和年龄(OR 1.058, 95% CI 1.037 - 1.079)也是导致高原人群COPD患病率较高的原因。
COPD患病率和HAP在高地地区最高,且独立相关。在这些资源匮乏的高地环境中,预防性干预似乎是必要的。由于这项研究是中亚地区第一个基于肺活量测定的流行病学研究,因此需要评估其通用性。
摘要
高室内PM2.5水平可以解释农村高海拔地区COPD患病率升高的原因:预防是关键!http:///wl.ly/hvc930mfekj.
介绍
慢性阻塞性肺疾病(COPD)是世界第三大死亡原因,占全球所有死亡的5.7% [1那2].超过90%的慢性阻塞性肺病相关死亡发生在低收入和中等收入国家,导致巨大的临床、经济和社会负担[3.那4.].了解风险因素和疾病负担最高的地区是针对慢性阻塞性肺病量身定做的方法的关键。
在全球范围内,大约4亿人住在高海拔(海拔1500米)[5.]但是它仍然是难以置信在这些设置中的COPD患病率较高。各种环境中的五项观测研究报告了矛盾的结果[6.-10].此外,两项研究汇总了来自各种流行研究的数据,而其中一个人在更高海拔地区描述了较低的COPD患病率[11,另一组在调整几个风险因素后没有发现差异[12].然而,在这些汇总研究中的任何一个都没有调整家庭空气污染(HAP)。注意,特别是在低资源设置中,HAP越来越多地报告为COPD的主要危险因素[2那3.那13-18].
HAP是由室内使用煤炭和生物质(例如动物粪便、木材和作物残体),也被称为固体燃料。在全世界90%的农村家庭中,使用固体燃料做饭和取暖是很常见的,这导致了对肺有不同程度损害的污染物。受影响最严重的是妇女和她们的孩子,因为妇女经常在通风不良的房子里,每天几个小时在火上做饭,让孩子靠近自己[13-15].2015年,HAP估计负责420万人死亡,10.31亿日减少的健康生活[19].
之前的一些研究确实报告了跨海拔的HAP暴露,但使用了自我报告的代理(如“固体燃料使用”)[7.那8.那10].没有客观测量的个人颗粒物质暴露在活的有机体内,以作准确的污染评估[20.]早期的研究也几乎完全集中于城市环境,但农村环境获得清洁燃料的机会更为有限,因此受到HAP的影响更为严重[14].
因此,在这项研究中,我们旨在比较COPD的流行及其在农村,低资源高地和低地之间的风险因素,并特别关注HAP。我们预计高海拔地区的气候条件越来越极端气候条件增加了对(固体燃料)加热和限制通气的需求,从而提高了COPD的风险。因此,我们假设HAP暴露在高海拔处更高,因此,COPD流行也更高。
方法
研究设计与设置
我们在农村吉尔吉斯斯坦进行了一个观察,横截面,基于人口的人口的研究。中亚的这个低层收入国家的人口为596万,平均预期寿命为71岁[21].在欧洲呼吸学会(ERS)“白皮书”中,它的呼吸系统死亡率是所有国家中最高的[188bet官网地址22].吉尔吉斯斯坦的海拔高度形成了鲜明的对比。最低的地区(崔∼750米)和最高的地区(纳林∼2050米)分别被选为低地和高地。Chui有75.6万农村居民(总人口92.2万),并拥有该国的首都比什凯克。邻近的纳林地区有245000名农村居民(总数为284,000人)[23].我们在2015年2月3日至5月7日期间收集了低地的数据,在2014年7月16日至9月13日期间收集了高地的数据。与高地相比,在一年中较冷的测量时期,低地被认为涉及到相对更多(基于固体燃料)的加热和较少的通风。因此,季节性的影响会导致对HAP暴露和呼吸道症状差异的低估。
本研究先于初级卫生保健综合小组(新鲜空气)项目的自由呼吸评估和减少烟雾暴露(荷兰审判登记册identifier NTR5759),是一项针对资源匮乏地区的慢性肺病的实施科学项目[24].
参与者
鉴于在制定方案时,吉尔吉斯斯坦或邻国没有关于慢性阻塞性肺病患病率的以往研究,我们根据先前在乌干达进行的新鲜空气研究确定了600名参与者的目标[25]和BOLD(肺病负担倡议)研究[26].为此,通过多阶段抽样方法随机选取50户每户。纳入所有18岁以上的知情同意的永久居民,因为HAP高暴露人群甚至在30岁之前就可能发展为COPD [25].现时患有呼吸道感染或有肺量测定禁忌的人士[27)被排除在外。我们获得了所有参与者的书面知情同意。所有实地研究人员都接受了伦理学和知情同意程序方面的培训。国家心脏病学和内科医学中心(吉尔吉斯斯坦比什凯克)研究伦理委员会批准了该研究(方案9;2014/3/1)。
人口统计学、慢性阻塞性肺病危险因素和呼吸道症状
一份标准化问卷,由经过验证的问卷组成,用于乌干达的FRESH AIR研究[25],被定制到吉尔吉斯斯坦(补充附录S1)研究人员使用当地语言(吉尔吉斯语或俄语)进行研究。研究内容包括人口统计、烹饪和取暖环境、COPD风险因素和呼吸道症状等问题(表1和2).
家居空气污染
HAP是通过空气动力学直径<2.5µm (PM)的颗粒物的时间加权平均浓度测量的2.5),使用SidePak个人气溶胶监测仪AM510 (TSI, Minneapolis, MN, USA)。在整个测量过程中,这些家庭的厨师被要求一直佩戴该设备。大部分测量开始于早上(平均时间11:41)相对11:48 h、 分别),因此至少需要准备一顿热餐。连续测量的中位时间为269 在低地和284 在高地上(补充附录S2).值得注意的是,我们最初的目标是测量24小时室内浓度,但由于在农村地区对装置电池充电的可能性有限,因此这不可行。
COPD诊断
由伦敦帝国学院(英国伦敦)的教师培训,评估了肺功能(EasyOne; Zurichintechnik,苏黎世,瑞士)培训,培训了伦敦帝国学院(伦敦伦敦)培训(EasyOne;瑞士)之后,在联合美国胸部社会(ATS)/ ERS指南[28].我们测定1秒内的用力呼气量(FEV)1)使用间隔物与400μg的沙丁酰胺醇前后强制生气能力(FVC)。COPD被定义为患有后支气管扩张器FEV1/ fvc比率<70%[29],严重程度根据全球慢性阻塞性肺疾病倡议(GOLD)分期进行分类[30.].具有完全可逆性的受试者被纳入分析(怀疑诊断为哮喘)。动脉血氧饱和度(S.阿宝2)用脉冲血氧仪(YX302指尖脉冲血氧仪;Timago International Group, Bielsko-Biała,波兰)。
数据分析
SPSS版本23(IBM,Armonk,NY,USA)用于分析。将跨高度的基线特性,COPD流行和HAP暴露与正常分布的连续变量的独立T检验进行比较,Mann-Whitney U-Tests用于非正常分布变量和Chi方向或Fisher对分类变量的确切测试。不可变化和强制进入多变量的逻辑回归模型,通过广义估算方程分析调整家庭内的聚类[31],用于评估风险因素和COPD之间的独立关联。HAP和其他已知的COPD预测因子(年龄,性别,教育水平和包装 - 多年的吸烟)[12]和海拔作为预测因素。由于病例数量有限,结核病(曾经诊断过的)没有包括在模型中。由于假定与第三/第四产业相比,在第一或第二产业工作的职业暴露较高,因此将其作为预测因素纳入[32].HAP被分为三类(补充附录S4)考虑到具有高值的非正态分布(在这个高范围内,我们没有假设HAP与结果的logit呈线性)。模型中的多重共线性不明显。p值<0.05,95%置信区间(不包括1)的优势比被认为具有统计学意义。
丢失数据的处理
一些住户和居民的登记不充分,导致了居民PM的各种重复和不确定性2.5测量。为了保证数据质量并在家庭中调整聚类效果,我们丢弃了分析中的这些原始和重复测量。失踪PM的参与者2.5和/或肺测量值也被排除在外。
结果
研究人群
所有599名受邀个人都同意参与这项研究。排除后,来自每个环境41个家庭的193名低地人和199名高地人仍在进行分析(图1).
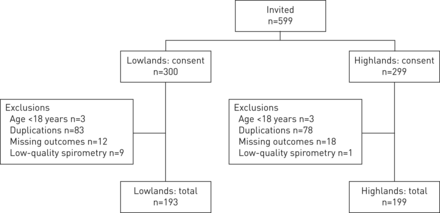
参与者的流程图。
慢性阻塞性肺病的人口特征和危险因素分布
高地人数明显较大,高度和体重较低(表1).他们的教育水平较低,在初级部门和较低的中学部门的频率更频繁地工作。高地人口包括较少的吸烟者,尽管他们的包装是显着提高。高地(无情地)更常见的患有结核病。
高海拔地区家庭空气污染
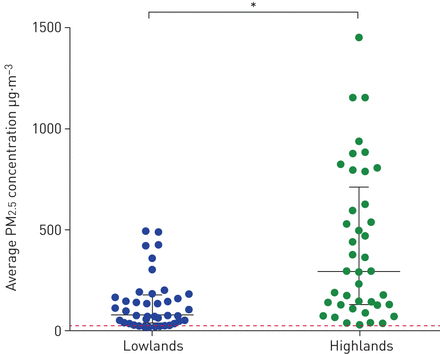
时间加权平均pm2.5(中位数(四分位差(IQR)) 290.0 (123.5-703.5))相对72.0(31.0-167.0)μg·m-3;P <0.001)(图2).此外,更高的最大PM2.5(中位数(IQR) 5822.0 (2308.0-9152.5))相对272.0(140.0 - -901.5)µg·m-3;p < 0.001)。在这两个地区,这些最大值大多在下午开始时达到(平均时间13:42:04)相对13:05:40 h)。测量持续时间在补充附录S2.高地人的烹饪和取暖环境也更容易产生HAP。例如,高地人的燃料使用风险明显更高(例如粪相对天然气),炉灶(例如开火相对改良炉灶)、通风(例如屋檐的空间相对开门),以及烹饪位置和持续时间。中提供了有关设置中这些因素的详细信息补充附录S3.
高原地区慢性阻塞性肺病患病率
COPD在高地地区更为普遍(36.7%)相对10.4%;p<0.001),尽管严重程度较低(GOLD分期≥2:24.7%相对70.0%;P <0.001)(表2和图3).在高地地区,COPD在男性和女性中平均分布,而在低地地区,绝大多数患者为男性(49.3%)相对80.0%;p < 0.001)。高原地区的COPD患者吸烟频率明显较低,暴露于PM明显较高2.5水平与低兰德(图4和补充附录S4).此外,氧饱和度在高地饱和度下显着降低(S.阿宝2:93.0%相对95.0%; p<0.001)。
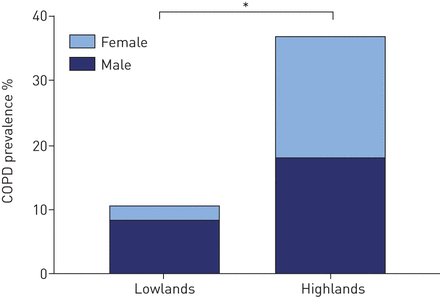
慢性阻塞性肺疾病(COPD)在低地地区流行相对苏格兰高地。*:差异有统计学意义(p<0.001)。
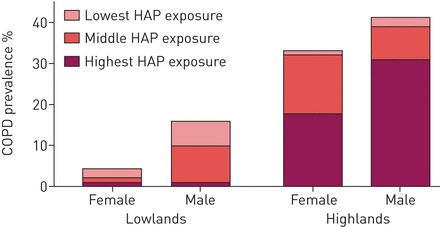
慢性阻塞性肺病(COPD)在低地和高地的性别和家庭空气污染(HAP)接触中的患病率。HAP暴露于泰格拉塞,具有时间加权平均颗粒物质的空气动力学直径<2.5μm≤72,> 72-293和>293μg·m-3.
COPD的预测因素
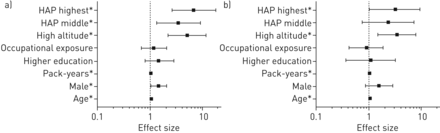
在两个海拔地区,共有93名参与者符合COPD标准。在不可变化的逻辑回归模型中,年龄,性别,包装年,海拔高度和HAP与COPD有关(图5和补充附录S4).在多变量logistic回归模型中,年龄、包年、海拔高度和最高HAP暴露水平与COPD呈正相关。肺功能下降,PM增加2.5曝光描述在补充附录S4.
慢性阻塞性肺疾病(COPD)的潜在预测因素:a)单变量分析和b)多变量分析。HAP:家庭空气污染。COPD(n=93)相对没有copd(n = 299)。广义估计公式分析调整为家庭内的聚类效应。每年年龄增加。高等教育意味着最高级别的教育高于中等教育。HAP暴露于泰格拉塞,具有时间加权平均颗粒物质的空气动力学直径<2.5μm≤72,> 72-293和>293μg·m-3.最低的类别是参考类别。数据以OR (95% CI)表示。注意,当COPD患病率>为10%时,OR不再近似于相对风险。*:差异有统计学意义(OR排除1的95% CI;p < 0.05)。
讨论
在本研究中,我们比较了吉尔吉斯斯坦农村低资源环境中高原和低地地区的COPD患病率及其危险因素,特别关注了客观测量的HAP。COPD患病率和HAP暴露(峰值和平均PM)2.5浓度)在高地人群中显著较高。除了生活在高海拔地区和暴露于高浓度的HAP外,更多的包年和更高的年龄也与慢性阻塞性肺病独立相关(在高原地区更常见)。我们的结果突出了农村高地人对慢性阻塞性肺病的特别脆弱性,并证实了人们日益认识到的HAP对呼吸健康的影响。
考虑到我们的年龄纳入标准相对较低(≥18岁),吉尔吉斯两国的COPD总体患病率都较高。我们低地的流行率与全球流行率相似,约为10%,但在高地观察到的流行率要高出3倍以上[26].我们对COPD的定义可能导致了这种高患病率,特别是在年龄稍大的高地人(固定FEV)中1/FVC比值已知会在老年人中过度诊断COPD [34])。此外,我们使用了白种人的参考值(农村、高海拔、中亚地区的值不存在),而吉尔吉斯人在中海拔(~ 1000-2000米)的研究报告称,他们的人口中有更大的植被覆盖度[35].较大的生理FVC值可能导致较小的FEV1/ FVC比率,因此在过度诊断中。最近哈萨克人口的研究发现患病率为6.7%[36].作者只研究了低洼地区的成年人(≥18岁),使用了相同的COPD定义,但研究的是城市而不是农村。考虑到城市环境中固体燃料的使用量较低,后一个因素可能解释他们观察到的COPD患病率较低。
根据我们的假设,随着高原地区COPD患病率的升高,我们观察到HAP暴露的显著升高。在农村地区的高海拔地区观察到更多的HAP似乎是合理的,因为更极端的气候条件增加了对(固体燃料)供暖和限制通风的需求。此外,高地人通常在初级部门工作,那里的粪便比清洁燃料更便宜,也更容易获得。因此,特别是在高地,我们的HAP测量值大大超过了平均25µg·m-3正如世卫组织24小时报告所述2.5空气质量指南[33].这些测量与PM一致2.5主要使用生物质燃料的其他家庭的浓度[13].我们的研究结果支持HAP在解释高海拔地区COPD高患病率方面发挥重要作用的假设。这一假设进一步与高地人群中(不吸烟)女性患者相对较多的情况相一致,就像在其他环境中女性高度暴露于生物质燃料烟雾[13-15那17那25那37].虽然HAP的致病机制尚未完全揭示,但HAP被认为可以改变先天性免疫反应,增强肺部和全身炎症,并促进氧化应激状态。这可能导致大分子细胞损伤,包括DNA改变[38].然而,BOLD结果提醒我们对气流阻塞的原因保持警惕,而不是HAP [39].
除了COPD和PM之间的强大和重要关系2.5在多变量分析中,浓度、海拔本身是另一个独立的预测因子,也在调整了年龄和包年之后。海拔高度可能直接影响COPD患病率,因为它与气道和总肺容量的增加有关。然而,如果这种增长是成比例的,证据仍然不确定(因此,如果和如何FEV1/FVC比率受到影响[40-42])。或者,高度可以间接地涉及COPD流行率通过(无节制的)因素。这些可能是更频繁的肺炎/肺结核病史,较低的体育活动水平[43那44],职业暴露更高[32]或更多(儿童)贫困/较低的社会人口发展(再次作为其他因素的中介)[2那45].
值得注意的是,中度/严重COPD(金阶段≥2)的患病率似乎在高地较低。这可能是由于对更高的环境氧气水平的严重生病的迁移[46],更好地获得吉尔吉斯首都的高级医疗保健或严重程度与固体燃料烟雾之间的潜在关系相对烟草烟雾(37].我们观察到的较低的高原氧饱和度水平似乎是合理的,因为高原的环境氧水平较低。此外,COPD患者中烟草和生物质燃料烟雾的双重暴露与低氧饱和度水平相关[47].然而,尽管双重暴露的COPD患者数量在高地地区明显较高,但双重暴露的参与者总人数是相同的。
如前所述,其他七项研究覆盖了不同海拔地区的COPD患病率,报告了相互矛盾的结果[6.-12].我们认为,这些相互矛盾的结果可以部分解释HAP暴露的差异,这些研究要么没有测量,要么通过替代测量,或者没有在分析中进行调整。在不同的研究背景下,HAP暴露、相关COPD患病率和跨海拔的差异可能存在显著差异。这些环境几乎都是在城市,有时是在高收入国家,这意味着由于更容易获得清洁燃料,更多极端的高海拔气候可能对HAP的影响较小[14]此外,在一项研究中,高海拔和低海拔地区的种族往往不同,这妨碍了肺功能的正确比较。
在我们的分析中,我们对客观测量的HAP进行了校正,并在农村、低资源环境和同一种族人群之间进行了一致的比较。海拔高度仍然是COPD的独立预测因素。目前在不同环境下进行的所有研究之间的冲突结果可能表明,慢性阻塞性肺病患病率可能与海拔本身无关。相反,它可能主要是通过海拔表达的(未测)因子介导的,HAP就是其中之一。
这项研究的一个主要优势是目标明确、个人监督的PM2.5根据ATS/ERS指南结合肺活量测定[28,而不是自我报告的存在危险因素或症状。这种方法准确地回答了最近对HAP和COPD之间关系的客观测量的呼吁[20.].这项研究也得益于高参与率。与会者表示,他们渴望得到额外的医疗照顾,因为在这些农村地区,获得保健服务的机会普遍有限。这种高速率阻碍了选择偏差,并增强了对其他设置的通用性。最后,我们介绍了中亚地区第一个基于肺活量测定的慢性阻塞性肺病流行研究[2].
还必须注意到一些限制。由于数据收集过程中的组织困难,我们不得不在这两种情况下排除各种参与者和家庭测量。然而,两种设置之间的差异在统计学上仍然显著,我们无法识别排除和纳入参与者之间的任何差异。另外,由于农村地区的电池和充电容量有限,我们无法进行24小时PM2.5测量。因此,在一天的同一时间内,对每个家庭进行了约4小时的测量,包括至少准备一顿热饭。因此,24小时点2.5浓度可能会降低,因为那些没有膳食准备的更长的时间。最后,鉴于低地的数据在今年的相对较冷的时间内收集,需要相对较高的(基于固体燃料的)加热和限制通风,HAP和呼吸道症状的差异可能低估。
总之,我们观察到,与吉尔吉斯斯坦农村的低海拔地区相比,高海拔地区的COPD患病率明显较高。两种环境下的HAP暴露率都很高,但在高原地区尤其如此。COPD和HAP之间存在着强而显著的关系,在调整其他风险因素后仍然显著。Altho尽管对其他农村、低资源高地的普遍性仍有待评估,我们的结果要求更多地关注COPD的认识、诊断和治疗。此外,这些环境中的决策者、医疗工作者和高地人应该通过提高对HAP的认识和减少HAP来关注预防(例如采用清洁炉灶)。这不仅有利于慢性肺部健康,也可以针对其他PM2.5有关疾病,例如缺血性心脏病、脑血管疾病、肺癌、低出生体重及早产、2型糖尿病及下呼吸道感染[16].
补充材料
致谢
这项研究是基于之前在乌干达进行的一项FRESH AIR研究。我们感谢Frederik van Gemert(荷兰格罗宁根大学医学中心)及其合著者分享他们的方案和问卷。我们感谢Beraki Ghezai (Lunger i Praksis, Oslo, Norway),他在吉尔吉斯斯坦介绍该项目、教育研究人员和将协议翻译成俄语方面发挥了重要作用。我们还要感谢已退休的Ron Wolterbeek和莱顿大学医学中心的统计学家Nan van Geloven。(荷兰莱顿),用于统计输入。我们感谢夏洛特·普特(LUMC)在设计这些数字时的支持。我们感谢国际初级护理呼吸系统组织从欧洲肺基金会获得赠款。最后,我们感谢所有与会者。这篇论文在2018年9月15日至19日在法国巴黎举行的ERS国际大会上作了口头报告(OA288)。
脚注
这篇文章的补充材料可从www.qdcxjkg.com.
作者贡献:T. Sooronbaev和A. Tabyshova将FRESH AIR研究适应了吉尔吉斯斯坦的环境和协调的数据收集。E.A. Brakema, A. Tabyshova, M.J. kastelyn和E. Molendijk分析和解释了数据。E.A. Brakema撰写了这份报告的初稿。所有作者都提供了评论,E.A. Brakema修订了报告。所有作者都对最终版本提出了意见。所有作者都可以访问所有数据。E.A. Brakema和N.H. Chavannes对提交论文发表的决定负有最终责任。
利益冲突:E.A. Brakema没有什么可披露的。
利益冲突:A.Tabyshova无需披露任何信息。
利益冲突:M.J.卡斯特琳没什么可透露的。
利益冲突:E. Molendijk无需披露。
利益冲突:R.M.J.J. van der Kleij没有什么可披露的。
利益冲突:范博文没有什么可透露的。
利益冲突:B.埃米洛夫无需披露任何信息。
利益冲突:M. Akmatalieva没有什么可披露的。
利益冲突:马德米洛夫先生没有什么可透露的。
利益冲突:法医努曼斯没什么可透露的。
利益冲突:威廉姆斯没有什么可披露的。
利益冲突:T. Sooronbaev没有什么可披露的。
利益冲突:N.H.Chavannes无需披露任何信息。
支持声明:本研究由欧洲肺基金会的健康肺部资助。该资助者在研究设计,数据收集,分析,解释或报告中没有作用。
- 收到了2018年6月26日。
- 公认2018年的11月2日。
- 版权©2019人队
本文是开放式访问,并根据创意公约188滚球软件归因非商业许可证4.0的条款分发。