摘要
基本原理2019年严重急性呼吸综合征冠状病毒2/冠状病毒病大流行凸显了对降低急性呼吸窘迫综合征(ARDS)死亡率的有效疗法的严重未满足需求。我们探索了细胞外烟酰胺磷酸核糖转移酶(eNAMPT),一种toll样受体(TLR)4的配体和先天性免疫和炎症的主要调节因子,是否是一种潜在的ARDS治疗靶点。
方法野生型C57BL/6J或内皮细胞(EC)-cNAMPT−−/敲除小鼠(靶向ECNAMPT缺失)暴露于脂多糖(LPS)诱导的(“一次打击”)或LPS/呼吸机联合(“两次打击”)诱导的急性炎症性肺损伤模型。一种nampt特异性单克隆抗体(mAb)成像探针(99米Tc-ProNamptor)检测NAMPT在肺组织中的表达。使用的是中和enpt的山羊多克隆抗体(pAb)或人源化单克隆抗体(ALT-100 mAb)在体外而且在活的有机体内.
结果免疫组织化学、生物化学和影像学研究证实,在两种临床前ARDS模型中,NAMPT肺组织表达均呈时间依赖性增加。在两种临床前模型中,静脉注射中和enampt的pAb或mAb均显著减轻了炎症性肺损伤(苏木素和伊红染色,支气管肺泡灌洗(BAL)蛋白,BAL多形核细胞,血浆白细胞介素-6)。在体外人肺EC研究表明,珐琅铂中和抗体(pAb, mAb)可强烈消除珐琅铂诱导的TLR4通路激活和EC屏障破坏。在活的有机体内野生型和EC-c的研究NAMPT−−/小鼠证实,在两种临床前ARDS模型中,ec来源的NAMPT对炎症性肺损伤的严重程度有高度显著的贡献。
结论这些发现强调了ec衍生的eNAMPT的作用以及对eNAMPT/TLR4炎症通路的生物靶向的潜力。结合预测的eNAMPT生物标志物和NAMPT基因分型分析,这为识别高危ARDS受试者提供了机会,以提供个性化药物。
摘要
在这些双重互补的临床前ARDS模型中,人源化的eNAMPT中和单克隆抗体(mAb)在降低ARDS的严重程度方面非常有效,这强调了针对ARDS/VILI的eNAMPT/TLR4途径的治疗潜力https://bit.ly/3ljEhBD
简介
2019年严重急性呼吸综合征冠状病毒病(COVID-19)大流行以及由COVID-19引起的急性呼吸窘迫综合征(ARDS)导致的死亡人数前所未有,这极大地突出了ARDS患者的多种需求未得到满足。其中包括缺乏经过验证的ARDS生物标志物,以及缺乏有效的美国食品和药物管理局批准的ARDS药物治疗来解决相关的致命多器官衰竭。虽然对ARD/呼吸机诱导的肺损伤(VILI)的病理生物学的认识有限,但一个关键的进展是对细菌和病毒诱导的进化保守的全身炎症网络的激活的认识[1- - - - - -3.],释放“细胞因子风暴”,增加肺和全身血管通透性、器官水肿和多器官功能障碍[4- - - - - -7],最终增加COVID-19-ARDS和非COVID-19-ARDS死亡率[8- - - - - -10].危及生命的器官功能障碍是由宿主对感染的反应失调引起的[6)介导的通过病原体相关分子模式和模式识别受体(PRRs)的相互作用,也可以被宿主核、线粒体和细胞质蛋白质激活,称为损伤相关分子模式(DAMPs)。DAMPs也会在缺氧、癌症、创伤和吸入性损伤等危险信号的反应中被释放出来,从而潜在地维持非感染性炎症反应[11].
在此之前,我们使用了临床前多物种ARDS模型以及基因组密集型方法[12,13]以识别新的ARDS生物标志物和可靶向通路[12- - - - - -18]并将烟酰胺磷酸核糖转移酶(NAMPT)鉴定为一种新的DAMP [19和有吸引力的ARDS靶标。我们发现NAMPT表达被多种ards相关刺激高度诱导,包括细菌感染、缺氧、休克、创伤和机械通气产生的过度机械应力[20.- - - - - -23].编码NAMPT的基因表达减少(NAMPT)通过小干扰rna, microRNAs和利用NAMPT+ /−杂合小鼠显著降低了临床前ARDS/VILI损伤的严重程度[17].
NAMPT是一种胞内酶活性调节烟酰胺腺嘌呤二核苷酸(NAD)生物合成的细胞酶[24,25],以组织和细胞特异性的方式造成损伤[26].然而,我们的研究更强烈地暗示,分泌的细胞外(e)NAMPT是NAMPT导致炎症性肺损伤和机械通气危重ARDS患者死亡率增加的主要机制[17,19,27].eNAMPT是炎症网络的主要调节因子通过与PRR toll样受体(TLR)4结合[19],诱导nf κ b介导的炎症细胞因子释放,增加与ARDS死亡率直接相关的血管通透性和多器官功能障碍[14,28- - - - - -30.].两个关键的观察结果将NAMPT的表达和功能与人类ARDS病理生物学联系起来。首先,单独的eNAMPT血浆水平[14,31- - - - - -33],或作为ARDS血浆生物标志物面板的一部分[14,31- - - - - -33],与ARDS严重程度和死亡率相关。其次,NAMPT改变启动子活性以应对过度机械压力的遗传变异[14,22,29,30.]和缺氧[23]也会增加ARDS的易感性和死亡率[14,22,29,30.].
在目前的研究中,我们探索了在“一次打击”(脂多糖(LPS))和“两次打击”(LPS/VILI)临床前ARDS模型中,eNAMPT作为可行的ARDS治疗靶点的验证。静脉注射enpt中和抗体,无论是多克隆抗体(pAb)还是人源化单克隆抗体(mAb),都能显著降低小鼠急性炎症性肺损伤的严重程度。此外,我们的研究证实了内皮细胞(EC)来源的NAMPT在ARDS病理生物学中的关键作用,扩展了先前的报道,即NAMPT在肺内皮、上皮细胞和浸润性白细胞中有稳定的空间定位表达,但没有评估细胞特异性NAMPT对ARDS严重程度的影响。使用ec特定条件NAMPT在敲除小鼠中,我们现在显示了ec分泌的eNAMPT在双重临床前ARDS损伤模型中的显著和明确的参与。这些研究强有力地验证了eNAMPT作为ARDS治疗靶点的可行性,并强调了一种中和eNAMPT的生物疗法直接解决未满足的提高ARDS/VILI死亡率的新策略的能力。
材料与方法
试剂
重组人eNAMPT购自Peprotech公司(Cranbury, NJ, USA)。抗p-NF-κB、pp-细胞外信号调节激酶(ERK)、pp-p38、pp-c-Jun n -末端激酶(JNK)、白细胞介素(IL)-6和IL-8(角质细胞趋化剂(KC))的免疫反应抗体购自Cell signaling Technologies (Danvers, MA, USA)和抗β-肌动蛋白(NF-κB)购自Invitrogen (Carlsbad, CA, USA)。山羊、兔子和小鼠二抗购自Life Technologies (Waltham, MA, USA)。IgG作为对照从Jackson ImmuneResearch (West Grove, PA, USA)获得。山羊抗人NAMPT pAb是定制生成的,如前所述[17].所有其他试剂均来自Sigma-Aldrich (St Louis, MO, USA)。
生成中和enpt的人源单抗
Aqualung Therapeutics (Tucson, AZ, USA)随后提供了两种中和enpt的人源单克隆抗体ALT-100和ALT-300在体外利用反式ec电阻试验筛选单抗[34,35], NF-κB活化生化分析[19),在活的有机体内利用双重临床前ARDS模型进行筛查。ALT-100被选为先导在活的有机体内治疗和ALT-300选择纳入组织nampt成像探针,99米Tc-ProNamptor。单克隆抗体生成和选择的细节在补充材料和方法.
99mTc-ProNamptor单抗成像
在小鼠、大鼠、非人类灵长类动物和人类之间存在极高的NAMPT蛋白序列同源性(95-99%),这强调了ALT-100和ALT-300单抗在我们进行的小鼠临床前研究中的实用性,包括含有ALT-300单抗的荧光蛋白和荧光蛋白99米tc标记探针用于NAMPT表达的组织成像,以人IgG作为对照[36,37) (ALT-300 Cy5.5或99米Tc标签可在补充材料和方法).小鼠皮肤炎症模型[38,39],通过局部应用12- o - tetradecanoylphorbol13 -acetate (TPA)诱导,验证Cy5.5-ALT-300探针检测NAMPT组织表达的能力体内。TPA敷于右耳表面,24 h后再敷,左耳用丙酮处理为阴性对照。在单独的实验中(n=3只小鼠),注射Cy5.5-ALT-300或Cy5.5-IgG(15-20µg)注射。第二次TPA/PBS应用后3小时,随后进行小鼠成像。评估的能力99米Tc-ALT-300探头检测在活的有机体内NAMPT组织表达,99米Tc-ProNamptor (1.0-1.5 mCi, >98%放射化学纯度)[40,41]或注射IgG对照Ab注射。在lps刺激后3小时,在一击模型和成像(量子成像探测器相机)中[42- - - - - -44].计数基于活动的度量99米Tc-ProNamptor生物分布体外在收获的肺中进行放射自显影(见补充材料和方法有关更多详情)。
鼠标菌株
在活的有机体内实验采用野生型雄性C57BL/6J小鼠(8-12周;Jackson实验室,Bar Harbor, ME, USA), ec特定条件NAMPT基因敲除小鼠(EC-cNAMPT−−/)的129/B6混合背景,或同窝NAMPTfl / fl控制。EC-cNAMPT−−/小鼠是通过杂交产生的NAMPT老鼠(NAMPTfl / fl)与经他莫西芬诱导的ec特异性Cre转基因小鼠(Tek-Cre/ERT2-1Soff) [45]与回交与柔性纯合子NAMPT老鼠。在最后一次剂量他莫西芬后,在使用前实施了2周的最小等待期EC-cNAMPT−−/实验用小鼠(参见补充材料和方法有关更多详情)。携带NAMPT flox转基因的ec特异性敲除小鼠与野生型窝仔相比,在表型性状上没有显示出明显的差异。生长速度、繁殖力和生育能力与野生型小鼠没有差异。同样,NAMPT flox小鼠与TIE2/ERT2 Cre小鼠杂交以产生条件NAMPT敲除系,在注射他莫西芬前后,与窝仔或亲本品系都没有表现出任何表型差异。
一击和两击临床前ARDS模型中的enpt中和策略
对于一次性ARDS模型,小鼠接受气管内LPS注射,并在LPS后18小时处死,如前所述[46- - - - - -48].对于两次打击的LPS/VILI ARDS模型,相似的LPS暴露小鼠在18小时后重新插管,并置于机械通气4小时(潮气量20 mL·kg−1,呼吸频率90次·min−1,呼气末正压0 cmH2O),如前所述[46- - - - - -48].在具体实验中,C57BL/6J小鼠接受了两种不同剂量的注射。-交付的enpt中和pAb或ALT-100单抗(4 mg·kg−10.4 mg·kg−1,分别)或IgG对照Ab (4 mg·kg−1)(详见补充材料和方法有关更多详情)。
埃文斯蓝染料外渗试验
如前所述,我们通过测量肺血管外埃文斯蓝染料来评估肺血管渗漏[58].简言之,给小鼠注射埃文斯蓝染料(0.05毫克;σ)注射.安乐死前60分钟。然后对肺进行灌注以去除血管内染料,切除并在PBS中均质。1体积肺匀浆与2体积甲酰胺孵育,在60°C孵育18小时后离心。使用iMark微孔板阅读器(BioRad, Hercules, CA, USA)在620 nm和740 nm处测量上清液的光学密度。埃文斯蓝染料的浓度校正血红素色素的存在使用以下公式620(纠正)=620(raw)−(1.1927×A720) + 0.0071。然后根据血管蛋白泄漏到肺组织的标准线性曲线计算渗出的埃文斯蓝染料浓度。
定量肺组织和免疫组化分析
苏木精和伊红染色
肺固定并切片进行常规苏木精和伊红染色和成像(×10放大,Olympus数码相机;日本东京)[50].
NAMPT染色
亲和素-生物素-过氧化物酶方法与兔抗人NAMPT pAb一起使用(1:1000稀释;如前所述,Bethyl Laboratories, Montgomery, TX, USA)用于肺组织中NAMPT表达的免疫组化(IHC)可视化[14,17,19].
NAMPT/β-actin/CD-31共染EC-cNAMPT−−/老鼠
肺组织切片EC-cNAMPT−−/小鼠与兔抗人NAMPT pAb (Bethyl)、β-actin或大鼠抗cd -31单抗孵育一夜(4°C),生物素化二抗(1小时,25°C)染色并成像(×10 objective, NA 0.4 Zeiss Axiovert显微显微镜;从德国)。
急性肺损伤严重程度评分量化
急性肺损伤严重程度评分(ALISS)被用于整合一击和两击临床前ARDS模型中的肺损伤指标,并在整个研究中标准化损伤水平在活的有机体内模型。评分系统,包括已发表的建议[52]客观地为每只研究动物根据四种损伤严重程度(H&E组织学定量、BAL总蛋白浓度、BAL总PMN细胞计数和促炎细胞因子IL-6血浆水平)分别评分(1-4分)。每只动物的最高得分是每只老鼠16分。一般情况下,ALISS得分1-4分代表完全无损伤,5-8分代表轻度损伤,9-12分代表中度损伤,> - 12分代表严重损伤。中提供了更多详细信息补充材料和方法.
跨内皮电阻测量
人类肺动脉EC (Lonza, Walkersville, MD, USA)按照前面描述的方法培养[53]并将其植入蒸发金微电极(37°C, 5%二氧化碳)上,使用细胞-基质阻抗传感系统(应用生物物理学,特洛伊,NY, USA)测量反式内皮电阻(TER),如前所述[54].每个微电极的TER值汇总并绘制与时间(平均±扫描电镜).
enpt、NFκB、丝裂原活化蛋白激酶、IL-6和IL-8的生化组织和血浆水平
按照之前报道的标准方案对肺匀浆进行Western blotting [23,49]以密度法定量肺组织NAMPT、NFκB、有丝裂原活化蛋白(MAP)激酶、IL-6和βν-actin(总蛋白控制)的表达。如前所述,采用ELISA法测量eNAMPT血浆水平[27,31],使用中尺度ELISA平台(Meso Scale Diagnostics, Rockville, MD, USA)测量血浆IL-6和IL-8 (KC)水平(描述在文献中补充材料和方法).
统计分析
连续数据比较采用非参数方法,分类数据比较采用卡方检验。在适用的情况下,采用标准的单因素方差分析,并使用Newman-Keuls检验进行组间比较。双因素方差分析(two -way ANOVA)用于比较来自两个或两个以上不同实验组的数据的均值。如果方差分析有显著性差异(p<0.05),则进行最不显著性差异检验事后.使用GraphPad Prism (Windows版本7.00;GraphPad软件,拉霍亚,加州,美国www.graphpad.com).p<0.05为差异有统计学意义。
结果
临床前ARDS模型小鼠肺组织NAMPT表达增加
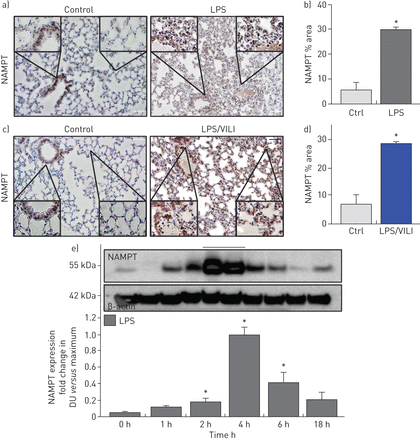
与对照组小鼠相比,暴露于一次性(LPS 18 h) ARDS模型(图1一个)或两次(LPS 18 h,通气4 h) ARDS/VILI模型(图1 c)显示NAMPT表达显著上调(肺泡上皮细胞,内皮细胞,巨噬细胞,中性粒细胞)图1 b, d(p<0.05),并在lps刺激小鼠的肺匀浆中得到证实。NAMPT蛋白表达在lps刺激后2小时开始显著升高,4小时达到峰值,18小时恢复到基线水平(图1 e).
临床前急性呼吸窘迫综合征(ARDS)模型小鼠肺组织中烟酰胺磷酸核糖转移酶(NAMPT)表达增加。采用兔抗人单克隆抗体(Bethyl, Montgomery, TX, USA)进行免疫组化(IHC)染色,观察NAMPT在肺组织中的表达。与对照组无挑战的C57BL/6J小鼠相比,暴露于以下小鼠的肺组织中观察到NAMPT表达显著增加:a)一次性脂多糖(LPS) ARDS模型(气管内LPS, 18小时)或c)两次临床前ARDS/呼吸机诱导肺损伤(VILI)模型(LPS 22小时,呼吸机暴露最后4小时,tidal volume 20 mL·kg−1).NAMPT在肺泡上皮细胞、内皮细胞、巨噬细胞和浸润性中性粒细胞中表达最为明显。b), d)定量总结NAMPT IHC染色的变化(Image J软件)(n>每组5只小鼠)。*: LPS或LPS/VILI的p<0.05与控制。e)我们评估了lps攻毒后不同时间肺匀浆中NAMPT蛋白的表达(Western blotting)。密度分析(每个时间点n=4)显示NAMPT免疫反应性随时间显著增加,在lps后4小时达到峰值。DU:密度单位。*: p < 0.05。比例尺=50 μm。
在活的有机体内NAMPT肺组织表达检测
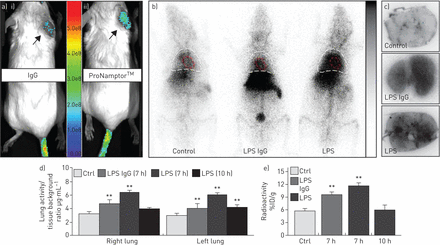
通过tpa诱导的耳朵炎症模型观察到ProNamptor单抗探针检测组织炎症的验证,与对照Cy5.5-IgG相比,观察到Cy5.5-ProNamptor积累显著增加(在活的有机体内注射后荧光成像)(图2一个).在未受刺激的对照组小鼠和lps刺激的小鼠中9米Tc-IgG对照或99米Tc-ProNamptor,在肝脏和心脏血池中有明显的放射性积聚,在肺中也有较小程度的积聚(图2 b).然而,在活的有机体内而且体外显像显示放射性累积明显增加99米暴露于一次性LPS ARDS模型的小鼠肺组织中的Tc-ProNamptor(7小时成像;图2 b)由体外放射自显影图像(图2 c).量化的99米lps刺激后7小时肺组织Tc摄取均显示非特异性IgG和ProNamptor显著增加;然而,的量级99米Tc-ProNamptor放射性摄取与IgG对照组和未感染小鼠相比显著增加(图2 cd)。的显著增长99米lps后7小时Tc-ProNamptor放射性标记摄取较lps后10小时大幅下降(图2 d,e),这一发现与中描述的肺组织匀浆中NAMPT蛋白表达水平一致图1 e.
ProNamptor检测烟酰胺磷酸核糖转移酶(NAMPT)表达在活的有机体内在“一次性”脂多糖(LPS)临床前急性呼吸窘迫综合征(ARDS)模型中。a)为了验证含胞外(e) nampt特异性单克隆抗体(mAb)的ProNamptor探针检测炎性损伤的能力,在12-O-tetradecanoylphorbol-13-acetate (TPA)诱导的炎性耳模型中进行了研究。典型的荧光图像i) Cy5.5-IgG和ii) enpt特异性成像探针Cy5.5-ProNamptor,在两只tpa注射小鼠右耳水肿后12小时获得。与注射Cy5.5-ProNamptor的小鼠相比,注射Cy5.5-ProNamptor的小鼠右耳的荧光积累明显增强(箭头)。b)有代表性的全身电离辐射量子成像探测器图像,分别摄于未激发的对照小鼠和lps激发的C57BL/6J小鼠99米Tc-IgG抗体探针或带99米Tc-ProNamptor。在lps灌注后7小时(3小时后)收集图像99米Tc-ProNamptor注入)。放大的胸部图像突出了在lps诱导的肺部炎症中检测NAMPT的表达。两种非特异性肿瘤均有放射性增加99米Tc-IgG Ab和99米Tc-ProNamptor探针在肝脏和心脏血池(红色轮廓)的脂多糖挑战动物。然而,观察到肺堆积增加99米Tc-ProNamptor(胸部区域用白色标出)。c)放射性积累显著增加99米Tc-ProNamptor在lps损伤肺中的作用(7小时,与IgG Ab-99米Tc和控制肺)进一步证实体外肺部放射自显像(代表性图像,n=4)。d), e)在活的有机体内定量图像分析体外生物分布测量(%注射剂量(ID)·g−1)显示显著增加99米Tc-ProNamptor在lps损伤后7小时的肺摄取与NAMPT摄取/表达相比下降10小时99米Tc-IgG抗体和对照肺。**:与对照组相比p<0.01。
enpt中和策略可减弱一次性临床前ARDS损伤
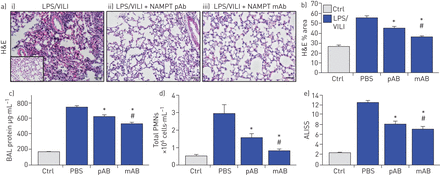
与对照组小鼠相比,一次性lps刺激ARDS模型的H&E肺组织染色显示肺泡炎症伴明显的中性粒细胞浸润和肺泡水肿(附图)(图3一).静脉注射中和enpt的pAb (4 mg·kg)−1)或ALT-100单抗(0.4 mg·kg−1)显著减轻组织学损伤(图3一),通过lps诱导的炎症指数的显著降低,即。BAL蛋白(图3 c)和PMN计数(图3 d).ALT-100单抗对肺的保护作用明显优于eNAMPT pAb,无论是通过H&E染色(图3 b)或综合急性肺损伤严重程度评分或ALISS (H&E染色,BAL蛋白,BAL PMN计数,血浆IL-6浓度)(图3 e).
细胞外烟酰胺磷酸核糖转移酶(eNAMPT)中和策略减弱“一次性”临床前急性呼吸窘迫综合征(ARDS)损伤。a)暴露于i)一击脂多糖(LPS)/ARDS损伤模型(18 h)小鼠的苏木精和伊红(H&E)肺组织染色显示,与对照C57BL/6J小鼠相比,间质和肺泡炎症伴明显的中性粒细胞浸润和肺泡水肿(插图);lps诱导的组织学损伤的严重程度在接受静脉注射enpt -neutralisingpolyclonal antibody (pAb) (4 mg·kg)的小鼠中显著降低−1,在时间0时注射LPS)或iii)人源化ALT-100单克隆抗体(mAb) (0.4 mg·kg−1(n>每组5只小鼠)。*: LPS-Ab值p<0.05与LPS-PBS控制;#:对于LPS-mAb, p<0.05与LPS-pAb。b) ALT-100单抗在减少lps诱导的炎症和损伤的组织学证据方面明显比eNAMPT pAb更有效。*: p < 0.05与LPS-PBS;#: p<0.05与帕布。c), d)注射。给药的enampt中和生物干预(pAb或mAb)显著降低脂多糖诱导的c)支气管肺泡灌洗(BAL)蛋白和d) BAL多形核细胞(PMN)计数的增加。*: p < 0.05与LPS-PBS;#: p<0.05与帕布。e)在急性肺损伤严重程度评分(ALISS)中,包括H&E染色、BAL蛋白、BAL PMN计数和白细胞介素-6血浆水平,再次验证了人源化ALT-100单抗优于eNAMPT pAb的疗效。* *: p < 0.01与LPS-PBS,# #: p<0.01与帕布。比例尺=50 μm。
enpt中和策略可减弱双击ARDS/VILI损伤
暴露于两次ARDS/VILI模型的小鼠(LPS暴露22小时,呼吸机暴露最后4小时)的H&E染色显示,与对照组小鼠相比,显著的炎症细胞浸润到肺实质,并伴有间质和肺泡水肿(插图)(图4一).与单次撞击LPS模型一样,两次撞击LPS/VILI模型的组织学损伤严重程度显著降低注射。使用中和enpt的pAb (4 mg·kg)−1)或ALT-100单抗(0.4 mg·kg−1) (图4一, b)。两种enampt中和生物策略也显著降低了BAL蛋白(图4 c)和BAL PMN计数(图4 d),与pAb相比,ALT-100单抗介导的保护作用更强(图4 e).
细胞外烟酰胺磷酸核糖转移酶(eNAMPT)中和策略减弱“两击”临床前急性呼吸窘迫综合征(ARDS)/呼吸机诱导的肺损伤(VILI)。a)暴露于脂多糖(0.1 mg·kg)的i)小鼠的苏木精和伊红(H&E)肺组织染色分析−1,18 h),然后机械通气(4 h,潮气量20 mL·kg−1)与对照C57BL/6J小鼠进行组织学比较(附图),发现显著的实质中性粒细胞浸润以及间质和肺泡水肿。LPS/VILI组织学损伤的严重程度在接受任何ii)的小鼠中均显著降低。4 mg·公斤−1,在时间0与LPS)或iii)人源化ALT-100单克隆抗体(单抗;0.4毫克·公斤−1,在时间0与LPS)。b)根据损伤的组织学定量,ALT-100单抗在减少两次临床前ARDS损伤方面明显比pAb更有效(图像J软件)。c),d)两种enampt中和生物干预(pAb或mAb)也显著降低了两次命中LPS/VILI模型后两次命中ARDS/VILI诱导的c) BAL蛋白含量和d) BAL多形核细胞(PMN)计数的增加。e)尽管两种中和eNAMPT的生物干预(pAb, mAb)都显著降低了LPS/VILI炎症损伤,ALT-100 mAb被证明比eNAMPT pAb更有效,这在急性肺损伤严重程度评分(ALISS)中得到验证(每组n=5只小鼠)。*: p < 0.05与有限合伙人/ VILI-PBS,#: p<0.05与帕布。
eNAMPT中和减弱LPS-和LPS/ vili -挑战的人肺EC信号和屏障反应在体外而且在活的有机体内
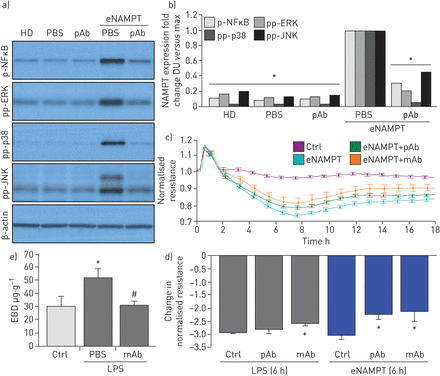
我们先前证明了NAMPT在临床前VILI模型中的表达主要在空间上定位于肺EC、肺上皮以及驻留和浸润的白细胞[13,14].在ARDS/VILI临床前模型中,我们试图将肺内皮细胞特异性地表征为循环eNAMPT的靶组织,并评估肺ec来源的NAMPT对急性肺损伤严重程度的贡献。最初的在体外利用人肺EC的实验证实,TLR4的eNAMPT连接诱导NFκB磷酸化[19]和MAP激酶激活(p38, JNK, p42/44 ERK),这些信号响应几乎被enpt中和的pAb (图5一个,b),以及enampt诱导的跨人肺TER下降,反映了pAb-和mab介导的对enampt诱导的EC屏障完整性丧失的保护(图5 cd)。ALT-100单抗,而不是中和enpt的pAb,也显著降低了lps诱导的屏障破坏(图5 d),结果与lps介导的eNAMPT分泌的贡献作用一致(最大在4小时;图1 e)导致EC屏障完整性的丧失和TER的降低。
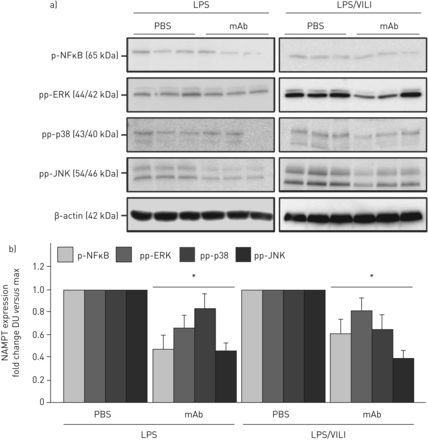
细胞外烟酰胺磷酸基转移酶(eNAMPT)中和策略减弱了eNAMPT诱导的人肺内皮细胞(EC)信号和屏障反应。a),b)单用人重组eNAMPT (1 μg·mL)刺激人肺内皮细胞−1, 1 h)或eNAMPT-多克隆抗体(pAb)混合物(eNAMPT 1 μg·mL−1+pAb 10 μg·mL−1, 1 h)。接下来将细胞裂解并检测磷酸化蛋白和总β-肌动蛋白通过免疫印迹。除了丝裂原激活蛋白(MAP)激酶激活的证据(pp-p38, pp-JNK, pp-42/44细胞外信号调节激酶(ERK)之外,enampt还诱导了NFκB的强烈磷酸化。Heat-denatured (100°C, 5 min)人重组eNAMPT (HD) (1 μg·mL−1, 1 h)作为阴性对照,确认eNAMPT效应不反映内毒素污染。加入中和enpt的pAb几乎完全消除了enpt诱导的NFκB磷酸化,并抑制了enpt诱导的MAP激酶激活(通过密度测量捕获的ERK、p38和JNK MAP激酶磷酸化检测到)(n=3)。c)在伴随实验中,将人肺ec镀在金微电极上,单独用重组人eNAMPT(1µg·mL)挑战−1),一种eNAMPT- pab混合物(eNAMPT 1 μg·mL−1pAb 10 μg·mL−1)或eNAMPT- alt -100单克隆抗体(mAb)混合物(eNAMPT 1 μg·mL−1ALT-100 10 μg·mL−1).与单独使用珐琅铂相比,珐琅铂中和策略(pAb和mAb)都减弱了珐琅铂诱导的EC屏障完整性下降。用脂多糖(LPS)(1µg·mL)刺激金微电极上的人肺ec−1),用PBS、eNAMPT pAb(10µg·mL−1)或ALT-100单抗(10µg·mL−1)在LPS刺激后立即添加。与LPS单独相比,ALT-100单抗和eNAMPT pAb也显著降低了LPS诱导的EC屏障完整性下降。对于跨内皮细胞电阻值(TER)研究,归一化电阻值>1表示肺EC屏障增强,归一化电阻值<1表示肺EC屏障破坏。d) TER下降和屏障完整性丧失的柱状图量化,其中数据表示为6小时后与正常未刺激对照组相比TER的变化(±扫描电镜,每个条件n=3个独立实验)。*:单用激动剂p<0.05与激动剂- pab或mAb。e)“一次性”lps刺激产生的肺组织匀浆(1 mg·kg)−1, 18 h),使用和不使用中和enpt的单抗(0.4 mg·kg)−1对肺组织中埃文斯蓝染料(EBD)的积累进行评估,作为血管外染料泄漏的反映,并报告EBD浓度(μg·g−1肺组织)[55].柱状图表明,通过预先添加ALT-10单抗,lps诱导的EBD积累显著增加被消除。*: p<0.05 LPS与控制;#: p<0.05 LPS与有限合伙人+马伯。DU:密度单位。
接下来研究循环的eNAMPT对肺血管屏障完整性丧失的贡献在活的有机体内最初是埃文斯蓝染料在肺组织中的积累,这是血管通透性的指标,证明了ALT-100单抗介导的EC屏障完整性在一次打击(LPS)临床前ARDS模型中的显著恢复(图5 e).验证我们的在体外我们检测了暴露于一次性和两次临床前ARDS模型的小鼠肺组织中MAP激酶信号通路的水平。图6证实了NFκB和MAP激酶家族效应因子(p38, JNK, p42/44 ERK)的激活,并通过肺组织匀浆中的磷酸化反映出来[19],在两种临床前ARDS模型中。重要的是,ALT-100单抗有效抑制了在两种ARDS模型中观察到的NFκB和MAP激酶家族激活,这与循环的eNAMPT对ARDS/VILI临床前模型中肺损伤严重程度的贡献一致(图6).
细胞外烟酰胺磷酸基转移酶(NAMPT)中和ALT-100单克隆抗体(mAb)在“一次打击”和“两次打击”临床前急性呼吸窘迫综合征(ARDS)/呼吸机诱导的肺损伤(VILI)模型中减弱丝裂原激活蛋白(MAP)激酶信号。a)一次性脂多糖(LPS)暴露的肺组织匀浆(1 mg·kg)−1, 18 h)和双击LPS/ vili暴露(LPS 22 h;机械通气4 h,潮气量20 mL·kg−1Western blot检测C57B6野生型小鼠的磷酸化蛋白和总β-肌动蛋白。LPS-和LPS/ vili -挑战小鼠表现出强大的nf - κ b和MAP激酶磷酸化(pp-p38, pp-JNK, pp-42/44细胞外信号调节激酶(ERK)),作为通路激活的证据。b)用中和enpt的ALT-100单抗(0.4 mg·kg−1,在时间0 h时)导致通过密度测量捕获的一次打击和两次打击暴露小鼠中NFκB和MAP激酶通路激活显著降低(n=3)。DU:密度单位。*: p < 0.05。
EC-specificNAMPT删除在活的有机体内减少一次和两次肺部损伤
我们使用了基因工程条件EC-cNAMPT−−/敲除小鼠,有条件NAMPT进一步探讨肺EC特异性NAMPT的表达和分泌在一击和二击肺损伤发展中的作用。肺组织免疫组化研究表明他莫昔芬治疗EC-cNAMPT−−/敲除小鼠的肺内皮NAMPT染色选择性缺失,而肺上皮NAMPT表达稳健(图7),反映了肺EC中NAMPT表达的条件缺失(与野生型小鼠相比)。一击或二击暴露的H&E肺组织染色检查EC-cNAMPT−−/基因敲除小鼠的炎症性肺组织损伤显著减少(图7 b-d),同时BAL蛋白水平降低(图7 e)和BAL PMN计数(图7 f)与同样暴露于同一窝的对照组小鼠相比。ec特异性提供的显著保护NAMPT删除在EC-cNAMPT−−/捕获小鼠进行综合肺损伤严重程度评分(ALISS,图7 g).
内皮细胞条件烟酰胺磷酸基转移酶敲除(cNAMPT−−/)小鼠在“一次打击”和“两次打击”急性呼吸窘迫综合征(ARDS)损伤模型中明显免受肺损伤。a)肺组织切片取自EC-cNAMPT−−/在他莫西芬治疗开始2周后(每天腹腔注射75 mg,持续1周)处死>小鼠,并制备组织载玻片,用细胞特异性荧光标记的NAMPT(绿色)和肌动蛋白或CD-31(红色)进行双重免疫组化(IHC)染色。与对照组肺内皮双重染色(共定位合并,左)相反,他莫西芬处理EC-cNAMPT−−/小鼠血管细胞中缺乏NAMPT染色,而肺上皮细胞和白细胞中NAMPT染色与我们的原始报道一致[14].这些结果体现了针对性NAMPT血管内皮细胞缺失表达。b-d)野生型(WT)小鼠苏木精和伊红(H&E)染色EC-cNAMPT−−/暴露于b)一击脂多糖(LPS) ARDS模型或c)二击脂多糖/呼吸机诱导肺损伤(VILI)模型的小鼠,在条件缺失EC的小鼠中,炎症性肺损伤显著减轻NAMPT, d)图像J量化总结。e-g)一次打击LPS-和两次打击LPS/ vili暴露EC-cNAMPT−−/小鼠表现出显著降低e)支气管肺泡灌洗液(BAL)蛋白水平和f) BAL多形核细胞(PMN)计数,g)在综合急性肺损伤严重程度评分(ALISS)评分中捕捉到这种保护。*: p < 0.05EC-cNAMPT−−/与同样暴露的同伴。比例尺=50 μm。
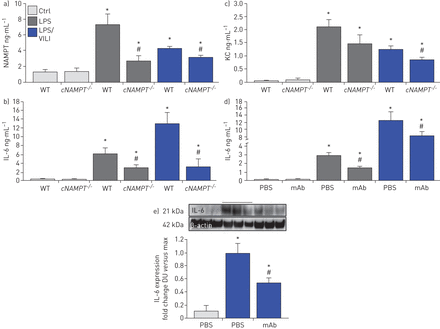
最后,我们探讨了ec衍生的循环eNAMPT与急性肺损伤严重程度的关系,并测量了一次和两次暴露的eNAMPT血浆水平EC-cNAMPT−−/和对照组小鼠。与对照组相比,一次命中和两次命中都暴露EC-cNAMPT−−/小鼠的血浆eNAMPT水平降低(图8)以及血浆中IL-6和IL-8水平的降低(小鼠中的KC),这两种炎症细胞因子通常是ARDS“细胞因子风暴”的组成部分(图8 b, c).与未处理的小鼠相比,ALT-100单抗处理的WT C57Bl6小鼠的IL-6和IL-8 (KC)血浆水平也显著降低(图8 d),通过降低两次命中的ards暴露小鼠的IL-6蛋白表达(用enpt中和的ALT-100单抗治疗)验证(图8 f).
内皮细胞烟酰胺磷酸基转移酶(NAMPT)缺失和ALT-100单克隆抗体(mAb)降低了“一次打击”和“两次打击”暴露急性呼吸窘迫综合征(ARDS)小鼠的血浆和组织细胞因子表达。a)在暴露一次和两次的窝伴对照组(Ctrl)中,血浆eNAMPT水平(ELISA)显著升高,而在同样暴露的内皮细胞中,循环eNAMPT水平显著降低(电子商务)-cNAMPT−−/基因敲除小鼠。*: p<0.05 WT LPS或脂多糖(LPS)/呼吸机诱导的肺损伤(VILI)与野生型(WT) Ctrl;#: p < 0.05。EC-cNAMPT−−/与昙花一现的/ two-hit-exposed同窝出生的。b),c)一次打击和两次打击中小鼠炎症细胞因子、白细胞介素(IL)-6和角质细胞趋化剂(IL-8)的血浆水平EC-cNAMPT−−/基因敲除小鼠的数量比同样暴露的同窝小鼠要少。d)用中和enpt的人源化ALT-100单抗治疗可降低暴露于一次和两次临床前ARDS损伤模型的C57B6 WT小鼠血浆IL-6水平的升高。*:仅LPS或LPS/VILI p<0.05与Ctrl;#: p<0.05 LPS或LPS/VILI mAb与LPS或LPS/VILI单独使用。e) Western blot检测一次性lps暴露的C57B6 WT小鼠肺组织匀浆中IL-6蛋白的表达,通过密度测量发现ALT-100单抗介导的IL-6表达显著降低(n=4)。*: p<0.05 LPS/VILI单独与Ctrl;#: p<0.05 LPS/VILI mAb与有限合伙人/ VILI孤单。
讨论
目前,还没有美国食品和药物管理局批准的ARDS治疗方法,目前的COVID-19大流行突出了这一严重未满足的需求。为了潜在地解决降低ARDS死亡率的药物治疗需求,我们之前发现了一种新的DAMP - eNAMPT [19],是一种具有潜在吸引力的ARDS靶点,其表达和功能与人类ARDS密切相关。例如,在细菌感染、缺氧、休克、创伤和机械通气产生的过度机械应激等ards相关刺激下,NAMPT表达高度诱导[20.- - - - - -23].此外,血浆eNAMPT水平是ARDS严重程度的生物标志物[14,17,22,29- - - - - -31,33),而NAMPT小等位基因频率升高的基因型(即。常见单核苷酸多态性)在黑人和非西班牙裔白人受试者中赋予ARDS严重程度和死亡率增加的显著风险[14,17,22,29- - - - - -31,33].我们早期的研究强烈暗示了eNAMPT对VILI和ARDS病理生物学的重要贡献[14,17,22,29- - - - - -31,33]通过TLR4连接和NFκB转录活性导致炎症级联的上游激活[19].因此,eNAMPT作为ARDS/VILI的可行治疗靶点具有实质性和令人信服的基础基础。
我们目前的研究强调了eNAMPT参与ARDS病理生物学的几个重要和新颖的方式。首先,我们利用互补方法验证了在一次打击(LPS)和两次打击(LPS/VILI)临床前ARDS模型中NAMPT肺组织表达的增加。免疫组化和生化研究显示,在两种临床前模型中,NAMPT肺组织表达均显著增加。利用放射性标记探针进一步验证了这一点,99米Tc-ProNamptor,具有暂时性的lps诱导的NAMPT肺组织表达增加,与肺匀浆中NAMPT表达一致。作为99米Tc-ProNamptor含有放射性标记的enpt中和单抗(ALT-300),潜在的存在99米Tc-ProNamptor作为一种新的分子成像治疗药物,可能从治疗上减少炎症损伤,这一假设有待于未来的研究解决。
这项工作的第二个重要意义是扩展我们在VILI小鼠模型中的早期研究,并直接探索enpt中和作为一种有效的ARDS治疗方法。之前气管内灌注的中和eNAMPT的多克隆pAb支持eNAMPT作为相关的VILI治疗靶点[17,19].我们现在扩展这项工作来演示4在两种临床前ARDS模型中,ALT-100(中和eNAMPT的人源单抗)显著降低了炎症性肺损伤的严重程度,并且明显比eNAMPT pAb更具保护作用。此外,我们使用双重临床前ARDS模型为我们的工作增加了显著的严谨性,并直接解决了ARDS药物干预的主要失败是由于使用单一临床前ARDS小鼠模型[56,57].
我们的临床前结果支持了我们早期的ARDS临床试验策略,该策略旨在将ALT-100单抗提供给在插管时出现呼吸衰竭的ARDS患者,即。机械通气开始前。该试验设计专门针对VILI的预防和抑制呼吸机诱导的炎症通路的扩增,以减少多器官损伤,从而最大限度地缩短机械通气的持续时间,提高重症监护病房(ICU)的生存率并降低医疗成本。先前不成功的ARDS治疗临床试验,主要针对单一细胞因子或细菌产物,可能受到靶向治疗交付延迟的阻碍[58,59],在先天免疫驱动的肺和全身炎症通路扩增发作后开始治疗。从临床试验的角度来看,在急诊室(ER)或进入ICU、插管和机械通气之前对即将出现呼吸衰竭的ARDS患者给予ALT-100的可行性是一项艰巨的挑战,但最近的ER - ICU临床试验支持了这一可行性。
我们的研究提供的另一个有价值的见解是强调ec来源的循环eNAMPT对ARDS病理生物学的关键重要性[14,35].而NAMPT除了在肺ECs中表达外,在犬科动物和小鼠villi感染模型的肺泡上皮、常驻白细胞和浸润白细胞中也有稳定的表达[13,14],每个细胞成分对ARDS严重程度的关键贡献以前是未知的。我们目前的在体外而且在活的有机体内研究证实了早期的工作,强调肺EC是肺EC通透性反应失调的关键eNAMPT细胞靶点[35].我们现在发现,珐琅铂介导的人肺EC TLR4和MAP激酶通路的有效激活和EC屏障完整性的丧失,这两种珐琅铂中和方式(pAb, ALT-100单抗)都强烈地取消了反应。ALT-100单抗对LPS诱导的TER屏障功能障碍下降的适度但显著的抑制,再次与EC在LPS反应中分泌的eNAMPT对增加血管通透性的贡献一致,并得到埃文斯蓝染料积累的显著减少的支持(图5 e)和MAP激酶信号的显著降低在活的有机体内(图6).直接询问ec衍生的eNAMPT的作用在活的有机体内,我们使用了EC-cNAMPT−−/有条件限制到内皮的eNAMPT靶向敲除小鼠系.EC-cNAMPT−−/与WT窝仔相比,在一次和两次撞击临床前ARDS损伤模型中,小鼠均明显受到保护,且血浆中eNAMPT、IL-6和IL-8 (KC)水平显著降低。这些结果反映了alt -100治疗后暴露于一次和两次ARDS模型的小鼠血浆和组织中IL-6水平的降低,这表明ec衍生的循环eNAMPT可能是ARDS病理生物学的重要贡献者。
总之,我们的研究强有力地证实了以eNAMPT/TLR4炎症通路为靶点的人源化的eNAMPT中和单抗是一种可行的治疗策略,可以解决对有效和特异性药物治疗的严重未满足需求,以提高ARDS/VILI死亡率。此外,我们还阐明了ec来源的eNAMPT在细菌感染和呼吸机诱导的机械应激引起的炎症性肺损伤中的重要作用。最后,众所周知,ARDS的巨大异质性一直是美国和全球ARDS临床试验网络成功进行治疗性临床试验的关键挑战。我们的研究表明,结合1)eNAMPT作为ARDS预测血浆生物标志物的可用性,或单独[14,32,33],或作为ARDS生物标志物面板的一部分[31];2)高风险的识别NAMPT基因型(14,29,30.];3)高效的eNAMPT中和人源单抗作为靶向生物治疗,存在新的ARDS临床试验设计的机会,该试验将患者分层注册,以测试针对eNAMPT/TLR4炎症通路的生物疗法,这是在当前COVID-19大流行形势下提供个性化ICU药物的一种有吸引力的机制。
补充材料
可共享的PDF
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:J.G.N. Garcia和S. Sammani:作品的概念和设计,作品数据的分析和解释,手稿的起草和修订,最终版本的批准出版;C. Bime, A.E. Cress, Z. Liu和D. Martin:作品的概念和设计,作品数据的分析和解释,关键知识内容的批判性修订和最终版本的批准出版;T. Bermudez, S.M. Camp, A.N. Garcia, C.L. Kempf, H. Quijada, D.G. Valera和J.H. Song:数据的收集和分析,手稿的修订,以及最终版本的出版批准;C. Barber, K. Burns, J.K. Burt, A.A. Desai, S.M. Dudek, E. Franco, A. Gaber, J.R. Jacobson, J.B. Mascarenhas, L. Moreno-Vinasco, V. Natarajan, R.C. Oita, V. Reyes Hernon, B. Sun和X. Sun:收集数据并协助处理和修改手稿
利益冲突:H. Quijada没有什么可透露的。
利益冲突:t·贝穆德斯没有什么可透露的。
利益冲突:c·l·肯普夫没什么可透露的。
利益冲突:d·g·瓦勒拉没什么可透露的。
利益冲突:a。n。加西亚没有什么可透露的。
利益冲突:S.M.营地没什么可透露的。
利益冲突:宋j.h.没有什么可透露的。
利益冲突:e·弗兰科没什么可透露的。
利益冲突:J.K.伯特没有什么可透露的。
利益冲突:B. Sun没有什么可披露的。
利益冲突:J.B. Mascarenhas没有什么可透露的。
利益冲突:K. Burns没有什么可透露的。
利益冲突:A. Gaber没有什么可透露的。
利益冲突:大分R.C.没有什么可透露的。
利益冲突:V. Reyes Hernon没有什么可透露的。
利益冲突:c·巴伯没有什么可透露的。
利益冲突:L. Moreno-Vinasco没有什么可透露的。
利益冲突:X. Sun没有什么可披露的。
利益冲突:A.E.克莱斯没有什么可透露的。
利益冲突:D. Martin在提交的作品之外对Aqualung有投资。
利益冲突:Z. Liu没有什么可透露的。
利益冲突:A.A. Desai报告了NIH R01 (HL136603)和诺华顾问的资助,在提交的工作之外。
利益冲突:V. Natarajan没有什么可透露的。
利益冲突:j·r·雅各布森没什么可透露的。
利益冲突:S.M.杜德克没什么可透露的。
利益冲突:C. Bime没有什么可透露的。
利益冲突:S. Sammani没有什么可透露的。
利益冲突:J.G.N. Garcia报告了在研究进行期间Aqualung Therapeutics, Corp.的赠款和非财务支持(提供研究材料);Aqualung Therapeutics, Corp.在提交的作品之外提供的补助金和个人费用;并拥有美国专利号9,409,983。
支持声明:这项工作得到了美国国立卫生研究院(NIH)/国家心肺和血液研究所(NHLBI)资助的P01HL126609, R01HL094394和P01HL134610。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年6月27日。
- 接受2020年11月5日。
- 版权所有©ERS 2021
本版本根据知识共享署名非商业许可4.0的条款发布。