摘要
基本原理COPD中没有有效的疾病活动测量方法。由于“活动性”疾病的预后较差(如。在ECLIPSE队列中,我们探讨了与8年全因死亡率相关的疾病活动的潜在标志物。
方法我们调查了1)相关临床变量随时间(1或3年)的变化与8年死亡率的关系;2)这些变量是否相互关联;3)是否有任何临床、影像学和/或生物标志物与任何活动成分相关。
结果结果显示:1)1年后,COPD住院、加重频率、体重指数(bmi)、气流阻塞、呼吸困难和运动(BODE)指数或健康状况(St George’s Respiratory Questionnaire, SGRQ)的恶化、全身炎症的持续与8年死亡率显著相关;3年时,同样的指标,加上1秒用力呼气量(FEV)1)下降,并在较小程度上出现计算机断层扫描(CT)肺气肿,显示相关性,因此可作为疾病活动的标志物;3) FEV变化1,炎症因子与CT肺气肿无相关性,多维指标(BODE和SGRQ)相关性中等;4)这些标志物的变化不能通过任何基线横断面测量来预测。
结论在COPD中,1年和3年加重频率、全身炎症、BODE和SGRQ评分和FEV的变化1下降是与8年全因死亡率相关的疾病活动的独立标志。这些疾病活动标志物通常是独立的,不能从基线测量中预测。
摘要
在COPD患者中,1年和3年恶化频率、全身炎症、BODE和SGRQ评分以及FEV的变化1下降是与8年全因死亡率相关的疾病活动的独立标志物https://bit.ly/2CyifcN
介绍
COPD是一种复杂、异质性疾病,是全球发病率和死亡率的主要原因[1].为了解决COPD临床实践中的复杂性和异质性,提出了一种基于“可治疗特征”的策略[2].
疾病严重程度和疾病活动是不同的属性,不一定相关[3.].在COPD中,严重程度传统上用1秒用力呼气量(FEV)来表示1)作为其预测值的比例,因为FEV1是一种良好的加剧预测因子[4,医疗费用[5]和死亡率[6].一些观察性研究已经确定了预测COPD死亡率的预后指标,优于FEV1.在此背景下,身体质量指数、梗阻、呼吸困难和运动(BODE)指数已被公认为确定COPD严重程度的有效多维指数[7].相比之下,在慢性阻塞性肺病中,没有像在其他疾病(如克罗恩病)中开发的那样有效的疾病活动测量方法[8],所使用的工具是结合症状与实验室值和/或功能限制的复合指数。目前,COPD疾病活动性的唯一可靠衡量指标是疾病严重程度的主观和/或客观衡量指标的变化。目前还没有建立横断面测量疾病活动性的生物标志物,尽管这些标志物是有用的[9- - - - - -12].
ECLIPSE (NCT00292552) [13是一项观察性纵向研究,定期对COPD患者进行为期3年的评估。此外,还获得了ECLIPSE亚群体招募后8年的生存状况。ECLIPSE对与疾病严重程度相关的变量进行了多项纵向评估,因此提供了一个独特的机会来调查这些疾病衡量指标的变化之间的关系,并将它们作为与关键结果(如死亡率)相关的疾病活动的替代标记进行探索[14].
我们试图调查相关变量随时间(1或3年)的变化如何与8年死亡率相关,作为一种确定疾病活动的潜在替代标志物的方法;这些组件是否相互关联,以帮助定义每个组件的价值;以及是否有任何临床、成像和/或生物标记物在基线时测量与任何识别的活动成分相关。
方法
ECLIPSE研究设计和伦理学
ECLIPSE研究的设计和报名标准已于先前发表[13].简而言之,在初步研究期间定期评估具有全球慢性阻塞性肺病(GOLD)等级II-IV COPD,加量和禁烟对照的参与者,并在初步研究期间进行3年,并记录生存状态以同意8 years. ECLIPSE complied with the Declaration of Helsinki and was approved by ethics committees of participating centres. All participants provided written informed consent.
本研究只包括了ECLIPSE研究中患有慢性阻塞性肺病的参与者。
测量
ECLIPSE的方法已经在前面描述过[15- - - - - -17].简单地说,美国胸科协会、医学研究委员会和圣乔治呼吸问卷(SGRQ)的修改问卷记录了患者报告的共病、呼吸困难和与健康相关的生活质量。也记录了研究前一年或3年研究期间的中度和重度恶化。
统计分析
人口特征总结为平均值±sd或百分比。疾病活动变量与8年死亡率之间的关系是通过将基线到1年和已知与死亡率相关的变量到3年的变化进行分类来确定的。这包括以下变量:FEV1下降;定量计算机断层扫描(CT)采用最低15%百分位密度法(PD15)测定肺气肿;波德指数;频繁发作(定义为每年两次或两次以上发作);SGRQ总分;以及选择的系统生物标志物。生存期为8年。分析个体临床危险因素和生物标志物的Kaplan-Meier曲线。使用Cox比例风险回归模型比较基于这些临床表型的变化类别之间的风险比,调整基线BODE、年龄和既往COPD住院治疗。此外,报告了基于变化的8年生存风险比和95%可信区间。 Diagnostics for optimising model fit and predictive capability used Akaike's information criterion and the adequacy index, respectively [18].使用Spearman的ρ探索疾病活性组分(和潜在基线标志物)之间的潜在相关性。所有测试执行(SAS版本9.2; SAS Institute,Cary,NC,USA)是双面的0.05个显着性水平。所有p值都是标称的;由于分析被认为是探索性的,因此没有对多种比较进行调整。
结果
参与者的特征和生存
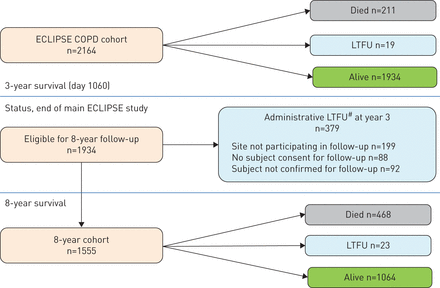
在2164名最初的ECLIPSE COPD患者中,1934名(89%)在3年随访结束时存活,可能可以纳入8年随访期。共有211名参与者在第3年死亡,19人在随访(LTFU)中失踪。对于8年生存评估,1555(80.4%)符合条件的受试者同意并参与了8年随访。其中,468人死亡,23人在第8年LTFU, 1064人被证实活着。受试者LTFU的临床和生理特征,无论是由于管理原因(主要是由于方案修订,n=379)或在8年时无法解释(n=42),在8年随访时介于活受试者和死亡受试者之间(图1).表1显示了1555名同意参与8年随访的参与者在第3年的基线特征和临床特征,按8年的生存状态进行分割。与幸存者相比,非幸存者年龄更大,有更严重的气流限制,报告了更多的呼吸症状和更糟糕的健康状况,6分钟步行距离更短,肺气肿更多,BODE评分更高,更多的共病,更有可能有COPD加重史。补充表E1显示,未参与ECLIPSE随访延长的患者的基线临床特征介于8年研究中死亡和幸存的患者之间。在8年期间,总共有679名COPD患者在ECLIPSE中死亡。Kaplan-Meier估计在此期间的死亡概率为37%。
ECLIPSE COPD研究中所有受试者试验报告合并标准图。#:停止参与研究或不同意8年生存状态的受试者或地点。LTFU:失访。
疾病严重程度和8年死亡率的标记
作为疾病严重程度的一项确定指标,基线BODE指数是8年死亡风险的良好预测指标(图2).我们通过将一组系统生物标志物添加到已知疾病严重程度(BODE、年龄和COPD住院情况)的基础模型中,评估了它们对8年死亡风险的可加性预测能力。白介素(IL)-6、中性粒细胞和表面活性剂蛋白D (SP-D)共同提高了该模型预测8年死亡率的能力(优化了Akaike在生物标志物协变量中的信息标准)。临床协变量(BODE、年龄和COPD住院时间)的基础模型提供了全基础加生物标志物模型的87%的预后价值(充分性指数=0.87)。
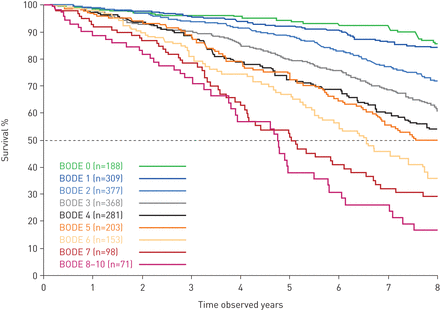
随访8年死亡率的Kaplan-Meier曲线,按基线体重指数、梗阻、呼吸困难和运动(BODE)指数进行分割。
疾病活动性和8年死亡率的标志
表2对研究的疾病活动变量提出危险比和死亡风险的95%置信区间。从基线到第一年的变化,COPD住院、两次或两次以上加重、BODE指数≥1单位恶化或SGRQ总评分≥4单位恶化以及炎症细胞因子持续升高均与死亡风险增加相关。当超过3年时,相同的变量,以及FEV1在8年的随访中,与死亡风险有更强的关联。CT肺气肿(PD15)的变化或下降显示与1年死亡风险的相关性较弱,3年死亡风险在名义上显著。
图3和4显示基于从基线到3年确定的每个变量的变化的8年生存率Kaplan-Meier估计(表2).阈值为20 mL·年−1和40毫升·−1对于FEV1根据Framingham后代队列的健康从不吸烟者和吸烟者的平均下降价值选择下降[19];所提供的阈值并不是建议最佳下降阈值。存活概率与FEV有关1改良剂的变化为84% (>20 mL·年)−1获得);稳定组为75%(下降±20 mL·年)−1);适度下降67%(下降20-40毫升·年−1);下降幅度为65% (>40 mL·年)−1).
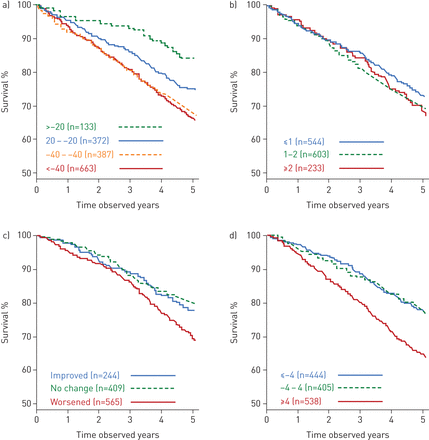
从3年到8年的死亡率Kaplan-Meier曲线为a)强迫呼气量下降1秒(mL·年)−1);B)计算机断层摄影下降(最低15th百分密度法−1·年−1);c)体重指数、梗阻、呼吸困难和运动(BODE)指数变化;d) St George’s Respiratory Questionnaire总分变化。
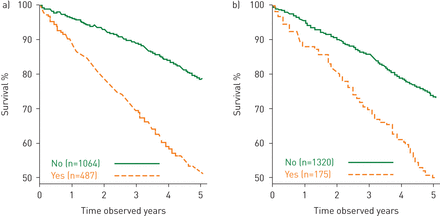
Kaplan-Meier从3年到8年度的死亡率曲线a)3年超过3年的COPD住院治疗;b)每年频繁恶化3年。
表3研究表明,疾病活动性的变化与肺功能严重程度无关,因为在GOLD严重程度分级(II/III)中,相同的变量具有显著性。在GOLD分级IV的患者中,仅FEV率1下降和住院在8年达到了统计学意义,但这个阶段的患者数量相对较少(n=173)。
表4显示出基质相关(斯皮尔曼ρ值)之间的疾病活动标记表2.单变量变化(FEV1炎症标志物与CT (PD15)之间无相关性。其中一些个体变量的变化与整合其中一些变量的多维指数(BODE和SGRQ)之间存在适度和预期的关系。
补充表E2显示这些疾病活动成分大多与任何基线、横断面测量无关。
讨论
这项对ECLIPSE COPD队列的长期分析有三个主要的新观察结果。一些变量(包括FEV)随时间(1年或3年)的变化1随访8年,COPD恶化、BODE指数、SGRQ评分和持续炎症的存在显著预测了死亡风险,提示这些变量应被视为疾病活动的替代标志物。这些变量的变化通常是相互独立的,这表明疾病活动的结构(就像疾病本身)是异质性和复杂性的。最后,尚不能从基线上获得的任何横断面测量来准确预测随时间的变化。总的来说,这些发现有助于为临床指导顺序测量的变量探索开发针对疾病进展的治疗方法。
先前的研究
COPD疾病严重程度的标志物与其预测临床相关结果(如死亡率)的能力之间的关系已得到广泛研究[20.- - - - - -23].我们的结果证实了原始BODE 3年报告中的观测结果的稳健性[7]作为对BODE指数提供的疾病严重程度的评估仍然是长期死亡率的良好预测因子,即使在为初始的3年观察期的人幸存下来。通过将较老年人和住院的存在补充,通过补充信息,通过电子医疗记录轻松确定。正如3年的后续行动所一样24],全身中性粒细胞、IL-6和SP-D水平与8年死亡风险增加相关。当将这些生物标志物水平添加到BODE指数、年龄和COPD住院率的基础模型中来预测8年随访时的死亡风险时,该模型的预后能力为13%。据我们所知,目前的研究是第一次调查多个候选的疾病活动替代标志物之间的关系,对不同疾病严重程度的COPD患者进行了长期随访(8年),以验证其与重要临床结果(全因死亡率)的关系。
新发现的解释
本研究提供了三种新的观察。首先,从基线到1年的COPD加剧,BODE指数,SGRQ评分和持续炎症的存在明显到8年死亡率的存在。当这些变化在3年确定时,这种关系变得更加强大。FEV.1下降,以及较小程度的CT肺气肿下降,也显示了与结果的关系。总的来说,这些观察提供了证据,表明这些变量的变化是疾病活动的替代标记。值得注意的是,这些纵向测量(IE。疾病活动随时间的变化)与它们的基线值不同,后者可能是也可能不是疾病严重程度的标志。
据我们所知,尽管之前的研究与FEV有关1以2- 6年为间隔进行测量的死亡率下降[25,26],只有一项先前的研究[27已经决定了可能需要多长时间来描述FEV的价值1在更短的时间内下降,并将其与结果的影响联系起来。该研究和这项研究的结果表明,时间跨度为1到3年。此外,FEV1这些结果很重要,因为随着电子病历使用的增加,在日常临床实践中识别这些患者是可行的。监测肺功能可以帮助识别有风险的个体,并进一步探索与衰退相关的机制,以支持旨在改善疾病进展的改良疗法的发展。
在观察的第一年,导致住院的恶化的存在是一个重要的预测因素,扩展了ECLIPSE中最初3年的发现[28和其他研究[298年的随访;在同一时间框架上形成两种或更多的温和加剧也与增加的死亡率增加。当疾病活动措施因从基线到3年的后续行动而确定的,结果证实,每年的COPD和至少两个恶化的住院都是死亡率的重要预测因子,因此是疾病活动的标志物。这建立了有针对性评估旨在防止这些事件的实际时间表[30.].
此外,1年后BODE指数和SGRQ总评分的恶化是8年死亡风险的预测因子。这些发现与之前的研究一致。Casanova等.[27表明,与FEV变化相比,BODE指数1年的变化变化较小,是更好的生存预测指标1在740例COPD患者中随访5年以上。在国家肺气肿治疗试验中,1年BODE指数的变化是该队列COPD患者2年和5年生存率的重要预测因素[31].此外,已知SGRQ评分与死亡率有关,4个单位的变化代表其最小的临床重要差异[32,33].在目前的研究中,1年内≥4个单位的SGRQ≥4个单位的恶化与随后的7年内的死亡风险增加有关。当发生变化超过3年时,BODE指数或SGRQ评分的恶化变得更加强大的预测因素,其死亡风险在8年后的后续行动。
持续性全身性炎症(IE。在连续两年获得的血液样本中,两种或两种以上的炎症生物标志物水平高),ECLIPSE研究中的死亡风险增加已经发表[34],并得到8年死亡率分析的结果。然而,我们只观察到CT肺气肿(PD15)的1至3岁之间的关系薄弱,具有全面的死亡率。这些观察结果并没有表明CT检测程度缺乏关联的肺气肿(IE。疾病严重程度的评估)和死亡风险,如以前记录的[35,36]但是,使用Eclipse中实施的方法检测到检测的变化并不像疾病活动的其他标志物那么强。也可能是进展的影响通过定量CT对早期COPD (GOLD I)或有COPD风险的患者(前GOLD 0)比已经有大量肺气肿的患者提供更多信息。
本研究的另外两个新发现涉及到这里确定的大多数不同变量与8年死亡率之间缺乏相关性,以及在基线时确定的横断面测量无法预测疾病活动。前者表明本文研究的变量是异质性和复杂性的,反映了COPD本身的结构。这项研究的结果表明,许多重要的和疾病相关的个人测量需要独立考虑,以评估疾病活动。在临床实践中,这些观察结果支持基于拟议的“可治疗特征”方法的管理策略[2].多维的BODE和SGRQ指数,以及恶化的频率和严重程度,更敏感地反映活动,但缺乏提供个性化治疗方法所需的特异性。就像生命中不同的肺功能轨迹一样[37,38],不同生物标志物所反映的COPD受影响的多个维度可能存在不同的轨迹。然而,我们在基线时确定的多个横断面测量结果都与我们确定的任何疾病活动成分没有显著相关,随后强调了识别和验证疾病活动的其他生物标志物的迫切需要。
优势和局限性
这项研究的重要优势在于,ECLIPSE队列是在一个前瞻性的临床环境中跟踪的,这些患者都是特征明确的慢性阻塞性肺病患者,他们遭受着广泛的气流限制。此外,疾病严重程度和疾病活动性的标志物(由它们随时间的动态变化确定)分别作为全因死亡率的预测因子进行了评估。
本研究的主要局限性是,8年生存状态评估是作为一项晚期方案修订实施的,由于没有得到所有地方的参与同意,19.6%的合格受试者在第3年底需要审查,主要是由于管理原因。然而,这组被删失的患者的基线特征介于幸存者和非幸存者之间,这表明他们是整个研究纳入的患者的代表。1555名同意进行8年随访的参与者的基线和3年特征与398名活着但不同意参加8年随访的参与者被提供补充表E1.总的来说,非参与者在大多数临床变量上的价值比那些参与研究的人更差。然而,与死亡率相关的这些参数的变化在轻度疾病患者中是明显的,这一事实进一步支持了我们的研究结果的相关性。数据的另一个限制是缺乏对死亡原因的裁定,正如在若干前瞻性干预试验中所做的那样[39- - - - - -41].评估了有限数量的血清和血液生物标志物,不包括最近描述的标志物,如胶原蛋白和弹性蛋白转换生物标志物[42,可用于评估COPD疾病活动的不同组成部分。最后,ECLIPSE人群是由专家招募的,通常是在具有临床试验专业知识的学术中心,并不代表基于人群的样本。
结论
这项对ECLIPSE研究中纳入的COPD患者的8年随访显示,FEV随时间(1或3年)的变化1在8年随访后,下降、恶化频率、BODE和SGRQ评分和全身炎症可作为疾病活动的替代标志物,与全因死亡率显著相关。疾病构成的不同变量相互独立,目前无法通过横断面措施进行预测。
补充材料
可共享的PDF
确认
维斯博是由曼彻斯特生物医学研究中心的国家健康研究所支持的。a . Lomas是国家健康研究所高级研究员,得到伦敦大学学院医院国家健康研究所生物医学研究中心的支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
ECLIPSE研究注册为临床试验www.clinicaltrials.gov标识号NCT00292552.有关葛兰素史克的数据共享承诺和要求访问匿名个人参与者数据和相关文件的信息可以在以下网站找到www.clinicalstudydatarequest.com
作者贡献:所有作者都对所报道的作品的概念或设计做出了重大贡献。N. Locantore和J.C. Yates参与了报告数据的获取。所有的作者都参与了分析和解释报告的数据。所有作者审查和/或严格修订的手稿的重要知识内容,并提供了最终批准的版本将出版。
利益冲突:B. Celli报告了葛兰素史克在进行研究期间对科学委员会工作的拨款和个人费用;阿斯利康(AstraZeneca)拨款和提供研究设施,葛兰素史克(GlaxoSmithKline)咨询和科学委员会工作的个人费用,勃林格殷格翰(Boehringer Ingelheim)、赛诺菲-安万特(Sanofi-Aventis)、梅纳里尼(Menarini)、Chiesi和Pulmonx在提交工作之外的咨询个人费用。
利益冲突:N. Locanore是GSK的员工和股东。
利益冲突:J.C. Yates是葛兰素史克的雇员,并拥有该公司的股份。
利益冲突:P. Bakke报告了葛兰素史克、阿斯利康和勃林格殷格翰的顾问委员会工作和讲座的个人费用,Chiesi的顾问委员会工作的个人费用,在提交的工作之外。
利益冲突:P.M.A. Calverley报告了葛兰素史克、勃林格殷格翰、诺华、赞邦、呼吸科和Recipharm在提交工作之外的个人费用。
兴趣冲突:C. Crim是Glaxosmithkline的员工和股东。
利益冲突:H.O. Coxson报告葛兰素史克在进行研究期间为科学委员会工作提供的拨款和个人费用。
利益冲突:D.A. Lomas报告葛兰素史克在研究进行期间的拨款和个人费用;葛兰素史克(GlaxoSmithKline)的顾问委员会工作和讲座的拨款和个人费用,Griffols的顾问委员会工作的个人费用,在提交的工作之外。
利益冲突:W. MacNee报告葛兰素史克在进行研究期间为科学委员会工作收取的个人费用;葛兰素史克和阿斯利康的个人费用,辉瑞的拨款和个人费用,提交的工作之外。
利益冲突:B.E. Miller是GSK的员工和股东。
利益冲突:H. Mullerova是葛兰素史克的前雇员。
利益冲突:S.I. Rennard是阿斯利康的前雇员,曾为GSK、维罗纳、Bergenbio和NovoVentures提供咨询,目前在提交的工作之外持有阿斯利康的股份。2007年之前,S.I. Rennard从烟草业获得了资金,用于与减少危害和烟草烟雾对干细胞的影响有关的研究,并就减少危害的主题与RJ Reynolds进行了咨询(不收取个人费用):RJ Reynolds提供的资金用于评估一种减少危害产品对正常吸烟者(1996年)和慢性支气管炎患者(1999年)的影响,以及评估戒烟对下呼吸道炎症的影响(2000年);参与菲利普莫里斯公司的多中心研究,评估烟雾暴露的生物标志物(2002年);由科学与健康研究所资助的一项临床试验(2005年)得到了烟草业的支持,以评估与戒烟和减少吸烟相关的呼出气体中的生物标记物(该研究得到了罗瑞拉德和RJ雷诺兹公司的资助);菲利普·莫里斯外部研究计划(2005)用于评估吸烟对小鼠循环干细胞的影响的拨款;在2007年之前,为RJ Reynolds公司提供减少伤害的咨询服务(不提供个人报酬)。没有活跃的烟草业资助的项目。与烟草公司和烟草公司支持的实体的所有联系在2007年终止。
利益冲突:E.K. Silverman报告了葛兰素史克的拨款、个人费用和差旅费,以及NIH的拨款,在研究进行期间。
利益冲突:E. Wouters报告了Nycomed和Boehringer Ingelheim BV咨询委员会工作的个人费用,阿斯利康和葛兰素史克讲座的拨款和个人费用,诺华和Chiesi讲座的个人费用,在提交的工作之外。
利益冲突:R. Tal-Singer是葛兰素史克的员工和股东。
利益冲突:A. Agusti报告葛兰素史克在开展研究期间的科研委员会工作的个人费用;阿斯利康、Chiesi和Nuvaira的个人费用,Menarini和葛兰素史克的赠款和个人费用,提交的工作之外。
利益冲突:J.Vesbo在研究期间报告了GSK的指导委员会工作的个人费用;来自Astazeneca,Chiesi和Novartis的讲座和咨询的个人费用,Boehringer Ingelheim的讲座和顾问的讲义和个人费用来自GSK的咨询,在提交的工作之外;并拥有Chiesi(丹麦)雇用的家庭成员。
支持声明:该研究由葛兰素史克公司赞助。一个指导委员会和一个由学术和赞助代表组成的科学委员会制定了原始研究设计、分析计划,并可以完全访问数据。研究发起者对手稿中的陈述没有任何限制。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年4月22日。
- 接受2020年6月20日。
- 版权©2021人队
此版本在Creative Commons归因非商业许可证4.0的条款下分发。