摘要
烟草烟雾相关慢性阻塞性肺疾病(S-COPD)受试者的单核细胞源性巨噬细胞(MDM)和肺泡巨噬细胞中,潜在致病菌(PPB)的下呼吸道定植与细菌吞噬功能缺陷有关。在发展中国家,非吸烟者中的COPD主要是由于生物量烟雾(BMS)暴露所致;然而,对于这些受试者的PPB定植及其与先天免疫受损的关系知之甚少。
我们研究了PPB负荷(链球菌引起的肺炎,流感嗜血杆菌,卡他莫拉菌和铜绿假单胞菌)BMS暴露的慢性阻塞性肺病(BMS-COPD)受试者与S-COPD和肺功能正常受试者进行比较。我们还检查了PPB负荷与MDMs吞噬活性和肺功能之间的关系。从18名健康非吸烟者、15名非COPD吸烟者、16名BMS暴露健康受试者、19名S-COPD受试者和23名BM受试者中收集诱导痰和外周静脉血样本使用定量PCR和荧光法分别测定诱导痰中的PPB负荷和MDM吞噬活性。
更高的细菌负荷肺炎链球菌,流感嗜血杆菌和铜绿假单胞菌在BMS-COPD受试者中观察到。在bms暴露的受试者中,PPB负荷的增加与MDMs和肺活量肺功能指数的吞噬缺陷显著负相关(p<0.05)。
BMS-COPD受试者气道PPB负荷增加与细菌吞噬功能和肺功能缺陷呈负相关。
摘要
生物量烟雾暴露的COPD受试者的细菌负荷与巨噬细胞细菌吞噬功能缺陷有关http://ow.ly/Q5ns30mNN0k
介绍
慢性阻塞性肺疾病(COPD)是一种进行性、衰弱性、炎症性气道疾病,通常由慢性接触有毒吸入污染物引起。它是全球第三大死因,也是印度第二大死因[1.,2.]吸烟是COPD发展的最确定的危险因素,尽管其人群归因比例<50%[3.]。来自发展中国家的最新证据显示,接触生物质燃料燃烧产生的烟雾(即。室内或家庭空气污染)也是慢性阻塞性肺病的一个重要风险因素,尤其是对女性[3.–5.]。据估计,印度70%的房屋和世界上约50%的房屋,特别是非洲、东南亚、南亚和南美洲国家的房屋,使用生物质燃料做饭和取暖[5.]。在印度农村人口中,大约85%的慢性阻塞性肺病发生在从不吸烟的人群中[4.]。
烟草烟雾相关慢性阻塞性肺病(S-COPD)受试者的气道经常被潜在致病菌(PPB)定植,而非慢性阻塞性肺病吸烟者和健康的非吸烟者的气道通常不被PPB定植[6.,7.]。PPB的存在与COPD患者复发性急性加重、气道炎症增加和肺功能进行性下降密切相关[8.,9]。加重是COPD的重要临床特征,也是发病率和死亡率的主要因素[10]。P阿尔等. [11]报告称,细菌定植增加了COPD受试者的病情加重频率,表明细菌负荷在确定病情加重的存在和严重程度方面发挥了作用。在慢性阻塞性肺病患者中,下呼吸道最常见的病原微生物是流感嗜血杆菌,链球菌引起的肺炎,卡他莫拉菌和铜绿假单胞菌[7.,9,11]。这些致病菌的负荷在COPD加重期间被发现增加,表明它们可能在因果关系中发挥作用[9,11]。
巨噬细胞是重要的免疫细胞,在清除气道中的PPB方面起着重要作用[12]。PPB的去除通过吞噬作用对于维持无病原体气道至关重要。然而,在S-COPD受试者中观察到巨噬细胞对细菌的吞噬活性受损。S-COPD受试者肺巨噬细胞对细菌的吞噬活性降低流感嗜血杆菌和肺炎链球菌[13,14]这被认为是慢性阻塞性肺病患者肺部持续感染和炎症的根本原因之一[8.,15]。
从肺部获取巨噬细胞以研究其吞噬功能需要侵入性程序,如支气管镜检查。血液单核细胞从循环迁移到肺部并分化为巨噬细胞,这些巨噬细胞的数量在COPD中被发现增加[16]单核细胞源性巨噬细胞(MDM)被广泛用作了解巨噬细胞吞噬活性的模型体外在许多炎性气道疾病,如慢性阻塞性肺病、哮喘和囊性纤维化[17–19]然而,我们和其他人已经证明MDMs可以作为肺巨噬细胞的替代物[17,18,20.]。之前对S-COPD受试者的研究报告称,与健康受试者相比,来自S-COPD受试者的MDMs表现出细菌吞噬缺陷,这种吞噬缺陷与肺泡巨噬细胞中没有显著差异[17].由于MDM易于安全获取,因此被广泛用于研究气道巨噬细胞生物学[21]。
MDMs的细菌吞噬缺陷已被证明与在S-COPD受试者呼吸道中PPB的更大定植有关[17,22],尽管这些研究需要在世界其他地区重复。但是,MDMs在暴露于生物质烟雾(BMS)的COPD(BMS-COPD)中的吞噬能力在本研究中,我们调查了BMS-COPD受试者的气道PPB负荷和MDMs的细菌吞噬活性,并将其与居住在印度农村的S-COPD和健康受试者进行了比较。
方法
研究对象
我们从胸科研究基金会(CRF;慢性阻塞性肺病队列(补充材料).采用COPD评估试验(CAT)和St George’s Respiratory Questionnaire (SGRQ)评估COPD患者的生活质量[23,24]。COPD的诊断是根据全球慢性阻塞性肺病倡议(GOLD)标准确定的,即。1例患者存在支气管扩张剂后用力呼气量 s(FEV1.)/强迫肺活量(FVC) <70%和FEV1.pred (< 80%25]。年龄匹配的对照组从相同的村庄招募,肺测量正常,没有潜在的临床异常和正常的胸部x线摄影。
H-BMS表型和BMS-COPD诊断标准至少基于2 每天接触BMS至少20小时 年头[26]。BMS暴露量表示为每年小时数(因生物质燃料燃烧而暴露于烟雾中的年数与每天在生物质燃料烟雾周围花费的平均小时数的乘积)。HS和S-COPD受试者均为吸烟者≥10包年。过去或现在有被动吸烟、肺结核、哮喘、肺癌或过敏史的受试者被排除在研究之外。此外,招募的COPD受试者在入选期间没有恶化/临床感染,并且在之前12个月内没有接受任何全身/吸入性皮质类固醇或抗生素治疗 周。
本研究获得所有受试者的书面知情同意,并经CRF机构伦理委员会批准。
肺量测定法
肺活量测定是按照欧洲呼吸学会/美国胸科学会指南进行的[188bet官网地址27]。数值以绝对容积或流量表示,或以基于年龄、性别、体重、身高和种族的预测百分比表示。
痰诱导
痰诱导采用3% (w/v)高渗盐水通过超声雾化器(欧姆龙,日本京都)雾化15-20分钟。对诱导的痰标本进行差异细胞计数。痰诱导和差异细胞计数的详细方案概述在补充材料.
定量磅的文化
对诱导痰进行细菌定量培养肺炎链球菌,流感嗜血杆菌,复活的和铜绿假单胞菌如中所述补充材料.
从痰样本中提取DNA
根据制造商说明,使用QIAmp DNA Mini Kit (Qiagen, Hilden, Germany)从存储的诱导痰样本中提取DNA,并在-20°C保存。使用NanoDrop ND-1000分光光度计(ThermoFisher Scientific, Waltham, MA, USA)进行DNA定量,0.8%琼脂糖凝胶进行质量检查。
标准细菌DNA
DNA肺炎链球菌(写明ATCC 49619 / DSM 24048),流感嗜血杆菌(ATCC 10211/DSM 11969)和复活的(ATCC 9143/DSM 9143)购自德国微生物与细胞培养集(莱布尼茨研究所DSMZ,德国莱布尼茨)。DNA从铜绿假单胞菌(ATCC 27853/MCC 2080)在国家细胞科学中心(印度浦那)的微生物培养收集处,根据制造商的说明,使用MoBio微生物DNA分离试剂盒(Qiagen)进行分离。
定量聚合酶链反应
采用SYBR Green方法进行定量PCR (qPCR)肺炎链球菌,流感嗜血杆菌,复活的和铜绿假单胞菌根据先前定义的痰样本研究方案,通过靶向验证引物(分别为Spn9802、P4脂蛋白、CopB和Pa23)[15,28]。引物序列及qPCR程序列于补充表S1和S2,分别。
活力测定
MDMs吞噬后,采用3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑(MTT)法(补充材料).
统计分析
Prism 7.0版(美国加利福尼亚州圣地亚哥GraphPad)数据的正态性由Shapiro–Wilk正态性检验确定。对于非参数数据,进行Kruskal–Wallis/Dunn多重比较检验;对于参数数据,进行ANOVA/Tukey多重比较检验。使用Spearman秩相关检验确定相关性。SPSS版本23.0(IBM,Armonk,NY,USA)用于进行多元线性回归分析。如果p<0.05,则认为差异显著。
结果
研究对象
纳入本研究的91名受试者包括18名H-NS、15名HS、16名H-BMS、19名S-COPD和23名BMS-COPD受试者。在91名受试者中,只有76名受试者提供了可用的痰样本(≥0.5 g每个样本的痰液塞),用于定量细菌负荷(14小时-NS、11小时、15小时-BMS、16小时-COPD和20小时-COPD)。人口统计详情见表1(76例)和补充表S3(91例)。
研究组之间的年龄没有显著差异。HS和S-COPD受试者吸烟包年数相似(p>0.05)。同样,H-BMS和BMS- copd受试者之间BMS暴露史相似(p>0.05)。S-COPD组CAT总评分显著高于BMS-COPD组(p<0.05),但SGRQ总评分和肺活量指标在COPD亚组(S-COPD和BMS-COPD)之间差异无统计学意义(p>0.05)。此外,在S-COPD和BMS-COPD受试者中,β-激动剂和抗胆碱能的使用无统计学差异。
qPCR检测病原微生物负荷
最初,通过比较男性受试者(H-NS、HS和S-COPD)和女性受试者(H-BMS和BMS-COPD)的痰样本,对PPB进行基于性别的比较。我们没有观察到每个PPB的负荷有任何显著差异(肺炎链球菌,流感嗜血杆菌,复活的或铜绿假单胞菌)和总PPB负荷(平均负荷肺炎链球菌,流感嗜血杆菌,M.莫拉菌和铜绿假单胞菌)在男性和女性受试者之间的气道中(p>0.05)(补充图S1和S2).
用于诱导痰qPCR检测肺炎链球菌和铜绿假单胞菌,临界值>1×104.基因组拷贝数·mL−1.被认为是(29,30.].为了流感嗜血杆菌和复活的qPCR检测,截断>1×105.基因组拷贝数·mL−1.被认为是(31,32].高于截止值的样品百分比肺炎链球菌,流感嗜血杆菌,复活的和铜绿假单胞菌分别为67.11%(76名中51名)、71.05%(76名中54名)、65.79%(76名中50名)、47.47%(76名中36名)。
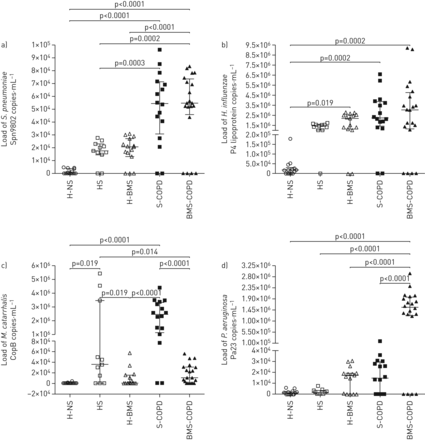
在H-NS科目中,负荷肺炎链球菌和流感嗜血杆菌与BMS-COPD和S-COPD受试者相比,诱导痰样本中可忽略不计(p<0.0001)(图1一个我们观察到肺炎链球菌和流感嗜血杆菌bms -慢阻肺和s -慢阻肺受试者诱导痰标本的含量显著高于H-BMS (肺炎链球菌:p<0.0001;流感嗜血杆菌: p=0.0002)和HS (肺炎链球菌:p<0.0001;流感嗜血杆菌:p=0.0002)受试者(图1一个b)有趣的是,在这项研究中复活的与BMS-COPD组相比,S-COPD组诱导痰的含量显著升高(p<0.0001) (图1 c).然而,负荷铜绿假单胞菌BMS-COPD受试者的诱导痰样本中的浓度高于S-COPD受试者(p<0.0001)(图1 d).
定量PCR法检测研究对象诱导痰标本中潜在致病菌的细菌载量:a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌,健康非吸烟者(H-NS) (n=14)、无慢性阻塞性肺病(COPD) (HS) (n=11)、生物质烟(BMS)暴露健康受试者(H-BMS) (n=15)、烟草烟相关慢性阻塞性肺病(S-COPD) (n=16)和BMS暴露慢性阻塞性肺病(BMS-COPD)受试者(n=20)。采用夏皮罗-威尔克正态性检验。数据显示为带有中位数(四分位范围)的点图。组内比较采用Kruskal-Wallis检验和Dunn多重比较检验。P <0.05为差异有统计学意义。
对健康对照组气道PPB负荷也进行了比较。我们没有观察到负载有什么不同肺炎链球菌健康对照组(H-NS、HS和H-BMS) (图1一个).然而,负荷H.流感嗜血杆菌H-BMS和HS受试者气道内的负荷量高于H-NS受试者,但仅H-BMS受试者气道内负荷量有统计学意义(p=0.019) (图1 b).尽管负荷M.莫拉菌在健康对照组中,负荷低于临界值M.莫拉菌与H-NS和HS受试者相比,HS受试者的气道阻力显著升高(p=0.019)(图1 c).有趣的是,铜绿假单胞菌与HS和H-NS受试者相比,H-BMS受试者的负荷增加,但该负荷无统计学意义(p>0.05) (图1 d).
由微生物培养确定的致病微生物负荷
在一个样本子集中,我们也通过微生物培养方法调查PPB的负载,并确认肺炎链球菌和流感嗜血杆菌BMS-COPD和S-COPD受试者的诱导痰样本与健康受试者相比显著升高(p<0.05)(补充图S3a和b).与qPCR结果相似,CFU·mL−1.价值观复活的(p<0.05) (补充图S3c),而铜绿假单胞菌(p<0.05) (补充图S3d).
在本研究中,考虑的致病性细菌种类的临界值为≥104CFU·mL−1.为肺炎链球菌,流感嗜血杆菌和复活的,及≥105.CFU·毫升−1.为铜绿假单胞菌[33]。通过微生物培养方法测定的样品超过临界值的百分比肺炎链球菌,流感嗜血杆菌,复活的和铜绿假单胞菌分别是52%(13名)、80%(20名)、40%(10名)和40%(10名)。
细菌负荷与肺功能的相关性
在显示了COPD受试者和对照组痰中细菌负荷的差异后,我们想确定这些差异是否与肺功能参数的变化有关。
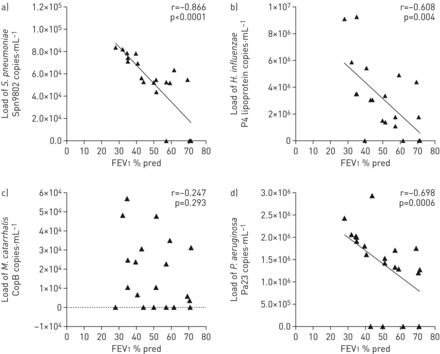
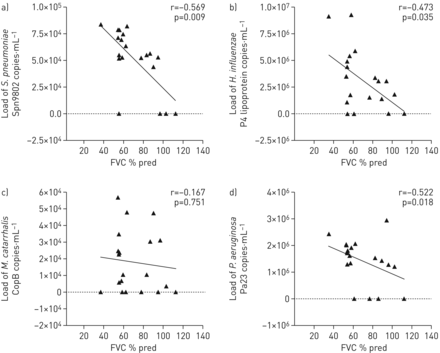
BMS暴露受试者(BMS-COPD和H-BMS)的气道负荷肺炎链球菌,流感嗜血杆菌和铜绿假单胞菌与FEV呈负相关1.% pred (p<0.05) (图2和补充图S4)、FVC % pred (p<0.05) (图3和补充图S5), FEV1./ FVC (p < 0.05) (补充图S6及S7).
1例诱导痰细菌负荷与用力呼气量的关系 s(FEV1.)生物质烟雾暴露的慢性阻塞性肺病受试者中pred % (n=20): a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌.采用夏皮罗-威尔克正态性检验。相关系数采用非参数Spearman相关分析计算。P <0.05为差异有统计学意义。
生物质烟雾暴露慢性阻塞性肺病患者诱导痰标本中的细菌载量与肺强迫肺活量% pred的关系(n=20): a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌.采用夏皮罗-威尔克正态性检验。相关系数采用非参数Spearman相关分析计算。P <0.05为差异有统计学意义。
同样,在烟草烟雾暴露的受试者(S-COPD和HS)中,负荷之间存在显著的负相关肺炎链球菌感染,流感嗜血杆菌和复活的和钒铁1.% pred (p<0.05) (补充图S8和S11)、FVC % pred (p<0.05) (补充图S9和S12), FEV1./ FVC (p < 0.05) (补充图S10和S13).
细菌负荷与年龄、吸烟史和生物量暴露史的相关性
通过多元线性回归模型,我们发现年龄与受试者的PPB负荷无关(p>0.05)(补充表S4), BMS暴露史与负荷呈统计学正相关肺炎链球菌,流感嗜血杆菌和铜绿假单胞菌(p < 0.05) (补充表S4).然而,吸烟史与负荷显著正相关肺炎链球菌,流感嗜血杆菌和复活的(p < 0.05) (补充表S4).
受试者组间痰巨噬细胞总数的比较
同时观察痰中巨噬细胞总数。我们观察到BMS-COPD受试者诱导的痰标本中巨噬细胞的数量高于H-BMS和H-NS受试者,但与H-NS受试者相比有统计学意义(p=0.0005) (补充图S14).同样,在S-COPD受试者中,与HS (p=0.0004)和H-NS (p<0.0001)相比,痰中巨噬细胞数量显著增加(补充图S14).
气道中痰液中巨噬细胞总数与细菌负荷的相关性
我们分析了气道中痰中巨噬细胞总数与PPB负荷之间的关系。痰液中巨噬细胞总量与负荷呈显著正相关肺炎链球菌和流感嗜血杆菌BMS-COPD和S-COPD受试者(p<0.05) (补充图S15和S17).有趣的是铜绿假单胞菌与bms暴露受试者(BMS-COPD和H-BMS)的痰中巨噬细胞总数呈正相关(p<0.05) (补充图S15和S16),而M.莫拉菌与吸烟暴露受试者(S-COPD和HS)的痰中巨噬细胞总数相关(p<0.05) (补充图S17和S18).
慢性阻塞性肺病患者细菌负荷与生活质量评分的相关性
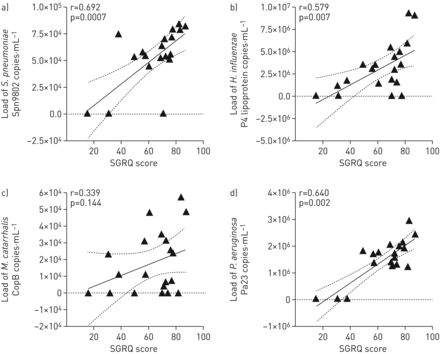
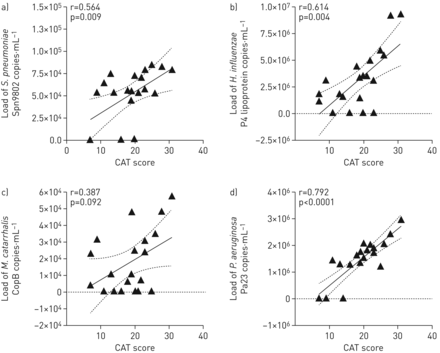
我们还研究了这些PPB在气道中的定植与COPD患者生活质量之间的关系。在BMS-COPD受试者中,总SGRQ评分与负荷之间观察到显著正相关肺炎链球菌(r=0.692,p=0.0007),流感嗜血杆菌(r=0.579,p=0.007)和铜绿假单胞菌(r=0.640,p=0.002)(图4).同样,总CAT评分与负荷之间存在显著正相关肺炎链球菌(r = 0.564, p = 0.009),流感嗜血杆菌(r = 0.614, p = 0.004)铜绿假单胞菌(r=0.792,p<0.0001),但不是复活的(图5).
生物质烟雾暴露慢性阻塞性肺疾病受试者诱导痰样本细菌载量与圣乔治呼吸问卷(SGRQ)总分的关系(n=20): a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌.采用夏皮罗-威尔克正态性检验。相关系数采用非参数Spearman相关分析计算。P <0.05为差异有统计学意义。
生物质烟雾暴露慢性阻塞性肺疾病受试者诱导痰标本细菌载量与慢性阻塞性肺疾病(COPD)评估试验(CAT)评分的关系(n=20): a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌.采用夏皮罗-威尔克正态性检验。相关系数采用非参数Spearman相关分析计算。P <0.05为差异有统计学意义。
在S-COPD受试者中,总SGRQ和CAT评分与负荷之间存在显著正相关肺炎链球菌,流感嗜血杆菌和复活的,但不铜绿假单胞菌(p < 0.05) (补充图S19和S20).
MDMs的吞噬活性
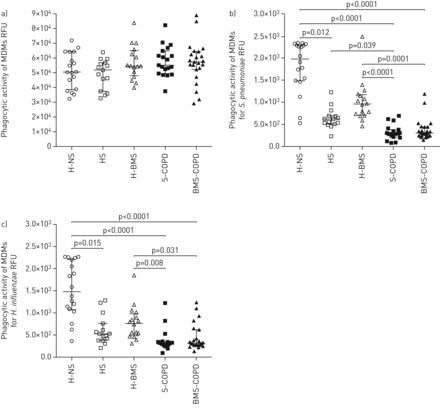
在确定COPD受试者气道细菌负荷增加后,我们检查了该缺陷是否与固有免疫反应降低(如吞噬功能降低)有关。我们观察到不同受试者组之间MDMs对惰性珠的吞噬功能没有差异(p>0.05)(图6),提示所有mdm均具有吞噬能力。我们还比较了男性(H-NS, HS, S-COPD)和女性(H-BMS和BMS-COPD)中MDMs的细菌吞噬活性;然而,我们没有观察到各PPB的MDM吞噬活性和总吞噬活性(珠的平均吞噬活性,肺炎链球菌和H.流感嗜血杆菌)男女受试者之间(p>0.05)(补充图S21).
单核细胞来源的巨噬细胞(MDMs)对荧光标记珠和细菌的吞噬:a)链球菌引起的肺炎, b)流感嗜血杆菌c)卡他莫拉菌和d)铜绿假单胞菌,健康非吸烟者(H-NS) (n=18)、无慢性阻塞性肺疾病(COPD) (HS) (n=15)、生物质烟雾(BMS)暴露健康受试者(H-BMS) (n=16)、烟草烟雾相关COPD受试者(S-COPD) (n=19)和BMS暴露COPD (BMS-COPD)受试者(n=23)。RFU:相对荧光单位。采用夏皮罗-威尔克正态性检验。数据显示为带有中位数(四分位范围)的点图。组内比较采用Kruskal-Wallis检验和Dunn多重比较检验。P <0.05为差异有统计学意义。
接下来,我们检测了这些mdm对荧光标记的热杀PPB (肺炎链球菌和流感嗜血杆菌)观察BMS-COPD和S-COPD受试者与H-NS受试者相比MDMs的吞噬功能受损(肺炎链球菌和流感嗜血杆菌: p < 0.0001) (图6 bc)此外,与H-BMS受试者相比,BMS-COPD受试者的MDMs显示出明显的细菌吞噬功能受损(肺炎链球菌:p=0.0001;流感嗜血杆菌: p = 0.031) (图6 b与HS受试者相比,S-COPD受试者的MDM表现出吞噬活性受损,但这种差异在统计学上并不显著(肺炎链球菌和流感嗜血杆菌: p > 0.05) (图6 b和c)。
此外,我们观察到H-NS受试者的MDMs与HS受试者相比,具有明显更高的PPB吞噬活性(肺炎链球菌: p = 0.012;流感嗜血杆菌: p=0.015),但与H-BMS受试者无统计学差异(肺炎链球菌和流感嗜血杆菌: p > 0.05) (图6 b和c).有趣的是,在不同部位的MDM吞噬活性无显著差异肺炎链球菌和流感嗜血杆菌COPD (BMS-COPD和S-COPD)和健康暴露(H-BMS和HS)受试者(p>0.05) (图6 b和c)。
MDMs吞噬细菌与诱导痰细菌载量的关系
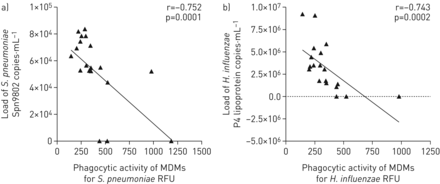
在确定先天免疫反应的缺陷后,我们想确定这是否与这些受试者气道中的PPB负荷有关。我们观察了来自bms暴露受试者(BMS-COPD和H-BMS)的MDMs的吞噬活性肺炎链球菌和流感嗜血杆菌与诱导痰细菌载量呈负相关(BMS-COPD:肺炎链球菌: r= -0.752, p=0.0001流感嗜血杆菌: r= -0.743, p=0.0002;H-BMS:肺炎链球菌: r =−0.699, p = 0.005流感嗜血杆菌:r= –0.556,p=0.034)(图7和补充图S23).同样,烟草烟雾暴露受试者(S-COPD和HS) MDMs的吞噬活性与增加的负荷呈负相关肺炎链球菌和流感嗜血杆菌诱导痰(补充图S24和S25).
生物量烟雾暴露的慢性阻塞性肺疾病(COPD)受试者(n=20)诱导痰样本中细菌负荷与单核细胞源性巨噬细胞(MDM)吞噬活性之间的关系:a)链球菌引起的肺炎及(二)流感嗜血杆菌.RFU:相对荧光单位。采用夏皮罗-威尔克正态性检验。相关系数采用Spearman相关分析计算。P <0.05为差异有统计学意义。
MDMs细菌吞噬功能与肺功能指标的关系
在显示了MDMs对PPB吞噬活性的差异及其与气道细菌负荷的关系后,我们想确定这些差异是否与肺功能参数的变化有关。我们观察到在BMS和烟草暴露的受试者中,MDM吞噬肺炎链球菌和H.流感嗜血杆菌与肺功能指数呈正相关(p<0.05)(补充图S26-S37).
MDMs细菌吞噬与人口统计学特征的关系
我们还研究了MDMs的细菌吞噬活性与人口统计学特征之间的关系。我们发现年龄与所有受试者的MDM吞噬活性无关(p>0.05) (补充表S5).BMS和烟草暴露史与MDM吞噬均呈显著正相关肺炎链球菌和流感嗜血杆菌(p < 0.05) (补充表S5).
MDMs的细菌吞噬功能与COPD患者生活质量的关系
我们研究了PPB的MDM吞噬活性与COPD受试者的生活质量之间的关系。对于BMS-COPD受试者,总CAT评分与MDM吞噬率之间存在显著负相关肺炎链球菌(r= -0.444, p=0.034)流感嗜血杆菌(r)= –0.416,p=0.048)(补充图S38).SGRQ总分与MDM吞噬率之间也存在类似的显著负相关肺炎链球菌(r= -0.453, p=0.029流感嗜血杆菌(r = 0.579, p = 0.007) (补充图S40).
S-COPD受试者也观察到类似的关系,总CAT和SGRQ得分与MDMs的吞噬活性呈显著负相关肺炎链球菌和流感嗜血杆菌(补充图S39和S41).
活力测定
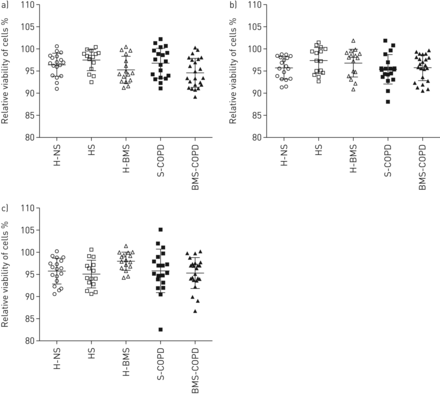
观察到的吞噬反应降低可能是由于细菌诱导的细胞死亡。为了研究这一点,采用MTT法测定细胞活力。在整个实验条件下,MDMs的活力为≥所有样品均为90%(图8).
荧光标记珠和细菌对单核细胞源性巨噬细胞(MDM)活力的影响:a)荧光标记珠,b)链球菌引起的肺炎和c)流感嗜血杆菌,健康非吸烟者(H-NS) (n=18)、无慢性阻塞性肺疾病(COPD) (HS) (n=15)、生物质烟雾(BMS)暴露健康受试者(H-BMS) (n=16)、烟草烟雾相关COPD受试者(S-COPD) (n=19)和BMS暴露COPD (BMS-COPD)受试者(n=23)。采用夏皮罗-威尔克正态性检验。数据显示为带有中位数(四分位范围)的点图。采用普通单因素方差分析,然后采用Tukey多重比较检验。P <0.05为差异有统计学意义。
讨论
巨噬细胞是防止PPB入侵的关键保护性天然免疫细胞。S-COPD受试者PPB负荷增加(如。肺炎链球菌,流感嗜血杆菌,复活的和铜绿假单胞菌),这可能会导致呼吸道反复感染[7.,9,11]。研究发现,S-COPD受试者呼吸道中这些PPB的负担与肺功能指标的下降和肺泡巨噬细胞清除PPB的障碍有关,这也反映在MDMs的反应中[14,15,17,22]在这项研究中,我们还观察到来自印度农村人口的S-COPD受试者的呼吸道中存在类似的PPB,这与MDMs的吞噬活性缺陷和肺功能指数下降有关。
BMS被认为是全球范围内COPD的更大风险因素,而不是烟草烟雾,因为接触BMS的人数太多[5.]。长期暴露于BMS可能与在S-COPD受试者中观察到的先天免疫缺陷相似。我们在此首次报道了在BMS-COPD受试者中,PPB在呼吸道定植与mdm的吞噬活性缺陷和肺功能下降的类似关联。
我们发现肺炎链球菌和流感嗜血杆菌BMS-COPD受试者和S-COPD受试者的痰中MDMs含量相似。因此,研究了BMS-COPD受试者的MDMs吞噬活性,并与健康对照组(H-NS、HS和H-BMS)进行了比较与S-COPD受试者相比,BMS-COPD受试者的MDM吞噬活性没有显著改变,但与健康对照组相比显著降低。这表明与先天免疫反应缺陷相关的类似机制可能适用于BMS-COPD和S-COPD受试者。毫无疑问BMS增加肺泡巨噬细胞的特定摄取,这可能导致吞噬功能缺陷[34–36]。然而,我们报道了未暴露于这些颗粒物的mdm的吞噬作用减少,并提示循环细胞中存在一种固有的共同缺陷机制。
先前的动物和人体研究报告指出,吸入的有毒污染物从肺部转移到体循环[37,表明肺和体循环之间有直接联系。暴露于烟雾中的有毒污染物可能会导致肺部过度炎症反应,从肺腔溢出,并导致全身炎症[38].据报道,肺泡巨噬细胞中Nrf2(核因子红系2相关因子2)信号的降低与COPD受试者这些细胞的吞噬活性和细菌清除率的改变有关,并且Nrf2激活剂萝卜硫素改善了这种反应[39,40].需要进一步的研究来探索Nrf2信号机制和BMS成分在天然免疫细胞吞噬活性中的作用。
在西方人群,复活的在S-COPD受试者的痰标本中发现,持续时间较短,被认为是加重的主要因素之一[41]。铜绿假单胞菌在一些稳定的S-COPD受试者中也有报道,并与疾病严重程度相关[41]。在我们的研究中,没有S-COPD受试者在病情加重期间取样,但仍定殖复活的有趣的是,我们观察到BMS-COPD和H-BMS受试者有更多的铜绿假单胞菌,而S-COPD和HS患者则更容易感染复活的. 如前所述,暴露于BMS有助于改变细菌群落[42]。在我们的研究中,我们还观察到PPB在气道的定植增加和MDM吞噬活性受损恶化了BMS-COPD受试者的生活质量(SGRQ和CAT评分)。需要进一步的研究来了解与之相关的潜在机制铜绿假单胞菌和M.莫拉菌巨噬细胞的集落和吞噬活性。
我们的研究有一些局限性。首先,本研究涉及鉴定诱导痰样本中的致病菌。采集样本后,诱导样本可能被上呼吸道或口腔微生物菌群污染。然而,有证据表明诱导痰是最敏感的诊断感染性阻塞性气道疾病的定性和定量方法[43]。第二,我们的研究有性别偏见,即。H-NS、HS和S-COPD受试者均为男性,而H-BMS和BMS-COPD受试者均为女性。然而,我们没有观察到男性和女性受试者在MDMs的PPB负荷和吞噬活性上的任何差异。性别不太可能直接影响巨噬细胞的吞噬活性、发展为COPD的风险和PPB的定植。这是一个真实的场景,印度女性主要参与烹饪和接触BMS。我们确实试图通过修正性别的肺活量指数和使用百分比预测值进行分析来尽量减少这种偏差。此外,我们没有观察到西方慢性阻塞性肺病患者的吞噬活性的任何性别差异(补充图S22).此外,先前的研究报告指出复活的呼吸道感染与性无关[44]。第三,为了评估mdm的吞噬活性,我们使用了非调理蛋白肺炎链球菌和流感嗜血杆菌这表明在本研究中,调理MDMs受体的活性受到限制。COPD患者肺泡巨噬细胞和MDMs中调理细菌的吞噬功能也受到损害[40]。在肺中,调理作用驱动吞噬作用是有限的,因为它不被认为是一个富含血清的环境。然而,表面活性剂蛋白和其他肺源性免疫球蛋白的调理作用是可能的。
总之,我们首次表明,非吸烟COPD患者与S-COPD患者相似,因为他们的气道中含有PPB,这与巨噬细胞吞噬功能缺陷有关。巨噬细胞的这种缺陷可能与接触有害气体的人更易产生气流有关障碍,这是烟草烟雾或BMS暴露的常见易感因素。
补充材料
确认
我们要感谢参与本研究的患者。我们要感谢Meena Raykar和Savita Walke(印度浦那KEM医院研究中心Vadu农村健康项目)对患者招募的支持。
脚注
这篇文章的补充材料可从www.qdcxjkg.com
作者贡献:J.D. london参与了CRF-COPD队列患者招募。CRF-COPD队列建立由S. Juvekar和S.S. Salvi监督。V.V. Das对招募的受试者进行了肺功能测试。B. Brashier建立了对受试者的诊断。B. Ghosh和A.H. Gaike在Shouche Y.S.的监督下进行了qPCR和细菌培养检测。K. Pyasi参与了对招募受试者的痰和血液样本的采集。K. Pyasi也对诱导的痰标本进行了差异细胞计数。由L.E. Donnelly培养B. Ghosh生成mdm并进行吞噬活性测定。B. Ghosh和K. Pyasi进行吞噬实验。B. Ghosh进行了统计分析,并在S.S. Salvi的监督下撰写了手稿。 P.J. Barnes and S.S. Salvi were the principal investigators of this study and conceived the idea for the study.
利益冲突:B.高希没有什么可披露的。
利益冲突:A.H.Gaike无需披露任何信息。
利益冲突:K.Pyasi无需披露任何信息。
利益冲突:B. Brashier没有什么可披露的。
利益冲突:达斯没有什么可披露的。
利益冲突:J.D. london没有什么可披露的。
利益冲突:S.尤文卡尔没有什么要披露的。
利益冲突:Y.S.Shouche无需披露任何信息。
利益冲突:L.E. Donnelly报告了Cempra、阿斯利康和勃林格殷格翰在提交工作之外的拨款。
利益冲突:S.S. Salvi没什么可透露的。
利益冲突:P.J.巴恩斯没有什么要披露的。
支持声明:该研究由印度医学研究理事会(印度)和英国医学研究理事会(英国)资助。本文的资金信息已存入Crossref资助者注册表.
- 收到2017年的11月2日。
- 认可的2018年11月20日。
- 版权所有©2019