抽象
我们研究了环境空气污染是否与肺间质病变(ILAs)和高衰减区(HAAs)相关,这是亚临床肺间质病变(ILD)在CT上的定性和定量测量。
我们进行录取动脉粥样硬化(MESA)研究的多种族研究在社区居民的分析。我们使用特定人群的时空模型来评估环境的污染(细颗粒物(PM2.5),氮氧化物(NOX)、二氧化氮(不是2)和臭氧(O3))在每个家庭。共有5495名参加者接受卤乙酸心脏CT的串行评估;2671名参与者进行了评估使用全肺CT在10年的随访ILAS。我们用多变量回归,并调整了年龄,性别,种族,教育,烟草使用,扫描技术和研究地点线性混合模型。
在NO . 1中,每40个ppb增加ILAs的几率增加1.77倍X(95% CI 1.06 ~ 2.95, p = 0.03)。总的趋势是,更多地接触NOX和更大的哈斯进展(0.45%的年增长率哈斯每40 ppb增量在NOX;9五% CI −0.02 to 0.92, p = 0.06). Associations of ambient fine particulate matter (PM2.5),没有X和不2不同种族/民族(p = 0.002, 0.007, 0.04,分别为交互作用)和非西班牙裔白人中浓度与HAAs进展的差异最大。
我们的结论是环境空气污染暴露用亚临床ILD相关。
抽象
暴露于环境空气污染与亚临床固体辐射的定性和定量测量有关http://ow.ly/5OfU30gt2q7
介绍
空气污染是导致不良呼吸结果的危险因素。许多研究表明,污染暴露与包括哮喘在内的多种肺部疾病的发病率和/或进展之间存在关联[1]、慢性阻塞性肺病(COPD) [2],支气管扩张[3]、呼吸道感染[4],慢性肺同种异体移植功能障碍[五]和肺癌[6]。一直存在对空气污染有助于病因或是否加速间质性肺疾病(的ILD),慢性肺疾病,其特征在于影响的200个老年人近出肺实质的炎症和纤维化的一组异质的进展的研究很少在美国 [7]。
ILD通常是不可逆的诊断肝纤维化实质在发病后。早期症状是非特异性的,经常归因于其他慢性肺或心脏疾病。由于临床表现的后期表现,并推测长期潜伏暴露与疾病发展之间,很多的ILD的潜在病因是未知的。
人们日益认识和对计算机断层扫描ILD的隐性形式的识别(CT)提供了前期调查的原因,而不是后果,ILD的一个独特的机会。间质性肺异常(ILAS),在肺的非依赖部分早期间质性改变视觉评估,是亚临床ILD的充分验证的定性测定[8]。亚临床固体的定量CT衰减表型,称为高衰减区(HAAs),也被证明是亚临床肺炎症和纤维化的一个标志[9-11]。
纵向研究估计,参与者ILAS的20-46%有进行成像异常,用约4%的显影普通型间质性肺炎(UIP)的特征[12]。即使在没有临床ILD的情况下,患有亚临床ILD的人群也会出现更多的呼吸系统症状、生理功能下降和更高的死亡率[10,13,14]。
吸入性接触石棉背后,过敏性肺炎和吸烟相关的间质性肺病的病理生物学。环境空气中的污染物可以发起或促进肺泡损伤,修复紊乱和纤维化的间质性肺病看到的周期,并已与间质纤维化患者的临床病情加重有关[15]。空气污染物,包括细和超细颗粒和交通有关的气体,可以在整个气道和肺泡沉积,造成的直接损伤或触发炎症和氧化应激。这可能潜在地导致肺泡细胞损伤或衰老,内皮功能障碍,单核细胞间质性炎症和成纤维细胞增殖。
空气污染物和ILD之间的关联并没有在人群研究先前调查。我们假设暴露于空气污染将与在社区居住的成年人亚临床ILD的定性和定量测量相关。
方法
研究设计和参与者
动脉粥样硬化的多种族研究(MESA)是由美国国家心肺血液研究所资助研究亚临床心血管疾病的前瞻性队列研究。MESA和辅助研究,MESA肺和MESA空气,在深度别处被描述,并作为采样帧用于该研究[10,16]。所有参与者获得知情同意和研究的合作中心批准了机构审查委员会。
简单地说,MESA招收6814人参加,来自各地的美国六大中心年龄45-84岁:巴尔的摩,MD;芝加哥,IL;洛杉矶县,加州;纽约市,NY;圣保罗,明尼苏达;和温斯顿塞勒姆,NC。与会者通过2002年至2000年间招募,并接受有关人口统计,家族史,病史和生活习惯的问卷。2005年至2007年,梅萨航空招募从罗克兰县,NY,河滨县,CA和洛杉矶郡,洛杉矶额外的257人参加。通过研究设计,所有参加者提供免费学习的一开始就知道心血管疾病;有基于肺病,呼吸道症状或吸烟史没有选择标准。 At enrolment and during the four subsequent examinations, participants had noninvasive assessment of cardiovascular status including cardiac CT scans, which image approximately 70% of the lung volume from main carina to lung. By design, all returning participants had a repeat cardiac CT scan at either examination 2 or 3, and 30% of the cohort had a third cardiac CT scan at examination 4. An additional subset of 3200 participants underwent cardiac CT scan again at examination 5, during years 2010–12, nearly all of whom had a full lung CT scan at this time.
补充资料中详细描述了我们研究中纳入的参与者的抽样方案。
肺间质异常
2010-12年(10年随访)采用MESA lung /SPIROMICS方案,悬吊全吸气时获得全肺MESA CT扫描,并使用0.625 mm片厚重建图像[17]。五名获得委员会认证的放射科医师之一(interreader kappa 0.47[0.14-0.80])对ILAs进行了全肺CT扫描,其中任何扫描被定义为“明确的”ILD或“可疑的”ILAs。“明确的”单侧肺纤维化被定义为多个肺叶的双侧纤维化,伴蜂窝状和牵引性支气管扩张在胸膜下的分布。当至少5%的肺非依赖性部分存在毛玻璃、网状异常、弥漫性小叶中心结节、蜂窝状、牵引性支气管扩张、非肺气肿性囊肿或建筑变形时,扫描被解读为ILAs“可疑”[18]。只有不到5%的肺部出现单独异常的扫描被解读为ILAs的“可疑”,并被纳入没有ILAs的那组参与者。在敏感性分析中,这些“模棱两可的”扫描被排除在外,正如之前所描述的那样[10]。
高衰减区
杂环胺上测量在MESA基线就诊进行非增强心脏CT扫描和选择的随访使用高度标准化协议[考试19]。先前一项使用MESA全肺扫描的验证研究表明,心脏CT扫描图像约占总肺容积的65-70%,包括大部分下叶,但排除了大部分肺前壁。定量图像衰减由训练有素的读者使用爱荷华大学成像实验室(美国爱荷华州艾奥瓦市)改进版的肺分析软件进行测量(类内相关系数0.93)[9]。HAA被定义为在- 600和- 250 Hounsfield单位(HU)之间衰减值的成像肺容积的百分比[9,10]。CT肺衰减的这一范围包括磨玻璃和网状异常,和更密集如肺不张,中,大血管和肺结节区域排除。肺气肿的百分比定义为低于-950 HU体素的百分比。
暴露评估
环境空气污染暴露估计使用基于土地利用回归和地质统计平滑住宅的历史数据(从一九八〇年至2012年报告)和时空预测模型的每个参与者。这些验证的模型进行了详细的别处所描述的[20,21]。
简而言之,在2005年至2009年期间,在27个长期地点、771个社区快照和697个参与家庭以外的地方测量了污染物。MESA Air利用这些测量数据来补充EPA空气质量系统监测地点的污染监测,发展了结合地理信息和空间平滑的社区特定时空模型。这些模型预测了从1999年到2012年每两周的住宅污染物浓度,并解释了90-97%的参与者住宅测量值的变化。
由于曝光有助于ILAS发展的一个长期的预期,我们估计使用前全肺CT扫描2周,居住,具体的预测的10年平均水平的长期环境的污染的曝光。为灵敏度的分析,我们还估计5-,20-和30年的曝光之前,全肺CT扫描。在20 - 30年的风险是仅适用于细颗粒物(PM2.5;粒子切断空气动力学直径2.5μm 50%)和模型是基于历史的年度平均接触发达时期可以密集点监控(22]。这些长期的住宅估算使用了每年平均的地址加权平均值2.5浓度。
为了模拟哈斯进展,我们预计长期暴露为平均2周住宅特有的预测从招聘到跟进。2000年,在浓度在招募参与者的地址被用来模拟基线横截面的关系。
统计分析
一个ll statistical tests were performed in SAS version 9.3 (SAS Institute, Cary, NC, USA) using a two-tailed α = 0.05 to define statistical significance.
我们使用多变量逻辑回归来检验在5次检查中,预测的10年污染物暴露与全肺CT扫描的ILAs发生率之间的关系。模型根据年龄、性别、种族、烟草使用(当前吸烟情况和包装年份)和地点进行了调整。敏感性亚分析进行了额外的调整,职业暴露,一个明确的风险因素的ILD。职业暴露是根据先前开发和应用的工作暴露矩阵(JEM)来定义的,该矩阵量化了对蒸汽、气体、灰尘和烟雾的暴露,但并不是对所有参与者都适用[23]。通过平均使用较长的曝光时间进行了敏感性分析20-和30年的PM的估计2.5从历史模型污染估计时,可用。其他研究表明,亚临床的影响是根据吸烟情况、种族和性别而不同的,所以,先天的,我们决定测试这些变量对效果的影响[9,11]。凡分层模型显示协会的不同幅度,我们还测试效果修改规定的污染物暴露和潜在影响改性剂之间的乘法互动。我们使用嵌套的主要作用和乘数模型试验统计学显着性之间的似然比检验。
线性混合模型,用于分析空气污染和卤之间的横截面的关联在基线检查和空气污染和卤的进展速度之间。杂环胺是日志中的模式转变,并返回转化,得到的百分比变化的估计。重复测量被模拟为的研究时间的函数,以模拟为相互作用随时间以检查污染物曝光并随时间卤乙酸的变化线性速率之间的关联时变曝光。参加特定的随机拦截和斜坡都包括在内。模特们调整了年龄,性别,种族/民族,受教育程度,JEM,身高,身体质量指数(BMI),腰围,吸烟,香烟包年,肾小球滤过率,像肺的总体积,肺气肿的百分比CT扫描,CT扫描仪类型和研究基地。潜在影响的修改是对吸烟状态,性别和种族研究了分层。
结果
共有6813名MESA与会者与有效HAA测量基线心脏CT扫描。其中,5965名参与者在研究期间至少有一个后续的心脏CT扫描。这些参与者470中缺少任一协变量信息或污染物的估计,留下被列入HAA进展的纵向分析,认为5495名参与者(见补充图S1)。每名参与者心脏CT扫描的平均数目为2.4。Ťhe mean follow-up time among the participants with at least two cardiac CT scans was 5.9 years, with a range of 0.9 to 11.4 years.
共有3137名MESA参与者,包括一些在MESA Air下招募的参与者,在MESA检查中接受了由放射科医生评估的全肺CT扫描。其中128个没有被ILAs读取,34个扫描无法读取。总共有246名参与者缺少10年的污染物估计数,58名参与者缺少其他协变量,在我们对ILAs的最终分析中,有2671名参与者进行了全肺CT扫描(见补充图S2)。在敏感性分析中,491例被认为是ILAs可疑的全肺CT扫描被排除在队列之外。
ILA和HAA分析(表格1)。Ťhe mean age of the full cohort at baseline was 62 years (SD10年)和3214(47%)是男性。基于研究设计的种族/民族差异:2621名(39%)参与者是白人,1893名(28%)参与者是非洲裔美国人,1496名(22%)参与者是西班牙裔美国人,803名(11%)参与者是华裔美国人。共有3085人(45%)从未吸烟,967人(14%)目前正在吸烟。
研究期间的平均空气污染浓度有所下降,详情载于其他资料[16]。平均污染浓度也因地点而异,其中颗粒物浓度最高2.5在洛杉矶和最高水平的硝酸盐(氮氧化物)X]和二氧化氮[NO2])在纽约市。污染物水平与臭氧除外相关(O3),与其他污染物呈负相关(见补充表S1、S2)。
污染物与肺间质异常的关系
在3137名与会者谁接受全肺CT扫描了ILAS的310(9.9%):289(9.2%)有扫描读作可疑ILD和21(0.67%)出现了符合标准的标准,相关的双边纤维化UIP模式扫描结果与在胸膜下分布蜂窝影和牵拉性支气管扩张。
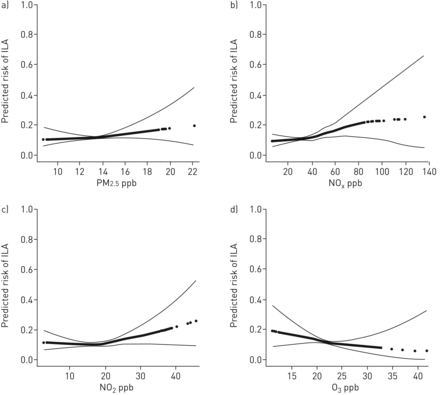
In multivariable-adjusted analyses, the odds of ILAs increased 1.77-fold per 40 ppb increment in NOX(95% CI 1.06 ~ 2.95, p = 0.03)。虽然ILAS不与环境相关的PM2.5,NO2啊,或者3浓度(表2;图1), there was modest evidence of effect modification by smoking status (values for interaction of p = 0.03 for O3,下午0。08分2.5,0.19 NOX和0.28 NO2),具有较少暴露至O3和更大的暴露于NOX和不2,每个与不吸烟者之间的ILAS可能性增加(相关表2)。例如,在各NO 40-ppb的增量X(95% CI 1.35 ~ 6.16, p = 0.006),而O3was associated with an odds ratio for ILAs of 0.30 (95% CI 0.10 to 0.93, p = 0.04;表2)从不吸烟者。
预测间质性肺异常(ILAs)的风险与污染物水平的增加。一)粒子切断空气动力学直径2.5μm(50%点2.5;细颗粒物)中,b)氮氧化物(NOX),C)二氧化氮(NO2)和d)的臭氧(O3)。效果估计来自一般的可加性模型,用点表示总体效果估计,用线表示95%置信区间。所有模型都根据年龄、性别、种族/民族、烟草使用(包年、吸烟情况)和研究地点进行了调整。
敏感性分析显示,1)排除了患有“模棱两可的ILA”(见补充表S4)的参与者,或2)对职业暴露进行了额外的调整(见补充表S5),导致了类似的结果。对5年、20年和30年污染物估计数的敏感性分析也得到了类似的定性结果(见补充表S6和S7)。
与高衰减区域相关
在招募时,MESA参加者的平均HAA为5.1% (SD(3.1%),占1.4%至46.6%。在研究期间,HAAs平均每年减少0.35% (95% CI 0.21 - 0.48%)。
在对潜在混杂因素进行调整后的初步分析中(表3),有朝HAA进展与NO趋势X:a 40 ppb higher NOXconcentration was associated with a 0.45% (95% CI −0.02% to 0.92%, p = 0.06) increase in HAAs per year. Effect estimates for NO2和PM2.5浓度在相似方向。
种族/修改后用于PM卤乙酸的污染物暴露和进展之间的关联2.5,NOX和不2(values for interaction p = 0.002, 0.007, and 0.04, respectively;表3)。对于每一种污染物,这种关联在非西班牙裔白人中最强。例如,一个5µg·m-3增量PM2.5浓度与非西班牙裔白人每年增加0.93% (95% CI 0.26 - 1.61%, p = 0.007)的HAAs和黑人每年增加0.45% (95% CI - 0.70% - 1.63%, p = 0.44)的HAAs有关。2000年的污染估计数字与2000 - 2002年的HAA统计数字之间没有一致的横断面联系(补充表S3)。
讨论
我们发现,暴露于环境氮氧化物与较高的ILAs患病率有关,而在非西班牙裔白人中,暴露于PM2.5,NOX, 和不2与哈斯氏病的进展相关,平均随访时间为5.9年。虽然一致性较差,但大O之间存在反向关联的趋势3浓度和亚临床ILD。这是第一次研究,以链接的空气污染,在社区居住的成年人肺部炎症和纤维化的CT的早期证据,将洞察假说,空气污染可能有助于ILD。
我们发现NO的相关性最强,且最一致X,主要是一氧化氮(NO)和一氧化氮(NO)的混合物2。这些结果与那些的Johannson等。[15]在对空气污染对ILD的影响的唯一现有研究。在436例特发性肺间质纤维化从韩国首尔(IPF)的纵向研究中,作者发现,更高水平的NO2over the previous 6 weeks were associated with increased risk of an IPF exacerbation. Epidemiologic studies have also established the importance of nitrate exposure with other respiratory conditions, including reduced lung function [24],哮喘[25慢性阻塞性肺病[26]。
没有X在临近道路的环境中,空气污染水平最高,这可能是一系列与交通相关的空气污染物(TRAP)的替代物,包括多芳碳、超细颗粒和其他化石燃料燃烧的产物。相比之下,阿3往往是在不久的道路环境下,由于两至O3通过流量产生的NO和因为ö清除3是一种二次污染物,这是光化学在对流层中通过太阳光的挥发性化合物的反应产生的[27]。这种负相关可能是负责对逆效应的趋势,我们有更高水平的O看到3。
在吸入,不X和TRAP结合与氨和其它小颗粒,以支气管树内深入渗透。虽然在整个呼吸道一些吸收,损伤的原发部位是在其中颗粒可通过气道巨噬细胞phagocytised终末细支气管,肺激活纤维nocioceptive或原因直接上皮损伤[28]。活性氧的生成介导的,这会导致气道,并与正在进行的细胞因子和趋化因子释放全身性炎症。小鼠模型已经表明,硝酸盐暴露引起的细胞损伤,上皮增生,增生,炎症和纤维化改变[29]。在遗传易感人群中,这可能启动或促进肺泡损伤、紊乱修复和ILDs中所见的纤维化的循环。
在这项研究中,种族修改接触污染的影响,在非西班牙裔白人的HAA进展的作用最强。从现有空气污染研究结果已经混合,以研究显示不同民族和种族群体小,更大或类似的效果大小[三十]。我们的研究结果可能表明,从不可测量的医疗差距等混杂因素的不利影响可能会淹没环境空气污染暴露的不良后果。类似的现象可驱动的差动作用的建议,即我们与吸烟状况,其中,所述关联可以在不吸烟者是最大[观察31]。可替换地,也有通过族群ILD的某些亚型,其可以占我们观察到空气污染的不同影响的发生率显著差异。
这是一项观察性研究,存在固有的暴露和结果错误分类、残留混杂和无法推断因果关系的局限性。我们对亚临床的定义是基于放射学上的发现而不是组织学上的改变。我们对肺密度的定量测量可能包括其他肺过程,如水肿、感染或肺不张。然而,正如我们之前对这一人群的研究所述,没有证据表明心功能、肥胖或肺部成像百分比会造成混淆[10]。此外,研究期间扫描技术的变化可能会带来分析中难以控制的混杂。
虽然我们的模型调整为各种混杂因素,有可能是残余混杂从不可测的变量,如其他环境因素(例如模具,禽类抗原等)。
虽然我们的暴露评估预测了参与者住所的环境污染物浓度,但它们可能不能准确反映参与者微环境中的污染物暴露。一个人体内的污染剂量可能因多种变量的不同而有很大差异,如户外活动时间、爱好、体育活动、通勤和度假。
从历史模型中得出的颗粒物暴露(20年和30年)的长期估计可能不如我们的其他污染物估计准确,我们的其他污染物估计没有从有限的数据中推断出时间周期,也受益于空间密集的空气污染监测数据。这种非差异暴露误分类将削弱与ILAs和HAAs的关联强度。
尽管有这些限制,我们观察到的效应表示在无症状社区居住的美国成年人的肺重要亚临床变化。我们采用先进的建模产生长期暴露于空气污染的个人估计,并研究了不同暴露时间滞后的影响。通过调整网站,我们能够消除对污染物水平城市变化中的城市和重点之间不可测量的干扰因素。
总之,我们发现,ILA用长期平均暴露于氮氧化物相关联;和在非西班牙裔白人,HAA进展用暴露于氮,二氧化氮和细颗粒的两种氧化物相关联。将需要更多的流行病学和翻译研究,以调查个别污染物的作用和识别潜在的生物途径这些关联底层。虽然确切的证据,至今下落不明,这项研究提供了证据,空气污染可能是ILD的潜在危险因素。如果证实,这将有病人重要的临床意义,并有助于帮助通知公共政策。
补充材料
披露
补充材料
R.G.巴尔ERJ-00559-2017_Barr
A. Gassetterj - 00559 - 2017 - _gassett
K.欣克利-StukovskyERJ-00559-2017_Hinckley_Stukovsky
E.A.霍夫曼ERJ-00559-2017_Hoffman
美国Kawuterj - 00559 - 2017 - _kawut
D.J.莱德勒ERJ-00559-2017_Lederer
l·谢泼德erj - 00559 - 2017 - _sheppard
S. VedalERJ-00559-2017_Vedal
致谢
作者感谢其他研究人员,工作人员和MESA研究作出的宝贵贡献的参与者。参与调查MESA和机构的名单,可以发现www.mesa-nhlbi.org。该编码的职业信息是由美国国家职业安全与健康(NORA 08年CRN SLB8)进行。
所有作者作出了重大贡献的手稿和采集,分析和解释数据的构思和设计。所有作者协助起草的手稿或重要修订工作的重要知识内容。所有作者认可了最终版本提交。
脚注
这篇文章有补充资料www.qdcxjkg.com
支持声明:N01-HC-95159,N01-HC-95160,N01-HC-95161,N01:MESA和工作在这个手稿是由美国国家心脏,肺和血液研究所(NHLBI)通过下面的资金和合同支持-HC-95162,N01-HC-95163,N01-HC-95164,N01-HC-95165,N01-HC-95166,N01-HC-95167,N01-HC-95168,N01-HC-95169,T32HL007287;通过UL1-TR-000040的国家研究资源中心(NCRR),UL1-TR-001079,R01 HL103676,R01 HL077612,R01 HL093081,RC1 HL100543和K24 HL131937;和环境健康科学研究所通过P50ES015915,P30ES07033,P30ES007033和K24ES013195。这项研究也已经由美国环境保护署(EPA的)科学的资助,以取得成果(STAR)计划和出版物的编写下的援助协议RD831697荣获由EPA华盛顿大学(华盛顿州,美国)。这项工作也得到了肺纤维化基金会和罗科Guinta研究基金资助。本文资金的信息已交存交叉引用出资者注册。资金来源的作用:这项研究是由一个指导委员会和一个外部科学咨询委员会(ESAC)监督。该NHLBI,美国国家职业安全和健康研究所(NIOSH),EPA,NCRR,罗科Guinta基金和肺纤维化基金会曾在收集,分析没有任何作用,或解释数据,报告的写作,或决定提交论文发表。所有作者都提供了对数据的完全访问权的决定提交稿件的所有作者共同负责。
免责声明:本报告未经美国环境保护署(EPA)正式审核。本报告中的发现和结论是作者的观点,不一定代表美国环保署或NIOSH的观点。EPA和NIOSH不认可本出版物中提到的任何产品或商业服务。
利益冲突:披露可以这篇文章在旁边找到www.qdcxjkg.com
- 收到了2017年3月17日。
- 公认2017年9月1日。
- 这项工作的内容是不是受版权保护。设计和品牌的版权©ERS 2017年。