抽象
肺动脉高压的比例(PAH)患者不与磷酸二酯酶5抑制剂(PDE5i)达到治疗的目的。喘息调查的安全性,可行性和交换的受益PDE5i到riociguat在这些患者。
休养生息是一个为期24周的开放标签,多中心,非对照研究。耐心in World Health Organization (WHO) functional class (FC) III, with 6-min walking distance (6MWD) 165–440 m, cardiac index <3.0 L·min−1·米−2and pulmonary vascular resistance >400 dyn·s·cm−5underwent a 1–3 day PDE5i treatment-free period before receiving riociguat adjusted up to 2.5 mg maximumt.i.d。探索终点包括在6MWD,WHO FC变化,N脑利钠肽(NT-proBNP水平)和安全性的末端激素原。
的61名患者,51(84%)完成的喘息。50(82%)接受伴随的内皮素受体拮抗剂。在第24周,平均±SD6米WDhad increased by 31±63 m, NT-proBNP decreased by 347±1235 pg·mL−1和WHO FC在28名患者(54%)的改善。32名患者(52%)有经验的研究药物相关的不良事件和10(16%)经历了严重不良事件(2(3%)研究药物相关的,在PDE5i无治疗期间无)。六例(10%)出现临床恶化,包括两个死亡(不与研究药物相关的)。
综上所述,部分多环芳烃患者可从PDE5i转至riociguat获益,但这一策略需要进一步研究。
抽象
切换到riociguat肺动脉高压患者的响应PDE5i改善运动能力和NT-proBNP水平不足http://ow.ly/e6xL30dXCgy
介绍
肺动脉高压(PAH)的特征在于angioproliferative肺血管病变主要影响在肺血管床的渐进闭塞的前毛细血管和小动脉的结果[1]。因此,右心室的负荷逐渐增加,如不及时治疗,最终导致右心衰死亡[2]。
PAH是一种不治之症,但一些治疗方法已被开发出改善症状和预后[3.,4]。对PAH患者目前的治疗目标是根据2015年欧洲心脏病学会(ESC)/欧洲呼吸学会(ERS)治疗指南[实现了低风险状态188bet官网地址3.]。PAH治疗可以启动作为单一疗法或作为联合治疗的药物靶向不同途径[4]。
对于PAH目标三种途径当代治疗:前列环素途径中,内皮素途径和一氧化氮(NO)可溶鸟苷酸环化酶(sGC的) - 环鸟苷酸(cGMP)途径[3.,5]。三种药物靶向NO-SGC-cGMP途径被批准用于PAH的治疗:2磷酸二酯酶-5抑制剂(PDE5i),西地那非和他达拉非;和sGC刺激剂,riociguat [6- - - - - -8]。从全球的角度来看,PDE5i是PAH最常使用的治疗方法,无论是作为单一疗法或组合疗法,特别是内皮素受体拮抗剂(ERAS)9- - - - - -14]。Riociguat并且以相同的途径PDE5i目标不同的分子靶标,并用PDE5i riociguat的联合给药是禁忌。这主要是基于开放延伸专利-PLUS研究,揭示了副作用,最重要的全身性低血压,在长期的风险增加,并没有积极的效益/风险比的证据[15- - - - - -18]。
临床资料表明,接受PDE5i的患者相当大比例没有达到治疗的目的。例如,在AMBITION研究中,患者的PAH接收他达拉非单一疗法73%,并与安立生坦组合那些接收的他达拉非的61%没有达到在第24周研究的令人满意的临床响应[19]。Furthermore, in the SERAPHIN study, event-free survival of patients receiving PDE5i monotherapy was approximately 50% at 3 years [20]。
对于病人没有到PDE5i持续应答,就切换到sGC刺激生物学原理。在健康受试者中,cGMP产生在肺血管平滑肌细胞(PVSMCs)从由NO的sGC的活化产生来自相邻内皮细胞释放21]。在肺循环的cGMP磷酸二酯酶-5(PDE5)介导的降解。抑制细胞内cGMP水平PDE5活性增加在受损NO信号传导的情况下,导致PVSMC增殖的血管舒张和抑制[22]。然而,在多环芳烃患者中,有证据表明生物利用度没有降低。在疾病进展过程中,内皮功能下降,导致无耗竭和细胞内cGMP浓度降低,可能导致PDE5i无效[21,23- - - - - -26]。Riociguat直接刺激sGC的,在NO [存在或不存在下细胞内cGMP增加27,28]。基于这种作用方式,riociguat可以用响应PDE5i不足患者受益。
在患者研究了治疗不足响应于PDE5抑制剂(喘息)的研究[所述Riociguat临床效果29]旨在探讨是否是安全的,可行的和有益的PAH患者谁也PDE5i的反应不足与riociguat更换PDE5i。
方法
学习规划
休养生息是一个为期24周的前瞻性,探索性,开放性,多中心的,不受控制的,单臂研究,包括来自九个国家在欧洲和北美(例ClinicalTrials.gov识别码NCT02007629)三十]。
耐心
年龄在18-75岁的有多环芳烃症状(包括特发性多环芳烃、遗传性多环芳烃、药物和毒性多环芳烃以及与先天性心脏病相关的多环芳烃)的男性和女性(包括特发性多环芳烃、遗传性多环芳烃、药物和毒性多环芳烃),对他达拉非(40毫克每日一次)或西地那非(至少20毫克每日三次)的稳定治疗反应不足(t.i.d。), maximum 80 mg每日三次) for ≥90 days were included. Patients were permitted to continue background therapy with ERAs if they had been receiving stable treatement for ≥90 days. Final inclusion criteria were: World Health Organization functional class (WHO FC) III, 6-min walking distance (6MWD) 165–440 m, cardiac index <3.0 L·min−1·米−2,mean pulmonary artery pressure (mPAP) >30 mmHg, pulmonary artery wedge pressure ≤15 mmHg and pulmonary vascular resistance (PVR) >400 dyn·s·cm−5。前30例患者采用较窄的血流动力学纳入标准(心脏指数<2.5 L·min)−1·米−2and PVR >480 dyn·s·cm−5),只是后来为了提高试验的可行性修正。排除标准在补充材料进行说明。
每个参与中心机构审查委员会批准的协议。这项研究是根据良好的临床实践指南和赫尔辛基宣言进行。所有患者签署知情同意书。
研究程序
有一个14天的筛选期,同时患者仍在接收PDE5i,在此期间获得基线测量。PDE5i were stopped 1–3 days before the first dose of riociguat to allow a PDE5i treatment-free period of 24 h for patients receiving sildenafil and 72 h for patients receiving tadalafil (figure S1) [15,16]。接收电子逆向拍卖患者继续他们的常规剂量,并且还继续等支持措施。Riociguat was started at a daily dose of 1.0 mgt.i.d。在8周的剂量调整阶段,riociguat剂量根据批准riociguat剂量调整方案单独地增加,即in 0.5 mg steps every 2 weeks until the highest tolerated dose, or up to a maximum dose of 2.5 mgt.i.d。[15,16]。The individualised optimal dose of riociguat reached at the end of this phase was continued for another 16 weeks. Patients were seen at weeks 0, 2, 4, 6 and 8 during the dose-adjustment phase and at weeks 12 and 24 during the maintenance phase.
患者行右心脏导管插入术在基线(同时还接受PDE5i),并再次在第24周6MWD,WHO FC和N脑钠肽(NT-proBNP的)浓度的末端激素原物在每次随访评估。筛选期间进行的测量用作基线,这是最后的记录的值,同时仍接收PDE5i。0周已开始riociguat前的最后记录值(PDE5i无治疗期后)。
一个t the end of the study, patients could participate in an extended drug-supply phase for 18 months or until reimbursement. If a patient discontinued study drug prematurely or did not enter the extended drug-supply phase of the study, there was a 30-day safety follow-up phase.
结果措施
所有的终点都是探索性的,包括:从基线到第24周的6MWD、NT-proBNP、WHO FC、肺血流动力学和EuroQol 5维问卷(EQ-5D)评分(生活质量)的变化;临床恶化比例;安全性和耐受性。还评估了综合反应终点。应答者被定义为在第24周临床无恶化,达到who FC I/II,且在6MWD增加≥30 m的患者。
临床恶化定义为:死亡;心房septostomy;肺移植;non-planned PAH-related住院;开始新的多环芳烃治疗(ERA,吸入或口服前列腺素)或改变已有的治疗,开始静脉或皮下前列腺素治疗;6分钟随钻测量中,>较基线值持续下降15%,>较上次测量值持续下降30%;世卫组织财务状况持续恶化;或出现或恶化的迹象/症状的右心衰没有反应的最佳口服利尿剂治疗。所有确定的和怀疑的临床恶化事件都由独立的中央裁决确认。统计分析的详情载于补充资料。
结果
耐心
的79名患者筛选,61名患者在喘息入选(图1)。大多数患者被诊断为特发性肺动脉高压(N = 56,92%),并全部在WHO FC III(表格1)。进入喘息,40名患者(66%)之前,接收西地那非和21(34%)接受他达拉非。14patients (23%) had been receiving PDE5i treatment for ≤6 months before entering RESPITE, and 47 patients (77%) had been receiving PDE5i treatment for >6 months (maximum: 10 years). At baseline, 50 patients (82%) were receiving combination therapy with ERAs (23 (38%) ambrisentan, 16 (26%) bosentan and 11 (18%) macitentan). 45 patients (74%) were receiving concomitant diuretic treatment at baseline and two patients (3%) commenced loop diuretics during the study.
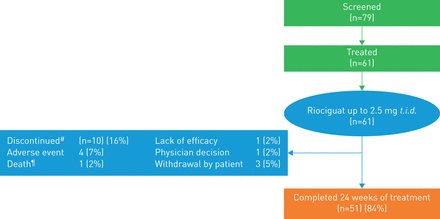
Patient disposition and flow in RESPITE over 24 weeks of treatment.#:初级中止的原因;¶:两个病人的主要研究(天27和49)期间死亡。在研究期间,两个人死亡的,一个是由于肺炎(撤出后病人,停药的主要原因)和一个硬膜下血肿。
Of the 61 patients enrolled in RESPITE, 51 (84%) completed 24 weeks of treatment and 10 (16%) discontinued treatment. Primary reasons for discontinuation included four adverse events, one death, one lack of efficacy, one physician withdrawal and three withdrawals by patient (one of whom subsequently died; see below). At week 24, of 51 patients remaining in the study, 47 (92%) were receiving the maximum dose of riociguat (2.5 mg每日三次)。剩余的四个患者(8%)接受riociguat 2.0毫克t.i.d。
功效
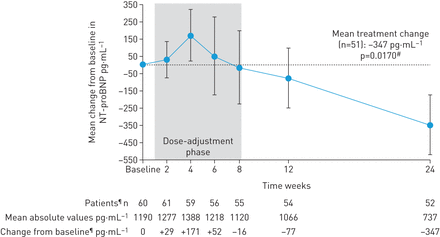
我n patients completing 24 weeks’ treatment, mean±SD6MWD较基线增加+31±63 m (95% CI 13-49 m;p = 0.0010;图2)。均值±SDNT-proBNP levels decreased by –347±1235 pg·mL−1,22%(95%CI的相对减少5-37%; P = 0.0170;图3)。在第24周,患者28/52(54%)得到了改善WHO FC(52%至WHO II FC,2%至WHO FC I; P <0.0001;图4)。所有人群在基线时的血流动力学变量见表格1。在基线和第24周的血液动力学参数成对值分别为可供49个例。在这些患者中,在第24周,平均±SDPVRwas reduced by –103±296 dyn·s·cm-5(95% CI –188 to –18 dyn·s·cm-5;p值= 0.0184),平均值±SDmPAP was reduced by –2.8±8.8 mmHg and right atrial pressure was reduced by –0.8±4.2 mmHg. Mean±SDcardiac index and mixed venous oxygen saturation increased by +0.3±0.5 L·min−1·米−2(95% CI 0.2–0.5 L·min−1·米−2;分别为p = 0.0001)和+ 1.0±6.3%,(表2)。对10名未完成研究的患者进行了额外的敏感性分析,以解决潜在的偏见。对于死亡或未终止访诊而退出的患者,其肺血流动力学的最后观察(LOCF)进行,而NT-proBNP的最后基线后测量进行,其可能的最差值为6MWD、who FC和EQ-5D。这一分析仍然显示了所有参数与基线相比的变化,这与在完成研究的患者中观察到的研究结果一致。虽然6MWD和NT-proBNP较基线的变化较低,且无统计学意义,但WHO FC (表2;表S1和S2)。
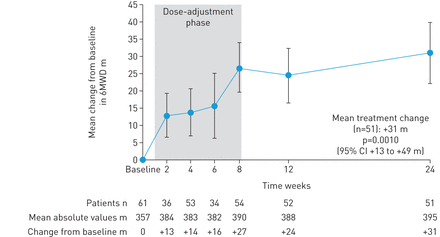
从基线的变化(最后记录的值,同时仍然接受磷酸二酯酶5抑制剂)在6-分钟步行距离(6MWD)随时间的喘息。数据是平均值±SEM;观察到的值。
自基线的变化在(最后记录的值,同时仍然接受磷酸二酯酶5抑制剂)N过在喘息时间脑利钠肽(NT-proBNP水平)的末端激素原。数据是平均值±SEM;观察到的值。#:从基线的相对变化计算p值;¶:缺少值在基线一个患者;N = 52在24周,由于已经经历了NT-proBNP水平的第24周评估在159天一个病人撤出基线的变化。
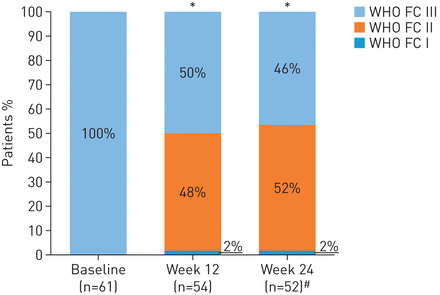
世界卫生组织功能分级(WHO FC)在基线(最后记录的价值,同时还接受磷酸二酯酶5抑制剂),第12周和第24周的喘息。数据是观察到的值。*:P <0.0001,从基线到周12和24变化;#:N = 52,由于一个病人在停药159天已经经历了WHO FC的第24周的评估。
一个t week 24, 16/51 patients (31%) met the combined responder end-point of freedom from clinical worsening, WHO FC I/II and an improvement in 6MWD ≥30 m. A sensitivity analysis that included patients who completed or withdrew from the study (n=60) showed that 16 patients (27%) achieved the combined responder end-point. Change from baseline to week 24 in EQ-5D scores, and worst-case imputed values for EQ-5D are presented in table S2. A事后分析进行,以确定患者是否在24周改变了他们的ESC / ERS风险类别,总体低风险假设时,可用变量> 50%,达到了低风险阈值。这被认为是在第24周在基线9例(15%)相比,在49例确定的状态(51%)25的情况。然而,还应当指出的是3位患者(6%)在第24周敏感性分析拍摄的高风险概况虑10例患者从研究过早中断导致的从患者41%的速度谁在第24周实现了低风险状态的6MWD riociguat的影响总人口,NT-proBNP和血流动力学似乎是独立于以前的类型PDE5i治疗(图S2),或同时使用ERA(表S3和S4的;图S3)。
临床恶化
六例(10%)出现一个或多个定义和裁定恶化的临床事件:两人死亡(见下文),谁开始了新的PAH的治疗,两名患者两名患者谁经历持续6MWD的恶化是由于肺动脉高压和一个病人谁经历体征/右心脏衰竭未优化的口服利尿剂治疗有反应的症状。没有临床恶化事件中的PDE5i无治疗期间发生的。
安全
不良事件
在研究中,58例(95%)出现不良事件,其中最常见的描述表3。四例(7%)发生不良反应,导致研究停药,其中2例(3%)与右心室衰竭乏力,1例(2%)(起始riociguat处理后的天+15和+158)(日2)和一个患者(2%)与症状性低血压(16天)。两名患者出现右心衰竭,并发一个经验丰富的肾功能衰竭和无症状性低血压,而其他同时有经验的呼吸困难。谁没有进入研究的延长药物供应相或中断研究的患者过早进行了为期30天的安全性随访。12例(20%)30天的安全性随访过程中发生不良反应,1例患者(2%)出现胆囊炎的严重不良事件。在随访期间,最常见的不良事件是鼻咽炎(N = 3; 5%)和外周性水肿(N = 2; 3%)。
特别关注的不良事件
晕厥喘息期间没有报道。10例(16%)出现低血压的不良事件,其中七经历了症状性低血压;六个事件被认为是温和的,三中度和重度一个。低血压导致剂量两名患者在两名患者减少或中断和停药。年代BP <95 mmHg was measured in three patients at week 0, four at week 6, three at week 12 and five at week 24. Mean systolic and diastolic blood pressures and heart rate during the study are shown in figure S4.
有一例咯血被认为是轻微的,与药物无关,被描述为咳嗽并偶有血斑。治疗干预是不需要的,病人继续研究药物没有经历额外的咯血发作。
严重不良事件
严重不良事件发生在10例(16%)。有3例右心衰竭,以及每个下腹痛,消化不良,乏力,胆囊炎,肺炎,硬膜下血肿,抑郁症,肾功能衰竭,介入手术和低血压(中度严重程度)一个案例。两个严重不良事件被研究者认为是研究药物相关的:右心室衰竭和乏力。No serious adverse events were reported during the PDE5i treatment-free period, and only two patients (3%) reported serious adverse events during the first 2 weeks of riociguat treatment.
死亡人数
两名患者(3%)在研究期间死亡:一人死亡是由于肺炎在55天病人已经停止对天+28(终止原因:患者停药)riociguat治疗后;其他死亡归因于硬膜下血肿以下的下降(天+50,不相关的低血压)。此前PDE5i治疗是西地那非谁死于肺炎和他达拉非的谁经历了硬膜下血肿患者的患者。无死亡被认为与研究药物相关。
讨论
喘息是第一个研究调查潜在的临床改善转换疗法这一目标不同的分子相同的信号通路在多环芳烃和提供了初步证据表明,这种方法不仅可以容忍和安全的,但也可能有利于PAH患者反应不足以前的治疗,包括PDE5i单一疗法或PDE5i /联合治疗时代。61例患者中有51例(84%)完成了为期24周的研究,在这些患者中,使用riociguat替代PDE5i改善了血流动力学变量、心脏生物标志物和临床终点(包括6MWD和WHO FC)。6MWD和EQ-5D的改善与之前报道的这些参数的临床相关性的最低重要差异相当[29,31,32]。然而,10名患者(16%)没有完成这项研究,主要是由于副作用或临床恶化。总的来说,10名患者(16%)经历了严重的不良事件;10例(16%)出现低血压(7例有症状);6名患者(10%)出现临床恶化事件。PDE5i无治疗期未发生严重不良事件或临床恶化事件,未发现新的安全信号。
在关键的专利-1研究中,缓解期的退出率高于2.5 mg最大臂(16%)与7%喘息和专利-1,分别地)。然而,基线特性也显着不同,在喘息100%的患者在WHO III FC与55% in the PATENT-1 2.5 mg maximum arm, and 48% of patients in the PATENT-1 2.5 mg maximum arm being treatment-naïve. Therefore, direct comparison between these groups may not be informative.
大部分参加试验的患者(82%)已接受联合治疗与PDE5i和ERAS包容之前,人口的74%在基线接收利尿剂。Despite stable and prolonged pretreatment, all patients had severe haemodynamic impairment, were in WHO FC III and had a 6MWD <440 m. According to the 2015 European pulmonary hypertension treatment guidelines, these patients would have been classified as intermediate risk, which is considered an inadequate response to therapy [3.]。应当指出的是,在一周的喘息24日,总人口(61分之25)的41%会被认为是有一个整体的低风险配置文件(其中的变量> 50%为低风险),与15%相比,基线。
波生坦和西地那非之间在后者[的降低的血浆水平的结果的电势直接相互作用33]已被建议作为为什么COMPASS-2的研究中,它增加了波生坦西地那非,并没有达到其主要终点[一个可能的解释34]。然而,在缓解期,没有迹象表明ERA类型或之前的PDE5i治疗影响6MWD、NT-proBNP、心脏指数或PVR。
虽然不是机械地学习,喘息的调查结果支持这一假设有缺陷的NO-GC-cGMP途径或许可以解释为什么有些患者对PDE5i治疗无足够的或持续的响应。在这些患者中,sGC的直接刺激可以比抑制PDE5的更有效,但这种假设仍未经证实。在6MWD看到从基线高达喘息的24周持续改进,可以支持这一理论。NT-proBNP水平显着减少在研究期间,虽然有趣的是,水平暂时在PDE5i治疗结束和riociguat的单独优化剂量之间的时间段增加。这一观察结果表明,PDE5i仍然有研究人群产生积极的影响,虽然没有足够的患者达到或维持治疗的目的。一个PDE5i treatment-free period of 24 h for sildenafil and 72 h for tadalafil was used before the start of riociguat treatment to avoid an exposure overlap, and riociguat was adjusted over an 8-week period. Although no clinical worsening events occurred during the PDE5i treatment-free period, stopping treatment remains a matter of concern, especially in patients receiving PDE5i monotherapy. Shorter switching periods might be preferable and future studies need to address this question as well as whether starting riociguat at higher doses with shorter dose-adjustment periods is safe and feasible. Furthermore, the three times daily dosing interval with riociguat compared with once daily dosing of tadalafil may affect patient adherence to treatment.
目前还不清楚的是,那些对sGC刺激剂的反应可能比PDE5i更有利的患者能否被识别先天的。NO合成的生物标记物已被证明关联与PAH [轻重24,35]并且可用于确定患者的受损NO信令谁可以从sGC的刺激中受益。
鉴于喘息的探索性和不受控制的性质,各种最终点是预先指定的,但被定义没有主要终点。这项研究旨在着手较大,随机,对照临床试验之前提供安全性和有效性的初步信号,视为同意先天的赞助商和指导委员会之间。由于没有新的安全信号,并改善从基线6MWD,WHO FC,NT-proBNP水平和血流动力学,随机,对照临床试验,以进一步调查从PDE5i切换到riociguat战略正在进行(Riociguat更换PDE5i治疗评价针对续PDE-5I疗法(替换);clinicaltrials.gov识别码NCT02891850)。
本研究的优势在于前瞻性、多中心研究设计;一个相对同质的病人群体;使用系统的安全性和有效性评估,包括在入组和研究结束时的侵入性血流动力学;以及对临床恶化事件的中央独立裁决。暂息治疗最重要的限制是没有对照组,这就排除了切换是否影响长期生存的猜测,也没有致盲。其他限制包括样本量小,以及相对较高的退出率(16%),这可能会给分析带来偏差。为了提供最保守的数据,我们尝试通过敏感性分析来解决这一潜在的偏差,使用最坏的可能值分别为6MWD、WHO FC和EQ-5D,以及肺血流动力学的LOCF。改善仍与研究的总体结果一致,但6MWD和NT-proBNP不再具有统计学意义,世卫组织FC的变化仍然显著。其他的限制包括缺乏一个长期的持续阶段,以及缺乏机械的数据来识别病人可能对转换有反应或没有反应。本研究中观察到两例死亡,这可能会引起关注,尽管调查人员认为这两例死亡(一例由于肺炎,另一例由于硬膜下血肿)均与药物相关,或由于多环芳烃恶化。 Given the lack of a control group and the rate of study withdrawals and clinical worsening events, further evaluation to clarify the safety of switching is required. We also acknowledge that the patients enrolled in this study could have been treated with double or triple sequential combination therapy as recommended in current guidelines and that comparisons with these treatment strategies cannot be made. Finally, RESPITE predominantly included patients with idiopathic PAH (92%) so the findings cannot be extrapolated to other forms of PAH.
结论
从喘息研究结果表明,与riociguat替换PDE5i可以是用于PAH患者谁必须PDE5i单一疗法或联合治疗与ERA和PDE5i不足临床反应的可行而有效的治疗策略。这项研究是对确定这一新的治疗策略是一种有效的方法来PAH患者管理的重要一步,但是从更大的附加数据,随机,需要对照研究,进一步建立这种方法的安全性和有效性。
补充材料
披露
补充材料
R.L. Benzaerj - 02425 - 2016 - _benza
D.布塞erj - 02425 - 2016 - _busse
P.科罗拉多ERJ-02425-2016_Colorado
P.A.科里斯erj - 02425 - 2016 - _corris
哈。GhofraniERJ-02425-2016_Ghofrani
E.格鲁尼格erj - 02425 - 2016 - _grunig
M.M.HoeperERJ-02425-2016_Hoeper
r . NaeijeERJ-02425-2016_Naeije
S.罗森克朗茨ERJ-02425-2016_Rosenkranz
G. SimonneauERJ-02425-2016_Simonneau
光盘。VizzaERJ-02425-2016_Vizza
致谢
编辑支持由阿德菲通信有限公司,Bollington,英国,拜耳公司提供支持。作者要感谢喘息的临床事件委员会,谁担任临床恶化事件的独立评委的成员。
脚注
这篇文章有补充资料www.qdcxjkg.com
本研究注册于ClinicalTrials.gov与标识NCT02007629。
支持声明:本研究由拜耳公司,德国柏林的支持。本文资金的信息已交存交叉引用出资者注册。
利益冲突:披露可以在这篇文章旁边找到www.qdcxjkg.com
- 收到2016年12月9日。
- 接受2017年7月12日。
- 版权所有©ERS 2017年
该版本采用知识共享署名非商业许可证4.0的条款分发。