摘要
残余肺血管阻塞(RPVO)和慢性血栓栓塞性肺动脉高压(CTEPH)都是急性肺栓塞的长期并发症,但目前尚不清楚与CTEPH相关的纤维蛋白原变异是否能预测RPVO。
我们使用Akaike信息标准,以初始梗阻程度、临床特征和纤维蛋白原相关数据作为候选变量,在两个前瞻性随访的急性肺栓塞患者队列中选择最佳的RPVO预测模型。我们通过偏差分析来衡量所选模型的拟合优度,并使用卡方检验来比较模型。
第一组102名受试者中有29人(28.4%)发生RPVO,第二组182名受试者中有46人(25.3%)发生RPVO。在第一个队列中得到的最佳拟合预测模型(p=0.0002)在第二个队列中得到验证(p=0.0005)表明纤维蛋白原b β链单唾液酸化与RPVO的发生有关。当推导过程排除临床特征时,在最佳拟合预测模型中,纤维蛋白原b β链单唾液酸化仍然是RPVO的预测因子(p=0.00003)。排除纤维蛋白原特征使预测模型恶化(p=0.03)。
纤维蛋白原b β链单唾液酸化是纤维蛋白的一种常见结构属性,有助于预测急性肺栓塞后的RPVO。纤维蛋白结构可能与发生RPVO的风险有关。
摘要
纤维蛋白原有助于预测肺栓塞后残余肺血管阻塞:PROMPT研究的结果http://ow.ly/G7pY30m2HU6
简介
急性肺栓塞后,肺动脉内的血栓性物质通常会分解,但在某些情况下会转变为永久性的梗阻性疤痕[1].≥10%的残余肺血管阻塞(RPVO)是肺栓塞后常见的,可减少体力活动,降低生活质量,恶化整体预后[2- - - - - -7].RPVO与呼吸困难有关[8],低氧血症[9],气体交换不足[9]、运动不耐受[2]及其他严重的临床损伤[9- - - - - -11].RPVO有复发风险[12]及慢性血栓栓塞性肺动脉高压[2,13],不常见的[14,15]但严重的肺栓塞并发症[16,17]梗阻范围广泛,肺动脉压升高[18].
富含纤维蛋白的血栓栓子转化为RPVO和CTEPH特征的永久性梗阻的机制尚不完全清楚。RPVO与“血栓性”或纤溶酶受损无关[2].我们观察到,一些CTEPH患者体内提取的纤维蛋白本身形成了抗溶凝块[19,20.]与分子构型的畸变[21]和凝块结构[22],反映了罕见的纤维蛋白原基因突变[20.].cteph相关的纤维蛋白原异常血症可能是更常见的纤维蛋白特征的一个模型,可能会使平衡从血块溶解向RPVO倾斜。
为了深入了解RPVO的发展,肺栓塞治疗后残留梗阻的预测(PROMPT)研究跟踪了两组急性肺栓塞患者,以确定RPVO的最佳预测因子。我们研究了纤维蛋白原翻译后修饰和其他常见的纤维蛋白结构属性是否有助于预测急性肺栓塞后RPVO的发展。如果纤维蛋白特性始终与RPVO相关,那么它们可能是其发展的机制之一。
方法
研究设计和研究人群
我们使用了两项单中心、前瞻性、观察性队列研究的临床数据和生物学材料,这些研究分别对一所学术教学医院(Hôpital Européen Georges Pompidou, Paris, France)的急性肺栓塞患者进行了研究。这两项研究得到了当地伦理委员会的批准。所有患者在入组前均提供书面知情同意书。
对于队列1,我们从我们的研究中心连续招募了肺栓塞患者,这些患者已被纳入FARIVE研究,这是一项多中心病例对照研究,评估了环境、遗传和生物学风险因素对首次静脉血栓栓塞(VTE)风险的相互作用。该研究包括年龄为>岁18岁且首次出现肺栓塞症状的连续受试者。如果患者患有活动性癌症,除非他们已经接受了成功的治疗,并且在过去5年内没有复发的证据,否则他们将被排除在外。此外,如果患者继发于其他相关病理,预期寿命较短,预计不可能随访或先前诊断为血栓性疾病,则排除在外。
在队列2中,我们招募了1999年2月至2006年5月期间在我们中心连续随访的肺栓塞患者,这些患者未被纳入FARIVE研究[2].本研究旨在评估急性肺栓塞发作后残余肺血管阻塞的临床意义。年龄为> ~ 18岁,完成口服抗凝治疗≥3个月且无复发肺栓塞的患者纳入研究。
在两个队列中,肺栓塞的诊断是通过高概率肺显像、胸部计算机断层扫描(CT)、肺血管造影、在报告的肺部症状没有鉴别诊断的情况下显示存在近端静脉血栓的超声或与下肢超声相关的非诊断性肺显像显示近端深静脉血栓形成来确定的。长期治疗的类型和持续时间由负责患者的医生自行决定。标准做法是治疗诱发性肺栓塞≥3个月,非诱发性肺栓塞≥6个月。
残余肺血管阻塞
所有患者均接受标准化通气/灌注比(V' /问急性肺栓塞后≥6个月进行肺扫描[23].一名训练有素的研究人员(BP)无视所有其他研究数据,根据预先指定的方案识别并评分不匹配的灌注缺陷[24].我们将RPVO定义为残余血管梗阻≥10%,对应于至少两个肺段的截肢(最小梗阻定义了诊断结果的高概率)V' /问肺扫描[25]),并与急性肺栓塞后的呼吸困难和运动不耐受有关[2].
人口学和临床资料
研究登记时使用标准化工具记录临床数据(包括急性治疗类型和长期治疗持续时间),并进行结构化访谈。除下节中描述的纤维蛋白原相关实验室数据外,所有实验室值均在Hôpital Européen乔治·蓬皮杜临床实验室测量。对每位患者的其他数据不知情的医生使用经过验证的评分来计算原始诊断CT扫描上的初始肺血管梗阻[26]或V' /问'扫描[24].所有受试者均未以肺血管造影作为初始诊断检查。
纤维蛋白的结构属性
入组后,通过静脉穿刺将血液样本放入含有抗凝血剂的管子中。血浆通过连续两次离心分离,并储存在−70°C下进行分析。在采血时在临床实验室测量血浆纤维蛋白原水平。
研究测定了从柠檬酸血浆中通过乙醇沉淀纯化的纤维蛋白原,并暴露于明胶Sepharose (GE Healthcare, pittsburgh, PA, USA)以去除残留的纤维连接蛋白,然后稀释至4mg·毫升−1[20.].在线补充附录1包括详细的分析方法,以前已经报道过[19,20.,22].下面简要介绍它们。
纤维蛋白原、凝血酶和氯化钙结合形成纤维蛋白凝块,每种结构试验都采用适当的量。我们测定了纤维蛋白凝块的浑浊度,这与镜检证实的纤维蛋白网络纤维的分散和分支相对应[20.,22].我们通过浊度降低率来测量纤维蛋白凝块对溶解的敏感性,在凝块暴露于纤溶酶原和组织纤溶酶原激活剂的混合物后连续测量[20.].我们测量了纤维蛋白凝块的渗透性,这反映了纤维蛋白聚合物形成的组织[22],由渗透性缓冲液通过纤维蛋白凝块的速率决定。具有较大孔隙的更有组织的纤维蛋白网络与具有较小孔隙的无序纤维蛋白网络相比具有更高的流量。我们使用十二烷基硫酸钠聚丙烯酰胺凝胶电泳测量了纤维蛋白的α-链交联程度,以反映血栓形成过程中形成稳定凝块的潜力[19].我们用了I125-标记抗体特异性的β15 42肽序列链(抗-β15 42)以测量纤维蛋白β链氨基末端在纤维蛋白凝块内的可达性(残基15-42),该残基与多种影响血栓重塑为血管内瘢痕的生理事件有关[27- - - - - -29].
我们使用液相色谱法测量了精确的纤维蛋白原质量,然后用质谱(LC/MS)来识别翻译后修饰[20.].我们分析了代表纤维蛋白原a α-链、b β-链和γ-链的LC/MS谱,并测量了与我们在cteph相关纤维蛋白原异常血症中观察到的变异相对应的质量峰的比例高度,以及代表相关纤维蛋白原链≥10%的任何其他质量峰。
统计分析
分类变量以n(%)表示,连续变量以均值±表示sd.采用t检验、Wilcoxon-Mann-Whitney检验、Fisher精确检验或卡方检验,对两组间所有可用的人口学、临床和纤维蛋白原数据进行比较。对每个队列进行RPVO预测因素的单因素评估,酌情使用相同的试验。
由于导致RPVO的裂解、炎症和细胞重塑的相互作用可能是通过临床因素和生物学因素之间的复杂相互作用发展起来的,因此仔细选择预测模型对我们的目标至关重要。如果使用简单的单变量分析,联合预测效果将被模糊[30.].为此,我们采用了基于赤池信息准则(AIC)的逐步多元逻辑回归方法[30.,31],以临床危险因素和纤维蛋白结构特性作为候选预测因子,在每个队列中选择最精简和最准确的RPVO多变量预测模型。如果以这种方式选择的最佳预测模型依赖于纤维蛋白的结构属性,那么该分析将支持纤维蛋白属性在急性肺栓塞后RPVO发展中的作用。基于人工智能的方法避免仅根据单个项或全局拟合的明显显著性来选择模型,这两者都可能被夸大;过拟合会受到惩罚[31].我们使用基于偏差的拟合优度,一个标准的逻辑回归指标,来评估每个队列中所选模型的质量。
对拥有完整数据(没有缺失值)的受试者的信息进行多变量建模,以进行模型比较。对于队列1,采用基于aic的逐步logistic回归来确定RPVO的最佳临床和人口学预测因素。然后,使用基于aic的逐步逻辑回归来选择预测RPVO的最佳模型,使用每个患者之前确定的相关人口统计学和临床指标,以及我们描述的纤维蛋白原实验的结果作为候选预测因子。我们使用受试者工作特征(ROC)曲线[32],寻找预测RPVO的最佳概率分界点,并评估模型的敏感性和特异性。然后,我们通过预测队列2的RPVO来验证队列1中推导出的模型。
为了确认特定纤维蛋白结构属性在RPVO中的作用,我们在队列1中再次进行了预测模型选择过程,仅将纤维蛋白原属性和初始梗阻程度(不包括临床数据)纳入候选预测因子池。梗阻的初始程度是残余梗阻的有力预测指标[2所有的预测模型都会包括它。我们感兴趣的是寻找额外的、独立的预测方法。最后,为了进一步验证纤维蛋白原的作用,我们使用残差卡方检验来确定包含初始梗阻和纤维蛋白原属性的模型是否比不包含纤维蛋白原属性的模型更能显著预测RPVO。
为了确认在队列1中确定的单个RPVO预测因子的普遍性,我们在队列2中重复了多元建模过程,但将候选变量限制在队列1分析中披露的变量。我们推断,两个队列中RPVO的预测变量可能与急性肺栓塞患者中RPVO的发展有关。如果从队列1中得到的一个变量没有包含在队列2的最佳预测方程中,或者如果它的系数方向相反,我们推断它不太可能预测其他肺栓塞人群的RPVO。
结果
人口问题
从2003年1月至2009年1月,137例患者被纳入队列1 (图1一个).2例(1.4%)患者没有进行RPVO评估,因为他们失去了随访;随访6例(4.4%)V' /问他的肺部扫描结果不见了。27名(20.9%)受试者的血浆样本无法用于纤维蛋白(原)实验室分析。排除在队列1的35例患者与纳入队列1的患者在年龄、性别、从症状到诊断的时间或残留梗阻方面无显著差异。纳入分析的102例受试者中,29例(28.4%)RPVO≥10% (表1).均值±sd从肺栓塞诊断到V' /问肺扫描8.3±2.5个月,持续灌注缺损程度8.1±11.7%。
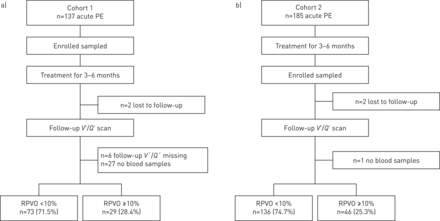
两个队列的研究大纲。a)在队列1中,在急性肺栓塞(PE)诊断时招募的137名受试者中,102名可评估,其中29名(28.4%)患有残余肺血管阻塞(RPVO)≥10%;b)在队列2中,在接受急性肺栓塞长期治疗后招募的185名受试者中,有182人可以评估,其中46人(25.3%)的RPVO≥10%。
1999年2月至2006年5月,185例患者被纳入第2队列(图1 b).2例(1.0%)患者失访。一名(0.5%)受试者无法获得用于纤维蛋白(原)实验室分析的血浆样本。被排除的患者在任何研究特征上都不是异常值。其余182例受试者中,46例(25.3%)RPVO≥10%。均值±sd从肺栓塞诊断到V' /问肺扫描为10.9±3.7个月,平均RPVO为6.8±12.7%。
比较两组间的受试者特征表1(一个全面的列表包括在在线补充附录2).队列1明显小于队列2(52.2±19.6岁)与61.3±18.5岁,p=0.0002)。队列1的癌症患病率较低(2.0%与12.1%, p=0.003),卧床休息患病率较低(8.8%)与20.3%, p=0.01),溶栓药物的使用率较低(0%与5.5%, p=0.02),下腔静脉滤器使用率较低(0%与4.5%, p=0.03)高于队列2。然而,VTE家族史在队列1中比队列2中更常见(31.4%)与18.0%, p = 0.01)。在症状出现后,第1组的肺栓塞诊断时间稍早于第2组(11.2±17.1天)与14.3±28.6 d, p=0.04)。
与RPVO相关的单因素分析显示在表2.在两个队列中,无RPVO患者的初始肺血管阻塞比有RPVO的患者更小。值得注意的是,cteph相关突变(纤维蛋白原SanDiegoIII) [20.],该患者的RPVO为29.5%。
第一队列中RPVO预测模型的推导
预测模型的创建和选择在队列1中的94名受试者中进行,他们拥有完整的临床和纤维蛋白相关数据集。当考虑所有候选变量时,预测RPVO概率的最佳模型包括血管梗阻的初始程度、纤维蛋白原b β链单唾液酸化、症状与诊断之间的天数以及纤维蛋白原-γ ' (表3).模型拟合优度极显著(零偏差与残差差=21.8,卡方p=0.0002)。ROC曲线下面积(AUC)为0.762 (p=0.0001)。敏感性为0.679 (95% CI 0.476 ~ 0.841),特异性为0.727 (95% CI 0.604 ~ 0.830)。
RPVO预测模型在队列2中的验证
从队列1中所有候选变量推导出的最佳预测模型应用于队列2中拥有完整数据集的141名受试者。AUC为0.693 (p=0.0005)。敏感性为0.622 (95% CI 0.448 ~ 0.775),特异性为0.692 (95% CI 0.595 ~ 0.777)。
利用纤维蛋白原特性在队列1中推导RPVO预测模型
当候选预测因子库排除临床和人口统计学数据,仅包含梗阻的初始程度和纤维蛋白原数据时,最佳预测模型的拟合优度仍然非常显著(零偏差和残留偏差之间的差异=26.2,卡方p=0.00003)。在该模型中,初始梗阻和纤维蛋白原b β链单唾液酸化仍然是RPVO的预测因素,其中还包括纤维蛋白原-γ '和纤维蛋白溶解速率(表4).AUC为0.802。然而,当候选预测因子池也排除了纤维蛋白原数据时,剩余偏差的卡方检验揭示,当包括纤维蛋白原数据时,最佳拟合模型不能预测RPVO(两个模型的偏差差=9.0,卡方p=0.03)。
利用队列1的预测器池推导队列2的RPVO预测模型
为队列2创建了一个预测模型,候选预测因子池仅限于为队列1执行的模型创建和预测因子选择过程确定的四个预测因子。当只考虑这些候选变量时,预测RPVO概率的最佳模型包括血管梗阻的初始程度、纤维蛋白原b β链单唾液酸化以及症状与诊断之间的天数。纤维蛋白原-γ '不再是一个显著的预测因子。模型的拟合优度仍然高度显著(零偏差与剩余偏差之间的差异=18.8,卡方p=0.0009)。AUC为0.702。
在一个事后分析显示,整个(两个队列)组中b β链单唾液酸化的中位程度为59.2%。在b β链单唾液基化水平低于中位数的一半患者中,19.4%的患者有RPVO,而在b β链单唾液基化水平较高的患者中,31.9%的患者有RPVO (p=0.0169)。
讨论
我们对急性肺栓塞后的两组患者进行了随访,以确定最能预测RPVO的因素。在两个队列中,纤维蛋白原b β链的高比例单唾液酸化始终是RPVO的预测因素。在其他候选变量中,只有血管阻塞的初始程度对RPVO的预测能力更强,这与我们之前的观察结果一致[2].
我们将RPVO定义为≥10%的肺部持续的肺灌注缺损(即。至少有两个肺段)。虽然我们在目前的研究中没有客观地衡量生活质量或其他症状结果,但我们之前报道过,我们对RPVO的定义(发生在29%的急性肺栓塞患者中)与呼吸困难、肺动脉压升高和运动不耐受显著相关[2].在具有这种程度的RPVO的肺栓塞患者中,16%随后被诊断为CTEPH [2].
模型选择的预测因子与RPVO的后续发展高度相关(在推导队列中p=0.0001,在验证队列中p=0.0005)。该模型的诊断准确性不够高,无法排除用于临床目的的预测RPVO(推导组和验证组的AUC分别为0.762和0.693)。然而,RPVO与纤维蛋白原性质之间的关系为一些患者在急性肺栓塞后发生RPVO甚至CTEPH的机制提供了深入的了解。未发现与遗传性血栓形成有关[2],这就增加了纤溶过程受损的可能性[33].我们的研究重点是纤维蛋白本身,因为在一些CTEPH患者中观察到纯化的纤维蛋白凝块对溶解的抗性[19,20.]在某些肺栓塞患者中[33,34].我们使用纤维蛋白的特性作为模型[21,22]我们在cteph相关的纤维蛋白异常灌肠中观察到的[20.].我们推断,翻译后修饰模式的变化可能会影响纤维蛋白的形成和裂解[35,36比cteph相关的纤维蛋白异常灌肠轻,但更常见,它们可能在急性肺栓塞后的血栓栓塞持续中起作用。
我们的研究结果支持了这样的假设:在静脉血栓栓塞后慢性综合征的病因学中,衰减人体对富含纤维蛋白的血栓的正常机制是一个重要的病理生理步骤[5,18].一种可能的机制是,纤维蛋白凝块的特性会延迟或限制纤溶酶介导的纤维蛋白溶解,或修改其他凝块溶解机制,如血管生成和炎症反应[18].我们的观察表明,纤维蛋白的结构属性可能会充分影响纤维蛋白凝块的结构,从而导致急性肺栓塞后凝块溶解不良和慢性疾病。
高比例的单唾液化b β链可预测两组肺栓塞患者的RPVO。唾液酸化发生在纤维蛋白原形成过程中,由于带负电荷的唾液酸的静电效应,对纤维蛋白聚合物的组织和分解有各种影响。实验唾液酸去除导致无序的纤维蛋白凝块形成[35,37,38],而过多的b β-链和γ-链唾液化也会导致异常血栓[22,36].当凝血可能有益时,如怀孕期间,单唾液酸化会增加[39]及急性感染[40].
我们研究的两个队列的结果在低纤维蛋白原-γ '的预测能力方面略有不同,这与纤维蛋白交联的调节有关。这种差异可能是偶然的。或者,它们可能反映了两个队列之间的微妙差异,甚至在急性肺栓塞发生时(从第一个队列中收集血液样本时)和几个月后(在第二个队列中采样时)纤维蛋白(原)特征的不同含义。
我们的研究受到以下事实的限制:在研究方案完成后,我们没有通过客观测量呼吸困难、血流动力学或后续临床结果来独立确认RPVO在患者中的临床意义。然而,我们已经在之前一系列类似的肺栓塞患者中验证了RPVO与这些发现之间的关联[2].我们也承认,第一队列中有20%的患者被排除在外,因为他们没有足够的血浆样本用于纤维蛋白原分析,这可能会在该队列的分析中引入潜在的偏倚。虽然我们没有披露急性或长期抗凝治疗类型与RPVO之间的关联,但该研究是在广泛使用直接口服抗凝药物之前进行的,因此我们无法评论这些疗法的影响。最后,尽管我们在RPVO率相似的两个队列中的发现是一致的,但它们应该在后续的前瞻性研究中得到证实。
结论
在研究的两个队列中,肺栓塞发生时肺血管阻塞的程度以及纤维蛋白原b β链单唾液酸化是急性肺栓塞后RPVO的预测因素。我们的结果证实了我们之前的观察,并支持纤维蛋白特性在急性肺栓塞后血栓的消退或持续中所起的作用,这与CTEPH的发展中所起的作用类似。异常的纤维蛋白特性可能有助于识别急性肺栓塞患者的高危RPVO患者,对他们进行辅助治疗以改变疾病进展可能会得到评估。例如,由于纤维蛋白原性质,如纤维蛋白原b β-唾液化可能在药理学上受到影响[39],这种改变纤维蛋白原或机体对纤维蛋白反应的干预措施对RPVO的影响可能具有临床意义。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
附录1。补充方法。erj - 01467 - 2018 - _appendix_1
附录2。补充表。erj - 01467 - 2018 - _appendix_2
确认
作者要感谢Russell Doolittle (University of California San Diego, San Diego, CA, USA)对实验方法和手稿的有益建议和建议。Jess Mandel(加州大学圣地亚哥分校,San Diego, CA, USA)也对手稿提供了有益的评论。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:B. Planquette招募患者,进行实验并帮助撰写手稿;O. Sanchez、J. Emmerich和G. Meyer帮助设计了这项研究,并对手稿做出了贡献;J.J. Marsh, P.G. Chiles, R.E. Moore和G.B. Gugiu进行了实验室实验,并对手稿做出了贡献;G. Le Gal策划分析并对稿件有贡献;T. Wolfson和A.C. Gamst进行了统计分析,并对手稿做出了贡献。T.A. Morris是该研究的主要研究者,计划了该研究,进行了实验并对手稿做出了贡献。
利益冲突:B.普兰奎特没有什么可透露的。
利益冲突:O. Sanchez报告了来自拜耳的资助、个人费用和非金融支持,来自MSD的资助、个人费用和非金融支持,来自Actelion的资助和非金融支持,来自BMS-Pfizer的个人费用和非金融支持,来自第一三共的资助,来自Chiesi的个人费用和来自勃林格殷格翰的非金融支持,在提交的工作之外。
利益冲突:j·j·马什没什么可透露的。
利益冲突:P.G. Chiles没有什么可透露的。
利益冲突:J.艾默里奇没什么可透露的。
利益冲突:G. Le Gal曾在Portola Pharmaceuticals、勃林格殷格翰、辉瑞、百时美施贵宝、LEO Pharma、第一三共和拜耳的临床试验中担任联合研究员,并在提交的工作之外,从拜耳、辉瑞、LEO Pharma、赛诺菲和bioMérieux获得了酬金,而不是工资。
利益冲突:G. Meyer报告了来自拜耳的资助和来自利奥制药、bms -辉瑞和第一三共的非财务支持,在提交的工作之外。
利益冲突:沃夫森没有什么可透露的。
利益冲突:A.C. Gamst没有什么可透露的。
利益冲突:R.E.摩尔公司没有什么可透露的。
利益冲突:G.B. Gugiu没有什么可透露的。
利益冲突:T.A. Morris报告了拜耳制药公司在研究期间的资助;拜耳制药的个人咨询费,以及Faegre Baker Daniels作为专家证人的个人费用,在提交的工作之外。
支持声明:该研究由拜耳制药,Fonds de Recherche en Santé Respiratoire,法国,R01HL095089的研究资助,并通过与UCSD DNA测序设施合作(部分由NIH资助2 P30 CA023100-23)进行DNA序列分析;以及希望之城质谱和蛋白质组学核心设施(部分由美国国立卫生研究院CA033572拨款支持),用于进行纤维蛋白原质谱分析。作者对研究设计、表现和手稿创作有完全的自由裁量权。本文的资助信息已存入交叉参考基金注册.
- 收到了2018年3月24日。
- 接受2018年9月24日。
- 版权所有©ERS 2018















