文摘
疾病表型的肺结节病临床而非免疫标准是有区别的。我们旨在描述CD4的模式+t细胞系可塑性基础之间的差异在临床表现和疾病急性形式,洛夫格伦综合征,异构,可能进步“non-Lofgren”形式。
33肺结节病病人和9个控制进行支气管镜检查和支气管肺泡灌洗。CD4+t细胞转录因子、趋化因子受体和t细胞受体表达、增殖和细胞因子的生产评估灌洗液和外周血使用流式细胞仪和多色FluoroSpot。
CD4+同时表达辅助t细胞细胞(Th) 1和Th17转录监管机构T-bet和RORγT (T-bet+RORγT+)被确定在洗胃,但不是血,所有科目,洛夫格伦更高学位的病人。T-bet+RORγT+积极细胞扩散,产生干扰素(IFN)γ和白介素(IL) -17中的趋化因子受体CXCR3和CCR6和与nonchronic相关疾病。t细胞receptor-restricted Vα2.3+Vβ22+t细胞强烈中的T-bet / RORγT和CXCR3 / CCR6。Lofgren患者细胞因子生产更多的异构,IL-17A显著升高,il - 10、il - 22生成和2,但IFNγ低。
在这里我们展示肺T-bet的存在+RORγT+CXCR3+CCR6+CD4+t细胞和Th17-associated细胞因子特别是在结节病的患者预后良好,表明Th1 / Th17-permissive环境与影响肺疾病决议。
文摘
肺CD4+t细胞表达T-bet和RORγT都发现特别是在结节病的患者预后良好http://ow.ly/10ai8H
介绍
结节病肉芽肿性间质性肺疾病原因不明,在细胞水平上的特征激活CD4的积累+t细胞在肺部(1]。虽然触发抗原(s)尚未确定,CD4细胞+t细胞被公认是驾驶疾病进展的关键球员。我们组之前建立了联系确定人类白细胞抗原(HLA) -DRB1等位基因,积累(TCR)限制CD4 t细胞受体+t细胞克隆和良好的预后(2),暗示特定的抗原识别和区分效应t细胞疾病决议。
近年来,CD4细胞+t细胞可塑性已经成为区域增加兴趣和重要性理解的动态免疫系统在疾病进展。子集“开关”,如。之间的调控t细胞(Treg)和辅助(Th) 17细胞,或与Th1 / Th17细胞“混合”表型实验设置和报道人类慢性炎性疾病(3- - - - - -7]。虽然结节病历来被视为Th1-driven疾病,Th17细胞最近还牵涉到疾病课程(8- - - - - -12]。到目前为止,很少有研究能够解决CD4的主题+t细胞可塑性的肺结节病的炎症,这驱使我们进行详细的CD4细胞表型和功能描述+t细胞从lineage-specific转录因子和细胞因子的角度。通过成对比较外周血和支气管肺泡灌洗液(BALF)细胞,本研究提供有价值的信息关于免疫细胞功能和肺上。
在结节病的病人通常被视为一组,详细研究了不同患者之间的差异的具体疾病表型洛夫格伦综合征(LS)和那些没有,从此被称为“构造”[13]。LS急性疾病患者通常表现的不同的临床症状,通常,有利的疾病过程(13,14]。构造的病人,然而,更多展示一种慢性疾病进展和发展中肺纤维化的风险更高。尽管临床差异,准确的免疫学机制这群仍然遥遥无期。在这里,我们专注于比较LS和构造的病人的CD4细胞水平+辅助子集和监管元素,为了更好地理解这两种不同的疾病的免疫学背景形式。我们显示,第一次,LS和构造形式之间的显著差异转录因子水平体外。功能,CD4+同时t细胞表达Th1和Th17监管者T-bet RORγT,分别展示增殖能力和趋化因子受体表达明显高于T-bet−RORγT−细胞,并有能力产生多种细胞因子。生产Th17-associated明显广泛的细胞因子在LS进一步表明,异质性在免疫调控可能对疾病产生积极影响的结果。
材料和方法
研究对象、支气管镜检查和支气管肺泡灌洗
支气管镜检查和支气管肺泡灌洗(BAL)如前所述执行15]。33新诊断结节病病人(七个女性),平均年龄为46.2岁,是包括在研究(表1)。所有患者HLA-typed和诊断为结节病根据标准建立的世界结节病和其他肉芽肿疾病协会(WASOG) [16]。具体地说,包括典型的临床和影像学表现,发现在支气管镜检查BAL包括CD4 / CD8比值升高,如果需要,积极的活检,排除其他诊断。八个病人被诊断为LS,定义为急性发病,经常发烧,胸部影像学发现双侧肺门淋巴结病,有时与肺浸润,结节性红斑和/或双边踝关节炎。25例构造。落下帷幕的时候,一个构造与强的松病人接受治疗。此外,BALF细胞从四个健康志愿者和五个其他肺部疾病患者(非特异性肺纤维化和过敏性肺泡炎)进行了分析比较。部分替代诊断患者包括补充健康受试者的低数量,以及区分的目的任何细胞特征固有的肺部炎症,而不是那些特定的结节病。知情同意是获得所有科目和伦理从斯德哥尔摩郡地区获得伦理委员会批准(批准号:2005/1031-31/2 2009/20-32和2011/35-32)。
流式细胞术、细胞内染色和多色FluoroSpot
协议的详细描述,用于表面和胞内抗体染色流式细胞术(图S1),细胞细胞因子的刺激和评估生产多色FluoroSpot和流式细胞术可以补充材料中发现的。
统计分析
整体细胞群的差异(详细列出辅料)患者组之间被单向方差分析,评估了非参数Mann-Whitney紫外线测试,Wilcoxon签署等级测试成对比较和非参数的斯皮尔曼等级测试。FluoroSpot细胞因子生产相比,使用双向方差分析和未配对t检验。分析使用GraphPad棱镜v.5.02软件(GraphPad软件公司,拉霍亚,CA,美国)。p < 0.05被认为是显著的。
结果
增加CD4+t细胞增殖和细胞因子在BALF生产
在所有结节病病人,我们发现CD4细胞+BALF的t细胞增殖明显高于血液中(图S2a)。CD4+t细胞刺激anti-CD3 / anti-CD28抗体还显示明显高于细胞因子总产量(干扰素(IFN)γ,白介素(IL) 2和IL-17A总和)BALF中(图开通),进一步表明通常更高的激活状态与血。
BALF CD4+t细胞表达T-bet和RORγT
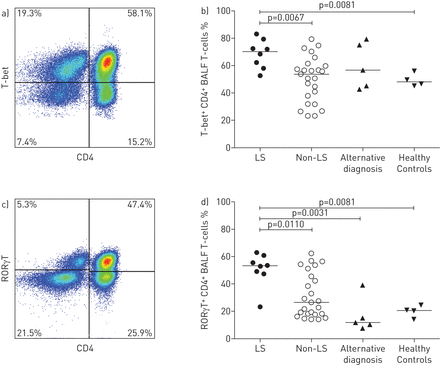
在所有结节病病人以及控制,大多数CD4细胞+BALF中t细胞表达了Th1调节器T-bet (图1一个)。LS显示病人的比例明显高于BALF T-bet+CD4+t细胞比构造或健康人(图1 b)。RORγT+CD4+t细胞也BALF中确定(图1 c),明显更频繁的在LS病人比在任何其他组(图1 d)。此外,很大一部分T-bet+CD4+t细胞被发现也表达RORγT(图S3)。反过来,几乎所有RORγT+CD4+在T-bet t细胞被发现+CD4+t细胞室(图S3)。
更高比例的T-bet和RORγT表达式在支气管肺泡灌洗液(BALF)洛夫格伦综合征(LS)患者。代表流式细胞术T-bet散点图一所示)+CD4+和RORγT c)+CD4+从一个LS患者BALF中t细胞的数量。b) LS患者伴有明显高于T-bet水平+CD4+t细胞在BALF比构造患者和健康对照组。d)也观察RORγT明显不同+CD4+t细胞(所有的比较都是使用双尾Mann-Whitney紫外线测试)。
T-bet+RORγT+CD4+BALF t细胞存在,但不是血,在LS最突出
我们发现CD4+t细胞同时表达T-bet和BALF中RORγT结节病病人和健康人,在某种程度上与其他肺部疾病患者(图2一个- - - - - -c,e),而他们几乎没有血(图2 d,f)。T-bet的比例+RORγT+t细胞明显更大的BALF LS病人的CD4(平均65.2%+比构造t细胞)患者(平均38.7%;p = 0.0078与LS),其他肺部疾病患者(平均19.5%;p = 0.0062与LS)或健康人(中位数23.4%;p = 0.0040与LS) (图2一个- - - - - -c,e)。无显著的相关性T-bet / RORγT表达与患者年龄、性别或胸部影像学阶段落下帷幕的时候被发现,无论是对病人群体作为一个整体还是当LS和构造是单独考虑。
T-bet和RORγT发生在支气管肺泡灌洗液(BALF),但不是血,所有的科目,这是最为明显的洛夫格伦综合征(LS)。代表流式细胞术散点图所示的同时T-bet和BALF中RORγT CD4的表达+从)一个LS病人t细胞,b)构造的病人,c)健康的个人和d)在结节病病人的血。e) LS病人表现出更高程度的T-bet / RORγT co-expression比任何其他组(比较了使用双尾Mann-Whitney紫外线测试)。f)相比,没有明显的double-positive人口可以分辨血液的病人组中。
由T-bet Foxp3表达+但不是RORγT+CD4+t细胞
验证T-bet / RORγT co-expression CD4细胞+t细胞并不是随机或非特定的、forkhead盒蛋白3 (FoxP3)包含在细胞内染色面板。几乎所有FoxP3+在T-bet细胞被发现+人口(图S4a),而RORγT+t细胞大体上没有表达FoxP3(图S4b)。总的来说,只有百分之几的CD4细胞+BALF中t细胞表达FoxP3(在构造在LS平均6.1%,6.8%,4.7%其他疾病患者和5.6%在健康个体),和病人组之间没有明显差异(图自己)。
同时CXCR3和BALF中CCR6 CD4的表达+t细胞
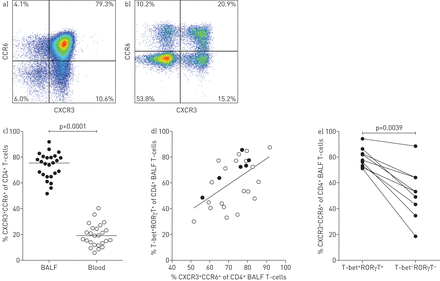
CD4的加强我们的发现+t细胞的肺结节病病人分享功能不同的血统,我们分析了表达式的Th1和Th17-associated趋化因子受体CXCR3和CCR6,分别与Th2-associated CCR4。我们发现,大多数CD4细胞+BALF中t细胞(平均75.3%),但是只有一小部分的血液(平均19.1%)中的CXCR3和CCR6 (图3一- - - - - -c)。CXCR3和CCR6是表示与CCR4(图S5a b)。同时表达CXCR3与T-bet CCR6相关/ RORγT co-expression,和LS患者尤为明显(图3 d)。此外,co-expression CXCR3和CCR6 T-bet更高+RORγT+比T-bet−RORγT−CD4+t细胞(图3 e)。
趋化因子受体CXCR3和CCR6中的更高程度的支气管肺泡灌洗液(BALF)比血,并与T-bet / RORγT表达式。代表流式细胞术散点图所示为辅助的同时表达(Th) 1 -和Th17-associated趋化因子受体CXCR3和CCR6,分别在BALF和b)结节病病人的血液。c) CXCR3 / CCR6 CD4的表达明显高于+BALF的t细胞比所有结节病病人血液(相比使用双尾Mann-Whitney紫外线测试)。健康个体的模式也是一致的,尽管平均较低同时表达。d)在洛夫格伦综合征(LS)(黑点)和构造病人(打开点),co-expression CXCR3和CCR6与co-expression T-bet和RORγT BALF CD4+t细胞(r = 0.4593, p = 0.0209使用非参数斯皮尔曼秩检验;线性回归R2= 0.2756,p = 0.0070)。e) CXCR3 / CCR6 co-expression也明显高于BALF T-bet+RORγT+比T-bet−RORγT−CD4+从同一个病人t细胞(而使用双尾Wilcoxon签署等级测试)。
T-bet+RORγT+CD4+t细胞增殖能力更高
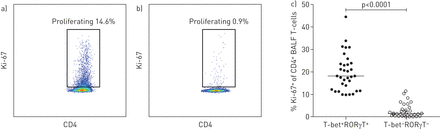
结节病病人,增殖(ki - 67的比例+T-bet)细胞显著增加+RORγT+室(图4一,c)、中值的18.1% ki - 67+细胞而T-bet为1.3%−RORγT−CD4+t细胞(图4 b,c)。这种模式也是一致的健康个体(数据没有显示)。此外,扩散是观察T-bet的比例更高+FoxP3+比T-bet+FoxP3−CD4+t细胞(图S4d)。之间没有显著差异可以观察到LS,构造和健康对照组增殖T-bet+RORγT+CD4+t细胞(数据没有显示)。
T-bet+RORγT+CD4+t细胞增殖能力高于相应的T-bet−RORγT−CD4+t细胞。代表流式细胞术散点图描绘ki - 67) T-bet表达式+RORγT+和b) T-bet−RORγT−CD4+在结节病病人的t细胞。c) T-bet+RORγT+CD4+t细胞增殖能力显著高于T-bet示威−RORγT−CD4+t细胞(相比使用双尾Mann-Whitney紫外线测试)。T-bet+RORγT−CD4+t细胞平均显示一个中间ki - 67表达,即。低于T-bet+RORγT+和高于T-bet−RORγT−CD4+t细胞(数据没有显示)。
TCR-restricted Vα2.3+Vβ22+CD4+t细胞co-express T-bet / RORγT和CXCR3 / CCR6
由于我们先前BALF CD4积累的结果+t细胞携带Vα2.3 / Vβ22细胞受体阳性的病人HLA-DRB1 * 03或HLA-DRB3 * 01 [2),与LS和预后良好(17),我们也调查T-bet和RORγT表达在这个特定族群。的患者纳入本研究,10 (6 LS和四个构造)Vα2.3的扩张+Vβ22+t细胞(定义为> 3乘以Vα2.3的平均百分比+Vβ22+CD4+t细胞在一个健康的人,即。> 0.5%的CD4细胞+t细胞(2])。其中,表示T-bet和RORγT平均85.0%,相比之下,71.4%对应的Vα2.3−Vβ22−CD4+t细胞(图S6a, b)。此外,co-expression CXCR3和CCR6观察Vα2.3比例更高+Vβ22+t细胞比Vα2.3−Vβ22−Vα2.3 t细胞(图S6a, c)+Vβ22+的表达明显高于t细胞也显示T-bet(图S7a)特别是RORγT(图S7b),当单独考虑。
IL-17A更高,il - 10、il - 22生成时,在LS - 2和降低IFNγ生产BALF细胞
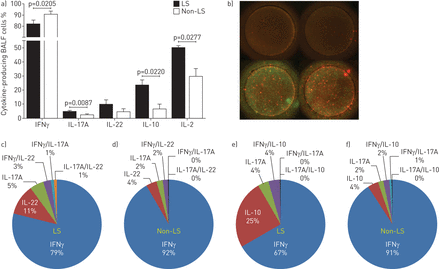
IFNγ是占主导地位的BALF细胞产生的细胞因子从LS和构造的病人,以FluoroSpot回应anti-CD3 / anti-CD28刺激(图5一个,b),但IFNγ-producing细胞的百分比显著低于LS比构造患者(p = 0.0205)。相比之下,LS患者有显著提高细胞的比例生产IL-17A (p = 0.0087), il - 10 (p = 0.0220)和2 (p = 0.0277),以及il - 22生成生产增加的趋势(p = 0.1865) (图5一个)。IL-17A, il - 22生成和细胞因子il - 10总构成明显更大的部分池LS(平均为5%、11%和25%,分别占总生产)比构造(分别为2%、4%和4%)(图5 c- - - - - -f)。IL-17A增加的趋势,il - 10、il - 22生成和- 2,并降低IFNγ生产LS与构造也在考虑spot-forming细胞的绝对数量一致,尽管差异没有达到统计学意义(图S8a)。无显著差异可以观察到LS和构造之间的同步生产IFNγ和2(图S8b)。
洛夫格伦综合征(LS)支气管肺泡灌洗液(BALF)中细胞产生一系列范围更广的辅助(Th) 17个细胞因子和低水平的干扰素(IFN)γ比构造BALF细胞。)FluoroSpot分析BALF细胞细胞因子的生产表现出显著降低的百分比IFNγ-producing细胞LS (n = 4)与构造患者相比(n = 6),和一个更高比例的白介素(IL) -17 -, IL - 10, IL-2-producing细胞(所有使用双尾比较t检验)。数据意味着±扫描电镜。b)代表的图像显示了重复如果BALF细胞从一个LS病人,以及与anti-CD3 / anti-CD28刺激后。IFNγ生产绿色所示,在红色和il - 22生成IL-17A橙色(显示为蓝色分析中有关酶联免疫斑点v.7.0援助iSpot软件(Autoimmun Diagnostika GmbH, Strassberg,德国))。cytokine-producing细胞的平均分布在两个病人组作为分析饼图所示组合c, d) IFNγ/ IL-17A / il - 22生成和e, f) IFNγ/ IL-17A / il - 10。生产的每一个细胞因子表达所有cytokine-producing细胞的比例,达到100%。
T-bet+RORγT+CD4+t细胞产生IFNγIL-17A或两者兼而有之
按照FluoroSpot数据,anti-CD3 / anti-CD28-stimulated BALF CD4细胞+t细胞表达T-bet和RORγT IFNγ为主,而且IL-17A,以流式细胞术(图6- - - - - -e)。除了预期的模式通过T-bet IFNγ生产+细胞(图6)和IL-17A RORγT+(图6 b),所有IL-17A-producing T-bet细胞被发现+室(图6 c),几乎所有IFNγ-producing RORγT细胞+(图6 d)。此外,IFNγ+IL-17A+,IFNγ+IL-17A−和IFNγ−IL-17A+在T-bet细胞都观察到+RORγT+t细胞人口(图6 e)。
T-bet+RORγT+CD4+t细胞产生干扰素(IFN)γ,白介素(IL) -17一个或两个。代表流式细胞术散点图里,大门在支气管肺泡灌洗液CD4细胞+t细胞显示)通过T-bet IFNγ生产+细胞,b)通过RORγT IL-17A生产+细胞,以及c)通过T-bet IL-17A生产+细胞和d)通过RORγT IFNγ生产+细胞。e)此外,当闸门T-bet和RORγT其次是后续控制IFNγ和IL-17A IFNγ+IL-17A+,IFNγ+IL-17A−以及IFNγ−IL-17A+在T-bet细胞都观察到+RORγT+CD4+t细胞的数量。
更高水平的T-bet+RORγT+CD4+t细胞与nonchronic疾病
33名患者参加的研究中,12名患者可以清楚地定义为“nonchronic”(没有病理变化和临床症状发病2年内)或“慢性”(与持久性的疾病超过2年之后第一次影像学变化观察)。nonchronic疾病患者表现出更高比例的BALF T-bet+RORγT+CD4+比慢性疾病患者t细胞(图7)。细胞因子的生产信息可供太少时这些主题的可靠的统计分析,趋势降低IFNγ和更高的IL-17A, il - 22生成时,BALF中il - 10 - 2生产nonchronic患者仍然可以分辨(数据未显示)。
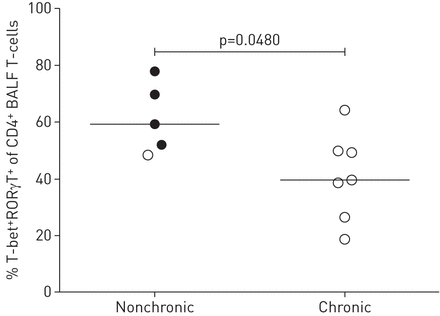
T-bet+RORγT+CD4+t细胞与nonchronic疾病。分层的洛夫格伦综合征(LS)(黑点)和构造病人(打开点),在他发病的可能确定(n = 12),到nonchronic或慢性疾病显示明显高于co-expression T-bet和RORγT解决疾病患者(相比使用双尾Mann-Whitney紫外线测试)。
讨论
尽管主要特征相似性等结节病肉芽肿的形成和BALF CD4 / CD8比值升高,LS和构造病人在症状性疾病表现和进展明显不同。事实上,LS甚至被建议考虑作为一个单独的疾病(13]。本研究的力量因此两患者亚组之间的歧视,以及执行的全面分析体外,细胞内的蛋白质含量和功能研究细胞因子的生产和肺细胞的增殖。在这里,我们显示,伴随的表达式的Th1和Th17转录监管机构T-bet CD4 RORγT+BALF中t细胞,但不是血液,结节病病人,描绘的优惠co-expression CXCR3和肺CD4 CCR6+t细胞。此外,我们展示的水平明显高于T-bet+RORγT+CD4+t细胞在LS与构造相比,在LS更广泛的细胞因子分布,显著提升T-bet协会/ RORγT表达式nonchronic疾病。
我们发现增殖能力和整体相比BALF中细胞因子的生产是提高所有结节病病人血液,表明CD4的激活+t细胞在肺部,之前报道(18]。
先前的研究描述了高架T-bet表达式在结节病病人与健康对照组相比,但没有指出LS和构造的区别,或疾病的阶段19]。这里,轻微但显著增加T-bet蛋白表达在LS耦合RORγT表达有着明显的区别,以及同时T-bet和RORγT的表情。稳定的同时表达T-bet RORγT回应在体外IFNγ/白介素刺激据报道[7),但在这里我们展示co-expression这些转录因子的一个组织体外设置未经刺激,表明先前的激活触发因素(s)在肺。Th1 / Th17 LS患者表型出现更加明显,通常有一个有利的疾病表型,和更高的T-bet / RORγT表达式与nonchronic疾病相关课程。lexberget al。(7]之前建议结合Th1和Th17效应能在单细胞水平具有生理优势,和这样的细胞可能在策划疾病更有效的决议。我们的发现这条线平行的推理,因为高度的增殖和高架co-expression CXCR3和CCR6 T-bet+RORγT+细胞意味着一个强有力的效应子集。最近,与Th17和Th22分化通路相关的基因被确定在LS患者中,但不是在那些构造(12),暗指一个更大的“Th17-like”反应在LS的影响。构造患者还发现基因的异构比LS患者(12),同时与这里给出构造转录因子表达的变化。
有趣的是,最近的一份报告发现IFNγ-producing Th17-polarised (Th17.1) BALF细胞结节病病人基于趋化因子受体表达(11]。我们的研究证实,Th1 / Th17细胞混合丰富的肺结节病病人,IFNγ主宰BALF细胞因子配置文件,而IL-17A产生程度较轻。然而,我们区分LS和构造的病人提供了一个比较的机会,之前没有可能的,例如,在研究Ramsteinet al。(11)所有的病人建立了慢性疾病或定义为构造。同样,我们更广泛的Th17-associated细胞因子的分析,以及转录因子和趋化因子受体的表达,可能导致不同的解释。而非致病性,IFNγ-induced Th17-to-Th1过渡t细胞表型,我们提出一个潜在的保护作用的Th1 / Th17细胞和Th17-associated肺细胞因子,和积极参与的一个塑料混合子集Th1和Th17细胞的功能特征。
在这项研究中,我们发现的比例明显高于Th17-related细胞因子,在LS IFNγ的频率较低。减少IFNγ和il - 10水平升高在LS与先前的研究一致的mRNA表达[20.,21),增加IL-17A生产(8]。考虑疾病在LS,观察到的细胞因子的生产模式表明,细胞因子的组合与不同的属性是有益的解决疾病而IFNγ孤单。LS - 2表达增加患者可能与调制Th细胞分化和增殖和高架T-bet表达(22),以及扩张已经建立Th17反应(23),从而导致了隐含的有利作用的细胞因子的肺。
当前的知识概述了塑料Th17子集,不稳定的表型,在微环境因素的影响。对小鼠的研究已经确定了“致病”和“不致病的”Th17细胞(24),后者由RORγT+优先的细胞产生il - 10和有更多监管的作用,特别是在粘膜组织(25]。在肺,IL-17——和IL-22-producing细胞与保护性免疫反应对几个相关病原体(26,27]。增加抗原IL-17A——IL-22-producing CD4的频率+记忆t细胞也在健康个体暴露结核分枝杆菌与感染患者相比(28]。此外,il - 22生成水平减少慢性结节病和特发性肺纤维化患者29日]。虽然anti-IL-17治疗表明承诺在慢性炎症性疾病,如风湿性关节炎(30.和牛皮癣31日),Th17反应的异质性在结节病复杂预测任何潜在的疗效。虽然IL-17与肉芽肿形成(10),高浓度的其他Th17-associated细胞因子il - 10、il - 22生成等nonchronic疾病建议组织本地化和平衡这些细胞因子影响疾病的结果,从而对治疗的反应。
在人类中,多功能Th1 / Th17效应CD4细胞+描述了t细胞在一些自身免疫条件(3- - - - - -5]。有趣的是,LS显示特征的自身免疫的临床表现,和我们组的近期数据显示波形蛋白作为一个潜在的自身抗原(2]。在这种背景下,TCR Vα2.3 / Vβ22-expressing CD4+t细胞是特别感兴趣的,因为他们似乎经历了克隆扩增后识别的特异性抗原在HLA-DRB1 * 03 (2]。的发现Vα2.3+Vβ22+细胞co-express T-bet RORγT以及CXCR3和CCR6程度高于相应的Vα2.3−Vβ22−CD4+t细胞增强之前报道的这些细胞分化效应细胞(2,32,33]。T-bet的高表达,在Vα2.3 RORγT+Vβ22+t细胞也支持T-bet的参与+RORγT+细胞疾病决议,更高频率的TCR-restricted细胞与更多的快速复苏17]。
它也是有趣的发现几乎所有BALF FoxP3+细胞内T-bet+隔间。T-bet表情一直在观察亚群有选择地调节Th1-driven炎症(34,35),以及在效应t细胞激活(36]。亚群缺乏T-bet和GATA-3也缺乏抑制能力,导致自身免疫(37]。高增殖T-bet的状态+FoxP3+细胞表明一个激活的细胞群,进一步掀起T-bet不仅在效应反应,而且在lung-specific免疫调节和预防有害自身免疫反应。
我们建议在CD4激活+在结节病t细胞,细胞因子身份部分取决于监管元素不同于转录“主监管机构”,并且T-bet和RORγT转录项目下游功能相关性疾病的结果,不仅仅依赖于细胞因子的生产。在某些情况下,这样的功能可以限制到肺部和相关,例如,迁移和细胞因子交付(由CXCR3指示/ CCR6 co-expression)或生存38]。此外,增殖T-bet的存在+RORγT+和T-bet+FoxP3+CD4+BALF中t细胞健康个体,以及提升T-bet / RORγT表达式解决疾病患者,肺组织内稳态表明积极的贡献。
这项研究的一个重要限制是不完整的纵向病人随访,以验证T-bet的角色+RORγT+t细胞的疾病。后所有病人从疾病发生在两年的积分,然而,超出了这个研究的范围,但应重新审视未来的一个话题。然而,当前的12例临床评估提供了一个指示这些细胞可能的角色在促进疾病的决议。理想的第二项研究应该解决长期疾病发展,目标是相关免疫参数在发病时间分辨率,响应性治疗对慢性(如果适用)和倾向。
而言,体外分析、细胞内染色的过程带来预期的限制,可行的细胞不能排序基于转录因子表达为进一步功能调查。此外,结节病的动物模型建立的缺乏限制了能力跟踪起源、迁移、功能可塑性和T-bet的寿命+RORγT+t细胞在活的有机体内,或者至少体外的疾病,这将提供最准确的表示这些细胞如何影响疾病的结果。
结束语
我们的发现表明肺微环境有利于Th1 / Th17表型,这些细胞,以及广泛的Th17细胞因子,与疾病表型有益肺结节病。这些结果努力增加临床及免疫学LS和构造之间的差异的理解,和对未来可能影响诊断和预后的应用在临床设置。
确认
作者感谢研究护士船舷上缘德森林Margitha达尔,海琳Blomqvist和生物医学分析贝妮塔Dahlberg优秀的援助在样本收集和准备(所有呼吸医学部门,卡罗琳斯卡大学医院桑纳,斯德哥尔摩,瑞典)。也得益于基督教Smedman Staffan保利和特蕾莎engtsson Mabtech AB (Nacka链、瑞典)富有成果的讨论,在阅读FluoroSpot板块协议修改和有价值的帮助。
作者的贡献如下。概念和研究设计:y .凯撒,r . Lepzien a Smed-Sorensen和j . Grunewald。数据收集:y .凯撒,r . Lepzien Kullberg和雷欧。执行实验:y凯撒和r . Lepzien。分析和解释:y凯撒,r . Lepzien s Kullberg a Smed-Sorensen和j . Grunewald。手稿准备:y Kaiser r . Lepzien a Smed-Sorensen和j . Grunewald。批判阅读手稿和知识评估:y凯撒,r . Lepzien Kullberg,雷欧,a Smed-Sorensen和j . Grunewald。所有作者阅读和批准最终的手稿。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:金融支持研究资助的形式收到瑞典心脏肺脏基金会,瑞典研究理事会垫Kleberg基金会国王奥斯卡二世禧基金会,斯德哥尔摩郡议会,瑞典胸部医师协会和卡罗林斯卡医学院。为这篇文章一直存放在资助信息FundRef。
利益冲突:没有宣布。
- 收到了2016年1月13日。
- 接受2016年3月29日。
- 版权©2016人队