摘要
本综述概述了肺通气/灌注比与气体交换的关系,强调了基本概念,并将其与临床情况联系起来。对于每个气体交换单元,肺泡和流出血液中氧气和二氧化碳的分压(PØ2和P有限公司2)是由肺泡通气与血液流量的比率(V“一种/ Q)。分流器和低V“一种/ Q地区就是两个例子V“一种/ Q“错配是低氧血症最常见的原因。”扩散限制,低通气和低灵感PØ2造成低氧血症,即使在没有V“一种/ Q′不匹配。与其他原因相比,分流引起的低氧血症对补充氧气的反应较差。气体交换单位很少或没有血液流动(高V“一种/ Q'区)导致肺泡死腔,增加通风浪费,即高效二氧化碳去除更少。由于呼吸驱动,以维持正常的动脉P有限公司2在美国,浪费通风最常见的结果是增加了微小的通风和呼吸的工作量,而不是高碳酸血症。肺泡-动脉氧张力差、静脉混合液和浪费通气的计算提供了定量评估的影响V“一种/ Q气体交换“不匹配。该类型的V“一种/ Q“错配导致的气体交换障碍在不同的肺部疾病中表现不同。”
摘要
综述呼吸-灌注关系、气体交换、基本概念及其与临床的关系http://ow.ly/wMUwq
介绍
虽然健康的肺高效地交换呼吸气体,低氧血症和高碳酸血症表示病理生理学和肺不能提供足够的气体交换。的气体被转移如何理解和低效的气体交换的原因是中央的照顾患者肺部疾病。在这篇文章中,我们将回顾气体交换的正常和病理机制。用简单的启动和建设更复杂,我们将强调基本概念和它们与熟悉的临床案例场景。
肺的结构
肺的结构非常适合有效地交换呼吸气体。通过气道和血管树,新鲜气体和静脉血被输送到大肺泡毛细血管表面并被移出。在成人中,吸入的空气进入气管的截面积约为3厘米2并输送至肺泡与~140 m的表面区域2,大致有一个网球场那么大[1]。同样,肺血管树以肺动脉为主,反复分叉为小动脉和毛细血管,覆盖肺泡表面85-95% [1]。异常薄膜只有1μm [2,3]分离肺泡气舱和血液舱,从而允许气体在它们之间迅速扩散。由于肺泡毛细血管内的相对大的血液体积,血液流动减慢和渡越时间为血液增加,通常以0.25〜0.75 S,从而允许气体交换更多的时间。显着的设计,其允许该气体交换系统到在胸腔内来构建由该工程技艺进行比较来折叠的信已突出显示,以便它装配到一个顶针[3]。
单肺单位
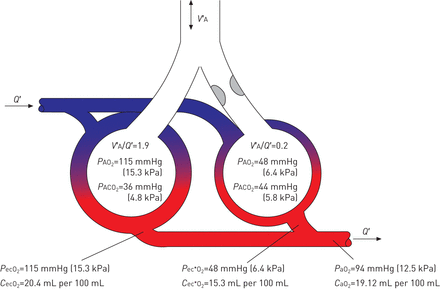
我们从一个简单的肺模型开始,它只包含一个气体交换单元(图1一个)。该单元的毛细管提供混合静脉血带O的低分压2(PVO2). O的分压2(PØ2)肺泡气体(PAO2)比毛细血管里的血要高得多2在毛细血管通过的过程中被动地从肺泡腔扩散到血液中(图。2A)。肺泡气体和血腔之间的隔膜对血液扩散的阻力很小PØ2在末端毛细血管血(P生态2)以达到平衡PAO2在血液离开单位之前。的动脉血氧因此,主要取决于PAO2。注意,在这个理想化的肺单位有什么区别PAO2和PØ2动脉血(PAO2)。至于原因,后面解释,肺泡 - 动脉Ø2张力差异(PA-aO2)在评估临床医学中气体交换问题的原因时非常有用,我们将在整个综述中使用它。虽然“梯度”一词也常被使用,但我们更喜欢用“差异”来强调两者之间的差异PAO2和PAO2不是由于它们之间的压力梯度。CO的分压2(P有限公司2)在混合静脉血(Pv¯有限公司2)比肺泡气体(PACO2因此,在肺泡-毛细血管膜上的扩散,导致了与O相反方向的净流动2从血液到肺泡气体(图2 b)。结果又是平等的P有限公司2肺泡气和最终毛细血管血(在PecCO2),因为扩散电阻是即使对于CO更少2比阿2。由于在用于O-分压和血液含量之间的关系的差异2和有限公司2,有大约尽可能多的CO2交换了5毫米汞柱(0.7 kPa)的混合静脉和动脉血的分压差,因为有O2用60毫米汞柱(6.7千帕)的差交换。O含量2血液中携带的血红蛋白是由血红蛋白浓度决定的,即血红蛋白结合O的比例2和PAO2(图1 b)。当我们在下面讨论多个肺单位模型时,重要的是要理解毛细血管末端的血供2内容(C生态2而不是P生态2中,来自不同单位是添加剂。
a)分压、气体和O的分数的符号说明2用于在单个肺单元不同的隔室,如在定义的内容表1。注意,对于一个单一的单元肺模型,动脉和最终毛细管值相等。b)在血红蛋白氧血红蛋白(Hb-O2)代表O的分压解离曲线2(PØ2),O2饱和度和O2静脉和动脉间室的血红蛋白含量为15克·分升-1。

一种)PØ2以及O的扩散2沿着毛细管允许P生态2相等PAO2在血液离开单位之前。注意,结果是aPA-aO2零。b)P有限公司2以类似的方式示出。在两个面板图中的时间尺度是指经过时间的红细胞通过肺泡毛细血管,通常0.25-0.75秒。对于一个术语表,请参阅表1。
动脉血氧不足的五种原因
单一单位模型(图1一个)来开始我们的低氧血症五个潜在原因的讨论,以及高碳酸血症。我们的第一个例子是扩散限制之一。
扩散限制
在病例1中,一名25岁的男性精英自行车运动员在进行心肺运动研究时发现,随着工作量的增加,动脉低氧血症逐渐恶化(在正常人中未见这种反应)。运动结束时动脉血气(ABGs)为:pH 7.18,P有限公司2动脉血(PACO2)30毫米汞柱(4.0千帕),PAO281毫米汞柱(10.8千帕)和动脉血红蛋白O2饱和度88%。
运动增加O的量2从动脉血液中的循环,这趋向于降低提取PVO2. 这个refore, more O2需要在肺中被吸收才能达到正常的动脉血氧合。运动还能增加肺部的血流量,从而缩短血液接触肺泡气体的时间。综合效果是更多的O2采取了在更短的时间需要(图3)。在心脏输出量非常高的情况下,过境时间可能太短,无法完全达到平衡PAO2和P生态2。这代表扩散限制低氧血症在运动员的原因实现极高心脏输出[4-6]。由于扩散限制而引起的低氧血症也可以在高原运动的正常人身上看到。在这种情况下,O的驱动压力2扩散由于能量较低而减少PØ2在灵感的空气中(PIO2)在海拔和血液通过肺泡毛细血管的时间较短,因为较高的心输出量。肺间质性疾病患者也可能出现弥散受限。患有这些疾病的病人可能有一个正常的PAO2在休息时,在运动时出现低氧血症,这可以解释为通过加厚的肺泡-毛细血管膜扩散的阻力增加的综合效应,减少PVO2和缩短的过境时间[7]。
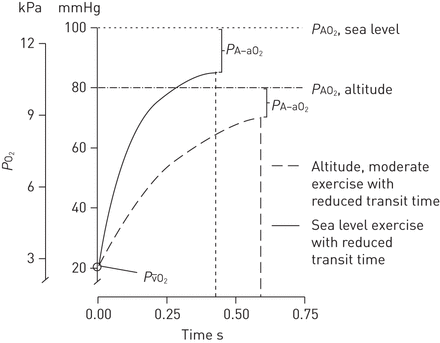
扩散限制是低氧血症五个原因之一(表2)。缺乏之间的平衡PAO2和P生态2创建一个增加PA-aO2。低氧血症在这些患者中,作为一项规则,很好地回应以补充Ø2。虽然这并没有纠正扩散限制,但它提高了PAO2和用于O-的扩散的驱动压力2进入血液。由于CO的扩散阻力小2,PACO2O型血患者是否正常2扩散限制。虽然扩散限制是我们的第一个原因在上市低氧血症表2从临床角度看,它是一个低的罕见原因PAO2。
通气不足
在第二种情况下,一个82岁的女性患有慢性肾功能衰竭腹膜透析(CAPD)最近从她的孙子染上百日咳。她的医生处方的含阿片样物质镇咳减少咳嗽。她现在昏昏欲睡,无法管理CAPD程序。一个ABG分析显示pH值7.17,PAO245毫米汞柱(6.0千帕)和PACO277毫米汞柱(10.3千帕)。
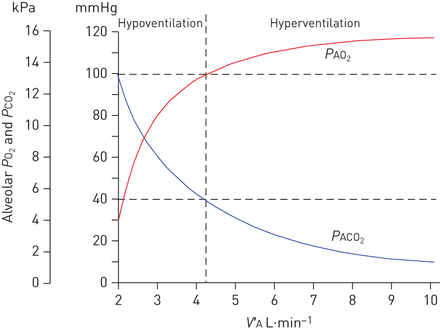
这种情况下凸显通气不足为低氧血症的原因。尽管定量关系是复杂的[8,9,这是可以直观理解的PAO2在我们的单牙槽骨单位(图1一个)受到O之间的比值的影响2交付(通风,V“一种)和O2去除(血流量,Q′)。因此,是的一个行列式PAO2是通风和血流量(之间的平衡或比值V′一种/ Q′)。在从壳体2,通气不足和正常血流导致低的患者V“一种/ Q’比率(较少的分娩和未改变的O2),这降低了PAO2因此P生态2。相反,过度通气(相对于血流的通气增加)增加PAO2和P生态2。PACO2也通过确定V“一种/ Q但CO2通过血流和CO输送2是通过通风换气,O2。因此,降低V“一种/ Q比例越高,结果越好PACO2和PACO2的标志,而增加的比例降低PACO2. 这个小号e relationships are illustrated in图4. 这个balance between O2交付和移除的结果是aPAO2可以使用肺泡气体方程(被量化箱1)。
甲亢和通气不足的影响PAO2(红色)和PACO2(蓝色),因此,也是onPAO2和PACO2如果没有其他V“一种/ Q这种不匹配是存在的。虚线表示的是V“一种,PAO2和PACO2. 这个diagram is derived assuming unchanged cardiac output, O2消费和一氧化碳2制造具有混合静脉值与变化而变化PAO2和PACO2。肺换气不足,PVO2和Pv¯有限公司2分别低于正常水平和高于正常水平。请注意V“一种对应于变化V“一种/ Q因为血流量(心输出量)保持恒定。因此,减少通风(低V“一种/ Q′比率)导致PAO2和PACO2在过度换气时向混合静脉值移动PAO2和PACO2为了他们的价值观。因此,低通气会导致低氧血症和高碳酸血症。增加FIO2结果是一个向上的偏移PØ2曲线时,P有限公司2曲线保持固定。在这个情况下,PACO2即使没有低氧血症也可能很高。对于一个术语表,请参阅表1。改编自 [10]。
因此,低氧血症是由低通气引起的PAO2并且是低的第二个原因PAO2上市表2。因为通过肺泡 - 毛细血管膜没有气体交换的障碍,PAO2和PAO2同样是减少的PA-aO2是正常的低氧血症由于低通气。在case 2中,肺泡气体方程(箱1)导致的估计PAO253毫米汞柱(7.1千帕)PA-aO2∼7 mmHg (0.9 kPa),正常值。由于换气不足引起的低氧血症可以通过补充氧来解决2,增加PAO2即使通气不足遗体纠正。Ø的一个重要方面2在这种情况下的治疗是,低通气,同时呼吸空气,将导致严重的低氧血症之前PACO2上升到危险的高水平。相反,提供补充的O2会导致PAO2和PAO2被保持在高于90毫米汞柱(12千帕),即使通气不足引起严重的高碳酸血症。临床上重要的必然结果是正常的脉搏血氧仪在患者呼吸空气读书是保持足够的通风良好的指示(正常PACO2)。然而,当患者在补充Ø2,正常的O2饱和度,不能用来判断通风是否足够。
低吸气氧分压
在情况3,一个21岁的很合身,登山通知,在上升的同时勃朗峰(4810米),她的手指头也青了,她的血红蛋白Ø2饱和度为65%。
虽然O的分数2在空气中,气压总是为0.21,在高海拔地区,气压的下降导致气压成比例地下降PIO2。使用肺泡气体方程(箱1)、与高度相符的气压(420毫米汞柱(56千帕))、通风系统无变化(PACO240毫米汞柱(5.3千帕))和0.8的R的预期结果PAO2在~28毫米汞柱(3.7千帕)和严重低氧血症勃朗峰的顶部。低PIO2,在高海拔或吸气时2分数 (FIO2) <0.21,因此是低氧血症的另一个原因。肺泡-毛细血管膜的气体交换也是正常的。低氧血症的原因减少了PAO2因此,PA-aO2是正常的。这怎么可能,然后登上勃朗峰?低氧血症增加呼吸驱动力,从而增加总V“一种/ Q比率和O2输送到肺泡,部分纠正PAO2和PAO2(图3)。增加通气导致低碳酸血症,定义为PACO2<40 mmHg (<5.3 kPa)。最近从在珠穆朗玛峰峰顶呼吸空气的登山者身上采集的ABG样本揭示了一种平均值PAO225毫米汞柱(3.3千帕PACO213毫米汞柱(1.7千帕)[11]。的第二种方法加注PAO2提高PAO2呼吸是辅助的吗2。大多数登顶珠峰的登山者都使用补充氧气2。
两肺模型
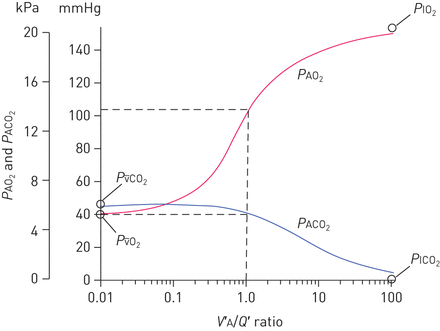
对于低氧血症的剩下的两个原因,两个示例的V“一种/ Q与之不匹配的是,我们必须转向多单元肺模型。肺的解剖结构具有多个平行的气体交换单元,在设计和气体交换能力方面令人着迷,但这也为区域内不均匀和不同的通气和血流分布提供了条件。如果局部通气和灌注不完全匹配,即每个单元的总血流和总通气的比例不相等,V“一种/ Q'比率将肺部区域之间变化,他们每个人都会有不同的PAO2和PACO2气体交换的效率也会降低。图5示出的范围PAO2和PACO2作为它们的函数的单位V“一种/ Q'比。为了证明气体交换如何变得效率较低具有不同的单位V“/ Q我们将从一个简单的两单元肺模型开始。
PAO2和PACO2与变化V“一种/ Q,在假设为正态值的情况下PIO2(150毫米汞柱(20千帕)),PVO2(40毫米汞柱(5.3千帕))和Pv¯有限公司2(45毫米汞柱(6千帕))。这些假设是不现实的,因为整个肺的变化PAO2和PACO2会引起混合静脉值的二次变化(图4在这方面是否更现实),但该图说明了V“一种/ Q肺泡和最终毛细管分压为在当总通风到血液流动足以维持正常混合静脉值的情况区域肺单位'比。需要注意的是降低V“一种/ Q比值低于~ 1的正常值会导致急剧下降PAO2和较少增加PACO2,两者接近混合静脉值显示在最左边。增加V“一种/ Q′比原因PAO2增加,PACO2降低,接近最右边显示的激发值。对于一个术语表,请参阅表1。改编自 [10]。
低V“一种/Q′单位
在病例4中,一位67岁患有严重肺气肿的女性的ABG值为7.35,PAO25mmhg (7.3 kPa)PACO2呼吸空气时5mmhg (7.3 kPa)。与补充啊2在3 L·分钟-1,血红蛋白Ø2脉搏血氧饱和度从87%提高到93%。
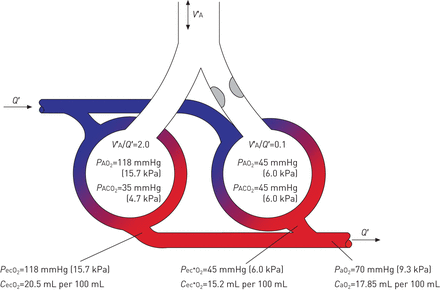
图6示出的血流,但通风的不均匀分布于两个单元的均匀分布,使得一个单元具有一个V“一种/ Q“这个比例是2.0,而另一个单元的比例是0.1。低V“一种/ Q比例低的结果PAO2在这个单位,因此,低O2内容和P生态2因为血液离开了这个单位。注意,这种效应与案例2中的低通气患者相似,但在本例中,它仅与肺的一部分有关。血红蛋白在正常状态下几乎完全氧化V“一种/ Q’比值意味着相对过度通气(高V“一种/ Q的比例),而另一个单位的结果只是略有增加O2离开本单位的血液含量。还要记住O2的动脉血液含量(CAO2)通过O的流量加权平均值来确定2内容,而不是局部的压力,用于从不同的单位的血液。低的整体效果V“一种/ Q因此,单位就被简化了PAO2并增加PA-aO2。低V“一种/ Q'单元是,因此,低氧血症的第四原因(表2)。低的影响V“一种/ Q′单位上PACO2与在效果少相比PAO2,因为公司2消除在所述单元具有高增加V“一种/ Q'比。在患者低V“一种/ Q区域,高碳酸血症也可以通过增加通气反应来预防PACO2。因为低V“一种/ Q“事实上,各个区域都是通风的,这对动脉氧合的不利影响可以通过增加空气流量来抵消。FIO2,从而增加PAO2,即使在低V“一种/ Q′地区。低V“一种/ Q因此,单位,不能是唯一的原因,低氧血症的患者没有反应增加FIO2。
分流器
在壳体5中,32岁的男性患有严重急性呼吸窘迫综合征(ARDS)继发性细菌性肺炎具有ABG上与机械通气FIO20.80,揭示了pH值7.28,PAO267毫米汞柱(8.9千帕)PACO261毫米汞柱(8.1千帕)。
图7显示一个单元没有任何通风,因此它不能参与气体交换的情况。因此,流经这个单元的血液构成了肺内分流。分流器可以看作是范围的一个极端V“一种/ Q比率为0。从这个单元流出的毛细血管末梢血流是一样的P生态2和C生态2当混合静脉血和来自其他单位的血液结合时,会减少动脉血的氧合。因此,分流是引起低氧血症的第五个也是最后一个原因(表2)。的CAO2还是O的流量加权平均值2从气体交换单元含量(C生态2)和分流的血液(Cec′O2)(图7)。分流量量化为心输出量的分数(Q“小号/Q“Ť)分配给nonventilated单元(框2)。对动脉血氧合的影响取决于这个分数和氧氧饱和度2的混合静脉血含量(CVO2)。对于一定大小的分流,降低CVO2会导致更糟糕的动脉氧合。干预的目的是增加混合静脉O2饱和度(小号VO2) (因此CVO2),例如提高CAO2通过增加血红蛋白浓度,降低O2消耗或增加心输出量,因此可能改善由大分流引起的低氧血症。然而,分流率已被证明随着心输出量的增加而增加[13,14];因此,这种干预可能会比预期的那么有效。增加PVO2和增加的肺动脉压,这会降低和抵消低氧血管收缩(稍后讨论),是推测性的解释为心输出量的上分流这种效果。
相比之下V“一种/ Q′区,分流增加FIO2在改善动脉氧合不太有效。随着分流,提高的效果FIO2是逐渐减少和非常大的分流,甚至FIO21.0具有影响不大PAO2. 这个reasons for the small effect are that raisedFIO2不能改善PAO2在不通风的单位,那一点额外的O2通过通风设备增加的血液流量不足以抵消血液分流的影响。变量之间的关系分流大小,FIO2和PAO2由异分流图中示出(图8)。大量肺内分流引起低氧血症的临床病例包括广泛的肺不张、严重肺炎和ARDS。在这种情况下,分流管可能超过肺总血流的50% [13,16-19]。心内从右到左的分流术也有同样的效果PAO2作为肺内分流。即使在正常的实验对象中,PAO2小于PAO2主要是由于2-3%的心输出量从右向左分流所致。其中大部分并不是严格意义上的肺内分流,而是将静脉血从支气管静脉和左心室底静脉加入动脉血中[12]。并联对CO的影响2交换讨论盒3。
死亡空间
在情况4的延续,67岁的女性重度肺气肿住院慢性阻塞性肺疾病(COPD)急性发作。ABG显示pH值7.21,PAO267毫米汞柱(8.9千帕)PACO285毫米汞柱(11.3千帕)。测量显示她的呼吸为12 L·min-1。
尽管每分钟通气量(V“Ë)大约是正常休息时的两倍,这个病人表现为PACO2,说明通气不足。这又如何解释呢?与每个灵感,在所有受试者中,潮气量的一部分(VŤ)被保持在传导气道中,因此,无助于气体交换。这个体积对应于解剖死空间,并且是约150ml(2-3毫升·千克-1)或正常的三分之一VŤ[12,21]。潮气量的正常死区分数(Vd/VŤ因此)是~0.3。图9说明两个单元具有相同的通风条件,但其中一个单元没有血流,因此构成肺泡死腔。一个临床原因可能是肺栓塞。肺泡死腔是指通气但无血流的气体交换装置V“一种/ Q比例是无限的。设备死区是指任何口罩、管道、等等它的功能就像解剖死亡空间的延伸。总死区(Vd)因此,由解剖死区、肺泡死区和任何器械死区组成。
分钟通气量是指每分钟呼出气体的总量,而有效肺泡通气量是指每分钟参与气体交换的气体量。相反,死区通风或浪费通风是总通风量的一部分,对气体交换没有贡献。通风浪费的这一部分通常表示为Vd/VŤ。有效肺泡通气量可以计算为V“一种= RR×(VŤ-Vd),其中RR为呼吸频率,或asV“一种=V“Ë×(1 -Vd/VŤ)。注意,有效的肺泡通气是由分钟通气和Vd/VŤ。增加Vd固有地意味着更大的分钟通气量需要维持有效的肺泡通气足够CO2去除。在增加Vd/VŤ不进行补偿性增加分钟通气导致减少PAO2和增加PACO2。在病例4中,高分钟通气不足以补偿增加的通气Vd/VŤ,从而导致高碳酸血症。增加PACO2也可能出现在那些镇静和机械通气的患者中,他们在设置新的肺栓塞时没有增加他们的分钟通气。
高V“一种/Q′单位
高V“一种/ Q“单元是根据血流比例过度通风的单元,例如,一个单元的通风为1 L·min-1但血流量只有0.1 L·min-1导致V“一种/ Q比率为10。虽然这个单位不代表肺泡死腔,但过多的血液流通会导致“死腔效应”,因为CO更少2会不会被抽掉一个通风高的V“一种/ Q的单位,而不是由通风更好的灌注区。由此可见,类似肺泡的死腔,增加了高V“一种/ Q'装置意味着需要更大的分钟通风以保持足够的气体交换。高V“一种/ Q“地区主要是由于低血流量正常通风的地方。这些区域的上ABGS的影响是小的,因为任何区域ABG组合物的贡献是流量加权。
两个以上单位的肺模型
到目前为止,我们关注的是一个或两个肺单位的模型。实际上,气体在整个肺内交换而产生PAO2和PACO2是由成千上万个不同单位流出的血液流量决定的吗V“一种/ Q′比率(图10)。[Riley称和Cournand[9的影响V“一种/ Q“气体交换的不匹配可以简单地认为是由三个不同的腔室组成的肺。V“一种/ Q'比例:一个隔室与理想V“一种/ Q′匹配(V“一种/ Q'= 1.0),一个完全没有通气(V“一种/ Q'= 0,分流器)和一个没有血流量(V“一种/ Q'=∞,死区)。
a)肺单位百分比(纵轴)不同V“一种/ Q“(横轴)在肺中的比率是一个整体V“一种/ Q'的1.0(每分通气量是相同的心输出量)。总体气体交换效率是通过跨不同的比例单元的传播确定的,与对应于具有1.0的比所有单元的分布很窄的最佳效率。该曲线示出了用具有比接近最佳大多数单位的正常的情况。单元向左虚线的具有低的比率,因此,有助于提高PA-aO2和静脉外加剂;这种影响随着偏离1.0的比率的增加而增加。虚线右侧的单元具有较高的比率,因此造成了通风的浪费;再一次,效果随着偏离1.0的比率的增加而增加。分流器和死区单元被绘制在水平轴的两个极端。b) R提出的三室模型说明iley称和Cournand[9为了量化V“一种/ Q“不匹配的静脉混合和浪费的通风。对于一个术语表,请参阅表1。
该模型是实际的,因为它是相对容易获得量化分流血流和死腔通气(在下面讨论)所需的测量。要明白,在计算假设中的作用是非常重要的V“一种/ Q“不匹配的PAO2和PACO2完全是由于分流和死腔通气,并且所有的气体交换与理想的单位发生V“一种/ Q'匹配。该模型没有反映真实情况,因为它忽略了与其他单位的气体交换V“一种/ Q′比率。
静脉混合
在三室模型中,分流血流的计算采用分流方程(框2)。计算出的分流管,或者更准确地称为静脉外加剂,相当于混合静脉血从右到左的分流管的数量,这将导致观察到的动脉氧合在低的情况下V“一种/ Q′地区。静脉混合的威力,因此,即使没有真正的分流器来增大。
使用所获得的值,而呼吸100%O2可以分化低氧血症由于低V“一种/ Q从一个真正的分流器的作用'区,因为从低的静脉混合V“一种/ Q“区是在这种情况下取消[12]。这种方法的一个问题是,呼吸100%O2由于吸收性肺不张,往往会增加分流量,使呼吸时分流度降低FIO2可能高估了。分流也可用在血液中溶解度低的惰性气体来测量[17,22]。值得注意的是,这种方法也不同于静脉混合物的计算,因为它排除了静脉血经肺、支气管静脉流入动脉血后的分流作用。
浪费通风(生理死区)
根据R的三室模型iley称和Cournand[9],生理死空间或浪费通风对应于总的死空间会导致CO的所观察到的损伤2消除(盒3)。我们更喜欢用“浪费通风”,因为它更好地描述这个数量的含义。在正常肺,浪费通风密切对应于解剖死腔。除了解剖死腔,浪费通风也从任何设备,肺泡死空间和很高的成绩V“一种/ Q' 单位。从分流区域的血液将有PecCO2等于混合静脉值,它升高PACO2并由此计算出的被浪费的通风;这已经创造了分流死角[21]。这是使用的效果PACO2代替PACO2;因此,尽管不增加死空间或高的效果V“一种/ Q“区域,它确实代表受损的CO2消除(23]。如上所述,有效的肺泡通气等于分钟通气减去浪费的通气。每分钟通风7.5 L·min-1和正常Vd/VŤ结果:有效肺泡通气5.25 L·min-1。慢性肺病可能增加Vd/VŤ到≥0.8;在这种情况下,≥25升的分钟通气·分钟-1需要的5 L·分钟的有效肺泡通气-1。浪费的通风措施,因此,估计效果V“一种/ Q“保持足够的气体交换所需的分钟通风不匹配。虽然没有测量,但对于病例4的患者来说,增加了PACO2尽管通风时间很长,但最可能的原因是浪费了大量的通风。
因为控制呼吸的目的是维持正常PACO2,浪费通气的增加需要增加分钟通气来维持不变的有效肺泡通气。因此,在大多数情况下,通风浪费增加的第一个后果并不是PACO2而是一种细微的换气方式的改变,因此也改变了呼吸的工作。慢性高碳酸血症可以被视为一种适应性反应,因为它意味着CO2移除可以通过较低的分钟通气来维持,从而减少呼吸的工作量。
潮汐末的动脉P有限公司2区别
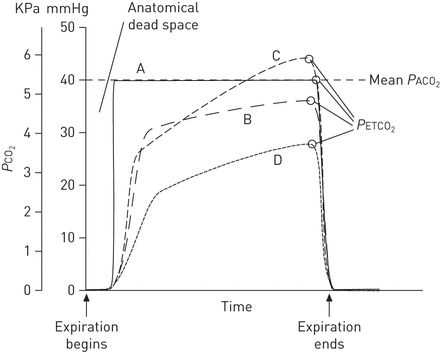
生理死腔式(盒3)之间的区别PACO2和P有限公司2混合呼出气体的(PECO2)来计算浪费通风的总分数。相比之下,之间的区别PACO2和P有限公司2混合呼出肺泡气排除的解剖和装置死空间,因此效果,估计高的程度V“一种/ Q“和肺泡死腔的区域。因为呼出的最后一部分VŤ由肺泡气体(4盒),end-tidalP有限公司2(PETCO2)可以用作混合替代测量PACO2. 这个PACO2-PETCO2因此,差异与死区和浪费的通风设备有关[28-30.]。值得注意的是,在记忆生理死亡空间方程时,模型研究表明(PACO2-PETCO2)/PACO2肺泡死腔率与肺泡死腔率的线性关系是否大于简单关系PACO2-PETCO2[29,30.]。虽然依赖于,例如,年龄,吸入/呼出的气体体积和通风模式中,一个PACO2-PETCO2<5 mmHg (0.7 kPa)被认为是正常[31,32],并由PETCO2少数正常受试者接近36毫米汞柱(4.8千帕)[33]。PACO2-PETCO2已被证明与急性呼吸窘迫综合征动物模型中的肺泡死腔分数和肺泡募集相关[34]。PETCO2在被示出图11并在4盒。
二氧化碳描记图显示P有限公司2呼出气体的(垂直轴)与单次呼气时的时间(横轴)。曲线A对应于单个肺单元模型的理论曲线,在该模型中,第一部分呼气仅由解剖死腔气体组成,没有CO2和呼出肺泡气的其余部分具有均匀的P有限公司2等于PACO2。在这个单单元模型中,PETCO2=PACO2=PACO2。曲线B对应的是一个正常数量的健康人的capnogramV“一种/ Q“不匹配。需要注意的是会有的差异小PETCO2(以开放圆圈标示)及PACO2。曲线C说明了如何增加V“一种/ Q′导致P有限公司2在整个呼气过程中增加呼出气体的量。在这种情况下PETCO2甚至超过了PACO2并有可能PACO2。虽然这是不常见的,它可以发生与缓慢呼气大VŤ或最大运动量。曲线d示出了具有增加肺泡死空间的情况下,导致之间增加的差PACO2和PETCO2,这可能见于肺栓塞患者。对于一个术语表,请参阅表1。
高低结合的效果V“一种/ Q′地区
与最优比较V“一种/ Q'匹配,要么区域通风或血流的重新分配必须导致低和高V“一种/ Q′地区。例如,血液从一个单元流向另一个单元将导致一个单元的血流灌注与通风成比例(高)V“一种/ Q'),另一单元被更灌注成比例换气(低V“一种/ Q′)。比较其对。的影响PACO2,的影响V“一种/ Q“不匹配的PAO2通常更明显,因为1)的数值的变化PAO2比里面的大吗PACO2和2)受损CO2消除经常被增加的分钟通风抵消,抵消的效果V“一种/ Q“不匹配的PACO2的影响要大得多PAO2. 这个net effect ofV“一种/ Q错配通常会降低气体交换效率FIO2而微小的通风会导致更低的血压PAO2和更高PACO2如果。V“一种/ Q“匹配是最理想的。
V“一种/Q与正常的肺不匹配
正常肺局部通气及血流不均匀。通气和灌注的异质性归因于气道和血管树几何形状的影响,以及由于重力导致的血流和肺顺应性的区域差异[35-39]。传统的地带模式[38[[endnoteref: 3]]预测灌注和通气均在重力方向上增加,从心尖到肺底呈直立姿势。然而,它们并没有以同样的速度增长V“/ Q'趋向于从顶点下降至基部。使用更高的空间分辨率的测量动物研究提出分形模型[40,41,血管树的不对称导致灌注不均匀性,这不能用重力引起的流体静力学梯度来解释。姿势、肺容积和气道正压的应用进一步影响局部通气和血流[36,37,42],仅举几个因素。尽管有这些不均匀性,有效的气体交换是可能的,通过通气与血流的紧密匹配,这归因于结构和重力[的共享影响35]。然而,两者之间的关联并不完美V′一种/Q'比例,因此,PAO2和PACO2到不同的肺部区域之间变化[35]。
在年轻健康的个体中,大部分的通气和血流分布到有V“一种/ Q“0.3和2.0 [之间的比率22,这往往会导致一系列的PAO2由90毫米汞柱至130毫米汞柱(图5)[43]。随着年龄的增长,通气和血流分布到更大范围的单位V“一种/ Q的比率,血液流动到低V“一种/ Q'区归因于依赖性肺区的降低的通风由于气道关闭[12,44]。因此,PA-aO2随年龄增长[12,44]。
评估动脉氧合
几个指数被用来评价PAO2和---关联FIO2。当呼吸空气时,PA-aO2提供了一种测量气体交换效率的灵敏方法,但它依赖于年龄。许多不同的研究对不同人群中相对较少的个体进行了抽样,以确定它们的分布PA-aO2在正常个体[45-48]。在所有的研究中,均值PA-aO2随着年龄的增大,因为这样做对围绕均值置信区间。表3合并两个较大种群的数据[45,46]。法向量的简化公式PA-aO2当呼吸空气是4毫米汞柱(7.5千帕为除法结果)(以年/ 4以下)。因为正常PA-aO2主要是由于静脉外加剂增多吗FIO2提出了PAO2超过PAO2和正常的值PA-aO2随着增加FIO2. 这个PAO2/FIO2比值在临床上和ARDS的定义中更常用。正常的下限PAO2当呼吸80毫米汞柱(10.7千帕)的空气时,相当于正常水平PAO2/FIO2比为> 400毫米汞柱(53千帕),而诊断ARDS需要PAO2/FIO2<300 mmHg (40 kPa)。的PAO2/FIO2也依赖于FIO2的呼气末正压(PEEP)和动脉静脉O级别2提取(49,50]并且,因此,一个困难的措施来解释。的PAO2/FIO2是不是在低氧血症的病因不同区分有用。
V“一种/Q“不匹配和血管张力
缺氧性肺血管收缩
缺氧性肺血管收缩(HPV)引起的预收缩的毛细管在具有低单位PAO2(<60 mmHg (8.0 kPa)),如有低血压者V“一种/ Q或分流[51-54]。HPV的作用是疏导血液缺氧单位流走,走向更好的通风设备,提高V“一种/ Q匹配和动脉氧合(图12)。例如在人类中,HPV由〜50%降低的血流量区域萎陷[55,56];对动脉氧合有益的影响可以从一个固定的从一个等分流管到另一个FIO2在异分流图(图8)。HPV的在校正功效V“一种/ Q“不匹配与缺氧肺区域的范围减小[53,57]。一个例子是低PAO2全肺内(如。由于严重的换气不足或高海拔)。在这种情况下,全身血管收缩使肺动脉压升高,但没有改善V“一种/ Q′匹配。动物和人类实验表明,人乳头状瘤病毒是不重要的V“一种/ Q'在正常肺匹配[53,58,59]。相比之下,HPV对于引起局部肺泡缺氧的患者至关重要[53),改善PAO2通过在COPD患者或ARDS [高达20毫米汞柱(2.7千帕)54]。HPV重要性的一个例证是,系统管理的血管扩张剂,抑制HPV,可能减少PAO2在这种病人中[60]。
补充COPD患者的氧气和二氧化碳潴留
HPV的的临床重要的一个进一步的说明是其为O作用2-诱导慢性阻塞性肺病患者高碳酸血症。虽然经常被认为是由于减少了对呼吸的动力,但有研究表明,补充O2对这些患者可增加PACO2尽管有持续的微小通风[61,62]。主要的解释是补充O2提高了PAO2在低V“一种/ Q,抑制局部HPV,增加这些单位的血流量。因此,血液被从通风良好的区域转移,转化为高压V“一种/ Q,增加了通风系统的浪费[61,62]。这是一个例证,说明增加的浪费通风如何减少有效肺泡通风(讨论以上),尽管不变的分钟通风。另外,因为低V“一种/ Q“单位有较高PACO2中,血流恢复到这些单元导致更多的CO2被传递到动脉。增加V“一种/ Q“不匹配为主导的机制造成Ø2然而,诱发性高碳酸血症仍然存在争议:其他研究表明分钟换气量的减少会导致分钟换气量的增加PACO2[63]。另一种解释是霍尔丹效应PAO2减少两个H的结合+和有限公司2以血红蛋白,从而增加物理溶解的CO的量2,因此,P有限公司2[12,64]。换句话说,对于任何给定的CO2内容,P有限公司2血红蛋白O越大,血糖越高2饱和。该霍尔丹效应估计来解释增长6-78%的PACO2在慢性阻塞性肺病患者服用补充O2[61,65,66]。
吸入扩血管
吸入性血管扩张剂可用于改善V“一种/ Q′不匹配。这一概念是,吸入性血管扩张剂按区域通风的比例分布到每个区域,因此,通风良好的区域更有血管扩张剂。局部血管张力降低导致血液流动从不通气区域向较通气区域转移,从而改善V“一种/ Q“匹配和气体交换。已证明吸入一氧化氮可减少分流[60,67]和改善患者动脉氧合与ARDS [60,68,69]。吸入前列环素也有类似的效果[70,71]。有趣的是,效果是COPD患者不太一致。在这种情况下,吸入一氧化氮可导致既改善和恶化的气体交换;后者可通过血管扩张剂也达到低来解释V“一种/ Q′地区。HPV的抑制增加了这些低血流量V“一种/ Q“导致动脉进一步去饱和的区域[67,72]。因此,吸入型一氧化氮的有益作用在低氧引起的低氧血症中可能不太一致V“一种/ Q'区域比以分流区域为特征的条件下。
V“一种/Q在肺部疾病“不匹配
慢性阻塞性肺病
慢性阻塞性肺病患者可能出现低氧血症、高碳酸血症或两者兼而有之。低氧血症的主要原因是灌注不足(低通气)V“一种/ Q')区域,其已被归因于气道疾病[73-76]. 在没有肺炎或肺不张等并发症的情况下,分流并不重要[7,74因此,低氧血症的反应是增加FIO2。高碳酸血症的原因是有效的肺泡通气量减少,这是由于过度通风造成的V“一种/ Q'区和肺泡死空间所造成的肺实质的破坏肺气肿[73-75]。只有当患者无法维持足够的肺泡通气所需的额外呼吸功时,高碳酸血症才会变得明显。心排血量的变化2消费,每分钟通气量已经显示出调控的增加效果V“一种/ Q“急性COPD加重患者的失配[74]。
ARDS
患者气体交换与急性呼吸窘迫综合征,常并发肺炎或败血症引起的,是由于大的肺部区域的通风损失特点是严重的低氧血症。一些研究表明,在这些患者动脉低氧血症主要是由分流血流可能超过心输出量的50%,造成的[13,16-19]。低V“一种/ Q“区域要么缺失,要么是低水平的次要原因。PAO2[16,17]。受损的扩散似乎并不有助于动脉低氧血症[16]. 窥视的效果V“一种/ Q“这些病人的错配尤其有趣。PEEP已被证明可以通过肺泡募集来减少非通气肺组织的数量,并通过减少分流血流量来改善动脉氧合[13,16,17,19,77,78]。增加的PEEP也被证明会增加总的死亡空间,这被解释为在非依赖性肺区,随着肺泡毛细血管的压迫,气道压力增加,未灌注的肺泡数量增加[16,77-79]. 窥视的效果dead space is attenuated if the negative effect of PEEP on cardiac output is counteracted by fluid loading to increase cardiac preload, which also illustrates that reduced cardiac output might increaseVd/VŤ[79]。相比之下,PEEP与肺泡复组合已经显示出减少浪费通风[80]。当使用PEEP在这些患者优化气体交换是,因此,需要平衡氧合,浪费了通风和心输出量的潜在有益和有害影响。另一个工具,以改善ARDS患者的气体交换是俯卧位治疗。动物实验和临床研究已证明,俯卧位降低分流V“一种/ Q不匹配,改善动脉氧合[81-83]。最近的一项临床试验表明,在ARDS早期采用俯卧位可提高生存率[84]。提高生存率的主要机制不是改善气体交换,而是区域通气分布更加均匀,从而减少了由通气器引起的肺损伤[83,85]。
肺栓塞
肺栓塞导致肺部区域没有或血流量减少(高V“一种/ Q,因此,增加了浪费的通风。不那么明显的是,再分配的血液流向其他肺区域,导致这些区域变得相对过度灌注,并转化为低V“一种/ Q的区域,造成低氧血症和增加PA-aO2. 这个reason for hypoxaemia is, thus, increasedV“一种/ Q错配但没有增加分流[86,87]。上ABGS效果由呼吸响应修饰以增加PACO2在美国,最终的结果往往是呼吸困难、低氧血症和正常甚至低氧血症PACO2。低氧血症可能通过循环衰竭导致低加重CVO2或心内右至左分流,都是由急性肺动脉高压引起。重要的是,不存在低氧血症或增加PA-aO2不排除肺栓塞[88,89]。同样,使用PACO2-PETCO2为了衡量浪费通风翔实,但在隔离是不明确的诊断肺栓塞[90]。而一个PETCO2测量表明增加了浪费的通气增加了肺栓塞的可能性[91],而正常数量的浪费掉的通风会减少这种可能性[33,92,这些措施的效用很大程度上取决于先天的肺栓塞的临床概率在个体患者[90]和肺血管树的级分,其参与[91]。
摘要
低氧血症有五种原因。减少PAO2可引起换气不足、低通气PIO2,扩散限制,低V“一种/ Q'区或分流。与其他的原因相反,低氧血症由于分流典型反应差增加FIO2。低V“一种/ Q“区域和分流是目前临床上最常见的导致低氧血症的原因。”
2)换气不足,低通气V“一种/ Q'区也IMPAIR CO2去除,但效果上的大小PACO2对高碳酸血症的通气反应较少且有所改善。
3)高V“一种/ Q“区域、肺泡和器械的死腔会增加通气的浪费,从而损害CO。2淘汰。增加通风浪费的主要反应是,在大多数情况下,增加每分钟通气量和呼吸的工作,而不是增加PACO2。
4) 影响V“一种/ Q气体交换效率的不匹配可以通过计算来量化PA-aO2,静脉混合和浪费的通风。
5)低和高V“一种/ Q这些区域会导致低氧血症、CO受损2消除和增加COPD患者的呼吸功。
6)分流是ARDS和肺炎患者低氧血症最重要的原因。
脚注
本系列之前的文章:否1:Naeije R,Vachiery J-L,Yerly P,等. 这个Ťranspulmonary pressure gradient for the diagnosis of pulmonary vascular diseases.欧元和J2013;41:217 - 223。第2号:休斯JMB,范德李一的T我,没有/ TL,CO肺功能检查的比值。欧元和J2013;41:453-461。第3号:Vonk-Noordegraaf A,Westerhof N.描述右心室功能。欧元和J2013;41:1419 - 1423。4号:哈姆扎维奥,莫内X,特布尔J-L。奇脉。欧元和J2013;42:1796至05年。5号:普利斯科星期。微重力和呼吸系统。欧元和J2014;43:1459 - 1471。6号:人类通气控制的病理生理学。欧元和J2014;44:495 - 512。
利益冲突:未申报
- 收到了2014年2月24日。
- 公认5月4日,2014年。
- ©ERS 2014