抽象的
特发性肺纤维化是一种进步,致命的疾病。这一前瞻性,随机,双盲,多期,并联集团,安慰剂控制的第二阶段试验(NCT00903331)研究了内皮素受体拮抗剂Macitentan在特发性肺纤维化中的功效和安全性。
符合条件的受试者是具有特发性肺纤维化的成年人<3年持续时间和常用的间质肺炎的组织学模式。手术肺活检。主要目的是证明Macitentan(每日每日10毫克)积极影响的强迫致命能力与安慰剂。
使用集中式系统,178个受试者随机(2:1)至Macitentan(n = 119)或安慰剂(n = 59)。从基线的中位数变化高达9月12日的强迫致命能力为-0.20升,安慰剂臂中的-0.20升-0.20升。总体而言,在肺功能试验或疾病恶化或死亡时间内观察到治疗之间没有差异。Macitentan和安慰剂的中位风险分别为14.5个月和15.0个月。丙氨酸和/或天冬氨酸氨基转移酶升高在正常出现的3.4%的Macitentan治疗的受试者和5.1%的安慰剂受体中的3倍上限超过3倍。
总之,主要目标没有达到。在每个治疗组中,macitentan长期暴露的耐受性良好,肝转氨酶升高的发生率相似,较低。
抽象的
在审判中,在IPF中,长期暴露于Macitentan在不符合其主要终点的审判中得到了良好的耐受性http:///wly/p0rdl.
介绍
特发性肺纤维化(IPF)是一种慢性纤维肺病[1].IPF主要发生于老年男性,其特征是放射学和/或组织病理学表现为通常的间质性肺炎(UIP),呼吸困难和肺功能的进行性恶化和预后不良[1,2].有限数量的研究表明IPF治疗中一些药理剂的潜在益处[3.- - - - - -6].
尽管IPF的发病机制尚不完全清楚,但强效血管收缩剂和生长因子内皮素-1已被证实参与了疾病的纤维化过程[7].然而,在具有IPF的受试者中,两个先前报告的口腔双内皮受体拮抗剂(ERA)波丝顿的试验不符合其主要终点[8,9而单一ERA ambrisentan的试验由于缺乏疗效而终止[10.].
一本新型双重时代的Macitentan已被证明可以防止肺纤维素诱导的肺纤维化大鼠模型中肺纤维化的发展[11.].为了研究macitentan在IPF患者中的有效性和安全性,前瞻性、随机、双盲、多中心、平行组、安慰剂对照、II期macitentan用于特发性肺纤维化临床(MUSIC)试验(NCT00903331)设计。
材料和方法
研究对象
根据美国胸部社会/欧洲呼吸协会声明的说法,如果他们曾经参加≥18年,则有资格参加审判≥18年,根据IPF的诊断188bet官网地址12.,病程<3年,并有UIP手术肺活检特征。
在评估资格期间,如果在随机化之前出现以下任何一种:由于IPF以外的条件,在随机化之前被排除在随机性之前;基线高分辨率计算断层扫描的广泛蜂窝(如间质肺病(Build)-3试验中的波丝坦使用的标准所定义的[9]);强迫肺活量(FVC) <50%预测或<1.2 L;肺对一氧化碳的扩散能力校正后的血红蛋白(DLCOpred) < 30%;剩余体积≥120% pred;或阻塞性肺疾病(定义为1秒用力呼气量(FEV)1)/ fvc <0.70)。完整的排除标准列表可用作在线补充材料。
此外,如果受试者在随机化4周内接受以下任何治疗,则不符合参与试验的资格:口服皮质类固醇(>20 mg·天)−1泼尼松或等同物);免疫抑制或细胞毒性药物(包括环磷酰胺和偶氮嘌呤);抗纤维化药物(包括Pirfenidone,D-青霉胺,血清序列,肿瘤坏死因子-α拮抗剂,伊马替尼,干扰素-γ);n-乙酰琥珀(> 600 mg·日−1长期规定为IPF);或口服抗凝剂(IPF规定的地方)。
MUSIC试验是根据《赫尔辛基宣言》的原则在选定国家的学术和社区医院进行的。在研究开始前,应获得所有相关伦理委员会和机构审查委员会的批准。所有受试者均获得书面知情同意。该试验已在ClinicalTrials.gov (NCT00903331).
学习规划
音乐审判是前瞻性,随机,双盲,多期,并联组,安慰剂控制的II期研究。主要目的是证明Macitentan(每日每日一次)受到影响的情况与安慰剂。次要目标是评估马西坦对IPF恶化或死亡时间的影响,并评估马西坦在IPF受试者群体中的安全性和耐受性。
每次来访时进行的研究评估的全部细节可作为在线补充材料获得。简而言之,受试者在筛选、随机化和此后每4个月评估一次,直到研究结束。
筛查评估包括人口统计学、病史、生命体征、伴随用药、实验室检查、肺功能检查、静息动脉血气、胸部高分辨率计算机断层扫描评估和外科肺活检标本的组织学分析。
在随机化时,使用基线呼吸困难指数进行评估受试者[13.]、生命体征、体格检查、伴随用药、FEV1,fvc,纠正DLCO和实验室测试。评估为4月间隔,直到治疗结束包括FEV1,fvc,纠正DLCO、过渡呼吸困难指数(TDI)、实验室检查、伴随用药和不良事件。
当最后一个没有停止治疗的随机受试者完成了12个月的治疗后,进行了研究结束访问。在这次访问中,FEV1,fvc,纠正DLCO, TDI, IPF伴随药物治疗和疾病恶化事件的评估。
在整个研究中记录了对安全性和耐受性进行调查的测量,并在研究药物停止后28天进行最终评估。遵循受试者,直到研究结束即使它们已停止治疗。
该试验的计划样本尺寸为156个受试者,有104名受试者需要接受Macitentan和52个接受安慰剂所需的52个受试者。认为这种样本大小是必要的,以检测80%功率从基线的安慰剂校正平均减少到≥0.10升的11个月;预期具有正常分布的参数,其标准偏差为0.20 L.
方法
在甄别及使用中央系统(互动语音/网页回应系统;S-Clinica,布鲁塞尔,比利时),受试者随机2:1口服马西坦(10 mg,每日上午1次)或安慰剂。第一次服用研究药物是在研究中心,在随机化和成功完成所有评估之后。受试者可在IPF常规背景治疗之外接受研究药物治疗(如果存在且在方案允许的情况下);背景:在整个研究期间,治疗剂量保持不变。
马西坦和安慰剂的片剂和包装没有区别。在整个试验过程中,研究人员、研究人员、受试者、监测人员和主办者对治疗分配仍然是盲的。只有在研究结束后,随机编码才可用来进行数据分析。
分析
结果措施
主要疗效终点是马西坦治疗的FVC从基线到12个月的变化与安慰剂。Macitentan的优越性被定义为安慰剂校正平均值±SD.差异≥0.10±0.20 L。
二次疗效终点是首先发生IPF恶化或死亡(所有原因)的时间,直至研究结束。IPF恶化被定义为1)肺功能试验(PFT)结果恶化(即。显示绝对肺活量从基线下降≥10%,绝对纠正肺活量从基线下降DLCO≥15%,≥4周后的确认试验不驳斥)或2)IPF的急性呼吸失代组分(即。受试者的病情在<4周内出现原因不明的快速恶化,呼吸越来越急促,需要补充≥5 L·min的氧气−1维持静息氧饱和度≥90%或动脉氧压≥55mmhg(海平面)或50mmhg(高空))。由于IPF恶化而不能进行pft的受试者被认为有恶化的结果,除非随后的评估证明这是错误的。
探索性疗效终点包括:1)TDI的评估[13.], TDI≥1者至12月的组间差异;2) PFT结果从基线到12个月的变化(特别是FEV)1并纠正DLCO);3)复合生理指数中的基线的变化增加[14.].还探讨了由基线人口统计学和临床特征分组的受试者的基准中的FVC的安慰剂校正变化(特别是年龄,性别,位置,FVC在基线上的基线),并在基线上使用基线)的基准。所有探索终点都被定义先天的在解开之前。
统计方法
对“全随机组”进行初级疗效终点的分析,其由所有随机受试者组成,无论他们是否接受了研究药物。评估FVC的FVC变化,并评估了使用Wilcoxon Rank-Sum试验进行的治疗比较,以渐近近似为T分布。NULL假设是,使用双面0.05型错误水平,从FVC的基准变化的干预措施之间没有差异。没有进行疗效的临时分析,并且在开始后对研究没有重大变化。在“每协议集”中重复了主要疗效分析,其中包括所有没有重大协议偏差的随机科目。
对于主要终点分析,在缺少FVC评估值的受试者中,应用了以下更换规则:1)在月12日之前获得的最后一个可用的基线测量作为缺失值的替代;2)如果受试者在评估前死亡,则值为0.0L的值取代缺失值;3)对于在第12月之前活着和经验丰富的疾病恶化的受试者,但事件和月12日之间没有FVC评估,FVC的最差价值(定义为基线之间观察到的最大百分比和所考虑的时间点。对于相同分析集中的所有受试者,缺失价值;4)对于活着的受试者并且在12月12日之前没有疾病恶化,但对于没有任何基线价值,没有可用的后基线价值,分析集中观测值(包括上部价值)的平均百分比变化适用于基线FVC值。进行了探索性重复测量分析(随机系数模型),以研究主要研究期间基线FVC的变化。
在全随机化集合中评估二次疗效终点。通过在没有95%置信范围(CL)的不同时间点的不同时间点的情况下,通过Kaplan-Meier估计来概述了数据。计划日志排名测试和危险比率直至研究结束。由于有关治疗危害的比例性的未满足的假设,后HOC.确定对数率和危害比率的治疗效果估计最高可达月12日(在横过治疗死亡率曲线之前施加审查)。
在全随机化集中评估探索终点。二分变量表达为致安慰剂的发病率和相对风险,含有95%的Cl。使用汇总统计(平均值,中位数,标准偏差,范围和95%CL)表示连续变量。
在全随机化集上进行安全分析,数据被概述地汇总。
结果
主题人口
审判于2009年5月19日开始。共有178名受试者从12个国家(澳大利亚(N = 27),加拿大(N = 15),法国(N = 26),德国(N = 13),以色列(n = 7),意大利(n = 8),斯洛文尼亚(n = 2),南非(n = 2),西班牙(n = 11),瑞典(n = 1),土耳其(n = 11)和美国(n = 55))。在178个随机受试者中,119种分配给Macitentan和59到安慰剂。基线人口统计和临床特征在治疗组之间均衡(表1).显示研究主题的处置图1.根据该方案,在最后一名随机受试者接受了12个月的治疗后宣布研究结束。审判于2011年6月30日结束。
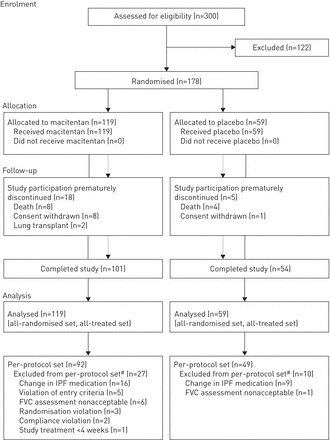
学习科目的处置。IPF:特发性肺纤维化;FVC:强迫致命能力。#:受试者可能已经表现出多种原因进行排除。
27名接受马西坦治疗的受试者和10名接受安慰剂的受试者被排除在每个方案组之外。在试验的每一组中,从每一方案中排除的主要原因是IPF伴随药物的改变而没有基础疾病恶化的记录。
功效测量
主要终点:从基线到FVC 12个月的变化
从基线到第12个月,马西坦组绝对FVC的中位(95% CL)变化为-0.20 L (-0.29 - -0.16 L),安慰剂组为-0.20 L (-0.28 - -0.13 L)。马西坦对植被覆盖度的中位(95% CL)处理效果为0.00 L (-0.09-0.08 L)。绝对植被覆盖度从基线到第12个月的平均变化、马西坦对植被覆盖度的平均处理效果以及与这些估计相关的汇总统计数据见在线补充表S1)。
当对每个方案组重复分析主要终点时,结果与全随机组一致(数据未显示)。
第一次发生IPF恶化或死亡的时间
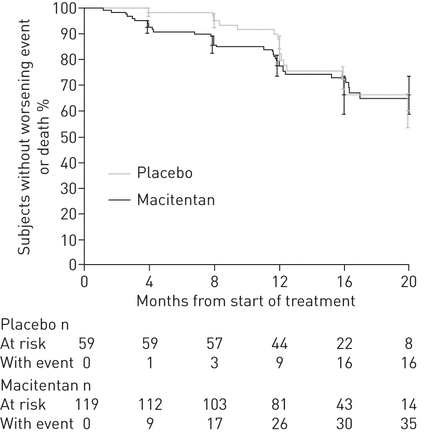
总共,35名接受马西坦治疗的受试者(29.4%)和17名接受安慰剂的受试者(28.8%)至少发生过一次IPF恶化或死亡。在IPF恶化至第12个月期间,观察到一种有利于安慰剂的早期趋势(后HOC.HR 1.56,95%CL 0.73-3.33;log-rank p = 0.2428)(无花果。2).这种差异主要是由于macitentan组中出现IPF早期急性呼吸失代偿的受试者数量更多(7名(5.9%)受试者)所致。与安慰剂(一个(1.7%)主题)。
Kaplan-Meier估计首次特发性肺纤维化恶化或死亡事件发生的时间。数据为全随机组受试者的Kaplan-Meier估计,95%置信限为4个月。
总体而言,在两种治疗组中,大多数事件被记录为IPF恶化,PFT结果劣化(Macitentan n = 25(21.0%);安慰剂N = 14(23.7%))。死亡,当考虑仅用于分析次要终点的分析,在CAMITUNTAN组的三(2.5%)受试者中发生,在安慰剂组中的两次(3.4%)受试者。
在线补充表S2中显示了IPF第4、8、12、20和24个月首次发生恶化或死亡的Kaplan-Meier估计时间。结果的敏感性分析(随机系数模型)进行后HOC.还显示Macitentan在FVC随时间变化的情况下没有治疗效果(数据未显示)。在线补充表S3中显示了显示疾病的第一次疾病和死亡的原因的数据显示在线补充表S3。
肺功能测试
从基线到12个月绝对肺活量,绝对肺活量的中位数变化1并纠正DLCO显示在表2.Macitentan与安慰剂的中位数差异为FEV1(-0.03 L, 95% CL -0.10-0.04;p = 0.45)。同样,对于纠正DLCOmacitentan和安慰剂之间的中位治疗差异较小且无统计学意义(0.03 mmol·kPa)−1·Min.−1,95%cl-0.17-0.23;p = 0.76)。
综合生理指标中的基线的中位数从基线变化,显示在表3.macitentan和安慰剂在复合生理指标上的中位治疗差异很小,没有达到统计学意义(-0.4,95% CL -2.4-1.6;p = 0.66)。
数据显示从基线到12个月的平均变化以及马西坦和安慰剂在绝对FEV方面的平均治疗差异1并纠正DLCO详见在线补充表S4。
过渡呼吸困难指数
月12日中位数(95%CL)TDI为-1.0(-3.0-0.0.0),用于治疗受试者和安慰剂接受者的0.0(-2.0-0.0)。Macitentan ARM中TDI≥1的受试者的数量为27(23.5%),安慰剂ARM为17(28.8%);相对风险降低0.19(95%Cl-0.37-0.52; p = 0.47)。
主题亚组的疗效
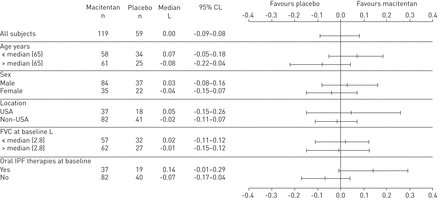
从年龄,性别,地点,基线的基线组合的受试者群体中,基线的基准级数的探索性分析的结果与基线基线的基线和使用口服IPF疗法的基线患者的亚群相似于主要分析中观察到的(无花果。3.).
在研究受试者的不同群体中,将安慰剂校正的中值从基线增加到12个月12月12日的第12个月。数据来自全随机集中的主题。IPF:特发性肺纤维化。
安全性和耐受性
Macitentan的中位数(范围)暴露于14.5(0.0-24.6)个月,安慰剂为15.0(6.3-24.3)个月。共有91名(76.5%)的碱治疗受试者和48名(81.4%)安慰剂接受调查治疗≥12个月。从治疗开始直到研究药物停止后长达28天,在CAMITUNTAN组(97.5%)和安慰剂组中的58名受试者中有116名受试者(98.3%)至少经历过一个不良事件。在≥10%的Macitentan处理的受试者中出现的不良事件显示在表4.总共有15名(12.6%)接受马西坦治疗的受试者和7名(11.9%)接受安慰剂的受试者经历了不良事件,导致研究治疗提前终止。37例(31.1%)服用马西坦的受试者和20例(33.9%)服用安慰剂的受试者至少发生过一次严重不良事件。最常见的严重不良事件显示在表5.总共有3.4%的Macitentan治疗的受试者和5.1%的安慰剂接受者在正常上限的上限上显示出丙氨酸和/或天冬氨酸氨基转移酶升高。在其他评估对调查治疗的其他评估之后的观察可以作为在线补充材料。
总共有13名受试者在治疗期间或停药后28天死亡:9名(7.6%)在马西坦组,4名(6.8%)在安慰剂组。最常见的死亡原因是IPF恶化(macitentan =2(1.7%),安慰剂=4(6.8%))和呼吸衰竭(macitentan =3(2.5%),安慰剂=1(1.7%))。
讨论
MUSIC试验是一项前瞻性、随机、双盲、多中心、平行组、安慰剂对照、II期概念验证研究,以组织学证实的IPF研究对象为研究对象,研究双ERA macitentan的有效性和安全性。MUSIC试验的主要目标是证明macitentan 10mg每日一次对FVC有积极影响与安慰剂,没有见过:在FVC中的基准的主要终点点,治疗之间没有显着差异,高达FVC的第12个月。此外,在任何次要措施中的治疗组之间没有观察到任何次要措施的差异,包括IPF恶化或死亡,并且在PFT结果的治疗相关变化的探索性研究中。每天一次长期暴露于Macitentan 10mg,耐受良好,肝脏氨基转移酶的发生率类似于安慰剂。
而先前在IPF患者中进行的两项双ERA波生坦试验均未达到主要终点[8,9由于缺乏效力,终止了单个时代Ambrisentan的一次试验[10.],在接受外科肺活检诊断为IPF的一组受试者的呼吸困难和健康相关生活质量中观察到波生坦治疗的一些有益效果[8,15.].在Bosentan的构建3试验结果之前启动的音乐试验[9[可用于分析,提供了探讨双时代,普利育丹的疗效和耐受性肺功能损害的研究人群的疗效和耐受性的机会。
在本试验中,双ERA macitentan治疗受试者耐受性良好。在macitentan治疗组中,超过四分之三的受试者暴露于该药物≥12个月。macitentan治疗组观察到的不良事件与安慰剂组相似,特别是丙氨酸和/或天门冬氨酸转氨酶升高率较低,超过正常上限的3倍。更大比例的受试者接受了马西坦治疗与安慰剂表现出外周水肿和贫血。已知液体保持和贫血与作为一类代理的时代相关的血液保留和贫血症,随着先前在具有肺动脉高压的受试者和慢性心力衰竭中报告的这些事件的风险增加了[16.- - - - - -21.].在死亡发生率方面,两个治疗组之间没有差异;相反,在12个月之前观察到的两组风险差异主要是由急性加重引起的。原因尚不清楚。观察到马西坦治疗组的咳嗽率较低与安慰剂收件人也值得注意,尽管我们对此没有解释。
在目前的试验中,选择从FVC中的基线的变化为主要终点。由于FVC和其他休息的PFT结果,因此在IPF的管理中使用FVC和其他休息的PFT结果来选择该终点。此外,FVC中的纵向降低已被证明在几项研究中是IPF中的显着预后指标[22.- - - - - -25.].一次探索性研究表明,在3个月内,FVC降低的可能预后值≥5%[26.].另一组估计24周内FVC的最小临床重要差异在2%到6%之间[25.].根据此类报告考虑了0.10L的处理臂与0.20升标准偏差之间的FVC之间的平均相对差异的选择[25.,26.],近似临床显着差异。FVC和校正纵向变化的方向和幅度DLCO在音乐试验中观察到易于镜像在具有IPF的对象的其他几项研究中观察到的人[8,9,27.,28.].同样,在本研究中观察到的复合生理指数从基线到12个月的中位数增长幅度与其他安慰剂接受者在类似研究期间的报告相似[29.].
内皮素-1的含义并可能有助于IPF下面的纤维化过程[7].然而,在几个研究IPF患者单、双ERAs的临床试验中,疗效无法得到证实[8- - - - - -10.],包括目前的试验。由于IPF是一种纤维增生疾病,其中涉及几种致病机制,因此成功治疗的关键可以涉及靶向多种途径的治疗组合[30.].
我们承认MUSIC试验有一定的局限性。FVC是衡量IPF临床状态的可靠和响应性指标,其中2-6%的下降与临床重要性有关[25.].但是,FVC没有完全验证为替代衡量标准,以获得更有意义的结果,包括生存[31.].因此,与全因、非选择性住院治疗或全因死亡相比,在本II期试验中选择FVC作为主要终点可能被认为是不利的[31.].在PFTS评估内的可变异潜力也可以在选择生理终点的选择中表示限制。此外,由于对处理危害的比例的未满足的假设,确定了在发生时间分析中的治疗效果估计后HOC..此外,缺乏剂量发现的研究意味着我们无法确定参加审判的受试者中较高剂量的Macitentan的潜在影响,如果有的话。
总之,音乐试验的主要目标,以确定Macitentan是否积极影响FVC的变化从基线到12个月12与安慰剂,没有满足。治疗组之间没有观察到任何次要或探查终点的差异。在每个治疗组中,macitentan长期暴露的耐受性良好,肝转氨酶升高的发生率相似,较低。
致谢
作者对参加音乐试验的所有调查人员表示感谢:N.Goh(过敏,免疫学和呼吸医学,阿尔弗雷德医院,墨尔本,墨尔本),A.Glanville(心脏和肺移植单位,圣文森特医院,Darlinghurst),M.麝香(晚期肺病单位,皇家珀斯医院,珀斯)和P.Hopkins(胸部部门,查尔斯医院肺移植,Chermside),澳大利亚;D。C。lien (University of Alberta Health Science Centre, Edmonton), C. Chan (University Health Network, Toronto), J.D. Rolf (Kelowna General Hospital, Respiratory and Allergy Cinic, Kelowna), P. Wilcox (St Paul’s Hospital, Vancouver), P.G. Cox (St Joseph’s Healthcare, Firestone Institute for Respiratory Health, Hamilton) and H. Manganas (Hopital Notre-Dame du Centre, Hospitalier de l'Universite de Montreal, Montreal), Canada; V. Cottin (Hôpital Cardiologique et Pneumologique Louis Pradel, Service de Pneumologie, Bron), D. Valeyre (Hopital Avicenne, Service de Pneumologie, Bobigny) and B. Walleart (Clinique des Maladies Respiratoires, CHRU Hopital Calmette, Lille), France; S. Andreas (Fachklinik für Lungenerkrankungen, Immenhausen), C. Neurohr (Klinikum der Universität München, Medizinische Klinik und Poliklinik 1, Großhadern Schwerpunkt Pneumologie, Munich), A. Guenther (Justus-Liebig-Universität Gießen, Zentrum für Innere Medizin, Medizinische Klinik II, Giessen), N. Schönfeld (Helios Klinikum Emil von Behring, Zentrum für Pneumologie und Thoraxchirurgie, Berlin) and A. Koch (Universitätsklinikum Köln, Herzzentrum/Klinik III für Innere Medizin (Kardiologie, Pneumologie, Angiologie und Intensivmedizin), Cologne), Germany; M. Kramer (Rabin Medical Centre, Pulmonary Institute, Petach Tikvah), R. Breuer (Institute of Pulmonology, Hadassah Medical Centre Ein Karem, Jerusalem), I. Ben-Dov (The Chaim Sheba Medical Center/The Institute of Pulmonology, Physiology and Exercise, Tel-Hashomer), G. Fink (Kaplan Medical Centre/Pulmonary Institute and Dept of Medicine, Rehovot) and Y. Schwarz (Tel Aviv Sourasky Medical Center, Dept of Pulmonary and Allergic Diseases, Tel-Aviv), Israel; C. Albera (Azienda Sanitaria Ospedaliera, San Luigi Gonzaga – Clinica Malattie Apparato Respiratorio, Turin), M. Confalonieri (Dipartimento di Pneumologia, Ospedale di Cattinara, Trieste), C. Saltini (Dipartimento di Medicina, Unità Operativa Complessa di Malattie dell'Apparato Respiratorio, Azienda Ospedaliera Universitaria Policlinico Tor Vergata di Roma, Rome) and S. Harari (U.O. Pneumologia, Ospedale San Giuseppe, Milan), Italy; M. Flezar, Bolnisnica Golnik, Golnik, Slovenia; M. Greenblatt and G.J. Ras, Centre for Chest Disease, Milpark Hospital, Johannesburg, South Africa; F. Morell (Neumologia, Hospital Universitatario Vall d'Hebron, Barcelona), J.L. Alvarez-Sala (Pneumology, Hospital Universitario Clinico San Carlos, Madrid), A. Xaubet (Pneumology Department, Hospital Clínic Barcelona, Barcelona), A. Sueiro (Hospital Universitario Ramón y Cajal, Madrid) and M.J. Linares (Pneumology, Fundacion Hospital Alcorcon, Alcorcon), Spain; M. Sköld, Lung Allergi forskningen, Karolinska Universitetssjukhuset Solna, Stockholm, Sweden; O. Kayacan (Dept of Chest Disease, Ankara University School of Medicine, Ankara) and N. Mogulkoc (Dept of Chest Disease, Ege University School of Medicine, Bornova-Izmir), Turkey; A. Chan (University of California Davis, UC Davis Medical Center, Main Hospital, Sacramento, CA), J. Chapman and J. Parambil (Cleveland Clinic Foundation, Cleveland, OH), N. Ettinger (St Luke’s Medical Group, Cardio-Pulmonary Associates, Chesterfield, MO), J. Golden (University of California – San Francisco, Ambulatory Care Center, San Francisco, CA), K.C. Meyer (University of Wisconsin, Hospital and Clinics, Madison, WI), J.J. Swigris (National Jewish Health, Denver, CO), G.L. Yung (University of California – San Diego, Medical Center, San Diego, CA), D. Antin-Ozerkis (Yale University School of Medicine, Winchester Chest Clinic, New Haven, CT), P.K. Mohabir (Stanford University Medical Center – Chest Clinics, Stanford, CA), L.J. Wesselius (Mayo Clinic Arizona, Scottsdale, AZ), J. de Andrade (Pulmonary, Allergy and Critical Care Medicine, University of Alabama at Birmingham, Birmingham, AL), F. Cordova (Temple Lung Center, Philadelphia, PA), Z. Safdar (Baylor College of Medicine, Houston, TX) and M. Wencel (Wichita Clinic, Wichita, KS), USA. The authors thank the members of the independent Data Safety Monitoring Board: H.J. Eisen (Drexel University College of Medicine, Philadelphia, PA, USA), C.M. O'Connor (Duke University Medical Center, Durham, NC, USA), B. Nashan (University Medical Centre Eppendorf, Hamburg, Germany) and D.L. DeMets (DL DeMets Consulting, Madison, WI, USA). The authors thank all contributors in the three central analysis laboratories and A. Gray (Elements Communications Ltd, Westerham, UK) for medical writing assistance, supported by Actelion Pharmaceuticals Ltd (Allschwil, Switzerland).
脚注
对于编辑评论看31..
本文提供了补充材料www.www.qdcxjkg.com
临床试验:本研究注册于www.clinicaltrials.gov.标识号NCT00903331.
支持陈述:为患有特发性肺纤维化临床(音乐)审判的Macitentan用于Macitentan的资金Actelion股价制药有限公司(瑞士Allschwil)。Actelion制药有限公司的代表参与了研究的设计和数据的收集、分析和解释。医学写作援助期间,准备这份手稿是由Actelion股价制药有限公司.
利益冲突:披露可以在本文的在线版本旁边找到www.www.qdcxjkg.com
- 已收到2012年7月6日。
- 接受2013年4月10日。
- ©2013年