文摘
特发性肺纤维化(IPF)是一种进行性肺病没有被证明有效的治疗。
一个多中心、双盲、安慰剂对照、随机III期临床试验是在日本进行的定义良好的IPF患者的疗效和安全性pirfenidone,小说antifibrotic口服剂,在52周。275名患者随机(大剂量1800毫克·−1;低剂量1200毫克·日−1;比2:1:2)或安慰剂组,267例为pirfenidone的疗效进行评估。截断符号之前,主要终点是修订;的变化肺活量(VC)是在52周的评估。二级终端包括无进展生存(PFS)时间。
在VC下降显著差异观察(主要终点)之间的安慰剂组(-0.16 L)和高剂量组(-0.09 L) (p = 0.0416);两组之间的差异(p = 0.0280)也被观察到在PFS(二级终点)。尽管光敏性,pirfenidone行之有效的副作用,在这项研究中,主要的副反应是温和的在大多数患者的严重程度。
Pirfenidone相对IPF患者耐受良好。pirfenidone治疗可能降低风险下降的速度,增加了PFS时间在52周。还需要更多的研究来证实这些发现。
特发性肺纤维化(IPF)是一种毁灭性的,进行性纤维化肺病有3 - 5年的平均生存没有被证明有效的疗法1,2。最近的研究表明,IPF发展慢性进行性纤维化上皮细胞损伤和异常的激活3,4。因此,治疗策略对IPF已经从糖皮质激素或免疫抑制剂antifibrotic代理,在最近的临床试验报告5,6。
Pirfenidone (5-methyl-1-phenyl-2 - (1 h)吡啶酮;赢家& Co .)、大阪、日本;美国MARNAC、达拉斯、TX)7- - - - - -9是一种很有前途的代理与IPF的治疗潜力,结合抗炎,抗氧化剂和antifibrotic效果在实验性肺纤维化模型10- - - - - -14。非盲后二期研究先驱7和一个开放1年日本留学9,双盲,安慰剂对照的临床试验pirfenidone日本IPF患者表现出较小的衰落肺活量(VC)患者接受pirfenidone 9个月15。过早地终止了审判独立的数据和安全监测委员会(DSMB)由于安慰剂组急性发作的发生率高于pirfenidone组。这些令人鼓舞的结果,促使我们进行三期1年临床研究检查治疗pirfenidone对肺功能恶化的影响和IPF患者疾病进展。
材料和方法
研究对象
IPF的诊断是依照美国胸科学会(ATS) /欧洲呼吸学会(ERS)共识声明188bet官网地址16第四版的特发性间质性肺炎的临床诊断标准指南在日本17。高分辨率ct (HRCT)扫描专家综述了胸部的胸部放射学家之前随机;两个6专家放射科医生独立评价HRCT图像同意并确定的模式通常的间质性肺炎(摘要)在场或不按照预先确定的协议在线(见补充材料)。在分歧的情况下,第三个放射科医生的解释最终决定的影响,以及患者的诊断可能在HRCT上摘要模式的存在证实了在外科肺活检组织病理学摘要模式样本。
合格的成人患者(20 - 75岁的年龄)和IPF诊断基于上述标准及会议以下动脉氧饱和度测量脉搏血氧仪(年代p O2)标准:1)血氧饱和度下降≥5%的休息之间的区别年代p O2和最低的年代p O2在6分钟稳态运动测试(6了);和2)最低年代p O2在6遇到≥85%,呼吸空气。6遇见过程是按照之前的研究协议在线(见补充材料)。排除标准:1)减少症状在前6个月;2)使用免疫抑制剂和/或口服糖皮质激素剂量> 10 mg·天−1在前3个月;3)除了IPF特发性间质性肺炎的临床特征;4)已知共存肺动脉高压的证据,哮喘、肺结核、支气管扩张、曲霉病或严重的呼吸道感染。
机构审查委员会批准的协议是在每个中心和书面知情同意了从招生之前所有的参与者。持续的疗效和安全性独立DSMB综述了结果。
研究设计
本研究是一个多中心,双盲,随机,安慰剂对照,三期临床试验旨在确定口服的疗效和安全性的pirfenidone IPF患者1年。符合条件的病人分配到三组:高剂量(1800毫克·天−1)、低剂量(1200毫克·−1)和安慰剂,2:1:2比,分别修改最小化方法,包括一些随机分配基于偏见硬币设计平衡基线年代p O218,19。
治疗方案
Pirfenidone 200毫克片剂和匹配的安慰剂供口服用赢家& Co .剂量逐步地增加如下:一个平板电脑t.i.d。口服接种前2周(高剂量600毫克·−1,低剂量600毫克·天−1和安慰剂0 mg·天−1每剂),然后两片t.i.d。2周后(高剂量1200毫克·−1,低剂量600毫克·天−1和安慰剂0 mg·天−1)和三个平板电脑t.i.d。其余48周(高剂量1800毫克·−1,低剂量1200毫克·天−1和安慰剂0 mg·天−1)网上(见补充材料)。尽管伴随使用皮质类固醇≤10 mg·−1(与强的松)允许在研究期间,伴随使用免疫抑制剂和其他实验人员在调查中不允许网上(见补充材料)。所有与会者都警告潜在的光敏性皮疹和被建议使用防晒霜在暴露在阳光直射。
疗效端点
主要终点是VC的变化从基线到52周。二级终端无进展生存(PFS)的时间和最低的变化年代p O2在6。定义的疾病进展的是死亡和/或从基线风险下降≥10%。VC数据时无法获得由于呼吸道症状恶化,包括急性恶化,也被归类为疾病进展。在日本的第二阶段研究15,6过程在协议指定在线(见补充材料)。第三终端肺功能测试(击球;动脉氧张力,alveolar-arterial氧张力差异静止,肺活量(TLC)和肺一氧化碳(的扩散能力DL,有限公司)),急性恶化20.的标志,血清水平间质性肺炎(sialylated碳水化合物抗原KL-6表面活性剂蛋白(SP) - d和SP-A;看到在线补充材料)和主观/客观症状(咳嗽、存在/没有痰,呼吸困难在日常生活与Hugh-Jones分类评估)。
VC测量每4周,而最低年代p O2在6遇到和其他击球测定每12周。急性恶化的IPF根据之前的报告和修订标准定义为急性加重日本的IPF在线补充材料(见附录)15,20.。
最低的变化年代p O2在6遇见在52周是原来的目的本研究主要终点。决定修改的主要终点的最低年代p O2VC在52周和评估最低的变化年代p O2在6遇到作为一个次要终点。这是推荐的独立DSMB,打破了之前的代码。这个决定是基于进化的知识评估IPF的客观测量21- - - - - -26,以及缺乏验证6研究(未发表的数据)和再现性的困难年代p O26分钟步行试验的测试测量期间(6 mwt)27。
统计分析
计划在总样本量是250:100,50和100名患者大剂量,低剂量和安慰剂组,分别。100年的样本大小的高剂量和安慰剂组确定模拟的基础上,提供一个统计的0.8检测假设的差异意味着最低的变化年代p O2从基线到52周两组之间在本研究的显著性水平为0.1(双边)(细节在网上补充材料)。尽管主要终点是最低的改变年代p O2研究开始后的VC,权力的基础上计算VC的变化是相同的(保持在0.8∼),因此,样本大小没有改变计划。随着低剂量组的目的是评估其概要文件在锥形pirfenidone治疗剂量,低剂量组的样本大小是通过减半的样本量大剂量和安慰剂组。多重性问题没有考虑因为之间的主要分析比较高剂量和安慰剂组。
分析VC和最低的变化年代p O2从基线进行ANCOVA使用相应的基线测量不。分析其他击球和血清水平的变化间质性肺炎的标志进行最少的显著差异基于单向方差分析的方法。最后观察原则结转(LOCF)采用转嫁缺失值如果病人数据可供≥4周后基线。为了避免偏见在处理缺失值,使用可用的混合模型方法重复变化的措施VC进行灵敏度分析。累计使用kaplan meier PFS率估计方法,而使用生存率较。发病率与确切概率法进行了比较。
结果
患者登记
2004年7月至2005年8月,325名患者在73年日本中心筛选,和275名患者被随机的三组:高剂量、低剂量和安慰剂。267的275名患者(108、55和104名患者大剂量,低剂量和安慰剂组,分别)被认为有资格获得全分析集。八个患者被排除在外,因为没有post-baseline资料(图1所示⇓)。第一个病人进入试验在7月13日,2004年,最后一个病人进入8月30日,2005年。
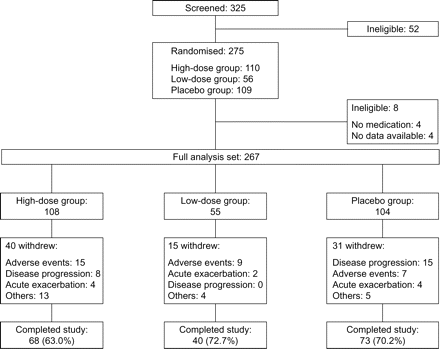
性格的病人。325个患者筛选73中心在日本和275名患者被随机的三组:高剂量(1800毫克·天−1pirfenidone),低剂量(1200毫克·天−1)和安慰剂组。疾病进展包括肺活量下降10%和呼吸道症状的恶化。
没有显著差异在人口和基线特征的分布在三组中,除了吸烟史(表1⇓)。文章分析并没有显示出显著的影响吸烟史的VC的变化。根据他们的击球时,病人被认为相对轻度功能障碍。246名患者(92%)治疗IPF之前没有收到,包括糖皮质激素。患者86例(40岁,15 - 31日在大剂量,低剂量和安慰剂组,分别)停用研究药物由于各种原因(如表2⇓)。的主要原因是疾病进展的安慰剂组,和pirfenidone治疗组的不良事件的发生。kaplan meier阴谋的时间停药三组如图E1的在线补充材料。之间的时间分布成对比较使用生存率较三组,但无显著差异。11例(4.1%)死亡研究:三,四和四大剂量,低剂量和安慰剂组,分别。
对主要影响终端
的调整手段的变化根据ANCOVA VC -0.09 L和-0.16 L高剂量和安慰剂组,分别用不同的0.07 L显著(p = 0.0416)。此外,调整意味着低剂量组为-0.08 L的变化;之间的显著差异也见过低剂量和安慰剂组(p = 0.0394)(图2所示⇓)。原油意味着在基线和周(52)和变化,调整手段,意味着改变ANCOVA和假定值列于表3⇓。之间没有显著差异,高、低剂量组。VC在52周期间的系列变化如图3所示⇓。
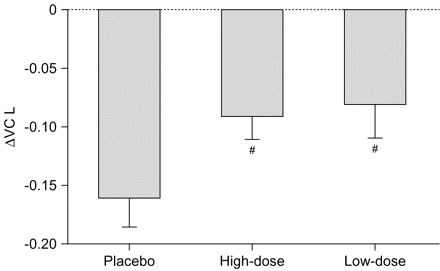
pirfenidone对肺活量(VC)在52周。数据意味着±se。#:p < 0.1,对比的调整意味着基于ANCOVA(正面和负面的变化代表恶化和改善基线,分别)。最后观察结转方法用于每组辍学生。安慰剂组:n = 103;高剂量组:n = 104;低剂量组:n = 54。
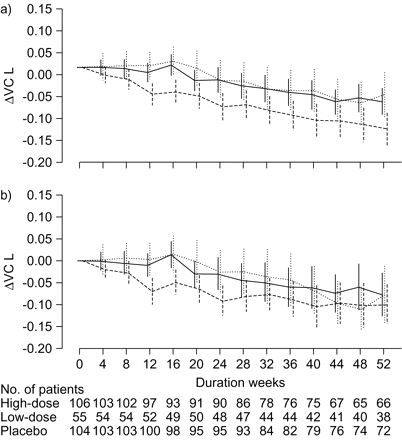
连续变化的肺活量(VC)每4周在52周。一)过渡块“最后的观察进行估算的意思是“向前发展。b)的原油意味着风险的变化。数据意味着±90%可信区间。- - - - -:高剂量pirfenidone组;·······:低剂量pirfenidone组;- - - - -:安慰剂组。
对二、三级终端的影响
二级终端PFS的时间和最低的变化年代p O2在6。PFS的分配时间对比了高剂量和安慰剂组的生存率较和发现显著差异(p = 0.0280;图4⇓)。此外,略微显著差异被发现在低剂量之间的分布和安慰剂组(p = 0.0655)。没有统计上的显著差异中发现平均最低的变化年代p O2在三组(表4所示⇓)。急性加重的发病率在研究后28天内或终止研究的六岁(5.6%)、3(5.5%)和5(4.8%),高剂量,低剂量和安慰剂组,分别。被看到在三组无显著差异。尽管低剂量和安慰剂组之间的差异意味着TLC的变化和变化DL,有限公司具有统计学意义(p = 0.0408, p = 0.0768)在52周,没有明显差异的变化其他击球或三组中血清标记物(表E1在线补充材料)。
kaplan meier情节特发性肺纤维化患者的无进展生存时间组。- - -:高剂量;- - - - -:低剂量;·······:安慰剂。符号在曲线上代表审查点停止研究治疗的患者由于疾病的进展以外的原因。与生存率较kaplan - meier曲线:高剂量组和安慰剂组之间p = 0.0280;低剂量组和安慰剂组之间p = 0.0655;p = 0.9106高剂量组和低剂量组之间。
遵从性和安全性
严重不良事件报告的频率≥5%在研究表5列出了(p < 0.05)⇓。光敏性、厌食、眩晕和高架γ-glutamyl-transpeptidase(γ-GTP)更常见的高剂量组比安慰剂组和光敏性,asteatotic湿疹、腹部不适和白细胞减少是更常见的在低剂量组比安慰剂组。相比之下,呼吸道感染,如鼻咽炎、上呼吸道炎症,常见的高剂量组显著低于安慰剂组。
这项研究的不良事件导致停药表2中列出⇑。高剂量组20例(18.3%)患者和11例(20%)低剂量组停止研究治疗,无统计差异14名(13.1%)患者相比安慰剂组。大部分的不良事件消失减少剂量或临时扣缴的药物。因此,治疗pirfenidone在IPF患者一般耐受性良好。
光敏性是主要的不良事件观察到51%的患者在高剂量组和低剂量组为53%。患者的光敏性,∼70%和80%高剂量和低剂量组,分别是轻微的病例和其余温和的情况下。虽然没有明显的差异之间的发病率高剂量和低剂量组,轻微的光敏性较高的百分比低剂量组。的严重程度的评价是主观的,根据病人的症状和现场调查员的判断。只有三个病人(∼3%)停止由于光敏性研究。
讨论
在过去的十年中,一些临床试验IPF进行世界范围内确定IPF的有效治疗方案,但是结果是负面的,让人失望。因此,一个有效的治疗方案与安慰剂比较控制还有待确定5,6,21,28。在这个试验中,高,低剂量pirfenidone组改进的VC,和PFS的分布比安慰剂组(图2所示⇑表3,⇑,图4⇑)。最近的研究证实,VC下降或用力肺活量(FVC)≥10%的基线的6 - 12个月是最重要的预测IPF患者的死亡率22- - - - - -24,26。因此,疾病进展时间定义为死亡和/或下降≥10%绝对测量风险的变化,被公认为一个适当的替代标记为生存6,23这也是适当的关于小FVC近日报道的变化29日。考虑到> 90%的患者没有接受任何治疗随机之前,我们的研究结果为此提供了第一个证据与药物治疗干预提高IPF患者PFS的时间。
没有发现显著差异最小的变化年代p O2组织在我们的研究中(表4所示⇑)。虽然这些明显的负面观察的具体原因不明,以下事实可以解释我们的观察与发现先前的研究之间的差异15和现在的一个:1)6见过在这之前的研究不是一个验证测试,和2)最后最低的变化年代p O2不能准确地评估因为∼20%的患者不能完成6见过在后续的最低吗年代p O2已达到82%(数据没有显示)。再现性的运动研究6 mwt和修改版本的6 mwt / 6遇到的混杂因素,未来的研究需要澄清之前等运动研究6 / 6 mwt会面6,28。
前面的II期临床试验在日本被提前终止,因为IPF急性加重的发病率15。然而,在目前的试验,没有发现差异在三组中急性恶化的频率。急性加重的发病率在安慰剂组为14.3%在9个月之前的研究中,这是观察在52周只有4.8%在最近的研究中,因此,先前的观察是没有证实本研究。这种差异的原因尚不清楚。在目前的研究中,急性加重发生在只有5%的患者1年期间相对轻度肺功能障碍。真正的发病率和患病率IPF是未知的急性加重;急性恶化已报告的频率之间的不同研究,这主要是回顾30.。然而,关于急性恶化值得进一步的研究我们的观察仔细评估一个定义明确的问题,更大的随访数据研究。
的事后分析基于呼吸功能类别在本研究进行比较的结果我们之前的第二阶段研究15。每个呼吸功能的改进评级被ATS的标准定义。没有显著区别高剂量组和安慰剂组(见图E2-1在线补充材料)。两项研究之间的差异的原因是未知的。然而,高剂量组和安慰剂组之间的差异显著(p = 0.0053),当被分析变化的VC的评级是基于一个较小的大小(见图E2-2在线补充材料)29日。
副反应更经常发生在患者在高和低剂量pirfenidone组是光敏性,一个著名的副作用与pirfenidone已经在先前的研究记录7,15。厌食症和高架γ-GTP是更常见的在高剂量组比安慰剂组,观察到在我们的二期研究结果相似15。虽然整个pirfenidone治疗组不良事件的发生率相对较高,未发现显著差异的频率之间的病人停止研究pirfenidone治疗组和安慰剂组。这可能是部分病人充分了解关于皮疹的副作用。尽管预期的表现皮疹,pirfenidone在IPF患者一般耐受性良好。
潜在的本研究的局限性包括改变主端点在研究过程中。尽管进化知识VC在12个月内的变化与生存相关22- - - - - -24,26,我们最初选择了最低年代p O26期间遇到了本研究的主要终点我们鼓励的小说在我们之前的观察研究15。改变VC最初打算是一个次要终点。承认6见过我们的第二阶段研究工作需要验证,验证研究计划评估最低年代p O2启动前6期间遇到的III期研究(研究支持的卫生和劳动科学研究资助)。VC和PFS被选为关键二级终端支持的主要终点,和测试VC和PFS的力量是基于样本大小计算的最低年代p O2第一个版本的协议本身。然而,在验证研究中面临的重大困难6见过几个病人退出了第三阶段的研究。因为评估的有效性的担忧pirfenidone基于最低年代p O2测量每12周与VC测量每4周,每个点之间的出人意料地大幅波动的可能性最低年代p O2随着可靠性/再现性的问题年代p O2测量运动如散步27和承认风险的变化或FVC越来越被用作在其他临床研究的主要终点5,21从最低,主要终点是改变了年代p O2在6开会VC在研究期间。虽然这主要终点的变化可能被视为一个主要限制在这项研究中,应该注意的是,决定改变终点之前优先级根据独立DSMB的建议,和样本容量不受影响。
我们承认处理缺失值的限制。人们普遍知道的结果分析可能有潜在的偏见当缺失的值由一个任意的估算方法,并没有完美的归责方法执行最好的在所有的情况下。在这项研究中,我们采用LOCF LOCF一直以来采用的先前的研究。我们认为LOCF不会使平衡支持这两个治疗组,如果没有实质性差异的辍学生。混合模型方法使用重复测量的变化在VC LOCF归咎为灵敏度分析还显示显著或显著治疗效果和支持LOCF分析。图3⇑显示变化的过渡情节VC / 52周。“LOCF估算手段”和“原油手段”在16周内的变化提出了有利影响pirfenidone辍学并没有影响。
其他潜在的限制我们的研究包括以下。1)选择性偏差,患者进入本研究需要能够执行6在基线依照协议;结果的选择组轻度功能障碍患者可能不会因此适用于所有IPF患者有不同程度的肺症状和功能障碍。2)缺乏一个中央的病理学检查。虽然我们承认这些限制,必须指出病人人口连续参加这项研究包括所有合格的和自愿的病人从一般与轻度功能障碍与IPF患者人群。
总之,三期临床试验的结果证明pirfenidone,小说antifibrotic代理,保留了VC和提高PFS比安慰剂在日本IPF患者有轻度功能障碍没有严重不良事件。未来的研究可能会进一步证实我们的发现。
支持声明
这项工作是支持的补助金和成员间质性肺疾病从日本卫生部、劳动和福利,也由日本呼吸道的社会成员的委员会弥漫性肺部疾病。
临床试验
这个临床试验是在日本注册药品信息中心(JAPIC) 9月13日,2005(注册号:japicctci - 050121)。
感兴趣的语句
语句对h .谷口,m . Ebina t . Ogura a . Azuma m .日本须贺y .田口,h .高桥k .醒来时佐藤,m . Takeuchi g .拉Kudoh和t . Nukiwa,研究本身可以发现www.www.qdcxjkg.com/misc/statements.dtl这个临床试验是在日本注册药品信息中心(JAPIC) 9月13日,2005(注册号:japiccti - 050121)。
确认
作者要感谢:m .安藤(表参道Yoshida医院、熊本、日本),美国Kitamura (Minami-Tochigi医院,枥木,日本),y纳街(Tanpopo诊所,仙台宫城县、日本)和a .近藤(新泻区路段Kensin中心、新泻、新泻、日本)的独立DSMB;和k . Murata(志贺医学大学医院,Ohtsu,志贺,日本),m .高桥(志贺医学大学医院),h·哈亚希(日本红十字会医院冈山日本冈山日本),美国诺玛(Tenri医院,Tenri、奈良、日本),t . Johkoh(日本大阪,大阪大学医院),h .荒川(Shimotuga Dokkyo医科大学医院、枥木、日本)和k Ichikado(熊本大学医院、熊本、日本)的成像中心判断面板。作者也感激大肠Tsuboi (Toranomon医院,Minato、东京、日本)的专家建议在6分钟稳态运动测试。最后,由于是扩展到m . Igarashi), t .巨大,t .们t . Tokura y土屋,s . Kakutani h .总裁和y冢本(所有赢家& Co . Ltd .,大阪,日本)对他们的意见和审查的手稿。
日本的Pirfenidone临床研究小组的成员如下。t . Betsuyaku(北海道札幌北海道大学医院)。y Sugawara (Kyowakai带广畜产呼吸道医院,带广畜产,北海道)。美国Fujiuchi(北海道旭川市Dohoku国家医院,)。k .山(岩手县盛冈岩手医科大学医院)。k . Konishi(盛冈Tsunagi温泉医院,盛冈)。宗像m(福岛医科大学医院,福岛)。木村y(东北大学医院,仙台宫城县)。y Ishii (Shimotsuga Dokkyo医科大学医院、枥木)。y Sugiyama (Shimotsuke有望医科大学医院、枥木)。 K. Kudoh (International Medical Center of Japan, Shinjuku, Tokyo). T. Saito (Ibarakihigashi National Hospital, Naka, Ibaraki). T. Yamaguchi (JR Tokyo General Hospital, Shibuya, Tokyo). A. Mizoo (Tokyo Kosei Nenkin Hospital, Shinjuku). A. Nagai (Tokyo Women's Medical University Hospital, Shinjuku). A. Ishizaka and K. Yamaguchi (Keio University Hospital, Shinjuku). K. Yoshimura (Toranomon Hospital, Minato, Tokyo). M. Oritsu (Japanese Red Cross Medical Center, Shibuya). Y. Fukuchi and K. Takahashi (Juntendo University Hospital, Bunkyo, Tokyo). K. Kimura (Toho University Omori Medical Center, Ota, Tokyo). Y. Yoshizawa (Tokyo Medical and Dental University Hospital, Bunkyo). T. Nagase (Tokyo University Hospital, Bunkyo). T. Hisada (Tokyo Teishin Hospital, Chiyoda, Tokyo). K. Ohta (Teikyo University Hospital, Itabashi, Tokyo). K. Yoshimori (Fukujuji Hospital, Kiyose, Tokyo). Y. Miyazawa and K. Tatsumi (Chiba University Hospital, Chiba). Y. Sasaki (Chiba-East Hospital, Chiba). M. Taniguchi (Sagamihara National Hospital, Sagamihara, Kanagawa). Y. Sugita (Saitama Cardiovascular and Respiratory Center, Kumagaya, Saitama). E. Suzuki (Niigata University Medical & Dental Hospital, Niigata). Y. Saito (Nishi-Niigata Chuo National Hospital, Niigata). H. Nakamura (Seirei Hamamatsu General Hospital, Hamamatsu, Shizuoka). K. Chida (Hamamatsu University School of Medicine, University Hospital, Hamamatsu). N. Kasamatsu (Hamamatsu Medical Center, Hamamatsu). H. Hayakawa (Tenryu Hospital, Hamamatsu, Shizuoka). K. Yasuda (Iwata City Hospital, Iwata, Shizuoka). H. Suganuma (Shimada Municipal Hospital, Shimada, Shizuoka). H. Genma (Fukuroi Municipal Hospital, Fukuroi, Shizuoka). R. Tamura (Fujieda Municipal General Hospital, Fujieda, Shizuoka). T. Shirai (Fujinomiya City General Hospital, Fujinomiya, Shizuoka). J. Shindoh (Ogaki Municipal Hospital, Ogaki, Gifu). S. Sato (Nagoya City University Hospital, Nagoya, Aichi). O. Taguchi (Mie University Hospital, Tsu, Mie). Y. Sasaki (Kyoto Medical Center, Fushimi, Kyoto), H. Ibata (Mie Chuo Medical Center, Tsu). M. Yasui (Kanazawa University Hospital, Kanazawa, Ishikawa). Y. Nakano (Shiga Medical University Hospital, Otsu, Shiga). M. Ito and S. Kitada (Toneyama National Hospital, Toyonaka, Osaka). H. Kimura (Nara Medical University Hospital, Kashihara, Nara). Y. Inoue (Kinki-Chuo Chest Medical Center, Sakai, Osaka). H. Yasuba (Takatsuki Red Cross Hospital, Takatsuki, Osaka). Y. Mochizuki (Himeji Medical Center, Himeji, Hyogo). S. Horikawa and Y. Suzuki (Japanese Red Cross Wakayama Medical Centre, Wakayama). N. Katakami (Institute of Biomedical Research and Innovation Hospital, Kobe, Hyogo). Y. Tanimoto (Okayama University Hospital, Okayama). Y. Hitsuda and N. Burioka (Tottori University Hospital, Yonago, Tottori). T. Sato (Okayama Medical Center, Okayama). N. Kohno and A. Yokoyama (Hiroshima University Hospital, Hiroshima). Y. Nishioka (Tokushima University Hospital, Tokushima). N. Ueda (Ehime Prefectural Central Hospital, Matsuyama, Ehime). K. Kuwano (Kyusyu University Hospital, Fukuoka). K. Watanabe (Fukuoka University Hospital, Fukuoka). H. Aizawa (Kurume University Hospital, Kurume, Fukuoka). S. Kohno and H. Mukae (Nagasaki University Hospital of Medicine and Dentistry, Nagasaki). H. Kohrogi (Kumamoto University Hospital, Kumamoto). J. Kadota, I. Tokimatsu and E. Miyazaki (Oita University Hospital, Yufu, Oita). T. Sasaki (Miyazaki University Hospital, Miyazaki). M. Kawabata (Minami Kyusyu National Hospital, Aira, Kagoshima).
脚注
社论评论见728页。
- 收到了2009年1月13日。
- 接受2009年11月20日。
- ©人期刊有限公司