摘要
在63例COPD患者的随机对照试验中,12周的ICS/LABA治疗下调了sars - cov -2相关基因的支气管上皮表达ACE2.和ADAM17与Laba单独相比。这可能对COPD中的Covid-19易感性/严重程度产生影响。https://bit.ly/3vznbvo.
到编辑:
观察性研究表明,COPD与2019年(Covid-19)严重程度和死亡率增加有关的冠状病毒疾病有关[1].吸入性糖皮质激素(ICS)通常用于治疗慢性阻塞性肺病,它与慢性阻塞性肺病中细菌性肺炎的风险增加和病毒免疫反应受损有关。这类药物是否影响严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)受体和辅助因子的气道表达(可能改变COVID-19的易感性和结局)目前尚不清楚。因此,在一项COPD患者的随机对照试验中,我们检测了ICS治疗对下气道支气管上皮细胞(BECs)中sars - cov -2相关基因表达的影响。
我们进行了裁军试验(招募2015年10月- 2019年6月;clinicaltrials.gov标识符nct02833480.;英国哥伦比亚大学/普罗维登斯卫生保健伦理审批H14-02277)检查两个长效β的影响2Agenist(Laba)/ ICS与COPD人士气道微生物组合的组合。经过4周的果肉(for)run-in,我们随机化参与者接受12μg,甲酚/芽苷(for / bud)12/400μg,或Salmeterol / fluticasone丙酸盐(Sal / Flu)25/250μg,每天两次12周。我们在治疗之前和之后根据标准方案(第六至第八发频道,右上叶)收集支气管刷样品,并通过RNA测序测量如前所述的基因表达[2].尚未报告共同原发性结果(12周内总细菌人口和多样性的变化)。但是,为了应对Covid-19大流行的紧迫性,我们进行了一个特设编码SARS-COV-2进入受体的基因分析(ACE2.那BSG.)和宿主共同因素(TMPRSS2那ADAM17那弗林)。
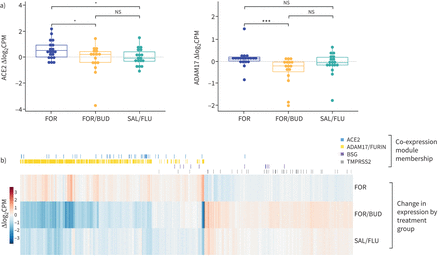
63名参与者(中位年龄64岁,男性83%,目前46%的吸烟者,预测61.36%的平均强制呼气量)被随机化。在人口统计学,肺功能,机理或最近的ICS使用方面没有差异(Kruskal-Wallis和Fisher的确切测试P> 0.05)。总体预处理基因表达的主要成分分析显示治疗组之间或在注册预注册ICS用户和非用户之间没有差异。54名参与者均可获得预治疗后和治疗后的基因表达数据(7名参与者未能出席后治疗后支气管检查,两者都没有足够的预处理RNA)。治疗12周后,For / Bud和Sal / Flu臂均显示出显着降低的变化ACE2.相对于单疗法的表达(威尔科克朗等级和试验P = 0.049和P = 0.041),并且FOR /芽臂显示出显着更低的变化ADAM17相对于单疗法的表达(Wilcoxon等级和测试P = 1.36×10-4)(图1A)。这表明ICS对这些基因的转录具有抑制作用。ICS治疗对表达没有影响BSG.那TMPRSS2要么弗林.当按基线吸烟状况分层时,结果相似ADAM17(/芽相对对于前吸烟者和P = 0.002的P = 0.01,但对于当前吸烟者而言),但对此并不重要ACE2..
支气管上皮细胞(BEC)基因表达在解除武装研究中。通过RNA测序(Illumina Nextseq 500; Illumina,San Diego,CA,USA)测定在支气管镜检查期间收集的BEC在支气管镜检查期间收集的BEC的基因表达用配对42×42bp读数测定。使用鲑鱼对排序数据对齐至Gencode基因组参考组件GRCH37释放组件31。低丰度基因(日志2百万数计(日志280%的>样本中CPM <1或TPM <2)被过滤掉,共留下15 667个基因。a)显示处理前后表达变化的箱形图(Δlog2CPM)ACE2.(编码SARS-CoV-2受体)ADAM17(编码金属蛋白酶,其切割血管紧张素转换酶(ACE)2蛋白,促进ACE2-SARS-COV-2复合物的内吞作用)。仅示出了具有预治疗后和治疗后的基因表达数据的参与者(63名随机参与者中的54例)。组之间的比较是通过Wilcoxon Rank-Sum测试。*:P <0.05,***:P <0.001。b)基因表达前治疗后变化的热图(中位数Δlog2在错误发现率(FDR) <0.1的情况下,至少有一个显著组间Wilcoxon秩和检验的基因(15 667个总基因中的977个)的CPM。列代表单个基因,并使用分层聚类(R中NMF包装中的“热图”功能)进行排列。福莫特罗(FOR)/布地奈德(BUD)和沙美特罗(SAL)/氟替卡松(FLU)治疗与FOR治疗相比,对基因表达的影响倾向于相反的方向。提示吸入皮质激素(ICS)对这些基因的表达有分级效应。此外,根据预处理表达的加权基因相关网络分析(WGCNA)确定的sars - cov -2相关基因共表达模块的成员,对每个绘制的基因进行注释(以对数表示)2(TPM + 1),软阈值功率β= 6,最小模块大小50基因)。IC治疗趋于降低与之相关的基因的表达ACE2.和ADAM17/弗林,而基因是联合的TMPRSS2和BSG.倾向于由ICS治疗上调。ns.:不重要的。
此外,我们探讨了ICS治疗如何使用聚类热图(图1B.)。Laba-of Laba和Laba / ICS治疗对基因表达有适度但相反的效果:在用于/芽和萨尔/流感武器的下调和武器中满足了用于臂的上调。反之亦然,提示ICS类效应。总的来说,尽管剂量相似(倍氯米松当量),FOR/BUD似乎比SAL/FLU对基因表达的影响更大。原因尚不清楚,但可能是由于BUD在气道上皮细胞中相对滞留较多[3.].
接下来,我们确定了与sars - cov -2相关的每个关键基因共同表达的基因(由加权基因相关网络分析确定[4.])随着ICS治疗而改变。ACE2.包含444个基因模块;根据《基因本体论》和《京都基因和基因组百科全书》的注释,该模块对I型干扰素(IFN-I)和病毒感染相关基因高度富集。ADAM17和弗林在1900个基因的同一模块中,富集了与天生免疫,细胞因子产生和传染性和自身免疫疾病有关的基因。BSG.和TMPRSS2每个都包含在788和985个基因的模块中,两者都富集了与细胞内方法相关的基因。然后,根据每个基因的共表达模块成员资格,我们注释了聚类热图。ACE2.和ADAM17/弗林模块基因聚集在热图中FOR/BUD和SAL/FLU治疗下调基因的区域,表明ICS下调基因与这些关键的sars - cov -2相关基因高度相关。
我们的分析扩展了我们之前的发现ACE2.基因和蛋白表达在BECs中增加[2]及肺组织[5.通过表现出来的人的人ACE2.被ICS治疗下调。我们的数据来自ICS/LABA治疗的随机对照试验,证实了最近的一项研究表明,ICS对糖尿病有下调作用ACE2.COPD患者的痰(BUD和FLU)和小鼠肺(BUD、FLU和倍氯米松)中的表达[6.].在这项研究中,与我们的结果一致,IC没有影响表达BSG.要么TMPRSS2[6.].另一组最近进行了一个后HOC.分析(7.[格罗宁根和雷明大学对阻塞性肺病(糖果)试验中皮质类固醇的研究,表明ACE2.COPD患者经FLU治疗后气道活检标本的表达下调。我们的数据补充了这些结果ACE2.下调可能是ICS类效应的结果,而且可能发生得更剧烈(仅在治疗12周后,而GLUCOLD研究中为26周)。
ACE2表达差异对COVID-19的相对重要性仍存在争议。呼吸道中ACE2蛋白的可用性增加可能会增加COVID-19的易感性和严重性;理论上,ics介导的下调ACE2.由本处及其他人士呈报[6.那7.因此,可能是保护的。相反,由于ACE2是肾素 - 血管紧张素系统的关键负调节因子,因此其下调可能易于肺损伤[8.].我们的基因网络分析显示ACE2.与与病毒的先天免疫应答有关的基因,特别是IFN-1相关的基因,并且该模块中的基因往往被ICS治疗抑制。动物模型表明,延迟的IFN-I对SARS-COV感染的反应可能导致过度的炎症和死亡[9.].事实上,慢性阻塞性肺病患者在病毒感染后IFN-I反应已经受损[10.].因此,COVID-19中的ACE2表达可能是一把双刃剑,但COVID-19中COPD和ICS治疗之间的任何相互作用都可能比仅通过ACE2表达的改变更复杂。
最近报道了一种新的,截断同种型的ACE2,其在肺上皮中转录独立和高度表达[11.].该同种型没有细胞外结构域并且不结合SARS-COV-2穗蛋白,这意味着其表达的变化可能对Covid-19风险没有影响。这一重要发现挑战了功能的概念ACE2.是一个ifn刺激基因,因为它似乎只是由IFN-I诱导的截断亚型。我们尝试了外显子水平分析来量化这种亚型,但我们的测序深度不足以产生可靠的结果。未来对这种新型异构体的研究将是理解我们当前发现的含义的关键。
据我们所知,我们发现ICS疗法下调了ADAM17人体中的表达是新颖的。SARS-COV-2穗蛋白诱导ADAM17依赖于ACE2外胚瘤的脱落,从而产生ace2的可溶性形式,促进病毒和细胞膜的融合[12.].抑制Adam17至少部分地阻断培养的上皮细胞中的SARS-COV进入[12.那13.].此外,Adam17在白细胞介素(IL)-6信号中起着至关重要的作用,在严重的Covid-19中激活14.];它被描述为促炎trans和抗炎经典- (即通过膜结合的IL-6受体(IL-6信号通路[15.].然而,任何影响ICS介导的ADAM17的下调可能对Covid-19易感性或结果都会在这个阶段投机。
尽管存在局限性(包括相对较小的样本大小,短短的随访期和缺乏伴随蛋白质表达或功能数据),但我们的结果表明,ICS改变了较低气道BEC与SARS-COV-2和Covid-19相关的基因的表达生物学。上部(鼻)的相对重要性相对这些基因在SARS-CoV-2传播中的低(支气管)表达有待进一步研究。然而,我们的结果为COVID-19中类固醇(STOIC)试验的结果提供了潜在的机制支持(clinicaltrials.gov identifier)nct04416399.),在吸入芽中表明早期Covid-19的紧急护理/住院减少了[16.].试验结果需要在COPD人口中确认,这增加了BECACE2.在确定我们的研究结果的临床相关性之前。在没有任何流行病学证据表明ICS疗法会增加COVID-19的严重程度或死亡率的情况下[17.],我们同意国际共识,即COPD患者的ICS治疗如果在临床上表明,直至提供进一步证据可获得进一步证据。
可分享的PDF.
致谢
作者感谢丁文杰和陶春红为圣保罗基金会COVID-19应对基金慷慨筹款和捐赠。我们感谢BRC-Seq(不列颠哥伦比亚大学(UBC),温哥华,BC,加拿大)的Ryan Vander Werff和Tara Stach进行RNA测序;以及Chung张和Julia Yang (UBC心肺创新中心),感谢他们在实验室标本方面的帮助。
脚注
数据共享声明:个人参与者基因表达数据是公开可用的通过基因表达综合(地理)www.ncbi.nlm.nih.gov/geo/(加入号码GSE162120)。解除武装学习协议可用https://clinicaltrials.gov.(标识符nct02833480.)。额外的个人参与者数据提出了本文报告的结果,在去识别后,将在发布到任何调查人员后立即提供,并在合理的要求后立即提供。建议应直接向主要调查员进行,唐D.In(don.sin@hli.ubc.ca)。
作者贡献:数据收购:S. MILNE,F.S.Leitao Filho,T.Shaipanich,S.F.van eeden,准leung,s. lam和d.d。罪;数据分析和解释:S. Milne,X. Li,A.I.Hernándezcordero,c.x.杨,五。Leitao Filho,C.W.T.杨,准梁和D.D.罪; drafting of manuscript: S. Milne and X. Li; critical revision of draft manuscript: S. Milne, X. Li, A.I. Hernández Cordero, C.X. Yang, F.S. Leitao Filho, C.W.T. Yang, S.F. van Eeden, J.M. Leung, S. Lam and D.D. Sin; all authors reviewed and approved the final version of the manuscript; all authors agree to be accountable for all aspects of the work including data integrity.
兴趣冲突:S. Milne在提交的工作之外向Novartis和Boehringer Ingelheim报告个人费用。
利益冲突:X.李没有什么可披露的。
利益冲突:C.X.杨没有什么可以披露的。
利益冲突:F.S.Leitao Filho没有什么可披露的。
利益冲突:A.I. Hernández Cordero没有什么可披露的。
利益冲突:C.W.T.杨没有什么可以披露的。
利益冲突:T. Shaipanich没什么可透露的。
利益冲突:S.F. van Eeden没有什么可透露的。
利益冲突:J.M. Leung没有什么可披露的。
利益冲突:S. LAM没有什么可披露的。
利益冲突:D.D.罪的报告从Astrazeneca进行赠款,在这项研究期间;从诺特里斯和Boehringer的讲座讲座的个人费用,从Astrazeneca的讲座,在提交的工作之外进行讲课和个人费用。
支持声明:DISARM研究由阿斯利康研究人员发起的拨款资助。RNA测序工作由圣保罗基金会- COVID-19快速应对基金提供资金。S. Milne和A.I. Hernández Cordero得到了MITACS加速计划的支持。梁振英先生由迈克尔·史密斯健康研究基金会-健康专业研究者奖和普罗维登斯健康护理研究所资助。D.D. Sin得到了COPD奖加拿大Tier 1研究主席和HLI de Lazzari家族主席的支持。本文的资金信息已存入Crossref资助者注册表.
- 已收到2021年1月14日。
- 公认2021年3月21日。
- 版权所有©作者2021。
此版本在Creative Commons归因非商业许可证4.0的条款下分发。用于商业再现权和权限联系权限{exernet.org