摘要
在2003年的几个月中,一种新发现的称为严重急性呼吸系统综合症(SARS)的疾病在全世界迅速传播1那2那3..将新的冠状病毒(SARS-COV)鉴定为SARS病原体4.那5.那6.那7.,引发严重的肺炎和急性,往往致命,肺部衰竭8..此外,受感染的个体之间的甲型流感,如西班牙流感9.那10以及新呼吸道疾病病毒的出现11那12由急性肺衰竭引起的高致死率13.在细胞系中,血管紧张素转化酶2(ACE2)已经被鉴定为潜在的SARS-CoV的受体14.SARS-COV感染的高致死性,其巨大的经济和社会影响,担心再生爆发以及作为生物武器的潜在滥用这种病毒使其能够了解SARS-COV的发病机制。在这里,我们提供了ACE2是至关重要的SARS-COV受体的第一个遗传证据体内.SARS-CoV感染和SARS-CoV的Spike蛋白降低ACE2的表达。值得注意的是,在小鼠体内注射SARS-CoV刺突可加重急性肺衰竭体内可以通过阻断肾素-血管紧张素途径来减弱。这些结果从分子上解释了为什么SARS- cov感染会导致严重的、通常是致命的肺衰竭,并为SARS和可能的其他呼吸道疾病病毒提供了合理的治疗方法。
主要
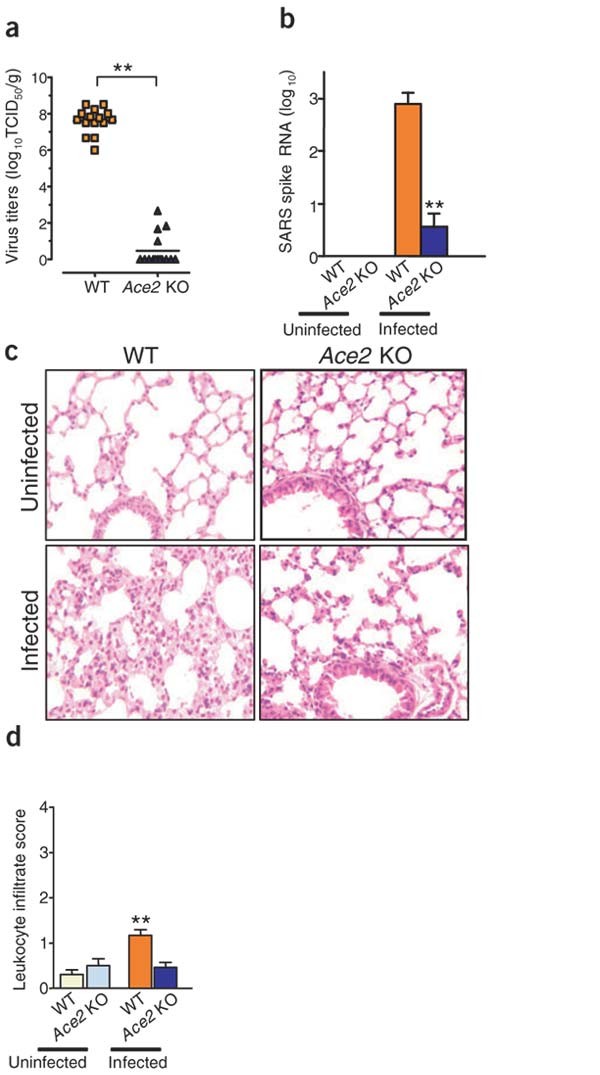
最近,ACE2在细胞系中被鉴定为具有功能的SARS冠状病毒受体14.但也可以从中识别出可能的第二个受体,CD209L(L-SIGN)在体外学习15.因此,尚不清楚ACE2对SARS-CoV感染是否确实至关重要体内.为了从基因上解决这个问题,我们感染了ACE2.基因敲除16并控制sars冠状病毒野生型小鼠。之前报道17,野生型小鼠SARS-CoV感染导致病毒在肺部复制和大量恢复(>107.组织培养感染剂量,可感染50%的单层细胞(TCID)50.T)每根克肺组织)传染病(图1一个).在ACE2.基因敲除小鼠,仅感染SARS-CoV的病毒的非常低的量可被回收(<102TCID.50.每克肺组织;图1一个)和SARS-CoV棘突RNA的拷贝数大大减少(图1 b).小鼠的SARS冠状病毒感染与轻度病变在肺发展(相关图1 c, d).此外,肺部病理改变减少了ACE2.与野生型小鼠比较的突变小鼠(图1 c, d).这些数据提供了第一个基因证据,证明ACE2确实是一个关键因素体内需要感染SARS病毒的有效复制SARS受体。
(一种那B.) sars冠状病毒复制(一种)和检测SARS-COV偶像RNA(B.)在野生型(wt)和ACE2.基因敲除小鼠。在感染第2天从肺组织中检测病毒复制。病毒滴度(平均对数)10TCID.50.每克肺组织)显示为单个小鼠。N=每组15人。使用实时RT-PCR测定SARS-COV尖峰RNA表达并标准化为小鼠Actb.数据显示为mean + s.e.m.。N=每组15人。Arunachal Pradesh,P.< 0.01。(C)肺组织病理学(原始放大倍数×200)和(D.)由白细胞浸润的肺损伤分数进行控制和SARS-COV感染的野生型和ACE2.基因敲除小鼠。肺标本SARS-CoV感染后采取的第6天。
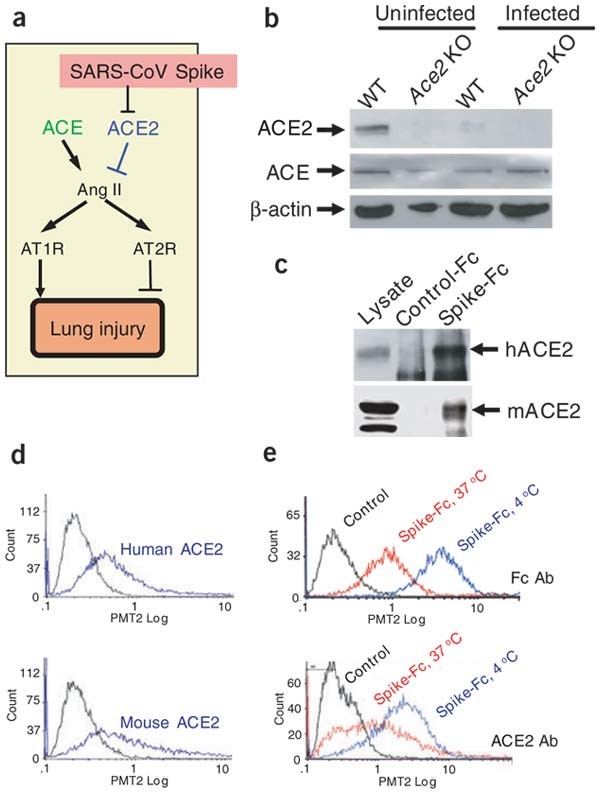
我们最近表明,肾素 - 血管紧张素系统在严重的急性肺损伤中具有至关重要的作用,并且SARS-COV受体ACE2在急性肺部失效中具有保护作用18(图2一个).值得注意的是,野生型小鼠的实验SARS-CoV感染体内导致肺中的ACE2表达相当减少(图2 b)表明降低的ACE2表达可能在SARS-COV介导的严重急性肺病变中具有作用。相比之下,在SARS-COV感染的小鼠中,ACE肺表达水平并未明显改变(图2 b).因此,我们推测,SARS冠状病毒可能是通过影响ACE2肺疾病。为了验证这一想法,我们建立了定义模型系统使用重组SARS-CoV的表面刺突蛋白,其是用于ACE2结合的必要的配体14.这个模型系统使我们避免了病毒复制或感染可能产生的二次效应体内并直接测试SARS-COV穗蛋白是否可能通过调节ACE2对急性肺损伤产生不利影响。
(一种)肾素-血管紧张素系统在急性肺衰竭和SARS-CoV作用的示意图。(B.) sars冠状病毒感染小鼠肺部ACE2蛋白下降,但ACE水平正常。肺匀浆制备对照和sars - cov感染野生型ACE2.第2天淘汰(Ko)小鼠并通过Western Blot分析。(C)重组Spike(S-1190)-Fc蛋白与人ACE2 (hACE2)和小鼠ACE2 (mACE2)的结合。Spike-Fc蛋白而非control-Fc蛋白分别下调了A549人肺泡上皮细胞和IMCD小鼠肾上皮细胞总细胞提取物中的hACE2和mACE2。总裂解物作为对照显示。(D.)穗-Fc蛋白与细胞培养中的人和小鼠ACE2的结合。将293用Hace2或MEFE 2转染的细胞与尖峰-CC孵育,并通过FACS(蓝线)检测结合。与尖峰-CC孵育的非杂种293个细胞,然后被Fc特异性抗体显示为对照(黑线)。(E.在Vero E6细胞中,在37℃与4℃相比,在37℃下与穗-Fc蛋白结合后,降低ACE2的细胞表面表达。使用ACE2特异性单克隆抗体与尖峰-CC孵育3小时,检测ACE2表面表达。使用Fc特异性抗体获得类似的数据,以直接检测表面结合的尖峰Fc并避免掩蔽ACE2表位。示出了代表性的FACS直方图,包括具有同种型匹配抗体的背景控制。
我们首先测试了重组SARS-COV偶像蛋白(补充图1与人类和小鼠的ACE2蛋白结合使用在体外下拉测定。我们的重组穗-CC蛋白确实拉下了人和小鼠ACE2(图2 c).SARS-COV尖峰-FC与人和小鼠ACE2的结合通过FACS-FC至293细胞过表达人或小鼠ACE2(图2 d).此外,Spike-Fc与Vero E6细胞内源性ACE2结合(图2 e).值得注意的是,在Vero E6细胞中,Spike-Fc与内源性ACE2的结合导致ACE2表面表达下调(图2 e和补充图1在线)。Spike-Fc还降低了人和小鼠293细胞中过表达ACE2的表面水平(未显示),并触发了小鼠ACE2转染但未控制cd4转染293细胞的合胞体形成(数据未显示)。因此,类似于其他病毒与受体的相互作用19, SARS-CoV刺突蛋白结合ACE2细胞系或SARS-CoV感染体内导致减少的ACE2蛋白表达。
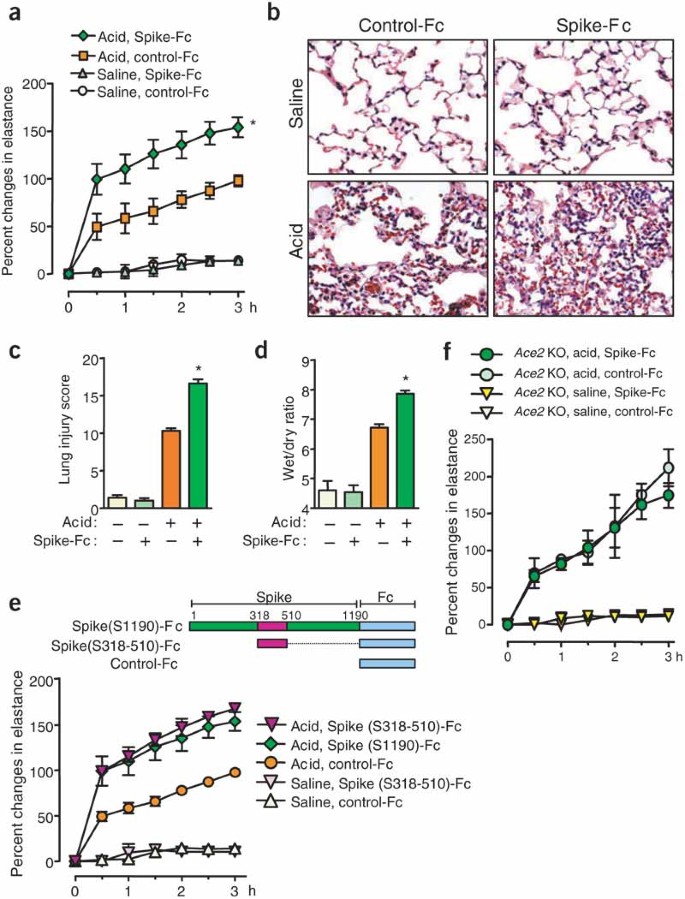
因为ACE2是一个至关重要的SARS冠状病毒受体(图1), SARS-CoV刺突蛋白结合ACE2下调ACE2表达(图2),以及在严重急性呼吸衰竭的ACE2表达的结果损失18,我们检测了SARS-CoV的Spike蛋白,这是关键的ACE2结合蛋白20.那21,可能影响急性肺损伤的严重程度体内.值得注意的是,Spike-Fc蛋白治疗加重了野生型小鼠的肺功能,而control-Fc蛋白没有显示出明显的效果(图3).此外,Spike-Fc处理酸激野生型小鼠后,肺实质的病理改变增强(图3 b, c和补充表1在线)和增加由湿/干肺重量比定义的肺水肿(图3 d).接下来,我们制作了一个spik缺失突变体,该突变体只包含先前绘制的ace2结合域(氨基酸318-510)21融合到人类Fc (图3 e和补充图1在线)。这种短穗(S318-510)-Fc蛋白含有最小的ACE2结合位点,也通过FACS检测与细胞系中的ACE2结合,并下调ACE2的细胞表面表达(补充图1在线)。Spike(S318-510)-Fc治疗后,野生型小鼠酸致急性肺损伤加重(图3 e).值得注意的是,体内给药Spike-Fc蛋白对肺衰竭的严重程度没有影响ACE2.基因敲除小鼠(图3 f),表明穗蛋白对急性肺损损伤的影响是ACE2特异性。
(一种)盐水后的肺弹性测量或穗-Fc蛋白 - (5.5 nmol / kg)或对照-FC-(5.5 Nmol / kg)处理的野生型小鼠。N每组= 5-7。*P.在酸损伤后,spike - fc处理和对照fc处理野生型小鼠的整个疗程中均< 0.05。(B.肺组织病理学。展示了具有代表性的图像。原始的放大,×200。(C)肺损伤得分(补充表1在线)。Arunachal Pradesh,P.<0.01相对于对照-Fc处理的野生型。(D.在有无酸致肺损伤的情况下,以肺湿/干重量比作为肺水肿的读数。*P.对照组与spike - fc处理小鼠的酸激反应之间的差异< 0.05。(E.)通过穗(S318-510)的严重急性肺部衰竭(S318-510) - 酸攻击小鼠中的富℃(5.5 nmol / kg)处理。方案(上面板)显示钉的ACE2结合域(S318-510)。肺弹性测量(下面的面板)显示尖峰(S318-510)-FC诱导酸性野生型小鼠的严重急性肺部衰竭,与尖刺相当(S1190)-FC。N每组= 5-7。P.与酸损伤后Spike(S318-510)-Fc或Spike(S1190)-Fc处理和对照-Fc处理的野生型小鼠相比,在整个过程中均< 0.05。(F) Spike-Fc蛋白- (S1190;5.5 nmol/kg)或对照fc - (5.5 nmol/kg)处理ACE2.敲除小鼠(KO)。N= 5-7为每个组。
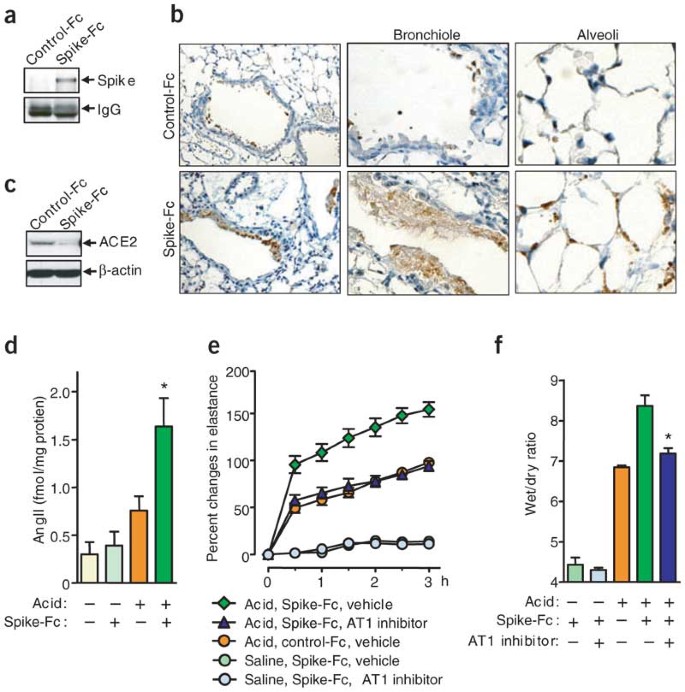
为了进一步阐明腹膜内注射型穗-Fc蛋白是否直接影响小鼠的肺病理学,我们检查了肺中注射的尖刺-Fc蛋白的定位。通过使用人FC特异性抗体的Western印迹在肺匀浆中检测到尖峰-Fc(图4),未检测到注入的控制FC。此外,使用免疫组织化学,我们发现穗-Fc蛋白局部定位成支气管上皮细胞,炎症渗出物和肺泡肺细胞(图4 b).值得注意的是,Spike-Fc主要定位于严重病变(图4 b).穗-CC蛋白的本地化类似于SARS-COV感染的小鼠中的尖峰抗原染色22.Spike-Fc处理导致酸处理野生型小鼠肺中ACE2蛋白表达下调体内(图4摄氏度),与sars冠状病毒感染小鼠ACE2蛋白下调(图2一个)和Spike-Fc蛋白处理的细胞在体外(图2 e).这些结果表明,SARS-CoV Spike蛋白可通过ACE2直接影响严重急性肺衰竭的发展。
(一种那B.)的腹膜内注射本地化穗(S-1190)-Fc肺组织英寸(一种)采用Protein G Sepharose下拉和人fc特异性抗体western blot检测Spike-Fc。小鼠IgG作为负载对照。(B.)肺免疫组化检测Spike(S-1190)-Fc或对照-Fc蛋白,使用人fc特异性抗体。Spike(S-1190)-Fc定位于支气管上皮细胞(左;原始放大,×100),炎性渗出细胞(中;原始放大图×200)和肺泡肺细胞(右图;原始的放大,×200)。(C)降低了Spike(S-1190)- fc处理小鼠肺中的ACE2蛋白表达。从control-Fc -和Spike(S-1190)- fc处理的野生型小鼠中制备肺匀浆,并用ace2特异性抗体进行western blot分析。(D.)生理盐水或酸误吸后Spike(S1190)- fc蛋白或对照- fc处理野生型小鼠肺中的AngII肽水平。酶免疫法检测血管内皮素ii水平。平均±s.e.m.。*P.< 0.05比较酸损伤后Spike(S1190)- fc -和对照- fc处理的野生型小鼠。(E.)用AT1R抑制剂氯沙坦(15 mg/kg)处理的酸加Spike(S1190) fc激发的野生型小鼠的肺弹性测量。N=每组4-6人。P.<0.05比较氯沙坦处理穗(S1190)-Fc激发的用载体处理的穗(S1190)-Fc攻击的小鼠的小鼠。(F)湿干氯沙坦的存在或不存在酸和穗(S1190)攻击的小鼠的肺中的重量比(15毫克/千克)。N=每组4-6只。*P.<0.05,将Losartan处理的野生型与酸损伤后3小时的氯沙坦处理的野生型与载体处理的野生型小鼠进行比较。
ACE2作为一个羧肽酶,从血管紧张素I (AngI)中切割一个残基,生成Ang1-9(参考文献)。23那24)和血管紧张素II (AngII)的单个残基生成Ang1-7(参考文献。23).相比之下,ACE2同源物ACE将十肽AngI切成八肽AngII25.因此,ACE2抵消ACE的功能和血管紧张素Ⅱ的生产负调节(图2一个).为了测试Spike-Fc注射是否确实影响肾素-血管紧张素系统的功能,我们分析了酸和Spike-Fc处理小鼠肺中的AngII水平。酸吸入增加了野生型小鼠肺中的AngII水平。值得注意的是,我们进一步观察到使用Spike-Fc (图4 d).为了通过增加血管生成和肾素血管紧张素系统的功能改变促进肺病促进肺病发病机制,我们阻断了Angii受体类型1(AT1R)26用特异性抑制剂。AT1R是介导血管诱导的血管渗透性和严重急性肺损伤的关键受体18.在AT1受体的抑制作用减弱确实在穗的Fc处理的小鼠急性重度肺损伤(图4 e).抑制AT1R也减弱了肺水肿(图4 f).综上所述,我们的数据表明,SARS-CoV峰值可以通过调节肾素-血管紧张素系统夸大急性肺衰竭。此外,抑制AT1R可以挽救SARS-CoV尖锋介导的肺衰竭。
据估计,西班牙流感病毒在20世纪初夺去了2000多万人的生命,大约0.5%的感染者是致命的9.那10,而SARS-COV感染的致死性甚至达到10%,即使现代化的重症监护治疗1那2那3..考虑到SARS的高致死率和全球范围内SARS爆发的巨大经济和社会影响,阐明疾病发病机制对于未来再次爆发时的治疗至关重要。此外,最近在人类中爆发的甲型禽流感(H5N1)导致了高达70%的急性呼吸衰竭死亡率12.在发现SARS-CoV之前,已知有两种冠状病毒(HCoV-229E和HCoV-OC43)会感染人类,但它们只会引起自限性上呼吸道感染(普通感冒的30%),从未报告会导致严重疾病27.这些人冠状病毒与sars冠状病毒发病机制的显著差异的分子决定因素尚不清楚。
我们的数据为严重的肺部衰竭和与SARS相关的致死率提供了分子解释:我们假设通过将SARS-COV尖峰蛋白与ACE2结合的ace2下调,使SARS-COV的感染结果下调。鉴于ACE2是肺水肿和急性肺部衰竭严重程度的关键负调节因素,SARS-COV偶像蛋白介导的ACE2下调则有助于肺病理的严重程度。这种情况会解释这个“相对无害”的冠状病毒的家庭成员如何变成了致命病毒。值得注意的是,具有SARS的小群体中的近期数据表明,影响ACE函数的插入缺失ACE多态性与疾病严重程度相关28暗示我们的发现确实与人类相关。
我们的数据提供了SARS发病机制和肾素-血管紧张素系统在肺衰竭中的作用之间的分子联系。因此,重组ACE2蛋白不仅可以阻断SARS冠状病毒的传播,而且调节肾素-血管紧张素系统也可以用于保护SARS患者,以及感染其他病毒的患者,如禽流感a株、发展为急性严重肺衰竭和急性呼吸窘迫综合征。
方法
对于方法的详细信息,请参阅补充的方法网上。
在活的有机体内SARS感染。
本研究使用的SARS-CoV(北京株,PUMC01分离株)由中国医学科学院、中国国家人类基因组中心提供。所有小鼠研究均由中华人民共和国卫生部科学技术司批准。小鼠经鼻接种病毒100 μl (105.23TCID.50.).第2天处死小鼠,取肺进行进一步分析。我们评估肺损伤评分如前所述30..
SARS-CoV刺突蛋白结合实验。
我们克隆了SARS-CoV刺突蛋白(Urbani株1 - 1190氨基酸)的编码序列或仅包含先前定位的刺突蛋白序列21ace2结合域(氨基酸318-510)与人IgG1的Fc部分产生融合蛋白。我们用亲和层析法从转染的CHO细胞中纯化了Spike-Fc蛋白。为在体外结合测定中,我们使用细胞裂解物从A549人肺泡上皮细胞或小鼠IMCD肾上皮细胞,我们拉下穗-Fc或对照人IgG-Fc蛋白使用蛋白G琼脂糖,随后通过Western印迹。用于流式细胞术,我们分离使用EDTA和PBS的2mM的混合物Vero E6细胞,并在4℃或37℃下3小时与钉-Fc或对照人IgG-Fc蛋白温育它们。然后,我们培养的细胞与ACE2特异性抗体或FITC缀合的人IgG特异性抗体。
重组Spike-Fc体内挑战在老鼠身上。
采用酸吸入致急性肺损伤小鼠模型18所有穗的Fc体内实验。在酸处理期间,小鼠腹腔注射Spike(S1190)-Fc、Spike(S318-510)-Fc或control-Fc(每个5.5 nmol/kg)三次(在酸处理前30分钟、1小时和2小时)。为了抑制AT1对Spike- fc介导的急性肺损伤,我们用AT1抑制剂氯沙坦(15 mg/kg)治疗Spike(S1190)- fc激发的小鼠。肺损伤评分如前所述30..
统计分析。
所有数据表示为平均值±S.E.M。在单一时间点测量用非配对分析T.- 试验(病毒滴度,SARS-CoV棘突-RNA水平),ANOVA和双尾T.-test(弹性变化百分比,湿/干比AngII水平)或Kruskal-Wallis测试(组织学评分)。时间过程采用重复测量(混合模型)方差分析与Bonferroni后T.测试。所有统计检验均使用GraphPad Prism 4.00 (GraphPad Software)和JMP (SAS Institute)程序进行计算。P.< 0.05为差异有统计学意义。
加入号码。
SARS冠状病毒(北京株,PUMC01分离株)的Genbank登录号为AY350750.
注意:补充信息可以在自然医学网站上找到.
加入代码
参考
- 1
曾,k.w等。香港出现多宗严重急性呼吸系统综合症病例。心血管病。j .地中海。348, 1977 - 1985(2003)。
- 2
李,n。等。香港严重急性呼吸综合征的重大爆发。心血管病。j .地中海。348, 1986 - 1994(2003)。
- 3.
Poutanen, S.M.等。在加拿大查明严重急性呼吸系统综合症。心血管病。j .地中海。348,1995-2005(2003)。
- 4.
Ksiazek, T.G.等。一种与严重急性呼吸综合征相关的新型冠状病毒。心血管病。j .地中海。348, 1953 - 1966(2003)。
- 5.
等。新型冠状病毒在严重急性呼吸综合征患者中的鉴别。心血管病。j .地中海。348, 1967 - 1976(2003)。
- 6.
罗塔,P.A.等。一种与严重急性呼吸综合征相关的新型冠状病毒的特征。科学300,1394-1399(2003)。
- 7.
Marra,M.A.等。SARS相关冠状病毒的基因组序列。科学300, 1399 - 1404(2003)。
- 8.
严重急性呼吸系统综合症(SARS)流行病学工作小组。世卫组织关于严重急性呼吸系统综合征(SARS)流行病学的共识文件。(http://www.who.int/csr/sars/en/WHOconsensus.pdf, 2003)。
- 9.
牛津,J.S.流感20世纪的流行病,特别是1918年的特刊:病毒学,病理和流行病学。Rev. Med。病毒。10,119-133(2000)。
- 10
更新账户:1918-1920年“西班牙”流感大流行的全球死亡率。公牛。嘘。地中海。76.,105-115(2002)。
- 11
TRAN,T.H.et al。越南10例禽流感A(H5N1)。心血管病。j .地中海。350,1179-1188(2004年)。
- 12
世界卫生组织。2004年9月7日人类感染甲型H5N1禽流感确诊个案(http://www.who.int/csr/disease/avian_influenza/country/ cases_table_2004_09_07 / en / print.html,2004年)。
- 13
Fouchier, R.A.等。甲型禽流感病毒(H7N7)与人类结膜炎和致命的急性呼吸窘迫综合征病例。Proc。国家的。学会科学。美国101, 1356 - 1361(2004)。
- 14
李,W。等。血管紧张素转化酶2是SARS冠状病毒的功能性受体。自然426, 450 - 454(2003)。
- 15
Jeffers, S.A.等。CD209L (L-SIGN)是严重急性呼吸综合征冠状病毒的受体。Proc。国家的。学会科学。美国20., 20(2004)。
- 16
克拉科沃,M.A.等人。血管紧张素转换酶2是心脏功能的重要调节因子。自然417,822-828(2002)。
- 17
的Subbarao,K。等人。现有感染和中和抗体的被动转移防止在小鼠呼吸道严重急性呼吸综合征冠状病毒的复制。J.Virol。78.,3572-3577(2004)。
- 18
伊迈等。sars冠状病毒受体血管紧张素转换酶2保护严重急性肺衰竭。自然(媒体)。
- 19
Pelchen-马修斯,A.,Signoret,N.,Klasse的,P.J.,Fraile酒店-拉莫斯,A。&沼泽,M.趋化因子受体贩卖和病毒复制。免疫素。录168.,33-49(1999)。
- 20.
杨振宇等。重症急性呼吸综合征冠状病毒的ph依赖进入是由刺突糖蛋白介导的,并通过DC-SIGN树突状细胞转移增强。J.Virol。78.,5642-5650(2004)。
- 21
黄,S.K.,李,W.,摩尔,M.J.,崔,H。&Farzan,M.A 193氨基SARS冠状病毒的S蛋白的核酸片段有效地结合血管紧张素转化酶2。J. Biol。化学。279., 3197 - 3201(2004)。
- 22
罗伯特,A.等。老年BALB/c小鼠作为老年人类严重急性呼吸综合征严重性增加的模型。J.Virol。79.,5833-5838(2005)。
- 23
Donoghue, M.等。一种新的血管紧张素转换酶相关羧肽酶(ACE2)将血管紧张素I转化为血管紧张素1-9。中国保监会,Res。87.E1-9(2000)。
- 24
Tipnis,S.R.et al。血管紧张素转化酶的人类同源物。克隆和功能表达作为卡普洛不敏感的羧肽酶。J. Biol。化学。275.,33238-33243(2000)。
- 25
科沃尔,P.,威廉姆斯,T.A。&Soubrier,F.肽基二肽酶 - 答:血管紧张素I转换酶。方法酶。248,283-305(1995)。
- 26
inagami,t。等。血管紧张素II受体的克隆,表达和调节。特急医疗生物学。377, 311 - 317(1995)。
- 27
Myint,S.H.人冠状病毒 - 简要评论。Rev. Med。病毒。4.35-46(1994)。
- 28
Itoyama, S.等。ACE1多态性与SARS进展。物化学。Biophys。Commun >,3231124 - 9(2004)。
- 29
邹凯等。PUMC01分离株sars冠状病毒基因组分析中国一学可学源学报25, 495 - 498(2003)。
- 30.
伊迈等。常规与高频振荡通气肺保护策略比较。j:。杂志。91, 1836 - 1844(2001)。
致谢
我们感谢C. Richardson和我们实验室的所有成员的讨论。我们也感谢B. Seed的讨论,并提供了产生重组Spike蛋白的系统。我们感谢朱q、阮l和张磊分享了未发表的小鼠SARS冠状病毒感染数据和病毒感染方案。这项工作得到了奥地利科学院分子生物技术研究所和奥地利国家银行Jubilaeumsfonds的支持。K.K.是由欧盟的居里夫人奖学金资助的。北京市科学技术委员会资助项目H030230010930,国家自然科学基金创新团队资助项目30421003,Joincare公司SARS基金资助项目。加拿大健康研究所和加拿大创新基金会提供了部分支持。
作者信息
从属关系
相应的作者
道德声明
利益争夺
奥地利科学院分子生物技术研究所已经申请了一项关于调节肾素血管紧张系统治疗肺水肿的专利。
补充信息
权利和权限
关于这篇文章
引用这篇文章
库巴,K.,今井,Y.,饶,S.et al。血管紧张素转换酶2 (ACE2)在SARS冠状病毒致肺损伤中的重要作用。Nat Med.11,875-879(2005)。https://doi.org/10.1038/nm1267
收到了:
公认:
发表:
发行日期:
进一步阅读
血管紧张素转换酶抑制剂(ACEI)或血管紧张素受体阻滞剂(ARBs)可能对COVID-19患者是安全的
《BMC传染病》杂志(2021)
Covid-19:打破全球健康危机
临床微生物学和抗微生物的血统(2021)
COVID-19和阿尔茨海默病:一场危机如何恶化另一场危机
翻译神经变性(2021)
肾素-血管紧张素-醛固酮系统阻滞剂治疗COVID-19高血压患者的临床结局:一项系统综述和meta分析
埃及心脏杂志(2021)
核内体酸化抑制剂抑制SARS-CoV-2复制,缓解hACE2转基因小鼠的病毒性肺炎
病毒学杂志(2021)