文摘
中东而严重冠状病毒感染,包括呼吸系统综合症冠状病毒(MERS-CoV),导致肺损伤与高死亡率,保护性治疗策略不批准临床使用。
我们阐明的分子机制还有抑制剂环孢菌素A (CsA)和alisporivir (ALV)限制MERS-CoV验证其适用性MERS-CoV现成治疗感染。
Calu-3细胞和初级人类肺泡上皮细胞(hAECs)感染MERS-CoV和治疗CsA或者ALV或抑制剂针对还有inhibitor-regulated分子包括钙调磷酸酶、核转录因子的激活t细胞(NFATs)或增殖蛋白激酶。小说CsA-induced通路被确定通过RNA序列和操纵基因击倒或中和抗体。病毒复制被定量实时PCR和量化组织培养感染剂量的50%。数据是在小鼠MERS-CoV感染模型进行验证。
CsA和ALV减少MERS-CoV滴定度Calu-3细胞和病毒RNA复制和hAECs改善上皮的完整性。而钙调磷酸酶和NFAT抑制减少MERS-CoV传播,封锁c-Jun n端激酶减少传染性病毒粒子释放但不是RNA的积累。重要的是,CsA诱导干扰素调节因子1 (IRF1),明显的III型干扰素(IFNλ)反应和抗病毒基因的表达。Downregulation IRF1或IFNλMERS-CoV传播增加CsA的存在。重要的是,口语应用CsA减少MERS-CoV复制在活的有机体内,关联肺IFNλ水平升高和改善结果。
我们提供的证据表明,还有抑制剂有效减少MERS-CoV复制在体外和体内通过upregulation炎症的抗病毒细胞反应,尤其是IFNλ。CsA可能因此感染治疗MERS-CoV代表一种很有前途的候选人。
文摘
还有抑制剂环孢菌素A和alisporivir激活宿主先天免疫interferon-λ的感应通过在人类肺上皮细胞和激活IRF1在活的有机体内,导致显著的抑制MERS-CoVhttps://bit.ly/37gzIBH
介绍
中东呼吸系统综合症冠状病毒(MERS-CoV)在2012年出现在沙特阿拉伯1),导致重复人类感染超过2500实验室确诊病例和高致死率约为35% (2]。在体外感染人类的肺组织,MERS-CoV目标支气管和肺泡上皮细胞(aec),导致分离和细胞凋亡的原子能委员会(3]。最近的报告分析已故MERS-CoV-infected患者的尸检材料显示MERS-CoV抗原在原子能委员会和上皮细胞集团多核合胞体在活的有机体内(4,5]。因此,人类感染严重的表现为肺炎与发展为急性呼吸窘迫综合征(4,5]。
到目前为止,没有疫苗或特定治疗MERS-CoV,或大流行小说严重急性呼吸系统综合症x 2 (SARS-CoV-2),只有被批准和治疗依赖于支持措施(2,6]。而在体外在非人灵长类动物的研究和实验证明的好处的I型干扰素(IFN)和抗病毒化合物,包括利巴韦林,反对MERS-CoV [7- - - - - -9),结果回顾病人组应用类似的治疗方案仍有争议(10- - - - - -12]。环孢菌素A (CsA)被发现抑制几个人类病原浸细胞系来自肾脏或肝脏上皮细胞(13- - - - - -16]。然而,CsA的分子机制影响浸,包括MERS-CoV,特别是它的主要靶细胞,肺上皮细胞,仍然难以捉摸。此外,临床前研究解决CsA的影响或相关化合物MERS-CoV复制在活的有机体内迄今为止一直缺乏。
CsA是阻止peptidyl-prolyl顺反异构酶(PPI)活动的还有参与多种细胞过程(如。蛋白质折叠(17])。此外,还有CsA形成三元复杂与(CypA)和钙调磷酸酶(CnA)块CnA-dependent激活核转录因子的激活t细胞(NFATs),这一过程占CsA的免疫抑制效应(18]。CsA也已被证明能够抑制增殖作用蛋白激酶(MAPKs) c-Jun n端激酶(物)和p38 [19,20.]。
这里,我们旨在阐明CsA的不同的信号通路影响MERS-CoV等临床相关模型的主要人类原子能委员会(hAECs)和小鼠MERS-CoV感染模型21,22]。我们证明CsA块MERS-CoV感染性粒子出口,这是依赖于物。此外,我们首次提供证据表明,CsA触发激活肺上皮细胞的抗病毒防御状态。我们表明,CsA的有力诱导干扰素调节因子1 (IRF1) III型干扰素(IFNλ)和多个干扰素刺激基因(isg)。此外,我们表明,口服应用CsA诱发IFNλ有力对策在活的有机体内,重要的是,大大降低MERS-CoV复制和改善疾病进展在被感染的老鼠。
方法
MERS-CoV感染
生物安全四级条件下实验MERS-CoV进行病毒学研究所的,菲利普斯马尔堡大学,德国。分离、培养hAECs如前所述[23]。人类肺组织从病人获得叶切除术后通知书面同意(部门的病理和手术,吉森大学德国吉森大学的伦理委员会批准;Az.58/15)。Calu-3细胞或hAECs被感染的感染复数0.1稀释在没有胎牛血清的DMEM / F12在37°C (FCS) 1 h。细胞被洗DMEM / F12 10% FCS与刺激/抑制试剂作为补充。24小时后感染、细胞加工为定量PCR (Maxima-SYBR /火箭qPCR-Mastermix热费希尔科学、沃尔瑟姆,妈,美国),上层的收获病毒滴定如前所述[24]。
在活的有机体内转导和感染
所有动物实验进行按照德国动物保护法律和被当局授权(G73/2017)。C57BL / 6小鼠购自查尔斯河实验室(美国马威尔明顿)和安置在无菌条件下。老鼠接受气管内的接种Adenovirus-hDPP4-mCherry(克隆ViraQuest Inc .,北自由,IA,美国)所描述的(21,25]。5天转导,老鼠通过鼻内感染路由组织培养(TCID感染剂量为50%50)1.5×105TCID50·毫升−1MERS-CoV EMC / 2012。50 mg·公斤−1·天−1CsA稀释在DMSO或DMSO孤独与螺母/巧克力奶油混合,并提供为自愿吸收的老鼠。每天摄入控制。CsA喂养开始前2天MERS-CoV挑战。老鼠被杀死4或7天邮报MERS-CoV感染。
核糖核酸测序分析
RNA完整性评估的Experion StdSens RNA芯片(Bio-Rad实验室、大力神、钙、美国)。RNA-seq图书馆准备使用TruSeq困mRNA库准备工具包(Illumina公司、圣地亚哥、钙、美国)。图书馆是量化生物分析仪(美国安捷伦科技,圣克拉拉,CA)和测序Illumina公司HiSeq 1500平台,rapid-run模式,single-read 50个基点(HiSeq SR快速集群装备v2, HiSeq快速SBS工具包v2, 50周期)根据制造商的指示。质量控制RNA-seq执行读取使用0.11.7 FastQC命令行工具版本。读取被对齐使用明星版本2.7.0d索引基于人类基因组hg38版本。Gene-specific读计数基于hg38 UCSC的基因注释提取使用Subread FeatureCounts包1.6.3版本。产生的阅读数量差异表达基因的导入r检测是使用DESeq2版本1.22.1完成的。后续的数据分析和可视化是使用自定义脚本。基因本体论(去)传播的分析使用enrichGO 3.10.1 clusterProfiler包版本的函数。测序数据在数组表示,加入数字e - mtab - 8222。
统计数据
所有数据都意味着±扫描电镜。统计学意义是由未配对分析双尾单向方差分析和t检验或事后multi-comparison测试表明各自的数据。一个假定值< 0.05被认为是显著的。
进一步的实验中可以找到的细节补充材料。
结果
CsA抑制MERS-CoV复制和发布在肺上皮细胞
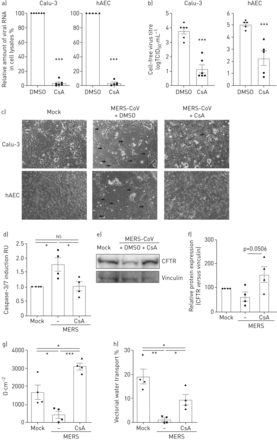
解决之前提出的抗病毒活性CsA的临床相关的细胞,我们被感染的人类支气管上皮细胞系Calu-3和初级hAECs MERS-CoV和分析细胞内病毒RNA和感染性粒子释放在DMSO溶液或CsA (图1 gydF4y2Ba)。Calu-3细胞和hAECs CsA治疗导致减少> 95%的病毒RNA (图1一个)和减少病毒滴定度在上层清液2.6 - -2.8日志10(图1 b)。按照报告从MERS-CoV病人尸检材料(4),MERS-CoV-infected Calu-3细胞和初级hAECs均显示凋亡细胞损失和形成多核细胞病灶(图1 c)。CsA减少细胞集落形成和显著降低细胞凋亡诱导(图1 cd)。排队,囊性纤维化跨膜电导调节(雌性生殖道)(图1 ef)和上皮钠channel-β(ENaCβ)(补充图E1)蛋白表达改善后增加CsA MERS-CoV-infected Calu-3细胞。此外,上皮结构完整性和矢量水运能力减少MERS-CoV-infected控制细胞在MERS-CoV-infected显著提高到正常水平,CsA-treated细胞(图1 g,h)。
环孢菌素A (CsA)抑制中东呼吸系统综合症冠状病毒(MERS-CoV)复制并释放人类呼吸道上皮细胞和初级人类肺泡上皮细胞(hAECs)。Calu-3细胞和hAECs感染了MERS-CoV使用感染复数的0.1,刺激和DMSO溶液或10µM CsA,分析在24 h后感染。)总RNA分离细胞溶解产物和病毒RNA内容被定量PCR分析。正常化后肌动蛋白、RNA含量变化CsA-treated细胞RNA在DMSO-treated正常对照组(100%)。b)病毒滴定度测定使用组织培养(TCID感染剂量的50%50)方法从文化浮层显示为logTCID游离50·毫升−1。c) MERS-CoV-induced细胞病变效应和疫源地形成(由箭头标记)在活细胞记录相衬显微镜的放大率×100。量化了d)凋亡诱导Caspase-3/7如果®Calu-3化验。俄罗斯:相对单位。e、f)细胞溶解产物被免疫印迹分析表达式的囊性纤维化跨膜电导调节(雌性生殖道)(168 kDa)和vinculin (120 kDa)。e)代表西方滴n = 3 - 4实验。f)相对定量模拟样本设置为100%。g h) Calu-3细胞种植在transwell过滤器和作为。上皮完整性被transepithelial电阻测量量化(g)和矢量水运输评价荧光素isothiocyanate-dextran量化48 h后感染(h)。(a, b, d - h)中的数据均值±扫描电镜n = 3 - 6的实验。统计学意义是由未配对的双尾t检验分析(a, b)和单向方差分析和Bonferroni多个对比测试(d - h),所有团体相互比较。*:p < 0.05;* *:p < 0.01;* * *:p < 0.005;ns:不重要的。(c)的显微图代表n > 5实验。
CsA治疗影响MERS-CoV感染通过CypA MAPK-signalling通路
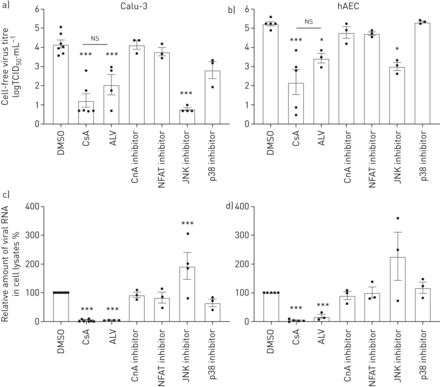
CsA是已知的行为通过还有多种信号通路,包括PPIase活动,CnA-NFAT轴和MAPK信号17- - - - - -20.]。使用特定的抑制剂,我们旨在干扰CsA-affected通路识别相关的分子信号事件参与CsA-mediated减少MERS-CoV感染。CnA的特定抑制剂抑制磷酸酶抑制肽(CIP),以及下游转录因子NFAT的抑制,导致小,统计上不重要的变化在Calu-3细胞和hAECs MERS-CoV病毒滴定度(图2 a, b)。CsA的non-immunosuppressive衍生物,alisporivir (ALV),结合PPIase但不诱导形成三元复杂CypA CnA,病毒滴定度减少了CsA的相似程度,表明它是CypA-PPIase活动引发的限制性影响MERS-CoV复制,而不是任何三元complex-mediated信号事件。此外,ALV细胞集落形成和上皮完整性损失减少了相似程度作为CsA (补充图E2)。应用特定物和p38 MAPK抑制剂透露,抑制物,但不是p38、减少MERS-CoV Calu-3细胞和hAECs滴定度(图2一个b)。然而,无论是CnA-dependent信号还是抑制物或者p38可以再现CsA-induced衰减MERS-CoV RNA的积累。此外,物抑制对细胞没有积极影响焦点后形成或上皮完整性MERS-CoV感染(补充图E3)。这些数据显示在MERS-CoV复制物活动的作用,不良反应在上皮完整性仍显示,病毒释放被阻塞。值得注意的是,应用ALV导致强烈减少MERS-CoV CsA (RNA水平相似图2 c,d)。在一起,这些结果表明,CsA-induced, CypA-dependent效应有重大影响的早期复制步骤MERS-CoV,强烈减少病毒RNA的积累,即使病毒版本之前,独立的中央社,NFAT或物。
影响环孢菌素A (CsA), alisporivir (ALV)和抑制CsA-dependent钙调磷酸酶(CnA) /核转录因子的激活t细胞(NFATs)和增殖蛋白激酶(MAPK)通路在中东呼吸virus-coronavirus (MERS-CoV)感染。Calu-3细胞(a、c)和人类肺泡上皮细胞(hAECs) (b, d)感染MERS-CoV使用感染复数为0.1。1 h病毒吸附后,细胞被刺激与CsA(10µM),其non-immunosuppressive衍生物ALV(10µM), CnA抑制剂(钙调磷酸酶抑制肽,20µM) NFAT抑制剂(50µM), c-Jun n端激酶(物)抑制剂(SP600125 10µM), p38 MAPK抑制剂(某人203 580,10µM)或DMSO溶剂控制。a、b)病毒滴定度测定使用组织培养(TCID感染剂量的50%50)方法从文化浮层显示为logTCID游离50·毫升−1。c, d)总RNA分离细胞溶解产物在24 h后感染和病毒RNA内容被定量PCR分析。正常化后肌动蛋白、RNA含量变化CsA-treated细胞RNA在DMSO-treated正常对照组(100%)。数据意味着±扫描电镜n = 6 - 8实验DMSO和CsA组和n = 3 - 5实验为ALV, CnA, NFAT、物和p38抑制剂。统计学意义是由单向方差分析和Bonferroni的多重比较分析测试,所有团体相互比较。统计学意义相比,DMSO控制。*:p < 0.05;* * *:p < 0.005;ns:不重要的。
CsA唤起一个IFN-driven抗病毒治疗在肺上皮细胞
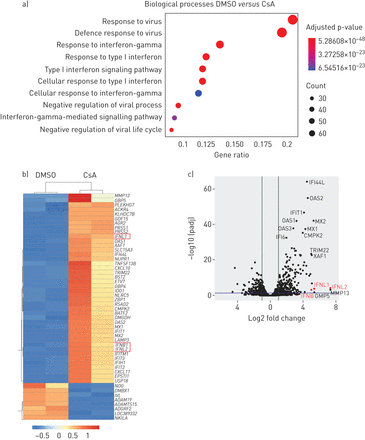
我们的数据表明,相对于其知名CnA / NFAT-mediated immune-suppressive对免疫细胞的影响,CsA可能唤起人类肺上皮细胞的抗病毒的状态。识别潜在的机制,我们对CsA - RNA-seq进行分析与DMSO-treated Calu-3细胞。值得注意的是,基因集富集分析基于术语显示,生物过程的最重要的调节CsA治疗包括对病毒的反应和后,重要的是,抗病毒干扰素反应(图3一)。根据这些结果,I型干扰素基因IFNB和III型干扰素基因IFNL1和IFNL2在前50名,或在吗IFNL1十大最调节基因在CsA-treated细胞(图3 bc)。许多调节基因是已知的isg,包括mx₁,(,OAS1,OAS2,IFIT1,IFIT2,IFIT3,LAMP3,BST2 / tetherin,RSAD2 / viperin和CXCL10(图3 b)。
环孢菌素(CsA)治疗诱发Calu-3肺上皮细胞的抗病毒反应状态。Calu-3细胞被刺激与10µM CsA或DMSO溶液处理车辆控制。在24 h后刺激,总RNA被提取出来并进行转录组分析(方法)。)代表分析基因本体论(去)生物过程是计算使用调节基因和log2褶皱变化> 1。十大最重要的生物过程策划的基因比。点代表的基因数量的大小调节基因列表中相关术语;点代表的颜色调整假定值。b, c)单个基因显示为一个热图(b)上市前50名的调控基因(向上和向下)和作为一个火山(c)的阴谋。IFNL1, 2和3是用红色突出显示。数据代表了两个独立的实验。
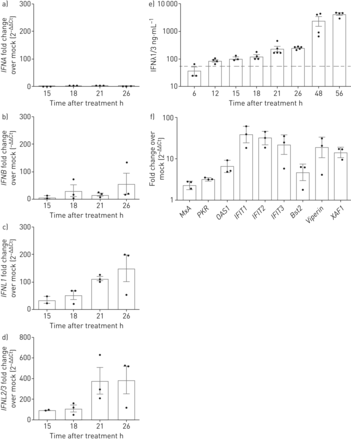
来验证我们的结果,我们分析了I型和III型IFN的mRNA表达的定量实时PCR CsA-stimulated或DMSO-treated Calu-3细胞。我们发现一个温和upregulationIFNB(57-fold变化模拟控制),没有明显的诱导IFNA(图4一b)。然而,我们发现一个强大的感应IFNL1和IFNL2/3信使rna(150 - 387倍的变化模拟控制,分别;图4 c,d),量化IFNλ1 IFNλ3蛋白质释放细胞培养上清液用ELISA演示了一个健壮的归纳在CsA除了早在12 h CsA治疗后,达到高峰值4222±890 ng蛋白质·毫升−156在48 h后CsA应用程序(图4 e)。同样,用ALV诱导治疗健壮IFNλ释放,达到一个类似的最大释放IFNλ72 h后(补充图E4)。我们接下来验证CsA-induced upregulation isg和确认选择包括isg的表达增加MxA,PKR,OAS1,IFIT1,IFIT2,IFIT3,Bst2 / tetherin,RSAD2 / viperin和XAF1在18 h治疗CsA相比vehicle-treated控制细胞(图4 f)。这些数据表明,治疗CsA坐骑的IFN-driven抗病毒反应肺上皮细胞。
环孢菌素A (CsA)诱发interferon-λ(IFNλ)mRNA和释放。Calu-3细胞被刺激10µM CsA,其次是模拟)总RNA隔离在15日,18日,21日和26 h后治疗。互补脱氧核糖核酸合成后,定量PCR分析IFNA,IFNB,IFNL1和IFNL2/3。褶皱变化DMSO-stimulated控制(模拟)(2−ΔΔCt)想象IFN-induction CsA的刺激。e)公布的量化IFNλ,上层清液CsA-stimulated Calu-3收集细胞后从6到56 h CsA治疗和IFNλ1/3由ELISA决定。f)选择IFN-stimulated基因的表达在CsA治疗分析18 h后治疗CsA定量PCR分析和褶皱变化DMSO-stimulated控制(2−ΔΔCt)。数据意味着±扫描电镜(n = 3 - 5 n = 3 (a e)和实验实验(f)。(e)中的灰色虚线表示最小的ELISA检测极限的制造商。
IFNλ感应是由IRF1 CsA治疗肺上皮细胞
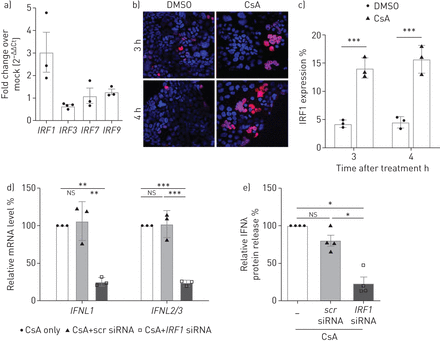
为了更好地理解转录项目导致CsA-treated IFNλ感应细胞,我们分析了irf的监管。我们的数据揭示的重要upregulationIRF1mRNA水平在治疗CsA,但不是的IRF3,IRF7或IRF9(图5一个)。IRF1是一个特定的催化剂IFNL基因表达(26]。因此,我们发现了一个IRF1-expressing细胞数量显著增加CsA-stimulated Calu-3细胞免疫荧光(图5 bc)。IRF1小核RNA)击倒明显减少了IFNL信使rna水平CsA-treated Calu-3细胞(图5 d)。IRF1可拆卸的抑制IFNλ释放> 75%相比控制(图5 e)。
干扰素调节因子1 (IRF1)介导的环孢菌素(CsA)全身的表达式interferon-λ(IFNλ)。)Calu-3细胞溶解产物收集4 h与10µM CsA或DMSO溶液处理后控制。总RNA分离和定量pcrIRF1,IRF3,IRF7和IRF9被执行。数据在DMSO溶液表现为褶皱变化(2−ΔΔCt)。b)的表达IRF1 CsA -或DMSO-stimulated Calu-3细胞间接免疫荧光法,分析了固定和permeabilised细胞。核和4′,复染色6-diamidino-2-phenylindole (DAPI)。c)的量化IRF1表达式,IRF1的比率积极的到DAPI积极的细胞计算至少10个随机选择的微观领域的三个独立的实验。d, e)IRF1被siRNA-transfection实验使用oligofectamine沉默。炒小干扰rna转染(scr)被用来控制。4 h后转染,Calu-3细胞治疗10µM CsA。d)上层清液收集后的18 h CsA治疗。IFNL信使rna进行了分析通过定量PCR和相对折叠感应相比non-siRNA-treated细胞(设置为100%)。e)上层清液siRNA-transfected和CsA-stimulated细胞,ELISA分析的相对数量相比IFNλnon-siRNA-treated细胞(设置为100%)。数据意味着±扫描电镜(n = 3 - 4实验),n = 3实验(罪犯)和n = 4 (e)的实验。统计显著性计算使用未配对的双尾t检验(c)和单向方差分析和Bonferroni多个比较测试比较所有组(d, e)。*: p < 0.05;* *:p < 0.01;* * *:p < 0.005;ns:不重要的。
抑制IRF1-IFNλ信号轴抵消MERS-CoV CsA的限制效果
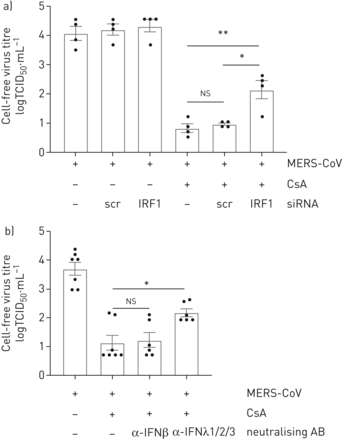
理解的程度的抑制MERS-CoV传播CsA-treated细胞是由IRF1-mediated IFNλ的生产,我们进行了降价IRF1分别或中和IFNλ游离。沉默的IRF1但不治疗,控制核导致显著增加在CsA-treated MERS-CoV-released病毒颗粒细胞(图6b)。此外,中和抗体针对IFNλ1,IFNλ2和IFNλ3或诱导IFNβ越少(图6 b)。中和的IFNβMERS-CoV复制CsA治疗后没有显著影响,而应用anti-IFNλ1/2/3治疗显著增加MERS-CoV病毒滴定度1.05日志10级别(图6 b)。这些数据表明,CsA的抗病毒作用至少部分由一个IRF1-IFNλ信号轴,和独立的I型干扰素。
抑制干扰素调节因子1 (IRF1) -interferon-λ(IFNλ)信号轴部分防止环孢菌素(CsA)全身对中东的影响呼吸系统综合症冠状病毒(MERS-CoV)复制。一)IRF1被siRNA-transfection实验使用oligofectamine沉默。炒小干扰rna转染(scr)被用来控制。在20 h转染,Calu-3细胞被感染的感染复数MERS-CoV 0.1。1 h病毒吸附后,细胞治疗10µM CsA或DMSO溶剂控制。24小时后感染,病毒释放决心使用组织培养(TCID感染剂量的50%50)方法。b) Calu-3细胞被感染的感染复数MERS-CoV 0.1和刺激与CsA或DMSO控制描述。同时,中和抗体(AB)针对IFNβ或同时添加了IFNλ1/2/3 CsA。24小时后感染病毒释放由TCID决定50。数据意味着±扫描电镜(n = 4 (a),实验和n = 6 - 7 (b)。实验统计显著性计算使用单向方差分析和Bonferroni多个对比测试,所有团体相互比较。统计学意义oligofectamin-only治疗组相比。*:p < 0.05;* *:p < 0.01;ns:无意义的。
CsA治疗移植IFNλ并导致减少MERS-CoV复制和肺部病理在活的有机体内
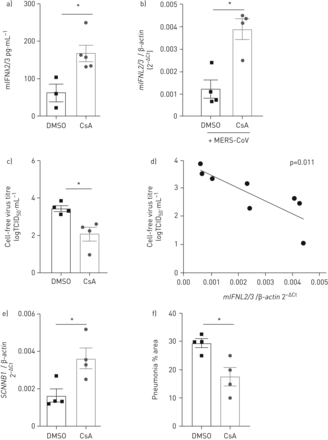
验证对MERS-CoV CsA的抗病毒疗效在活的有机体内最近,我们使用MERS-CoV感染小鼠模型建立。这是基于人类的气管内的交货DPP4受体肺上皮细胞通过adenoviral传导,导致严重的MERS-CoV感染,表现为坏死性间质性肺炎(22]。我们每天治疗的小鼠通过口服摄入DMSO溶液或CsA,开始前2天模拟或MERS-CoV感染。口服CsA应用导致CsA ng血清水平的202 - 356毫升−1(平均270±17 ng·毫升−1浓度),相比之下,病人在治疗CsA(达到的水平补充图E5(27,28])。因此,CsA治疗显著诱导释放IFNλ支气管肺泡灌洗液(图7)。IFNL诱导显著升高在DMSO CsA治疗组相比,治疗组在第七天邮报MERS-CoV感染(图7 b)。口语应用CsA显著降低病毒滴定度(3.45±0.15与2.1±0.36 TCID50·毫升−1在DMSO溶液与在第七天邮报MERS-CoV感染(CsA组)图7 c)。CsA治疗并没有改变adenoviral转导效率(补充图E6)。值得注意的是,表达的水平IFNL反向与MERS-CoV负载在感染后的第七天肺匀浆(图7 d)。显著减少病毒滴定度和显著的相关性IFNL诱导和MERS-CoV抑制也可以证明在感染后的第四天补充图E7)。的表达SCNN1B基因(ENaCβ)作为标记上皮完整性提高肺匀浆MERS-CoV-infected小鼠治疗CsA (图7 e)。虽然广泛水肿的形成存在于大部分MERS-CoV-infected老鼠,它没有CsA-treated集团(补充图E8)。重要的是,肺面积的百分比显示组织病理学改变由于MERS-CoV感染显著减少了CsA治疗感染后的第七天(图7 f)。的集体,我们已经表明,口服应用CsA诱发IFNλ在小鼠的肺和施加强有力的抗病毒活性在活的有机体内。
环孢菌素(CsA)治疗移植interferon-λ中东(IFNλ)和减少呼吸系统综合症冠状病毒(MERS-CoV)复制体内。)老鼠CsA(50毫克公斤−1·天−1)或DMSO溶剂控制。经过6天的每日口服应用程序,鼠标IFNλ水平(mIFNλ)的ELISA分析支气管肺泡灌洗液。b-f)小鼠感染通过气管内的路线以腺病毒为人类构建编码DPP4和mCherry (Ad-hDPP4)。口服应用CsA(50毫克公斤−1·天−1)或DMSO溶剂控制在第三天开始传导,而老鼠感染1.5×105TCID50·毫升−1MERS-CoV通过鼻内的路线在第五天转导。老鼠被杀,肺孤立MERS-CoV感染后7天。肺匀浆用于b)量化相对IFNL2/3TCID mRNA和c)确定病毒载量50。d)之间的相关性MERS-CoV滴定度IFNL2/3信使rna表达水平效率计算皮尔逊相关。e)的相对数量SCNNB1(ENaCβ)RNA测定通过定量PCR MERS-CoV-infected和DMSO -肺匀浆与CsA-treated老鼠。f)肺固定和加工进行组织学分析。肺地区典型的特点是间质炎症MERS-CoV-induced肺炎(22整个肺后被量化处理。统计显著性计算使用一个未配对的双向学习任务(a, b, c, d, g)。*: p < 0.05。TCID50:组织培养感染剂量的50%。
讨论
冠的出现在2002年,2012年和SARS-CoV-2 MERS-CoV 2019年,三个家庭的物种Coronaviridae揭示了有效地在人与人之间传播的能力,与高死亡率引起严重的疾病。冠和MERS-CoV都列在优先级列表的疾病,世界卫生组织蓝图和人畜共患x和储层压力通常被认为是现在已经被证明是一个新兴大流行性病毒的来源。
因为没有特定的治疗是批准MERS-CoV或冠状(2),目前的治疗策略支持(29日,30.]。治疗包括重组I型干扰素和抗病毒药物(如。lopinavir /例如)应用药物治疗MERS-CoV和得出的结果只有温和的功效与有争议的回顾性研究,从前瞻性研究和数据或缺乏随机对照试验(29日,31日- - - - - -33]。由于人类DPP4受体特异性的,到目前为止很少有动物模型可以研究MERS-CoV发病机理和MERS-CoV-directed抗病毒化合物。在这项研究中,MERS-CoV感染老鼠了通过气管内的传递人类DPP4-encoding腺病毒,这可能导致低级炎症本身和非齐次受体分布在肺内,在有限的时间框架。然而,即使这种模式不可能完全概括原生细胞分布或受体的密度在人类肺癌、转导效率高(≥95%,数据未显示)允许高效的病毒传播上下呼吸道航空公司快速发展为严重肺损伤(22)和温和的发病率的变化(34]。这绕过了模型相关的神经亲和力,如有些转基因小鼠hDPP4 (35),和适应的必要性病毒隔离通过多个段落,这可能影响其易感性介入策略。虽然此前接触过腺病毒唤起温和的组织学变化,包括血管周的和细支气管淋巴细胞浸润(数据没有显示)、粒细胞MERS-CoV感染会导致明显的区别,组织性与肺泡水肿形成如前所述(间质性肺炎22]。
CsA在内的抑制剂广泛的病毒家族,包括不同浸(14,36- - - - - -41]。然而,研究CsA对x和感染的功效以前依赖导致肝脏和肾脏细胞株(14- - - - - -16,而结果原发性肺上皮细胞缺乏目标。最近,CsA限制MERS-CoV演示体外(13]。不过,见解对机械的细节和CsA的应用是否会影响MERS-CoV感染在活的有机体内仍然难以捉摸。
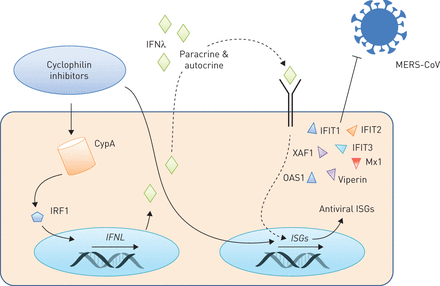
我们现在证明CsA MERS-CoV应用程序块,在mRNA水平和降低感染性病毒颗粒释放的数量,它极大地提高了MERS-CoV感染后上皮屏障的完整性。使用不同的抑制剂阻止CsA-targeted通路,我们发现CsA-induced封锁MERS-CoV RNA合成既不能复制的抑制已知CsA-targeted MAPK和NFAT激活的封锁。值得注意的是,ALV,有效块CypA PPIase活动但影响NFAT-dependent途径只有在非常高的浓度(42),减少MERS-CoV RNA积累有效CsA,表明CypA在这些过程中起着举足轻重的作用。事实上,我们揭示了一个前所未知的激活的基因参与先天免疫反应和病毒复制的限制政府的CsA肺上皮细胞。此外,我们表明,抑制CypA通过CsA或者ALV,既有效地阻止CypA PPIase活动使用浓度(42),导致的一个显著upregulation III型干扰素mRNA和蛋白水平。这是由IRF1和抗病毒isg伴随着表达式(图8)。其中,干扰素诱导蛋白tetratricopeptide重复1 (IFIT1)特别报道影响MERS-CoV的发病机制,突出我们的研究结果的相关性(43]。
环孢菌素A (CsA)和alisporivir (ALV)限制中东呼吸系统综合症冠状病毒(MERS-CoV)通过诱导interferon-λ(IFNλ)。还有抑制剂,包括CsA或其non-immunosuppressive衍生物ALV,还有众所周知的调节器(CypA)和诱导激活干扰素调控转录因子1 (IRF1)。随后,III型干扰素基因的转录(IFNL)是调节和IFNλ释放在体外和在活的有机体内。CsA进一步诱发IFN-stimulated基因的表达(isg),可能由汽车和旁分泌信号通过IFNλ。CsA-induced isg包括分子与已知的抗病毒效果,如。OAS1 IFIT1,进而传达CsA的限制性影响MERS-CoV复制。
类型III干扰素最近成为关键球员抗病毒先天免疫反应的病毒感染在粘膜上皮表面(44- - - - - -47]。他们有效地限制不同的呼吸道病毒,如。限制了从上到下航空公司(44,46- - - - - -48]。与I型干扰素、III型干扰素不触发有害的免疫反应导致在流感感染免疫病理23,25,44,49]。这可能会被证明是至关重要的上下文中CsA-dependent刺激IFNλ在x和,因为严重的人类x和感染,如。MERS-CoV,尽管数据仍然有限,SARS-CoV-2,特点是一个强大的细胞因子诱导的免疫病理(5,50,51]。
除了定义一种新型促炎、抗病毒CsA对肺上皮细胞引起的表达谱,本研究还首次证明,口服应用CsA降低病毒载量的在活的有机体内MERS-CoV感染模型。CsA是获得批准的药物在临床使用自1980年代。而长期治疗(在几周和几个月)与CsA可以诱发副作用(如。肾毒性(48]),我们在应用短时间间隔口服摄入CsA在急性感染。我们的研究结果表明在活的有机体内、口服应用药物血清水平超过6天结果有效地抑制肺病毒感染和肺炎进展,强调CsA是一种很有前途的药物为治疗MERS-CoV妄。
值得注意的是,我们的在体外研究还表明,中和III型干扰素没有完全扭转MERS-CoV-restrictive CsA的效果。我们建议CsA影响MERS-CoV在病毒复制多个步骤。事实上,我们已经表明,CsA MERS-CoV传播行为通过抑制物,这是另一个CsA的下游目标(19,20.]。物抑制MERS-CoV RNA的积累但没有影响强烈的数量减少传染性病毒粒子释放。虽然确切的潜在的分子机制仍有待定义,这一发现表明,CsA可能施加添加剂影响限制MERS-CoV复制。而应用程序批准重组干扰素治疗病毒感染和恶性肿瘤,严重的副作用已经与系统性干扰素应用程序(52]。CsA再利用(即)x和感染的治疗,可能有几个优势干扰素治疗,如。额外的抗病毒效果比仅由IFNλ副作用优惠在短期使用,有益的影响对于一个过度免疫反应描述x和疾病(53,54)和证明口服可用性(55]。CsA因此代表了一种有前途的治疗选择对抗人类x和感染,可能延长过去MERS-CoV当前流行SARS-CoV-2应变和未来浸的威胁。
补充材料
可共享的PDF
确认
执行工作与生活MERS-CoV BSL-4设施的菲利普斯大学,德国马尔堡。我们感谢茱莉亚•斯宾格勒拉里萨哈曼和斯蒂芬妮jarm(吉森大学内科医学部门二世和马尔堡肺中心(UGMLC),吉森,德国),和Jorg施密特,科尼利厄斯罗德,桑德罗Halwe,德克·贝克尔和马克Ringel(菲利普斯马尔堡大学病毒学研究所马尔堡,德国)的优秀技术和实验支持。我们感谢拉尔夫Bartenschlager(分子病毒学的部门,海德堡大学海德堡,德国)提供alisporivir。
脚注
测序数据在数组表示,加入数字e - mtab - 8222。
可以从本文的补充材料www.qdcxjkg.com
利益冲突:l . Sauerhering没有披露。
利益冲突:a . Kupke没有披露。
利益冲突:l·迈耶没有披露。
利益冲突:大肠Dietzel没有披露。
利益冲突:j·霍普没有披露。
利益冲突:公元格鲁伯没有披露。
利益冲突:美国Gattenloehner没有披露。
利益冲突:b·威特没有披露。
利益冲突:l·芬克没有披露。
利益冲突:n .霍夫曼没有披露。
利益冲突:t·齐默尔曼没有披露。
利益冲突:a . Goesmann没有披露。
利益冲突:a . Nist没有披露。
利益冲突:t Stiewe没有披露。
利益冲突:美国贝克没有披露。
哈罗德的利益冲突:美国没有披露。
利益冲突:c . Peteranderl没有披露。
支持声明:这项工作是支持的德国研究基金会(KFO309 P2 / P8;项目编号:284237345;SFB-TR84 B2、项目ID: 114933180;SFB1021 C05,项目ID: 197785619),德国肺癌研究中心(DZL),由德国感染研究中心(DZIF)和心肺研究所(CPI), EXC 2026年,项目编号:390649896。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2019年9月16日。
- 接受2020年6月3日。
- 版权©2020人队
这个版本分布在创作共用署名非商业性许可证的条款4.0。