摘要
背景及时诊断严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)感染是治疗和预防的前提。抗体检测对RNA检测的血清学特征及补体诊断价值有待论证。
方法收集80例pcr确诊的2019冠状病毒病(COVID-19)患者的系列血清。检测了抗SARS-CoV-2的总抗体(Ab)、IgM和IgG抗体,并描述了感染过程中的抗体动态。
后果抗体、IgM和IgG血清转阴率分别为98.8%、93.8%和93.8%。第一个可检测的血清学标记是Ab,其次是IgM和IgG,中位血清转化时间分别为暴露后15、18和20天(d.p.e)或发病后9、10和12天(d.p.o)。抗体水平从6d.p.o开始迅速上升。并且伴随着病毒载量的下降。在疾病早期(0 ~ 7日龄),Ab的敏感性最高(64.1%),IgM和IgG均为33.3%;p < 0.001)。2周后,抗体、IgM和IgG的敏感性分别达到100%、96.7%和93.3%。当检测到相同的抗体类型时,酶联免疫吸附测定法与其他形式的免疫测定法无显著差异。
结论SARS-CoV-2感染期间会诱发典型的急性抗体反应。血清学检测为疾病后期的RNA检测提供了重要的补充,用于病原特异性诊断,并为评估患者的适应性免疫状态提供了有用的信息。
摘要
SARS-CoV-2感染后诱导抗体反应,观察抗体试验与RNA试验的互补诊断价值。抗体试验对SARS-CoV-2感染和CoV-19的临床管理和控制至关重要。https://bit.ly/3fQZwZp
介绍
2019年12月初,首次报告一种新型冠状病毒(严重急性呼吸综合征冠状病毒2 (SARS-CoV-2))可导致致命的人类肺炎,不久在中国湖北省省会武汉市发现了人际传播[1].病毒在中国迅速传播,然后在全球许多其他国家传播。截至2020年5月6日,该病毒已在215个国家造成350万例2019冠状病毒病(COVID-19)实验室确诊病例和24.3万例死亡[2]。世界卫生组织(WHO)宣布新冠病毒-19为国际关注的突发公共卫生事件,并在全球范围内对其进行了“非常高”的风险评估[3.].中国最近的一份报告显示,COVID-19感染的中位(四分位差)潜伏期为4(2-7)天[4].发烧、咳嗽和疲劳是最常见的症状[1].严重者可迅速发展为急性呼吸窘迫综合征和感染性休克。>80%的患者出现胸部ct异常,特别是毛玻璃影和双侧斑片状阴影[4].>80%的患者有淋巴细胞减少,以及∼60%的患者C反应蛋白升高[5].然而,COVID-19感染的临床和实验室结果与一些常见呼吸道病原体(如流感病毒)感染引起的肺炎没有区别,肺炎链球菌和肺炎支原体[6].因此,及时诊断SARS-CoV-2感染对提供适当的医疗支持和通过隔离预防传播至关重要。
目前,SARS-CoV-2感染的诊断几乎完全依赖于基于pcr技术的病毒RNA检测[7].不幸的是,RNA检测在现实世界中的灵敏度并不令人满意,特别是在使用上呼吸道采集的样本时[6,8- - - - - -10]。在武汉,RNA检测的总体阳性率估计为∼30–50%的新冠病毒-19患者入院时[11].此外,现有RNA检测的总体吞吐量受到高度限制,因为它们需要高工作量,需要熟练的操作人员进行检测和样本收集,并需要昂贵的仪器和特殊的操作场所[12].因此,方便的血清学检测有望有所帮助。然而,目前关于抗体对sars - cov -2感染的反应的知识非常有限。抗体检测的诊断价值还有待明确证明。有多少患者会产生抗体反应,抗体从暴露到阳性需要多长时间?短潜伏期和长潜伏期的病人有什么明显的区别吗?抗体检测对不同疾病阶段的患者有什么敏感性?抗体反应和病毒载量下降之间是否有暂时的联系?为了回答这些问题,我们研究了80例COVID-19患者在住院期间的抗体应答特征,采用免疫测定法检测总抗体、IgM和IgG。
方法
研究设计和参与者
根据国家卫健委发布的《新型冠状病毒感染的肺炎防控方案(第六版)》确诊1例[13].简言之,确诊病例应符合三个标准:1)发热和/或呼吸道症状;2)肺影像学异常;3) SARS-CoV-2核酸阳性。如出现以下任何临床表现,患者的严重程度为危重:1)急性呼吸窘迫综合征或氧饱和度<93%,需要有创或无创机械通气;2)冲击;3)器官功能衰竭和需要重症监护病房支持的并发症。不符合上述标准的COVID-19患者为非危重病例。
该研究共纳入了80例COVID-19病例,所有患者都在2020年1月19日至2月9日期间住院,并愿意捐献血液样本。所有入选病例均经实时定量逆转录酶PCR (qRT-PCR)检测确认为SARS-CoV-2感染。从临床记录中获取发病日期、临床分类、住院期间RNA检测结果和个人人口学信息。在病毒传播期间,在当地社区共登记了300名健康人士。所有控制人员均未报告与任何新冠肺炎确诊患者有过密切接触。本研究经浙江大学第一附属医院医学伦理委员会审核批准。批准文号2020 - iit - 47)。每位被试均获得书面知情同意。
逆转录聚合酶链反应实验室确诊COVID-19
对每个患者优先采集痰标本。如前所述,在未产生痰液的地方,采集深咳后的唾液[14].先用等量的蛋白酶K溶液(0.4 mg·mL)处理痰液−1)室温下静置20分钟。取治疗后的痰液或唾液200 μL,采用瑞士巴塞尔罗氏公司(Roche, Basel, Switzerland)的MagNA Pure LC 2.0进行总核酸提取,每个样品洗脱50 μL。以核衣壳基因和开放阅读框实验室基因为靶点,采用商业化的一步实时逆转录聚合酶链反应(RT-PCR)方法(Bio-Germ,中国,上海),使用5 μL总核酸按照说明书进行检测。
抗体测定
采用三种酶联免疫吸附试验(ELISA-Ab、ELISA-IgM和ELISA-IgG)、三种胶体金横向流动免疫试验(LFIA-Ab、LFIA-IgM和LFIA-IgG)和两种化学发光微粒免疫试验(CMIA-Ab和CMIA-IgM)检测血浆样本中SARS-CoV-2的总抗体(Ab)、IgM抗体和IgG抗体。ELISA试剂和LFIA试剂由北京万泰生物制药企业有限公司(中国北京)提供,CMIA试剂由厦门InnoDx生物技术有限公司(中国厦门)提供。总抗体检测基于双抗原夹心免疫分析,IgM抗体检测基于μ链捕获免疫分析。用哺乳动物细胞表达的含有SARS-CoV-2棘突蛋白受体结合域(RBD)的重组抗原进行总抗体和IgM抗体检测。IgG抗体试剂盒为间接免疫分析,SARS-CoV-2重组核蛋白在大肠杆菌中表达大肠杆菌这些试验中使用的抗原是北京万泰生物制药企业有限公司的内部制剂,相同的抗原或抗原对用于ELISA、CMIA和LFIA试验。
ELISA和CMIA的测量过程由自动ELISA分析仪HB-300E(嘉兴CRED医疗器械有限公司,中国浙江)和自动CMIA分析仪Caris 200(厦门UMIC医疗器械有限公司,中国厦门)按照厂家说明进行。有关程序的详情见补充材料.当进行LFIA-Ab和LFIA-IgM检测时,将10 μL样品移至样品接收区,然后加入两滴样品缓冲液。对于LFIA-IgG,用样品缓冲液稀释1000倍,然后在样品接收区加入80 μL的稀释液。加入样品15 min后,用肉眼观察LFIA结果并记录。分别用75、29、15 min得到ELISA、CMIA和LFIA的结果。
统计分析
潜伏期定义为最早接触SARS-CoV-2日期与最早出现症状日期之间的时间间隔。非正态分布的连续数据被描述为中位数(IQR),并用Wilcoxon检验进行比较。分类数据汇总为计数和百分比。敏感性和特异性的95%置信区间用二项精确检验进行估计。未配对比例采用χ 2检验或Fisher’s exact检验,配对比例采用McNemar’s检验。采用Kaplan-Meier法计算累积血清转换率。所有统计分析使用SAS 9.4 (SAS Institute, Cary, NC, USA)进行。
病人及公众参与
没有患者参与设置研究问题或结果测量,也没有患者参与研究的设计和实施。
传播宣言
不可能/不适用向这些群体传播。
后果
入组COVID-19患者的特征
在收治的81例COVID-19患者(2020年2月9日之前)中,80例(99%)纳入了研究(表1).患者的中位(IQR)年龄为55(45-64)岁,38.7%为女性。危重患者的年龄明显大于非危重患者(p<0.001)。45例患者(15例危重患者)入院时,根据与确诊患者有明确的密切接触,通过流行病学检查确定其发病前接触SARS-CoV-2的时间。潜伏期0-23天,中位数(IQR)为5(2-10)天。截至2020年2月15日,共有32例(40%)患者(所有非危重病例)康复出院;没有死亡。
性能SARS-CoV-2抗体检测试剂盒
对80名COVID-19患者和100-300名健康人进行了不同免疫检测。抗体、IgM和IgG的血清转换率分别为98.8%(79 / 80)、93.8%(75 / 80)和93.8% (75 / 80)(表2显示了三种方法的综合灵敏度)。最后一份血液样本来自唯一一名没有血清转化的患者,是在发病后7天(d.p.o)采集的。对于Ab、IgM和IgG测试,elisa似乎表现最好,尽管差异一般不显著。因此,除特别注明外,以下血清学分析均基于elisa结果。
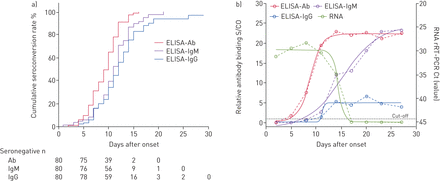
抗体、IgM和IgG的血清转化依次出现,中位发病时间分别为9、10和12次 分别为天(图1一个).危重患者与非危重患者血清转化时间差异无统计学意义(补充图E1).抗体的血清转化明显快于IgM和IgG (p<0.001)。累积血清转化曲线显示,症状出现后第16、21和29天,抗体、IgM的转化率分别达到100%和97.1%。抗体水平从6d.p.o开始迅速上升(图1 b).随着抗体水平的增加,病毒载量co下降。对于处于疾病早期的患者(0-7 d、 与ELISA-IgM和ELISA-IgG(两者均为33.3%;p<0.001)相比,ELISA-Ab显示出最高的灵敏度(64.1%)(表3).当患者进入晚期时,Ab、IgM、IgG检测灵敏度显著升高,2周后分别达到100%、96.7%、93.3% (p<0.05)。
80例冠状病毒病患者自发病以来的累积血清转化率和抗体水平动态2019。a)总抗体(Ab)累积血清转化率曲线根据Kaplan–Meier方法绘制ELISA检测到的IgM和IgG。在收集第一份样本之前,患者的血清学状态被确定为阴性。b)抗体水平被替代,并使用相对结合信号与每个分析的截止值(信号截止值)相比较来表达四条参数logistic拟合曲线(实线)用于模拟抗体水平的趋势。rRT-PCR:实时逆转录酶PCR;Ct:周期阈值
SARS-CoV-2暴露后的抗体动态
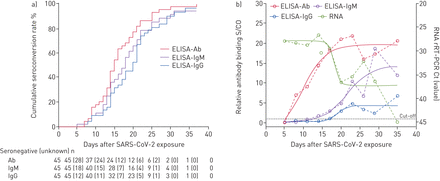
由于长期暴露患者难以确定确切的感染日期,因此对45例暴露时间已确定的患者进行了最早暴露日期后而非感染后的抗体动力学研究(图2)抗体、IgM和IgG的血清转化依次出现,且水平迅速上升,暴露后的中位天数(d.p.e.)分别为15、18和20天(图3).危重患者暴露后血清转化的中位时间与非危重患者无差异(补充图E2).病毒载量的下降与抗体水平的增加同时发生。抗体、IgM和IgG的累积阳性率分别为100%、94.2%和96.7%。自接触后5天内报告症状的患者分为短潜伏期组(0-5天),其余患者分为长潜伏期组(6-23天)(表4).两组之间在年龄、疾病早期病毒载量或危重状态风险方面没有显著差异。然而,短潜伏期组的中位血清转化时间比长潜伏期组短(13 d.p.e.)。对21 d.p.e。;p < 0.001)。相比之下,短潜伏期组发病后血清转化的中位天数比长潜伏期组长(10 d。对7 d.p.o。;p < 0.05)。
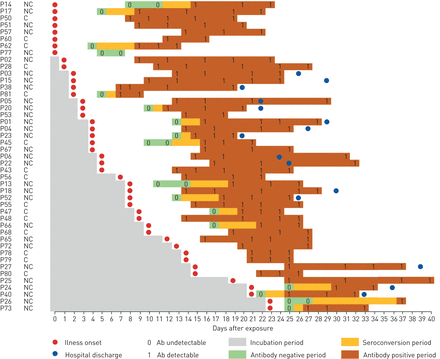
45例暴露时间确定的患者的总抗体动态。根据患者的潜伏期长短进行分类。每个病人的临床严重程度在病人ID旁边都有描述。每个患者的血清学状态仅在采集期间显示,没有向后或向前延伸。NC:非关键;C:关键;阿瑟:抗体。
45例冠状病毒病患者自发病以来的累积血清转化率和抗体水平动态2019。a)总抗体(Ab)累积血清转化率曲线根据Kaplan–Meier方法绘制ELISA检测的IgM和IgG。在采集第一份样本之前,患者的血清学状态为阴性。对于采集第一份样本时结果为阳性的患者,在采集第一份样本之前的血清学状态未知且为阴性指定为阴性。括号中显示了暴露后指定天数内的这些患者人数。b)使用相对结合信号与每次分析的截止值(截止信号(S/CO))进行比较,以替代和表达抗体水平.使用四条参数逻辑拟合曲线模拟抗体水平的趋势(实线)。SARS-CoV-2:严重急性呼吸综合征冠状病毒2;rRT PCR:实时逆转录酶PCR;Ct:周期阈值。
讨论
目前的研究表明,几乎所有(98.8%,80例中有79例)新冠病毒-19患者在发病过程中转变为血清阳性 d、 第一个可检测的抗体是总抗体,其次是IgM和IgG,平均血清转化时间为15 d、 p.e.(9) d、 p.o.),18 d、 p.e.(10) d、 )和20 d、 体育(12) d、 这与在SARS-CoV-1感染中观察到的非常相似[15,16].有趣的是,抗体水平的增加伴随着病毒载量的下降。
目前,与确诊的SARS-CoV-2患者密切接触后的隔离期为14天。目前尚不清楚在隔离期间无法通过RNA检测筛查出的感染比例。然而,有记录表明,一些密切接触者在解除隔离后出现症状并导致传播[17].人们认为,抗体测试可能会提高检测感染的敏感性,但此前没有证据显示。我们的数据显示,14 d.p.e的累积血清转换率为45.5%。这一结果表明,如果在去隔离之前进行抗体测试,大约有一半的携带者可以被筛选出来。20 d.p.e时,累积血清转换率达75%。(11 d.p.o)。7例(15.6%)患者14 d前无任何症状。,其中4例患者22 d.p.e仍为阴性。(1例)25d。e(3例)。因此,分离后随访2周的抗体检测和呼吸道症状监测将有助于进一步降低传播风险。
中位数(IQR)潜伏期为5(2-10)天,与以前报告的非常相似[4,18].潜伏期长的患者自接触后血清转化所需的时间明显长于潜伏期短的患者(21 天对13天;p < 0.001)。相比之下,潜伏期较长的患者抗体出现在发病后的早期(7d .p.o。对10 d、 p.o.;p<0.05)。由于不同组别的年龄分布相似,宿主的免疫能力似乎不会对这一差异产生偏见。因此,这很可能是由于宿主的病毒摄入剂量较低或病毒繁殖效率较低。然而,较长的潜伏期不会改变病毒在宿主体内的初始病毒载量出现症状或有经历危急状态的风险。因此,除了发病时间外,对疑似感染的抗体阴性结果的解释还应考虑暴露时间。发病后血清转化速度越快,意味着潜伏期越长。
最近,克uan等. [4]报告了从出现症状到需要机械呼吸机支持的中位时间为9.3天。因此,及时诊断并在7d内入院。可能是降低COVID-19感染致死率的关键。Z郝等. [19]报道,在患者症状出现后的第一周,总RNA阳性率<70%,而在第二周下降到50%。若干报告表明,许多患者最终通过每日重复取样和检测进行RNA检测确诊,许多病例与SARS-CoV-2暴露在流行病学上密切相关,并具有典型的肺部放射学结果,但RNA仍为阴性[6].在我们的研究中,患者入院时RNA阳性率为100%,但也不能排除部分患者因无法检测到病毒RNA而未确诊。在我们的研究中RNA阳性率较高的另一个原因是我们使用了深痰样本进行RNA检测,而其他许多医院更方便和流行的咽/鼻拭子。提示深痰、支气管肺泡灌洗等下呼吸道标本可能更可靠地检测SARS-CoV-2 RNA。
与RNA检测类似,在疾病早期发现阴性抗体不能排除感染的可能性。我们的研究表明,7 d。达到64.1%,然后在下周上升到>90%。相对较长时间的血清转化表明,对于寻找以前暴露的患者或亚临床携带者,特异性血清学不应取代RNA检测,但可能是一个重要的补充。此外,几乎所有患者都将转化为抗体阳性和滴度迅速增加的事实强调,如果对康复期样本进行检测,抗体测试在确认或排除SARS-CoV-2感染诊断方面的使用。
结果表明,采用相同的检测方法(ELISA、CLMA或LFIA),总抗体检测的敏感性高于IgM和IgG (p<0.001),特异性总体上具有可比性。总抗体检测采用双抗原夹心法。它原则上可以检测任何类型的抗体,包括IgM、IgG和IgA。此外,这两个工厂的相同的抗体分子需要绑定到涂布抗原和enzyme-conjugated抗原,保证测试的特殊性,然后允许高浓度抗原用于涂料和第二绑定增加的敏感性分析。因此,本研究中总Ab检测的灵敏度优于IgM和IgG检测也就不足为奇了。通常,IgM被认为是当前或近期感染的标志,而IgG被认为是感染后或近期感染的标志。总Ab的含义不是那么直接,在临床实践中很少使用。然而,如果敏感性是最优先考虑的,并且经常用于输血产品筛查,如艾滋病毒和丙型肝炎病毒,则总的Ab测试超过IgM和IgG。对于当前迫切需要的SARS-CoV-2感染敏感诊断,为了遏制传播,Ab试验可能是比IgM或IgG更好的选择,特别是考虑到病毒入侵人类社会不到4个月,抗体诱导感染后的患病率接近于零。最近,Lassauniere等. [20.结果表明,与本研究相同的万泰SARS-CoV-2抗体ELISA总抗体检测在灵敏度和特异性上优于仅检测特异性IgG或IgA。香港研究组也报告说,抗体血清转换发生在发病后10天左右,而且患者在血清转换阶段的病毒载量比早期低[21].有趣的是,在他们的研究中,更多的患者血清中IgG的转化比IgM更早。我们注意到,在他们的研究中,IgG和IgM抗体检测采用了间接ELISA方法,尽管μ链捕获法更适用于IgM检测。这可能是因为IgG和IgM检测方法的分析灵敏度不同。
本研究对基于ELISA、CMIA和LFIA的抗体检测进行了验证,总体表现良好。CMIA具有自动化操作、高通量、快速、客观、定量等优点,但需要昂贵的专用仪器。ELISA具有低成本、客观、高通量等优点,已广泛应用于世界各地的医学实验室。LFIA是一种快速的现场检测,不需要特殊的仪器,非常方便,易于操作,但结果的阅读是主观的。不同免疫检测方法的建立为用户提供了灵活的选择。
到目前为止,已经发表了一些关于SARS-CoV-2感染后抗体反应的报告[19- - - - - -23]。虽然这些报告中呈现的抗体反应概况大体相同,但报告的IgM和IgG血清转化顺序相互冲突。这可能是因为这些研究中使用的检测方法的敏感性不同。
我们研究的局限性包括以下方面。1)只纳入有症状的感染;因此,对无症状感染的抗体反应是否遵循类似的特征仍有待确定。2)血液标本采集时间多为发病后1个月,无法估计抗体持续时间。3)抗体水平未精确滴定,总抗体(RBD)、IgM (RBD)、IgG(核蛋白)采用不同抗原,未探讨抗体应答程度与临床严重程度的相关性。4)潜伏期未采集血样,发病前血清学状态人为阴性可能高估了血清转化所需时间。为了更好地了解SARS-CoV-2感染的抗体应答谱,准确解释血清学结果的临床意义,还需要进一步的研究。
综上所述,SARS-CoV-2感染过程中产生了典型的急性抗体应答。血清学检测是RNA检测对病原特异性诊断的重要补充,也是评估患者适应免疫状态的有用信息。强烈建议在临床管理和公共卫生实践中应用有效的抗体检测,以提高COVID-19感染的控制水平。
补充材料
可共享的PDF
确认
我们感谢浙江大学第一附属医院所有医务人员的工作和贡献。衷心感谢北京万泰生物制药企业有限公司的乔珊、贾雪蓉、贾宝亮、孙文杰、张继培、邱爽;厦门Innodx生物科技有限公司宋柳伟、文顺华、孙荣华、沈继培;感谢厦门联迈医疗器械有限公司的徐飞海的技术支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
数据可用性:我们将共享个人参与者的数据,这些数据在去除身份(文本、表格、图表和附录)后,作为本文报告结果的基础。该研究最终分析的主要结果发表6个月后,数据将公布,结束于2年后。这些数据将与建议使用数据的研究人员共享,这些研究人员的建议已被一个独立的审查委员会批准,该委员会为个人参与者数据荟萃分析确定。建议应提交到chenyuzy@zju.edu.cn。要获得访问权限,数据请求者需要签署数据访问协议。
利益冲突:彬楼没有什么可透露的。
利益冲突:李廷东没有什么可披露的。
利益冲突:郑书发没有什么可披露的。
利益冲突:苏英英没有什么可披露的。
利益冲突:李志勇没有什么可透露的。
利益冲突:刘伟没有什么可透露的。
利益冲突:费羽没有什么可透露的。
利益冲突:葛胜祥没有什么可透露的。
利益冲突:钱大洲没有什么要透露的。
利益冲突:全元没有什么可透露的。
利益冲突:林莎没有什么可透露的。
利益冲突:洪聪明没有什么可披露的。
利益冲突:姚向阳没有什么可透露的。
利益冲突:张学杰没有什么可透露的。
利益冲突:吴定辉没有什么可透露的。
利益冲突:周国良没有什么可披露的。
利益冲突:侯王衡没有什么可披露的。
利益冲突:李婷婷无需披露。
利益冲突:张雅丽没有什么可透露的。
利益冲突:张世银没有什么可透露的。
利益冲突:剑凡没有什么可披露的。
利益冲突:张军无需披露任何信息。
利益冲突:宁少霞没有什么可透露的。
利益冲突:于晨没什么可透露的。
支持声明:本研究由国家传染病防治重大专项(2017ZX10103008)和厦门市科技重大专项(3502Z2020YJ01)资助。资助方不参与研究设计、数据收集、数据分析、数据解释或报告的撰写。除了施普林格自然作者服务中心的语言编辑外,没有任何组织对提交的作品给予支持。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年3月19日。
- 接受2020年5月8日。
- 版权©2020人队
这个版本是在知识共享署名非商业许可4.0的条款下发布的。