抽象的
早期过敏性变态反应(atopy)是变态反应性疾病(如特应性哮喘)发展的第一步。儿童和青少年中与特应性和特应性哮喘相关的基因和途径尚未得到很好的描述。
在9-20岁(EVA-PR学习)和250队中的460帕多斯·富国队(EVA-PR研究)和250队队列中,在白细胞和白色血细胞(WBCS)或全血中的特性和特应性哮喘的转录组合哮喘的研究(TWA)进行瑞典青少年(BAMSE学习)。进行途径浓缩和网络分析以进一步评估顶部发现,使用顶部差异表达基因(DEGS)的表达水平建立特性和特应性哮喘的分类模型。
在研究队列的META分析中,既有先前涉及的基因(e、 g.IL5RA和IL1RL1以前未在双弯(新颖)中未报告的基因与特性和/或特应性哮喘显着相关。包含的特性的顶级新基因SIGLEC8(p = 8.07×10−13),SLC29A1(p = 7.07×10−12) 和SMPD3(p = 1.48×10−11).表达定量性状基因座分析鉴定了多种哮喘相关基因型表达对,例如RS2255888 /阿洛克15..途径富集分析发现,在调整后的p<0.01下,有16条途径显著富集,包括与t辅助细胞1型(Th1)和Th2免疫应答相关的途径。使用最高的DEGs和少数人口统计学/父母历史变量建立的分类模型准确地区分了特应性哮喘受试者和非特应性对照受试者(曲线下面积0.84)。
我们使用来自WBC和全血样品的转录组和青少年来确定儿童和青少年的特性和特应性哮喘的基因和途径。
抽象的
在波多黎各和瑞典儿童,一款TWA通过特工和40次哮喘识别59次,包括SIGLEC8和IL17RB.在前瞻性研究中,来自wbc的转录组数据可用于开发特应性/特应性哮喘的预测模型。http:///wly/kf6v30nync.
介绍
在过去的几十年里,过敏性疾病的流行在美国和世界范围内都有所增加。儿童早期对过敏原(特应性)的敏感先于儿童后期发生过敏性疾病,包括食物过敏、过敏性鼻炎和特应性哮喘[1].波多黎各和瑞典儿童承担高度的土木和哮喘[1- - - - - -3.]. 在对学龄儿童的研究中,估计波多黎各人哮喘和过敏性鼻炎的患病率分别为16.1%和48.4%[2,4].在7-8岁的瑞典儿童中,目前喘息和过敏鼻炎的患病率分别为13%和13.8%[5].
基因组关联研究最近的荟萃分析(GWASS)确定了哮喘的18个易感性基因座[6[过敏性鼻炎的41个易感性基因座[7].然而,这些基因位点只占哮喘(~ 3.5%)和过敏性鼻炎(~ 7.8%)遗传率的一小部分,而转录组学等替代方法可以帮助确定特应性疾病的“缺失遗传率”。另一种互补的方法是研究中间表型,如特应性,因为特应性的易感基因经常与常见过敏性疾病的易感基因重叠[7].
与迄今进行的许多GWASs相比,特应性和哮喘的转录组范围关联研究(TWASs)很少,所有这些研究都受到样本量适中和没有复制或复制不足的限制[8- - - - - -12].例如,从受试者(n = 50)和没有(n = 50)哮喘的鼻胶片中的靶向RNA测序的研究表明鼻转发组谱可以识别受试者IL13- 驱动的哮喘和T-辅助细胞2型(TH2) - 辐射免疫应答[9].在另一项研究(包括大部分是成年人)、RNA序列资料从鼻刷牙是用来首先开发一组90个基因区分对象对轻中度哮喘(n = 53)与对照组(n = 97),然后测试“分类器面板”40学科(n = 13)和没有(n = 27)哮喘(10].尽管该小组在训练队列中表现良好,但外部复制是有限的,因此不能自信地确定具有哮喘易感性的个体基因。
虽然气道上皮研究已经显示出有希望的结果,但血液样本很容易收集,并经常用于流行病学研究。循环CD19的转录组学全基因组分析+来自41名成人的b淋巴细胞提供了增加的提示证据IL4R.与对照主题相比,粉尘螨过敏和哮喘的主题中的表达[11].在具有哮喘的年轻青少年的另一个研究中,来自CD4的微阵列表达谱+T淋巴细胞在特应性状态下有差异表达[12然后,在30个受试者的队列中,5个“特应签名”基因被标称重复。哮喘控制的后期一致性研究集中于血液中的转录组成分,随着哮喘控制的程度而变化[13].
在这里,我们从波多黎各的儿童和青少年的白血细胞(WBCS)中的第一个特性和特应性哮喘的调查结果报告,并在瑞典儿童队列中进行了验证研究。
方法
进一步的细节是给出的补充材料.
研究人群
EVA-PR (epigengenetic Variation and Childhood Asthma in Puerto Ricans)研究是一项9-20岁波多黎各人哮喘病例对照研究,招募方法与之前在圣胡安(Puerto Rico)大都会区使用的研究方法相似[14,15].在543名参与的儿童中,460次测量到波多黎各的五个常见过敏原(灰尘螨(Der P 1),蟑螂(BLA G 2),猫皮(FEL D 1),狗皮屑(CAN F 1)和小鼠尿蛋白(mus m 1))[16[来自WBC的WBC计数和差异,以及来自WBC的RNA,并因此包括在当前分析中。该研究得到了波多黎各大学(圣胡安)和匹兹堡大学(帕茨堡,帕,美国)的机构审查委员会批准。书面父母同意和同意是从所有参与者获得的。
RNA测序和数据预处理
除去血红蛋白(RNA完整性数> 7)后,使用350ng从WBC中提取的350ng高质量的RNA进行测序。根据制造商的协议,使用带有Richo-of金高通量试剂盒(Illumina,San Diego,CA)的Truseq Stranded Total RNA文库预备套件进行了图书馆制备。使用NextSeq 500/550高输出套件2(Illumina)在NextSeq 500上运行图书馆。
使用FASTQC执行RAW RNA测序FASTQ文件的质量控制[17].低质量的读取和3 '适配器修剪与修剪丰富![18]和Cutadapt[19].然后将修剪的读数对齐以参考人类基因组HG19与明星[20]随后使用RSEM在Illumina Igenomes数据库中注释[21].从下游分析中除去具有低对准百分比和具有低表达的基因的样品。在预处理后,在最终分析中,共保留16880个基因和460个样品。
如前所述,利用HumanOmni2.5 BeadChip平台(Illumina)获得的全基因组基因型数据计算主成分[22]. 使用插补服务器对非基因型单核苷酸多态性(SNPs)进行插补[23],使用单倍型参考财团R1.1 2016 [24]作为参考小组。
班斯研究
我们还使用Affymetrix人体转录组阵列2.0(Affymetrix,Santa Clara,CA)分析了269名16岁儿童(儿童[谷仓],过敏,Milieu,斯德哥尔摩,流行病学),瑞典语基于人口的群组(具有哮喘和鼻炎的过采样)[25]. 在进行质量控制(RNA完整性数值>6)和异常值检测后,250份血液样本的基因表达数据被纳入当前的特应性和特应性哮喘分析中,包括可用的白细胞计数和差异表达。使用ImmunoCAP系统(瑞典乌普萨拉赛默飞世尔/Phadia)测量过敏原特异性IgE水平。
统计分析
在EVA-PR和BAMSE中,Atact被定义为至少一个正IgE(≥0.35IU·mL−1)的过敏原测试。特应性哮喘被定义为当前的哮喘(医生诊断的哮喘和当前的喘息)和EVA-PR中的特应性哮喘,以及当前的哮喘(使用GA的改进版本进行评估2LEN问卷2)和ALATE在禁止体中[26].
使用DESEQ2基于原始计数表分析差异表达基因(DEGS)[27]对于EVA-PR和RIMMA中的RNA测序数据,用于BAMSE中的微阵列数据。在EVA-PR和BAMSE的两种中,以WBC亚型(嗜酸性粒细胞,淋巴细胞,单核细胞和中性粒细胞的比例(嗜酸性粒细胞,淋巴细胞,单核细胞)调节多变量的特应哮喘模型。还针对哮喘状态调整了所有多变量特性的特性型号。在EVA-PR,另外调整所有模型,用于衍生自基因型的前五个主要成分,以考虑人口分层。施加零平均正常的预计在非阻塞系数上,以确保折叠变化与参考水平的选择无关。接下来,我们使用使用R包元的内部代码进行固定效果模型对群组特定结果进行了荟萃分析[28,29].采用错误发现率(FDR)方法对多次检测进行调整。
在EVA-PR中,我们进行了表达数量性状基因座(eQTL)分析(距离<1 使用R包矩阵eQTL对特应性疾病进行荟萃分析,获得最高结果[30].
路径与网络分析
在特性和特应性哮喘的荟萃分析中对顶部(FDR调节的P <0.1)进行巧精力途径分析,以鉴定富集的规范途径和基因网络[31].然后,我们计算我们发现队列中基因表达水平之间的部分相关性,首先在所有受试者中,然后通过哮喘状态分开,使用R包FastGGM [32,是在高斯图形模型框架下检测条件基因网络的强大工具。
特应性和特应性哮喘的分类模型
采用惩罚最大似然逻辑回归建立EVA-PR中特应性和特应性哮喘的分类模型。我们首先建立了两个模型进行比较:一个仅包括人口统计学和父母史变量(年龄、性别和父母哮喘史)作为预测因子,另一个包括人口统计学变量,随机选择基因的亲代史和基因表达水平。接下来,我们在荟萃分析中使用top DEG构建了一个模型,另一个模型使用top DEG加上人口统计学变量和父母历史。分别为特应性哮喘和特应性哮喘建立模型。
结果
研究参与者的主要特征如所示表格1.在EVA-PR中,与对照组相比,特应性患者明显更有可能是男性和哮喘患者。与EVA-PR的参与者相比,正如一项基于人群的队列研究所预期的那样,BAMSE的哮喘受试者比例更低,年龄范围更窄。
特应性哮喘
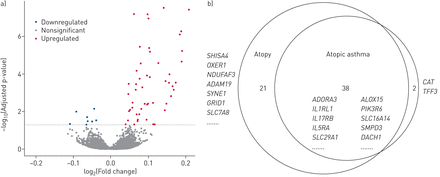
在针对WBC亚型和其他协变量调整的特性的多变分析中,我们在FDR调节的P <0.05时鉴定了EVA-PR的69次。在BAMSE中,在FDR调节的P <0.05下没有DEGS,但EVA-PR的69次中的17个在P <0.05差异表达,两项研究中的效果大小估计(补充表S1).接下来,为了增加DEG分析的统计力,我们将两种队列中的结果与转录组宽的META分析中的结果组合在一起,其通过ATOPTED鉴定了59次,以FDR调节的P <0.05(图1一个和补充图S1).表2.列出该荟萃分析中的前20个基因(通过p值),在这两项研究中,基因表达与Atact之间的关联方向一致。
基因表达的Meta分析证明了特征受试者和对照受试者之间基因表达的显着差异。DEG:差异表达基因。a)显示日志的火山图2(折叠变化)和-log10(调整后的p值)。特应性受试者和对照受试者之间具有统计学意义的差异由红色(上调)和蓝色(下调)符号表示。一个基因被认为有差异表达的统计标准是错误发现率调整p<0.05。b).描述特应性受试者与对照受试者、特应性哮喘受试者与非特应性非哮喘对照受试者分析中deg的分布的维恩图。
对于Atopate的顶部进行,我们发现FDR调整的P <0.05的43种富集的途径。表3列出了前20条富集途径,其中最显著的两条是Th2途径和Th1/Th2激活途径。其他上位通路包括神经生长因子(NGF)和腺嘌呤/腺苷挽救I。
特应性哮喘TWAS
然后我们进行了特征性哮喘的转录组分析,在该分析和Atopt的结果之间发现了大量重叠(图1 b和补充表S2).在经fdr调整p<0.05的情况下,我们在EVA-PR中鉴定了49个特应性哮喘的DEGs。在BAMSE中,在fdr校正p<0.05时,没有差异表达,但EVA-PR中49个与特应性哮喘相关的差异表达中有5个在BAMSE中有差异表达,p<0.05,效应大小估计相似。在fdr调整后p<0.05的meta分析中确定了40个deg。对于特应性哮喘,通路富集分析揭示了脂质代谢相关通路(例如二十二碳六烯酸信号)和花生四烯酸信号(例如类花生酸信号)(补充表S3).
eQTL分析
接下来,我们进行了独联体- EVA-PR的-eQTL分析,其鉴定了3772个SNP,其与我们的顶部基因显着相关,来自FDR调整的P <0.05(补充表S4).此类SNP包括GTEX数据库中的多个EQTL(例如rs2255888在阿洛克15.和rs35092096CCR3.) [33].有趣的是,多个SNPs与表达IL1RL1(一种已知的哮喘易感基因)[6].
网络分析
进行网络分析以说明Atopate的顶部Degs之间的相互作用(补充图S2),首先在所有受试者中,然后分别在特应科受试者和对照受试者中。即使在全球表达谱上调节,这些基因之间的部分相关性仍然很强。对于最差异表达的基因,这尤其如此,SIGLEC8. 我们还发现,对照组中的一些强相关性在特应性儿童中显著减弱,比如基因对il34.和Cysltr2..
接下来,我们根据特异反应性meta分析中的59个DEGs(经fdr调整的p<0.05),用EVA-PR中每千碱基百万值的日志转化转录本进行分层聚类,识别出四个个体簇(图2).在这种分析中,Atopate的患病率不同于前两个集群之间,但在最后两个集群之间不相差(补充图S3).然而,当我们在这四种簇中的样品中比较嗜酸性粒细胞比例时,我们发现具有更高表达的样品对于特性的顶部较高的样品在外周血中具有更多的嗜酸性粒细胞(图3).然后,我们测试了针对特性或特应性哮喘的顶部DEGS的表达水平和外周血中每个细胞亚集的比例(补充表S5).在Atopt的前59℃下,51个基因显着相关(FDR调整为P <0.05),嗜酸性粒细胞在外周血中。然而,少数顶部DEG与其他细胞类型的比例相关(例如APRT和TMEM160淋巴细胞比例,和Pepd.患嗜中性粒细胞比例)。所有前40只可用于外周血中的嗜酸性粒细胞显着相关。接下来,我们基于已知的细胞比例和置换来解构WBC的表达谱,以便使用CiberSort研究细胞类型特异性差异表达[34].38个基因在嗜酸性粒细胞中显著富集(fdr调整后p<0.05)。在这38个基因中,24个基因属于特应性基因,20个基因属于特应性哮喘基因。
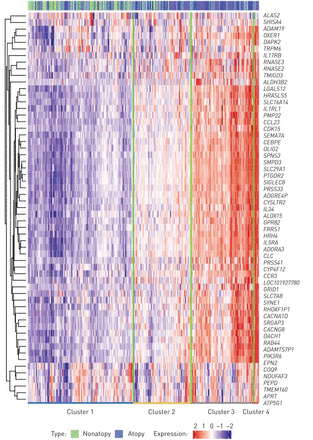
基于meta分析中最高差异表达基因的层次聚类。四个簇被确定,大多数基因从簇1上调到簇4。
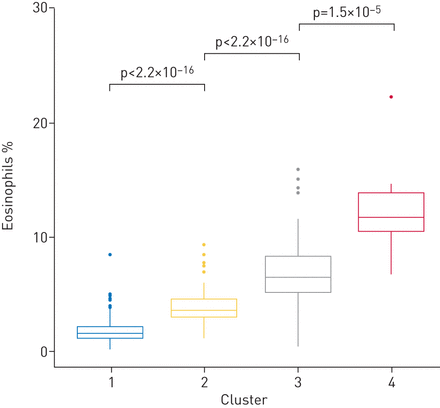
中所鉴定的各簇嗜酸性粒细胞比例比较图2,在Kruskal-Wallis检验中显示出全球范围内和个别聚类之间的显著差异。盒须图显示了中位值的四分位范围(盒)和上下限在盒范围(须)的1.5 IQR内;异常值由单个数据点表示。
特应性和特应性哮喘的分类模型
最后,我们仅使用人口变量和父母历史,在特性哮喘的特性哮喘下实现0.56的曲线(AUC)值下的区域和父母历史来建立探索队列中的分类模型。在添加随机组基因的表达水平后,这些结果类似于(未示出的数据)。单独使用顶部作为预测因子时,对于特性和特应性哮喘,模型分别达到0.77和0.81的AUC值。然而,分类模型的性能大致改善了顶部的表达水平,将人口变量和父母史的表达水平作为预测因子,为特性为0.77的AUC值和0.84用于特应性哮喘(图4).对于采取的特性,我们使用了51个基因(在荟萃分析中进行FDR调整的P <0.05,以适用于群组),同时用于特应哮喘,我们包括前33个基因(在Meta-Analysis中FDR调整的P <0.05)适用于Atopic哮喘,在两个队列中提供)。
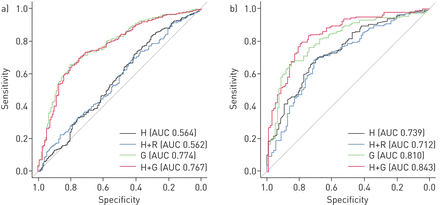
a)特应性哮喘和b)特应性哮喘的分类模型。H:年龄、性别、父母哮喘史为预测因素;R:随机选择的基因表达谱(与G数目相同)作为预测因子;G:最高差异表达基因预测因子的表达谱(meta分析中错误发现率调整后的p<0.05);AUC:接收机工作特性曲线下的面积。
讨论
在wbc的TWAS中,我们通过460名波多黎各儿童的特应性和特应性哮喘鉴定了DEGs。同时,我们进行了TWAS的特异反应性和过敏性哮喘250年瑞典儿童,产生无意义的结果由于小样本大小,但产生了复制我们的一些顶级的发现在波多黎各的孩子p < 0.05,同一方向的协会和具有类似效果的估计。接下来,我们对来自两个研究队列的TWASs进行了荟萃分析,通过特应性鉴别出59个DEGs,通过特应性哮喘鉴别出40个DEGs。
在我们的META分析中,ATATEPT的顶部是SIGLEC8,其具有一个细胞外结合域,可诱导嗜酸性粒细胞凋亡,并抑制肥大细胞中fc ε ri依赖的介质释放[35]. 单核苷酸多态性SIGLEC8在候选基因研究中与哮喘和嗜酸性食管炎相关[36,37]但是在最近的GWASS的META分析中,该基因与哮喘无关[6].有趣的是,在我们的特应性荟萃分析中,前20个基因之一的表达(OLIG2,编码少突胶质细胞转录因子2),此前报道下调RNA和蛋白水平SIGLEC8外周血嗜酸性粒细胞[38].此外,表达水平OLIG2和CCL23一项来自693名不同种族的儿童和成人的数据的荟萃分析显示,全血中异位性哮喘(我们在特应性哮喘方面的顶级deg之一)与疾病控制欠佳显著相关[13].两个都OLIG2和CCL23是TREM-1(髓系细胞中表达的触发受体-1)/脂多糖信号基因,TREM-1是模式识别受体诱导的炎症反应的关键放大器。
其他首选研究结果得到了其他人类研究的实验证据或结果支持。SLC29A1参与腺苷调节抑制肥大细胞依赖性脱粒的抑制[39].il5ra.,在我们之前的研究中与哮喘有关的基因[40,调控Th2细胞分化和Th2细胞效应功能[41].而且,il5ra.和阿洛克15.(在我们的顶部基因中也与哮喘受试者的受试者的血液样本的转录组分析显着相关[36].这与我们的现有结果一致[42,结合我们的层次聚类分析和其他互补分析的结果,进一步强调了嗜酸性粒细胞依赖机制在特应性和特应性哮喘发病机制中的关键作用。
我们的研究结果为IL17RB特别有趣。在小鼠模型中,过敏原攻击触发白细胞介素(IL)-4途径,促进过敏气道炎症和气道反应性。反过来,IL-4途径的激活会诱导IL-25和IL-17RB在血清和肺部的表达[43,44].在之前对哮喘患者的研究中,IL17RBCD4在外周血中的表达+T细胞与血清总IgE显着相关[45,尽管只对男性有效。与关键角色一致IL17RB在人类的遗传性疾病中,基因缺失IL17RB显著减轻小鼠的过敏反应[44].
我们确定了其他可能的特应性和特应性哮喘候选基因。SMPD3,编码鞘磷脂磷酸氨酯酶3 [46,在慢性阻塞性肺疾病患者的小气道中呈高甲基化和下调[47].Pik3R6.,气道平滑肌细胞中IL-17A基因靶点[48,已经被证明与接触二手烟在1秒内的强迫呼气量相互作用。其他基因,如ADAMTS7P1,EPN2和rab44.,在TWASs中未见报道,值得进一步研究。
Atepy的Degs通常与Atopic哮喘的那些重叠。我们的大多数顶级调查结果与基因型数据相关,并强调遗传易感性对特性。此外,基于部分相关的网络分析揭示了重要的次数之间的密切相互作用。
与已知的特应性机制一致,我们发现最富集的两个途径是Th2和Th1/Th2激活途径。我们分析的其他顶级途径是NGF(过敏性气道炎症和气道平滑肌细胞增殖的关键因素)[49]和腺嘌呤/腺苷抢救I(腺嘌呤已被禁止用于过敏或严重哮喘)[50].
我们将wbc中基因表达和特应性哮喘的研究结果与先前气道上皮和哮喘基因表达的荟萃分析结果进行了比较[51].在我们的研究中,Atopic哮喘的前40次,七种通过气道上皮的哮喘表达了7个差异(补充表S6).其中一些差异可能是由于先前气道上皮分析中包括了特应性哮喘和非特应性哮喘的病例,而另一些差异可能表明了特应性哮喘基因表达的真正组织特异性差异。我们还将我们的结果与先前欧洲对104名中度至重度哮喘受试者和16名健康志愿者的痰转录组学研究结果进行了比较[52].在该研究中,鉴定了三种转录组相关的簇,其中其中一种富集IL-13 / TH2途径。在包含该簇的20个基因中,七种也与我们的META分析中的特性或特应性哮喘(FDR调整的P <0.05)相关(PRSS33.,CLC.,LGALS12,阿洛克15.,OLIG2,HRH4.和CCR3.).
我们将meta分析中最高的DEGs与血液和气道上皮样本中特应性哮喘和特应性哮喘的表观基因组全关联研究(epigenome-wide association studies, EWASs)中发现的最高CpG位点进行了比对。在鼻上皮的EWAS中,含有或接近前30个CpG位点的基因最近都没有与特应性相关[53]在我们的研究中,DEG是由特应性哮喘引起的,但在我们的研究中,两个DEG是由特应性哮喘引起的(il5ra.和SIGLEC8)在全血的ewas中,哮喘是差异甲基化地区的一部分[54,55].
我们的分类模型的结果进一步支持了我们顶级调查结果的有效性,以及在未来的纵向研究中使用WBCS开发特拉科特和特应性哮喘的预测转录组织面板的合理性。尽管使用来自成人气道上皮的转录组数据的特应组哮喘的分类模型表现出更高的准确性(AUC 0.99)[10相比于本研究(AUC 0.84), wbc比鼻腔或支气管上皮更容易收集[10].
两种类型的样本(白细胞计数)存在差异与全血)和用于评估基因表达的平台(RNA测序与在EVA-PR和BAMSE之间。这一点,再加上两项研究在种族和样本量上的差异,可能解释了我们在BAMSE中EVA-PR的发现缺乏显著的重复。然而,先前的一项特应性皮炎转录组学研究发现,除了低表达水平的基因外,RNA测序结果与微阵列之间普遍存在良好的相关性[56].此外,我们发现,对于BAMSE中EVA-PR的一些顶级发现,名义复制率p<0.05,具有一致的方向和估计的效应大小。虽然在经过FDR多次检测校正后,在BAMSE中没有显著的与特应性哮喘或特应性哮喘相关的DEGs,但在BAMSE中与特应性或特应性哮喘相关的顶级基因(显示在补充表S7)富集了能量耦合的质子和离子跨膜转运途径。
总之,我们在波多黎各和瑞典儿童的组合转录组科分析确定了Atopy Attopy和40次哮喘40次,包括SIGLEC8和IL17RB.在未来的前瞻性研究中,来自wbc的转录组数据可用于建立特应性和特应性哮喘的预测模型。
补充材料
致谢
我们感谢所有参与的儿童和家庭。BAMSE团队要感谢Charles Auffray(法国里昂欧洲系统生物学和医学研究所)和他的团队生成了转录组学数据。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
作者贡献:W。陈,E。Melén和J.C.Celedón构思并设计了这项研究。Y江,O。Gruzieva和S.K.Merid进行了初步分析并解释了数据。E福诺,T。王,E。阿科斯塔·佩雷斯,G。卡尼诺,我。库尔,J.M.安东和J。Bousquet参与了数据收集和数据分析。Y江,W。陈和J.C.Celedón准备了手稿的初稿。所有作者都审查了草稿的知识内容,并批准提交最终版本的手稿。
利益冲突:Y.江无所事事。
利益冲突:O. Gruzieva没有什么可披露的。
利益冲突:王涛没有什么可透露的。
利益冲突:E. Forno没有什么可披露的。
利益冲突:N.布塔维没什么可透露的。
利益冲突:T.孙没有什么可透露的。
利益冲突:S.K. Merid没什么可透露的。
利益冲突:E. Acosta-Pérez无需披露。
利益冲突:一、库尔没有什么可披露的。
利益冲突:G. Canino没有什么可透露的。
利益冲突:J.M. Antó没有什么可披露的。
利益冲突:J. Bousquet报告了来自Chiesi、Cipla、Hikma、Menarini、Mundipharma、Mylan、Novartis、Sanofi-Aventis、Takeda、Teva和Uriach的咨询委员会工作、咨询和讲座的个人费用,并在提交的工作之外拥有Kyomed的股份。
利益冲突:E.Melén没有披露。
利益冲突:W. Chen没有什么可披露的。
利益冲突:J.C.CeleDón已收到GSK,Merck和Pharmavite的研究资料,以外的工作。
支持声明:来自美国国家卫生研究院(NIH)的Grants HL079966,HL117191和MD011764(主要调查员:J.C.CeleDón)支持这项研究。E. Forno的贡献得到了NIH Grant HL125666的支持。江泽民得到了中国奖学金委员会的支持。瑞典心脏龙基金会,瑞典研究委员会,斯德哥尔摩委员会(ALF),在Karolinska Institutet和Medall的流行病学战略研究方案(SFO)的战略研究计划(SFO)得到了支持的副群体支持(过敏的机制;欧洲Union Grant协议编号261357)。E.Melén得到欧洲研究理事会的批准(授予协议编号757919,部落)的支持。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2019年1月15日。
- 接受2019年3月2日。
- 版权©2019人队