文摘
背景Anlotinib已经证明在临床试验中可有效延长无进展生存(PFS)和总生存期(OS)耐火材料先进nonsmall细胞性肺癌(NSCLC)患者。然而,潜在的分子机制和预测生物标志物anlotinib仍不清楚。
方法anlotinib管理的回顾性分析294名非小细胞肺癌患者进行筛选的潜在生物标志物anlotinib-responsive病人。转录组和功能进行了分析理解anlotinib的抗肿瘤分子机制。血清CCL2水平变化进行分析检查的相关性anlotinib响应反应者和nonresponders之间。
结果Anlotinib治疗有利于延长操作系统在非小细胞肺癌患者窝藏积极司机基因突变,尤其是病人窝藏上皮生长因子受体(EGFR)T790M突变。此外,anlotinib抑制血管生成在一个NCI-H1975-derived异种移植模型通过抑制CCL2。最后,anlotinib-induced血清CCL2水平降低与PFS的好处和操作系统有关难治性晚期非小细胞肺癌患者。
结论我们的研究报告一本小说anlotinib的抗血管生成机制通过的抑制CCL2 NCI-H1975-derived异种移植模型,表明血清CCL2水平变化可能被用来监视和预测临床结果anlotinib-administered耐火材料使用三线治疗晚期非小细胞肺癌患者或超越。
文摘
潜在的分子机制和预测生物标志物的anlotinib NSCLC患者中仍不清楚。在这项研究中,anlotinib-induced CCL2减少导致小说的见解为其抗血管生成机制和响应预测。http://ow.ly/YZL930mXlfV
介绍
肺癌是全世界癌症相关死亡的主要原因。nonsmall细胞肺癌的发病率(NSCLC)据报道,是每000人39.05,占∼85%的肺癌患者(1]。∼75%的病人拥有先进的不可切除的非小细胞肺癌,起初诊断,5年生存率小于15% (2,3]。组织学检查非小细胞肺癌(LUSC)主要由鳞状细胞癌和腺癌(LUAD) [4]。一线和二线治疗晚期NSCLC包括司机基因的抑制和全身化疗。三线药物治疗没有合并方案(5]。全身化疗的非小细胞肺癌包括传统的化疗药物,抑制剂的血管生成和转移抑制剂(6]。尽管晚期NSCLC患者获得巨大的好处从一线和二线疗法,药物有说服力地延长无进展生存(PFS)和总生存期(OS)在三线或三线治疗仍然是有限的。多目标药物可以延长PFS和操作系统引入一个新的机会在难治性晚期非小细胞肺癌患者接受三线或三线治疗之外(7- - - - - -10]。
Anlotinib是一个多目标受体酪氨酸激酶抑制剂(TKI)证明抗肿瘤效应在各种癌症8- - - - - -12]。先前的研究已经表明,anlotinib抑制肿瘤生长的抑制血管生成和细胞增殖信号通路(8,13,14]。重组酶化验在体外表明anlotinib选择性地抑制血管表皮生长因子受体(VEGFR) 1、2和3,血小板源生长因子受体(PDGFR) -α-β和纤维母细胞生长因子受体(FGFR) 1、2、3和4。此外,anlotinib抑制肿瘤细胞生长通过c - kit的抑制,受潮湿腐烂、Aurora-B c-FMS和DDR115- - - - - -17]。
最近的临床试验表明,anlotinib疗法可以延长晚期NSCLC PFS和操作系统在耐火材料受三线或三线治疗之外(7,9,10]。底层机制可能归因于anlotinib-induced块血管生成。然而,阻断血管生成的分子机制尚未完全的特征。此外,识别生物标志物,可用于监测和预测晚期非小细胞肺癌患者的临床反应anlotinib迫切要解决的问题,改善临床结果。因此,在目前的研究中,我们试图探索anlotinib的底层抗血管生成机制和确定可能的生物标志物监测和预测anlotinib治疗晚期非小细胞肺癌患者的临床结果接收三线或三线治疗。
方法
病人和样品
临床试验和样品准备进行根据我们先前的研究[7,9]。审判(改变- 0303)注册在ClinicalTrials.gov标识号码NCT02388919。
Anlotinib响应分层子组
根据组织病理学分类,所有非小细胞肺癌患者分为LUSC或LUAD。PFS和操作系统进行分析的基础上,组织病理学分类所有注册anlotinib-administered NSCLC患者。积极和消极的司机基因突变的分类(上皮生长因子受体(EGFR), ROS1或碱性)被用来评估应对anlotinib LUAD病人。此外,积极的司机的亚型基因突变进行评估分析相关性PFS和操作系统。最后,转移的数量(分层超过三个转移和三个或更少的转移)注册LUAD患者在初始评估是用来评估响应anlotinib LUAD病人。
RNA-seq
RNA-seq和生物信息学分析化验进行根据我们先前的研究[18,19]。中提供了详细信息补充材料。这项研究的原始数据是可用在EMBL数据库加入e - mtab - 5997数量:www.ebi.ac.uk arrayexpress /。
动物实验
实验用Balb / c裸小鼠(上海实验动物中心、上海、中国)进行为福利按照国家指导方针。感应程序NCI-H1975-derived异种移植模型,分组、药品监督管理局,肿瘤体积测量和样本集合中所描述的补充材料。
定量分析
组织学分析(包括苏木精和伊红())染色和immunofluorescent组织化学分析),信使rna表达分析和ELISA分析进行常规程序。中提供了详细信息补充材料。
Anlotinib应答分析预测
我们旨在了解血清CCL2水平变化是否可以用来预测NSCLC患者的临床反应anlotinib。437 NSCLC患者参与改变——0303年的研究,和294名患者接受anlotinib疗法。的294患者中,有14个anlotinib急救员(PFS > 80天)与合格的血液样本在基线,最好的回应和进步的疾病,同时进行。比较之间的差异反应者和nonresponders,我们随机挑选出14 anlotinib nonresponders (PFS≤80天)在基线和进步与合格的血液样本疾病时间点。司机基因突变状态的非小细胞肺癌患者第一次活检所示补充表S1。根据标准方法血清分离从血液。CCL2水平检测通过ELISA如前所述。CCL2水平相比,非小细胞肺癌患者在不同的时间点。CCL2水平变化anlotinib治疗后计算基于CCL2水平在不同的时间点。Anlotinib应答分析预测进行了基于CCL2水平变化。
统计分析
PFS和操作系统被概括为中间值和双面的95%的置信区间和使用kaplan meier方法进行分析。Mantel-Cox测试是用于执行kaplan meier GraphPad棱镜5中生存分析(美国圣地亚哥,CA)。所有在体外实验中,扣除RNA-seq进行至少三个生物复制。数据意味着±sd。使用双尾的数据进行t检验,生存率较或单向方差分析事后Bonferroni调整。差异被认为是重要的在p < 0.05, p < 0.01, p < 0.001。
结果
LUAD病人窝藏积极司机anlotinib治疗后基因突变有更好的操作系统
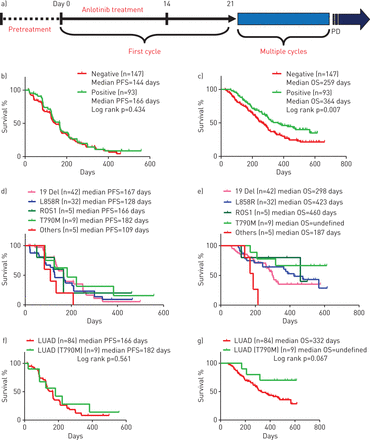
所有非小细胞肺癌患者(n = 294)收到anlotinib治疗连续两周,然后停止一个星期(图1一个),直到疾病进展的观察(PD)。检查anlotinib响应的非小细胞肺癌患者,我们将病人分成LUSC (n = 54)和LUAD (n = 240)根据病理分类。kaplan meier分析表明,没有差别的PFS和操作系统之间的曲线LUSC和LUAD anlotinib疗法(补充图S1a)。在注册病人,LUAD占绝大多数的非小细胞肺癌患者。因此,我们进行了亚组分析的LUAD病人。与驱动程序的操作系统相比gene-negative病人(n = 147),司机的gene-positive病人(n = 93)后被大大延长anlotinib疗法。然而,没有显著差异当PFS分析(图1 b和c)。随后,kaplan meier分析检查司机基因的突变类型之间的相关性和PFS或操作系统。病人窝藏ROS1或表皮生长因子受体T790M突变有更好的响应anlotinib比其他类型的驱动基因突变(图1 d和e)。进一步分析显示,患者窝藏EGFR的操作系统T790M是大大超过那些与其他司机基因突变类型,尽管PFS依然无足轻重的差异(图1 f和g)。此外,非小细胞肺癌患者窝藏超过三个转移有较短的PFS和操作系统比非小细胞肺癌患者窝藏三个或更少的转移(补充图印地)。有趣的是,我们发现一些LUAD病人没有一个司机基因突变也有一个很好的应对anlotinib疗法(补充图S1c-e),建议可选择的潜在生物标记区分从nonresponders anlotinib反应者。
回顾性分析anlotinib III期临床试验表明,肺腺癌(LUAD)患者的总体生存与司机基因突变类型相关联。一)anlotinib III期临床试验的时间。kaplan meier块b)无进展生存(PFS)和c)总生存期(OS) nonsmall细胞性肺癌(NSCLC)患者接受anlotinib治疗的负面(n = 147)和积极的基因突变(n = 93)驱动程序。中位数(95% CI) PFS 147(131 - 163)天与166(143 - 189)天,中位数(95% CI) OS 259(234 - 284)天与364(332 - 396)天。分析d) PFS和e)操作系统anlotinib-treated LUAD病人窝藏表皮生长因子受体(EGFR)和其他积极的突变。kaplan meier情节f) PFS和g)操作系统的驱动程序gene-positive LUAD EGFR在接受anlotinib治疗的病人T790M- (n = 84)和表皮生长因子受体T790M艾滋病患者(n = 9)突变。中位数(95% CI) PFS 166(144 - 188)天与182(53 - 311)天,中位数OS (95% CI) 332(299 - 365)天与未定义的。帕金森病:疾病进展的。
Anlotinib诱发NCI-H1975细胞的细胞毒性在体外和在活的有机体内
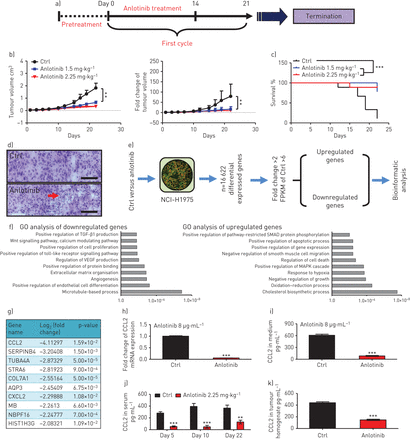
了解潜在的分子机制可能是一个先决条件来识别有价值的生物标志物anlotinib反应者。在这里,我们发现NCI-H1975 anlotinib显然敏感细胞在体外通过诱导细胞凋亡,细胞入侵抑制,细胞周期阻滞和细胞迁移抑制(补充图S2a-i)。这些结果显示多个anlotinib在NCI-H1975细胞的细胞毒性效应。检查anlotinib是否能抑制肿瘤生长在活的有机体内我们管理anlotinib NCI-H1975-derived异种移植模型。时间轴的在活的有机体内实验中所示图2一个。经过一个周期的anlotinib治疗,肿瘤生长明显抑制,和生存时间明显增强,与可接受的毒性剂量(图2 b和c和补充图S2j-l)。广泛组织坏死,评估)染色,发现anlotinib-treated NCI-H1975-derived异种移植模型中,肿瘤腔,作为评估使用计算机断层扫描,显示耐火anlotinib后晚期非小细胞肺癌患者治疗(图2 d和补充图就是S1c和d),表明抗血管生成可以在anlotinib-induced肿瘤抑制发挥重要作用。
转录组分析表明anlotinib-induced CCL2封锁与anlotinib-induced抗血管生成有关。时间轴的实验在活的有机体内。b)皮下肿瘤体积的测量控制(Ctrl)和anlotinib团体;评估肿瘤生长的褶皱变化。数据意味着±sd,n = 9。c)与Ctrl kaplan meier治疗组小鼠的生存曲线,anlotinib·kg(1.5毫克−1)和anlotinib·kg(2.25毫克−1)。n = 9。d)代表图像的苏木精和伊红染色NCI-H1975-derived异种移植肿瘤与anlotinib治疗后22天与Ctrl。放大10×;酒吧= 25µm规模。三个视图的一个部分动物;n = 9老鼠每组。e)流程图识别调节和表达下调基因的转录组Ctrl与anlotinib。f)的功能性浓缩anlotinib-induced表达下调和调节基因通过基因本体论(去)分析。1128个表达下调基因(褶皱变化> 2)和636年调节基因(褶皱变化> 2)受到基因本体分析。g)排名前十的表达下调的基因在NCI-H1975 anlotinib治疗后细胞。NCI-H1975细胞暴露于anlotinib(8µg·毫升−1为24小时);h)褶皱的变化mRNA的表达CCL2使用逆转录酶定量PCR检测。数据意味着±sd,n = 3;我)CCL2水平在中使用酶联免疫试剂盒进行评估。数据意味着±sd,n = 4。j) CCL2水平血清NCI-H1975 tumour-bearing裸体小鼠anlotinib治疗期间(第五天,第十天,天22)。数据意味着±sd,n = 9。k) CCL2水平的肿瘤匀浆NCI-H1975-derived异种移植肿瘤22天。数据意味着±sd,n = 9。FPKM:每千碱基片段百万;TGF:转化生长因子;VEGF:血管内皮生长因子;MAPK:增殖蛋白激酶。* *:p < 0.01;* * *:p < 0.001。
转录组分析表明anlotinib-induced CCL2封锁是参与anlotinib-induced血管生成块
基于anlotinib引起的细胞毒性和组织坏死的观察,我们下一个试图理解底层的分子机制通过transcriptome-wide差异基因表达分析(图2 e)。结果表明,多个生物过程或信号通路参与anlotinib-induced细胞毒性(图2 f和补充图S3)。表达下调的基因中,有趣的是,我们发现某些angiogenesis-related生物过程(包括血管生成,积极调节内皮细胞分化和微管过程)是最丰富(图2 f)。
CCL2是肿瘤治疗的一个重要血管生成目标20.]。在这里,我们发现CCL2转录表达下调17倍以上anlotinib治疗后在体外(图2 gTCGA队列和h)。分析表明,高CCL2表达式与减少在非小细胞肺癌患者生存显著相关(补充图S4a和b)。然而,基因coexpressed LUAD CCL2,白细胞介素6,并不与anlotinib-induced抗血管生成(补充图S4c-g)。因此,我们进行了一系列分析描述CCL2表达式在体外和在活的有机体内。CCL2水平在中明显减少曝光后非小细胞肺癌细胞系(NCI-H1975、NCI-H2228 A549, NCI-H1650和NCI-H2228) anlotinib (图2我和补充图S5)。CCL2水平和血清中肿瘤组织也显著减少后anlotinib管理局(图2 j和k)。根据这些观察结果,我们提出anlotinib-induced抗血管生成可能主要归因于减少CCL2内容。
Anlotinib抑制MMP9的表达在体外和在活的有机体内
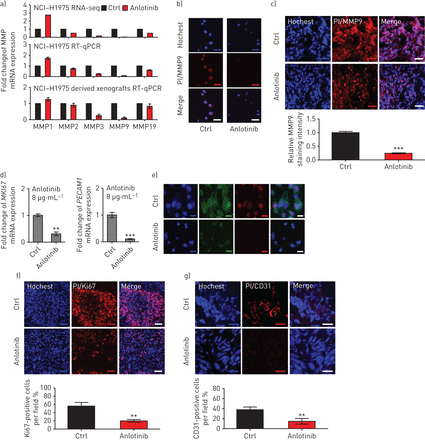
先前的研究已经报道,angiogenesis-related CCL2抑制蛋白表达的差别,对这些基因的信号通路在体外和在活的有机体内(20.,21]。在目前的研究中,我们发现,在基质金属蛋白(基质金属蛋白酶)(MMP3包括MMP1、MMP2, MMP9和MMP19), MMP9的mRNA表达几乎封锁anlotinib治疗后在体外和在活的有机体内(图3一)。此外,MMP9蛋白质anlotinib治疗后明显下降(图3 b和c)。因此,核扩散和vascularisation后被显著地抑制anlotinib管理局(图3 d- g)。因为高MMP9水平有助于肿瘤vascularisation [22),我们的研究结果表明,anlotinib-induced抗血管生成的抑制可能归因于CCL2-MMP9轴。
Anlotinib抑制NCI-H1975细胞衍生的血管生成在体外和在活的有机体内。基质金属蛋白酶(MMP)的mRNA表达anlotinib-treated(8µg·毫升−1)NCI-H1975细胞和anlotinib-treated·kg(2.25毫克−1)NCI-H1975-derived异种移植肿瘤。数据意味着±sd,n = 3。b)代表的图像MMP9-stained NCI-H1975细胞有或没有anlotinib(4µg·毫升−1)管理。放大10×;酒吧= 100µm规模。每组八个图像。c)代表的图像MMP9-stained NCI-H1975-derived异种移植后肿瘤组织anlotinib·kg(2.25毫克−1)治疗22天。每个动物三个视图的一个部分。数据意味着±sd每组,n = 9老鼠。放大20×;酒吧= 50µm规模。d) mRNA的表达MKI67和PECAM1评估使用逆转录酶定量PCR (RT-qPCR) anlotinib后(8µg·毫升−1)治疗在体外。数据意味着±sd,n = 3。e)代表CD31和Ki67的图像表达anlotinib-treated(2µg·毫升−1)NCI-H1975细胞。CD31贴上FITC(绿色)和Ki67贴上π(红色)。每组5个图片。酒吧= 25µm规模。代表图像f) Ki67-stained和g) CD31-stained NCI-H1975-derived异种移植后肿瘤组织anlotinib·kg(2.25毫克−1)治疗22天。每个动物三个视图的一个部分。数据意味着±sd每组,n = 9老鼠。放大10×f);酒吧= 100µm规模;g)放大20×;酒吧= 25µm规模。控制:控制。* *:p < 0.01;* * *:p < 0.001。
Anlotinib抑制血管生成通过CCL2-MMP9轴
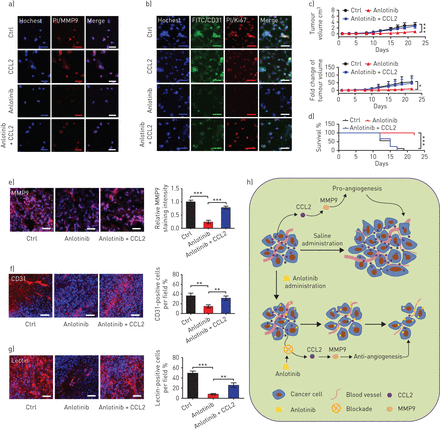
进一步了解CCL2在anlotinib-induced抗血管生成的作用,人类重组CCL2添加到anlotinib-treated NCI-H1975细胞或注入NCI-H1975-derived异种移植模型。我们发现外生CCL2大大抵消anlotinib-induced细胞毒性(包括诱导细胞凋亡、抑制细胞入侵细胞周期阻滞和抑制细胞迁移)在体外(补充图S6)。此外,我们评估的影响补充外源性CCL2 NCI-H1975 angiogenesis-related和扩散的蛋白质在体外,我们发现,外在CCL2明显恢复MMP9的表达水平,CD31和Ki67 (图4一和b)。
补充外源性CCL2恢复anlotinib-induced抗血管生成在体外和在活的有机体内。NCI-H1975细胞暴露于CCL2 ng(50毫升−1)和anlotinib(6µg·毫升−1),单独或一起,24 h。)代表表达基质金属蛋白酶9 (MMP)的图像。每组八个图像。酒吧= 20µm规模。b)代表CD31和Ki67的图像表达。CD31标签与异硫氰酸荧光素(FITC;绿色)与碘化propidium Ki67贴上(π;红色)。每组六个图像。酒吧= 100µm规模。 c) Measurement of subcutaneous tumour volumes of control (Ctrl), anlotinib (2.5 mg·kg−1)和anlotinib·kg(2.5毫克−1)+ CCL2(µg·5公斤−1,注射。隔日)。数据意味着±sd,n = 9。d)与Ctrl kaplan meier治疗组小鼠的生存曲线,anlotinib anlotinib + CCL2;n = 9。代表图像的e) MMP9-stained f) CD31-stained和g) lectin-stained NCI-H1975-derived异种移植肿瘤组织22天。每个动物三个视图的一个部分。数据意味着±sd每组,n = 9老鼠。放大20×;酒吧= 50µm规模。h) anlotinib抑制血管生成的示意图通过阻塞CCL2-MMP9轴。肿瘤细胞分泌CCL2到肿瘤微环境。然后促进neovascularisation CCL2激活MMP9表达式。政府在NCI-H1975 anlotinib块CCL2-MMP9轴细胞和NCI-H1975-derived异种移植,导致血管生成的抑制作用。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
为在活的有机体内评估,我们发现肿瘤体积和肿瘤体积显著增加的褶皱变化anlotinib-treated模型注射CCL2 (图4 c)。此外,存活时间急剧下降后CCL2管理局(图4 d)。与观测一致在体外,intratumoural MMP9表达明显恢复(图4 e)。重要的是,外在CCL2显著中和anlotinib-induced抗血管生成(图4 f和g)。这些结果表明,高CCL2水平不仅与vascularisation,还有助于抵消anlotinib-induced血管生成块。总的来说,这些结果表明,anlotinib抗血管生成效应通过的抑制CCL2-MMP9轴(图4 h),建议anlotinib-induced CCL2封锁可以与响应相关anlotinib难治性晚期非小细胞肺癌患者。
血清CCL2水平变化反映并预测在难治性晚期NSCLC患者anlotinib响应
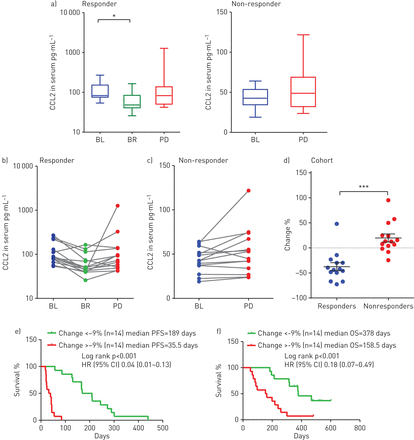
鉴于CCL2 anlotinib治疗的积极参与,我们接下来问CCL2水平是否可以用来预测anlotinib的响应。与anlotinib 28治疗非小细胞肺癌患者中,我们发现反应患者的血清CCL2水平(n = 14)显著降低在进步的疾病,最好的回应和增加13反应显示减少血清CCL2水平最好的回应。在nonresponders (n = 14)、血清CCL2水平进步疾病增加,11 nonresponders显示增加CCL2水平(图5一个- c)。此外,我们观察到反应者的血清CCL2水平明显高与nonresponders基线(补充图S7a)。kaplan meier分析表明血清CCL2水平基线预测潜在的肿瘤反应难治性晚期非小细胞肺癌患者治疗期间与anlotinib (补充图S7b和c)。
血清CCL2水平变化与无进展生存(PFS)和总生存期(OS)耐火材料先进nonsmall细胞性肺癌(NSCLC)患者anlotinib。与anlotinib治疗晚期非小细胞肺癌患者,血清CCL2在基线水平评估(提单),在最佳反应(BR)和进步的疾病(PD)。变质性模式的)CCL2 anlotinib-responsive和anlotinib-nonresponsive NSCLC患者。n = 14。b)在不同时间点血清CCL2水平anlotinib-responsive NSCLC患者(n = 14)。c)血清CCL2水平绘制在提单和PD anlotinib-nonresponsive NSCLC患者的时间点(n = 14)。d)百分比的变化在晚期非小细胞肺癌患者血清CCL2 anlotinib处理,从基线到2个月。数据意味着±sd,n = 14所示。e) kaplan meier PFS分层的情节CCL2水平变化与anlotinib治疗晚期非小细胞肺癌患者。n = 28;cut-off-high: 50%;削减off-low: 50%,中位数(95% CI) PFS 189(131 - 247)天与35.5(25-46)天。f) kaplan meier情节的OS分层CCL2水平变化与anlotinib治疗晚期非小细胞肺癌患者。n = 28;cut-off-high: 50%;削减off-low: 50%,中位数(95% CI) OS 378(306 - 451)天与158.5(110 - 243)天。*:p < 0.05;* * *:p < 0.001。
正如上面提到的,在非小细胞肺癌细胞株(图2 g我和补充图S5),NCI-H1975-derived异种移植模型(图2 j和k)和非小细胞肺癌患者(图5 b),我们观察到显著减少CCL2 anotinib治疗水平。除了血清CCL2水平基线,我们问CCL2水平的变化是否可以用来预测anlotinib响应。因此,我们调查了anlotinib治疗后血清CCL2水平的变化。令人惊讶的是,我们发现早期CCL2水平变化显然是与响应anlotinib (图5 d)。随后,我们使用一个值分界点评估anlotinib响应。PFS戏剧性地长在NSCLC患者早期血清CCL2水平的下降比那些早期增加(图5 e)。类似的结果观察队列操作系统分析时使用这个分层。与非小细胞肺癌患者增加CCL2水平anlotinib治疗后,患者的OS CCL2水平下降大大延长(图5 f)。
讨论
作为一种口服多目标TKI, anlotinib展览效果在各种癌症7,9- - - - - -12]。我们的临床证据表明anlotinib延长PFS和难治性晚期NSCLC患者的操作系统7,9,10]。虽然临床试验结果表明,anlotinib可能具有抗血管生成作用抑制疾病进展,潜在的分子机制尚不清楚。此外,传统的分层方法评估或预测反应的新抑制剂效率较低识别最好的救援人员从非小细胞肺癌患者。为了解决这些问题,我们在此试图理解anlotinib-induced抗血管生成效应的机制,确定一个生物标志物,可以用来屏幕anlotinib反应者。
标准治疗方案已经建议晚期NSCLC患者作为一线和二线药物。线和三线治疗难治性晚期NSCLC缺乏一个统一的标准,这被认为是一个棘手的问题为肺癌研究社区。最近,美国国家综合癌症网络提供了三线治疗方案,包括化疗和免疫治疗,对耐火材料先进的非小细胞肺癌(5]。然而,多目标TKIs仍然是值得追求的。我们发现anlotinib可以作为口服多目标TKI三线或三线治疗之外在难治性晚期非小细胞肺癌患者7,9,10]。生物标记中扮演重要角色为肺癌治疗药物开发。第一代TKIs LUAD病人窝藏EGFR突变提供极大的好处(删除或L858R 19日)(23,24]。晚期非小细胞肺癌患者窝藏50%积极PD1 / PDL1表达式或更高的肿瘤突变负担获得更多受益于检查站抑制剂(如pembrolizumab nivolumab和atezolizumab) (25- - - - - -27]。在这项研究中,我们发现LUAD病人窝藏司机gene-positive突变,尤其是病人窝藏EGFRT790M突变,获得更多受益于anlotinib疗法基于操作系统的分析而不是PFS分析。这一现象的根本原因可能是由于政府的第三代TKIs(比如AZD9291)或恢复对第一代TKIs敏感28,29日]。尽管激烈的努力已经对识别基于已知的分子生物标志物特征,仍然很难区分anlotinib救援人员从所有晚期非小细胞肺癌患者。
理解anlotinib的分子机制可以促进生物标志物识别。先前的研究已经表明,anlotinib选择性地抑制生长因子受体,包括VEGFR(1、2和3),PDGFR(α,β)和FGFR(1、2、3和4),其他(8- - - - - -10,13,14]。Anlotinib发挥其抗肿瘤作用在肿瘤细胞line-derived异种移植动物模型(8]。此外,anlotinib抑制肿瘤细胞生长的抑制c - kit, Ret, Aurora-B, c-FMS DDR1 [15- - - - - -17]。CCL2水平升高在肿瘤微环境或血液与肿瘤血管生成(22,30.,31日]。CCL2激活导致血管生成和转移的肺癌,乳腺癌和胰腺癌等(20.,21,32]。大多数肿瘤分泌CCL2, vascularisation pro-angiogenesis关键因子,刺激肿瘤和肿瘤生长和转移提供营养33,34]。在这里,我们观察到anlotinib抑制NCI-H1975细胞增殖通过CCL2封锁在体外和在活的有机体内。此外,anlotinib-induced肿瘤坏死是由于血管生成抑制通过阻断CCL2-MMP9轴在NCI-H1975-derived异种移植模型。
有价值的生物标志物有助于反应的预测新药(23- - - - - -27]。因此,确定一个合适的生物标志物对于区分反应者和nonresponders anlotinib迫在眉睫。这里,我们观察到在此CCL2血清水平的变化与应对anlotinib治疗晚期非小细胞肺癌。此外,我们报道,血清CCL2水平变化可以预测anlotinib急救员在难治性晚期非小细胞肺癌患者中,尽管血清CCL2水平基线可以用来预测anlotinib反应者在这个研究。然而,据报道,血浆CCL2水平不同种族、不同人群的年龄和吸烟35,36]。考虑anlotinib诱发CCL2水平的显著变化在非小细胞肺癌细胞株(图2 g我和补充图S5),NCI-H1975-derived异种移植模型(图2 j和k)和非小细胞肺癌患者(图5 b),我们发现CCL2水平的变化,而不是CCL2水平本身,可以更有效地预测anlotinib响应。应该执行和大规模前瞻性研究来评估其潜在的生物标志物anlotinib疗法。
结论
本研究不仅揭示了anlotinib-induced抗血管生成的重要分子机制通过CCL2-MMP9轴的抑制,但也提供了见解,血清CCL2水平可作为预测生物标记区分anlotinib救援人员从nonresponders难治性晚期非小细胞肺癌患者接受三线或三线治疗。
补充材料
确认
作者感谢病人的参与,调查人员对他们的支持。感谢王Xunqiang和魏史(Chia-tai专业制药有限公司、连云港、中国)为他们的帮助和支持。
脚注
在ClinicalTrials.gov alter - 0303试验注册标识号NCT02388919。
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:实验设计的构思和林丙辉汉,j . Lu L.M. Lu k·李和X.D.赵。临床试验是由林丙辉汉,k . Li h .钟T.Q.楚,X.Y.张J.Y.太阳和r . r . Li钟。临床前实验由j . Lu h .钟Y.Q.杨硕士阿拉姆,j .吴邦国委员长和X.W.李。临床分析、生物信息学分析和统计分析由j . Lu X.Y.张Y.Q.卢,J.L.徐陈怡如张X.D.赵和j·吴。手稿是由j . Lu和修订X.D.赵和林丙辉汉族。
利益冲突:陆j .没有披露。
利益冲突:h .钟没有披露。
利益冲突:楚没有披露。
利益冲突:x张没有披露。
利益冲突:r·李没有披露。
利益冲突:j .太阳没有披露。
利益冲突:r·钟没有披露。
利益冲突:y杨没有披露。
利益冲突:阿拉姆硕士没有披露。
利益冲突:y卢没有披露。
利益冲突:j .徐没有披露。
利益冲突:y张没有披露。
利益冲突:j .吴没有披露。
利益冲突:李x没有披露。
利益冲突:x赵没有披露。
利益冲突:k .李没有披露。
利益冲突:陆l .没有披露。
利益冲突:汉族没有披露。
支持声明:这项工作是由上海领先的人才项目(2013);该计划从上海交通大学系统生物医学创新中心(项目号15 zh4009);转化医学的关键程序从上海交通大学医学院(项目号15 zh1008);中国国家自然科学基金(项目号81673015);项目高峰高原的上海交通大学医学院——“研究医生”(项目号20161434);Chia-tai专业制药有限公司;和上海市科学技术委员会的项目(项目号16140902700)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年4月10日。
- 接受2018年11月29日。
- 版权©2019人队