摘要
表皮生长因子受体(EGFR)基因分型对于治疗指南至关重要,例如在肺腺癌中使用酪氨酸激酶抑制剂。传统的EGFR基因型鉴定需要活检和序列检测,这是侵入性的,可能会受到难以获取组织样本的影响。在这里,我们提出了一个深度学习模型,使用非侵入性计算机断层扫描(CT)预测肺腺癌中的EGFR突变状态。
我们回顾性收集了来自两家医院的844例肺腺癌患者的术前CT图像、EGFR突变和临床资料。提出了一种端到端的深度学习模型,通过CT扫描预测EGFR突变状态。
通过对14 926张CT图像进行训练,深度学习模型在两个主要队列(n=603;AUC 0.85, 95% CI 0.83-0.88)和独立验证队列(n=241;AUC 0.81, 95% CI 0.79-0.83),与以往使用手工制作的CT特征或临床特征的研究相比有显著改善(p<0.001)。深度学习评分在egfr突变型和egfr野生型肿瘤中显示出显著差异(p<0.001)。
由于CT常规用于肺癌诊断,深度学习模型为EGFR突变状态预测提供了一种无创且易于使用的方法。
摘要
深度学习为肺腺癌EGFR突变预测(AUC 0.81)提供了一种无创方法,较手工制作的CT特征或临床特征有显著改善http://ow.ly/LtDJ30nhc5Q
简介
肺腺癌是一种常见的组织学肺癌类型,表皮生长因子受体(EGFR)突变的发现彻底改变了其治疗方法[1,2].在一线治疗中,检测EGFR突变至关重要,因为EGFR酪氨酸激酶抑制剂可以靶向EGFR基因内的特定突变,并已导致改善EGFR突变肺腺癌患者的预后[3.,4].活检的突变测序已经成为EGFR突变检测的金标准。然而,由于肺肿瘤的广泛异质性,测量EGFR状态的活组织检查可能不得不定位组织区域。5,6].此外,活组织检查会增加癌症转移的潜在风险[7].此外,重复的肿瘤取样,难以获取组织样本,DNA质量差[8]以及相对较高的成本会限制突变测序的适用性[9].在这些情况下,需要一种非侵入性和易于使用的方法来预测EGFR突变状态。
计算机断层扫描(CT)作为癌症诊断的常规技术,提供了一种非侵入性的方法来分析肺癌[10- - - - - -12].最近的研究表明,从肺癌CT图像中提取的特征与基因表达模式有关[13- - - - - -16]并显示出对EGFR谱的预测能力[17- - - - - -19].虽然图像评估不能取代活检,但图像驱动的研究可以提供补充活检的额外信息[5,9].例如,CT成像提供了肿瘤及其微环境的完整范围,使我们能够通过考虑肿瘤内的异质性来预测EGFR突变状态。此外,通过CT成像预测egfr突变状态有助于我们在患者存在多个肿瘤时选择最可疑的肿瘤进行活检。此外,CT成像是非侵入性的,在整个治疗过程中很容易获得。
早期研究表明,CT语义特征和定量“放射学”特征对EGFR突变状态具有预测价值[9].然而,这些方法只能反映一般的图像特征,对EGFR突变缺乏特异性。此外,基于特征工程的放射组学方法依赖于精确的肿瘤边界注释,这需要人类的标记工作。由于放射学特征仅在肿瘤区域内计算,因此忽略了微环境和肿瘤附着组织。相比之下,先进的人工智能模型可以通过深度学习方法等自我学习策略来克服这些问题[20.- - - - - -22].得益于强大的特征学习能力,深度学习模型在皮肤癌分类中表现出了人类专家级别的表现[23]、眼病诊断[24]和预测非侵袭性肝纤维化[25].此外,深度学习模型在辅助肺癌分析方面表现良好[26- - - - - -29].与基于特征工程的放射组学方法相比,基于深度学习的放射组学不需要精确的肿瘤边界注释,可以从图像数据中自动学习特征[30.].此外,基于深度学习的放射组学可以提取适应特定临床结果的特征,而基于特征工程的放射组学只能描述可能缺乏结果预测特异性的一般特征。
在本研究中,我们提出了一个深度学习模型来挖掘与EGFR突变状态相关的CT图像信息。我们的方法是一种端到端管道,只需要在CT图像中手动选择肿瘤区域,不需要精确的肿瘤边界分割或人为定义的特征,这与基于特征工程的传统放射学方法不同。该模型可以自动从CT图像中学习EGFR突变相关特征,并预测肿瘤发生EGFR突变的概率。此外,深度学习模型可以发现与EGFR突变状态密切相关的可疑肿瘤子区域,旨在快速促进临床医生对患者的治疗决策。为了评估深度学习模型的性能,我们从两家独立医院(844名患者)收集了一个大型数据集,并提供了所提出的深度学习模型的独立验证结果。
材料与方法
病人
天津医科大学(天津,中国)和上海肺科医院(上海,中国)的机构审查委员会批准了这项回顾性研究,并放弃了获得患者知情同意的需要。符合以下纳入标准的患者被纳入本研究。1)组织学证实为原发性肺腺癌;2)对肿瘤标本进行病理检查,并证实有EGFR突变记录;3)术前CT增强资料。1)年龄、性别、分期等临床资料缺失,排除患者;2)术前治疗;或3)CT检查与后续手术间隔时间超过1个月。最后,两家医院的844例患者被用于本研究。我们根据医院将患者分为主要队列和独立验证队列。 The primary cohort included 603 patients from Shanghai Pulmonary Hospital between January 2013 and July 2014. The validation cohort included 241 patients from Tianjin Medical University between January 2013 and February 2014. The primary and validation cohorts were used for developing and validating the deep learning model, respectively. CT scanning parameters and detailed descriptions about the datasets are presented in the补充的方法.
关于分子特征,肿瘤标本是通过手术切除获得的。在四个酪氨酸激酶结构域(外显子18-21)上发现了EGFR突变,这些结构域在肺癌中经常发生突变。突变状态是通过一种扩增难解突变系统和人EGFR基因突变检测试剂盒(北京ACCB生物技术有限公司,北京,中国)来确定的。如果检测到任何外显子突变,则确定肿瘤为egfr突变;否则,肿瘤被鉴定为egfr野生型。因此,在本研究中,我们专注于预测肺腺癌患者的这些二元结局(egfr -突变型和egfr -野生型)。
深度学习模型的开发
深度学习是一种层次神经网络,旨在学习原始数据到所需标签之间的抽象映射。将深度学习模型中的计算单元定义为层,并将其集成以模拟人脑的分析过程。主要的计算公式是卷积,池化,激活和批量归一化。在建立深度学习模型的计算过程的术语定义在补充的方法.
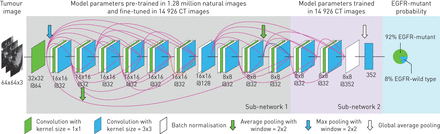
图1图示EGFR突变状态预测的管道。为了应用深度学习模型,根据以下规则(由J. Shi和Y. Liu)手动选择包含整个肿瘤的立方感兴趣区域(ROI): ROI应包括完整的肿瘤区域,包括肿瘤的边缘。这个规则在实践中很容易使用,因为我们不需要肿瘤精确地位于ROI的中心(补充图S1说明了用户选择的几个roi)。然后在每个CT切片中通过三阶样条插值将ROI调整为64×64像素,并输入深度学习模型。通过卷积层和池化层的顺序激活,深度学习模型给出了图像的egfr突变概率。为了做出可靠的预测,所有肿瘤的CT切片都被输入到深度学习模型中,平均概率被视为肿瘤的egfr突变概率。具体来说,所有相邻的三个CT切片被组合成一个三通道图像,并被输入到深度学习模型中进行预测(补充图S2).
深度学习模型的说明。该模型由内核大小为3×3和1×1的卷积层、批处理规范化层和池化层组成。子网络1与DenseNet的前20层共享相同的结构[31],它使用128万张自然图像进行了预训练。在表皮生长因子受体(EGFR)突变数据集中训练子网络2,旨在捕获图像特征与EGFR突变标签之间的关联。当我们将肿瘤输入深度学习模型时,它可以预测肿瘤发生egfr突变的概率。CT:计算机断层扫描。
在模型训练中,我们使用迁移学习来训练前20个卷积层(子网络1 in图1),由取自ImageNet数据集的128万幅自然图像[31].这种迁移学习技术由于扩大了训练数据,在疾病诊断中表现出了很好的效果[23,32].然后,最后四个卷积层(子网络2在图1)使用来自肺腺癌肿瘤的14926张CT图像进行训练。中给出了构建模型的详细信息补充的方法.
对于肿瘤的CT图像,深度学习模型无需任何预处理或后处理或图像分割,直接预测肿瘤发生egfr突变的概率。使用本研究的主要队列生成的深度学习模型可在http://radiomics.net.cn/post/110.来自验证队列的部分CT图像可以下载作为测试深度学习模型的示例。
深度学习模型的可视化
由于深度学习的端到端方式,深度学习模型的推理过程对于用户来说并不直观。为了进一步理解深度学习模型的预测过程,我们使用可视化技术来分析模型学习到的特征。深度学习模型中最重要的组成部分是卷积层。因此,我们从两个角度对卷积层进行可视化,以理解深度学习模型的推理过程:1)对卷积层提取的特征模式进行可视化;2)可视化每个卷积层对不同肿瘤的反应。
卷积层由多个卷积滤波器组成,每个卷积滤波器提取不同的特征。通过过滤器可视化算法[33,34],我们可以将卷积滤波器提取的特征模式可视化,并将此特征模式定义为深度学习特征(补充的方法).
为了进一步探索深度学习特征的意义,我们观察了每个卷积滤波器对不同肿瘤的响应。给定一张肿瘤图像,深度学习模型中的每个卷积滤波器都会生成一个响应图,指示肿瘤中相应的特征模式。响应映射的平均值被定义为响应值。一个好的卷积滤波器应该在egfr突变型和egfr野生型肿瘤之间有不同的响应值。因此,可视化卷积滤波器在不同肿瘤组中的响应值可以帮助我们评估卷积滤波器的性能。
统计分析
使用SPSS Statistics 21 (IBM, Armonk, NY, USA)进行统计分析。采用独立样本t检验评估egfr突变型组与egfr野生型组患者年龄平均值的显著性。同样的统计分析用于评估egfr突变组和egfr野生型组之间深度学习评分的差异。采用卡方检验评价各组性别、肿瘤分期等分类变量的差异。此外,我们使用DeLong检验来评估不同模型之间受试者工作特征(ROC)曲线的差异。p值<0.05为显著。我们的深度学习模型的实现使用了Keras工具包和Python 2.7 (Python软件基金会;www.python.org/).
结果
患者临床特点
患者的临床特点表1.在年龄和性别方面,主要队列和验证队列之间无显著差异(年龄p=0.083,性别p=0.321)。两组患者的肿瘤分期在统计学上存在差异,这可能是由于地区差异,因为两组患者来自中国两个不同的城市。为了消除这种差异,我们在两个队列中进行了分层分析,以验证深度学习模型的鲁棒性。egfr突变型与egfr野生型患者的年龄、性别、分期等临床特征差异较大;因此,我们利用这些特征来构建临床模型,与深度学习模型进行比较。
深度学习模型的诊断验证
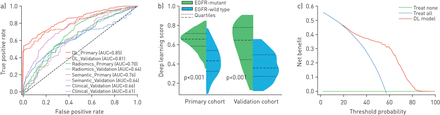
表2列出了深度学习模型的预测性能,其中我们使用了ROC曲线下面积(AUC)、准确度、灵敏度和特异性作为主要测量指标。在我们的研究中,所有的结果都用于肿瘤水平的预测,这相当于反映了受试者水平的评估,因为每位患者只有一个肿瘤。在主要队列中,通过五倍交叉验证,深度学习模型显示出良好的预测性能(AUC 0.85, 95% CI 0.83-0.88)。在独立验证队列中进一步证实了这一性能(AUC 0.81, 95% CI 0.79-0.83)。主要队列和验证队列之间的紧密AUC表明,深度学习模型在预测未见过的新患者的EGFR突变状态方面具有良好的泛化性。得益于128万张自然图像的迁移学习,深度学习模型没有出现过拟合问题。两个队列中深度学习模型的ROC曲线见图2一个.此外,深度学习评分显示,在两个队列中,egfr突变组和egfr野生型组之间存在显著差异(在主要队列和验证队列中p<0.001;图2 b).
深度学习模型的预测性能。a)初级/验证队列中深度学习(DL)模型、放射组学模型、语义模型和临床模型的受试者工作特征曲线。b)主要队列和验证队列中表皮生长因子受体(EGFR)突变组和EGFR野生型组之间的DL评分。c) DL模型决策曲线。绿线表示将所有患者治疗为egfr野生型的获益,蓝线表示将所有患者治疗为egfr突变型的获益。红线显示了使用DL模型的好处。
此外,我们进行了分层分析,以验证深度学习模型对肿瘤分期的诊断性能。补充表S1和补充图S3说明深度学习模型在肿瘤的各个阶段都取得了良好的效果。此外,无论肿瘤分期如何,深度学习评分在egfr突变组和egfr野生型组之间显示出显著差异。
图2 c绘制深度学习模型的决策曲线。这条曲线表明,如果患者或医生的阈值概率为>10%,使用深度学习模型预测肺腺癌中的EGFR突变状态比治疗所有患者方案或不治疗方案都能获得更多益处[35].这突出了深度学习模型的临床应用。
深度学习模型与其他方法的比较
在早期研究中,临床特征、语义特征[17,36]和定量“辐射”特征[9]用于EGFR突变状态预测。因此,我们建立了一个临床模型、一个语义模型和一个放射组学模型,与所提出的深度学习模型进行比较。临床模型以性别、分期、年龄为特征,采用半径基核支持向量机(SVM)预测EGFR突变。语义模型使用了之前研究中报告的16个语义特征和多元逻辑回归(详细信息见补充方法和补充表S4) [17].放射组学模型通过PyRadiomics工具包提取了1108个特征[37],采用递归特征消除(RFE)方法选择了8个特征。最后,在辐射组学模型中建立包含100棵树的随机森林用于EGFR突变预测。
的量化表现表2ROC曲线图2一个表明,深度学习模型优于临床模型,差异具有显著性(AUC 0.66, 95% CI 0.62-0.70, p<0.0001;AUC为0.61,95% CI为0.58-0.64,p<0.0001)。此外,在两个队列中观察到语义模型的显著改善(主要队列的AUC为0.76,95% CI为0.72-0.80,p<0.0001;AUC 0.64,验证队列95% CI 0.61-0.67, p<0.0001)。放射组学模型的相似改善在两个队列中得到证实(主要队列的AUC为0.70,95% CI为0.66-0.74,p<0.0001;AUC 0.64,验证队列95% CI 0.61-0.67, p=0.0002)。
发现可疑肿瘤区域
由于深度学习是一种端到端的预测模型,它直接学习肿瘤图像和EGFR突变状态之间的抽象映射,因此解释预测过程非常重要,这样我们就可以估计预测的可靠性。我们使用了一种深度学习可视化方法[33,34]以找出与EGFR突变状态最相关的肿瘤区域(补充的方法).这一重要区域在我们的研究中被定义为可疑区域。当深度学习模型预测EGFR突变状态时,它会告诉临床医生哪个区域同时引起模型的注意。
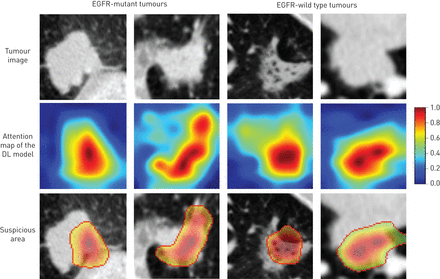
图3描述深度学习模型发现的可疑区域。对于肺腺癌肿瘤,深度学习模型生成了一个注意图,表明肿瘤中每个部分的重要性;我们以0.5为临界值,保留高反应区(可疑肿瘤区)。这些区域比肿瘤的其他区域更重要,因为它们引起了深度学习模型的注意。如下面一行所示图3,深度学习模型发现的可疑区域在不同肿瘤中有所不同。例如,可疑区域图3一是否肿瘤与胸膜之间的组织,而可疑区域在图3 b是肿瘤边缘。基于这些观察,深度学习模型将这两种肿瘤解释为egfr突变。相比之下,深度学习模型关注的是脑洞区图3 c并预测为egfr野生型。由于深度学习模型只需要肿瘤原始CT图像作为输入,不需要任何肿瘤分割,因此可以将一些正常组织输入模型。然而,该模型能够发现肿瘤内部的可疑区域,而不是被正常组织干扰。图3 d图示纵隔附近的肿瘤。在这种情况下,深度学习模型的ROI包括肿瘤外的一些正常组织。然而,深度学习模型在肿瘤内部发现了一个可疑区域,而不是正常组织。通过深度学习模型推断可疑肿瘤区域与EGFR突变状态密切相关。因此,它可以潜在地为临床医生提供一个活检位置,以避免因肿瘤内异质性引起的假阴性诊断。可疑肿瘤区域与其他肿瘤区域的差异可通过结合正电子发射断层扫描- ct数据进一步解释。
发现可疑肿瘤区域。根据深度学习(DL)模型的注意图,我们使用0.5作为分界值来获取可疑区域。EGFR:表皮生长因子受体。
深度学习特征分析
深度学习的优势主要来自于它的自动特征学习能力。通过从14 926张肿瘤图像中学习,深度学习模型检测出与EGFR突变状态密切相关的特征。
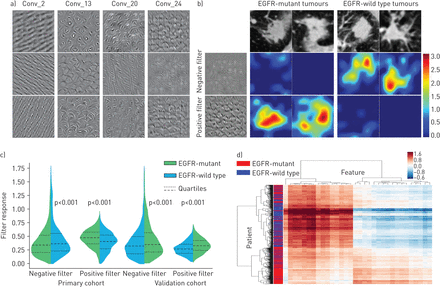
为了更好地理解深度学习特性,我们可视化了深度学习模型中的几个卷积滤波器(图4一).浅卷积层学习低层次的简单特征,如水平边和对角线边(Conv_2)。更深的卷积层学习更复杂的特征,如肿瘤形状。例如,Conv_13层中的过滤器对圆形或拱形形状有强烈的反应,因为大多数肿瘤包含圆形或拱形结构。随着深入,特征变得更加抽象,并逐渐与EGFR突变状态相关(Conv_20, Conv_24)。在补充图S4,我们比较了转移学习(在CT数据中训练)之前和之后的卷积滤波器。这个图表明卷积滤波器学习了不同的特征模式,这些特征模式与初始状态不同。此外,迁移学习使得过滤器更特定于CT数据,特别是在更深的网络层。
深度学习特征分析。a)卷积滤波器(Conv_)来自深度学习模型的第2层、第13层、第20层和第24层。每个卷积层包括数百个过滤器,每层中只说明了前三个过滤器。b)阴性过滤器和阳性过滤器在表皮生长因子受体(EGFR)突变/野生型肿瘤中的反应。阳性过滤器对egfr突变型肿瘤有强烈反应,阴性过滤器对egfr野生型肿瘤有强烈反应。所有肿瘤图像均来自验证队列。c)两组正、负滤波器的响应值。d)纵轴为肺腺癌患者(n=844)的无监督聚类,横轴为深度学习特征表达(特征维数=32,Conv_24层)。
为了进一步证明深度学习特征与EGFR突变状态之间的关联,我们从最后一个卷积层中提取了两个卷积滤波器(正滤波器和负滤波器)。这两个过滤器捕获了不同的纹理模式(在图4 b)对egfr突变型和egfr野生型肿瘤有反应。当我们将egfr野生型肿瘤注入深度学习模型时,负过滤器产生了强烈的反应,而正过滤器几乎被关闭。类似地,当我们将egfr突变肿瘤喂给深度学习模型时,阴性过滤器被抑制,但阳性过滤器被强烈激活。如所述图4 c,阳性/阴性过滤器对egfr突变型和egfr野生型肿瘤的反应在所有队列中有显著差异(p<0.001)。在图4 d,说明了整个数据集(844个患者)中来自最后一个卷积层(Conv_24)的深度学习特征的聚类图。深度学习特征表现出明显的聚类,对egfr突变型和egfr野生型患者有不同的反应。同时,可以大致分离不同EGFR突变状态(EGFR-突变型/-野生型)的肿瘤(纵轴为图4 d).
为了比较深度学习特征和辐射特征的重要性,我们将来自Conv_24层的32个深度学习特征与1108个辐射特征结合起来,并使用RFE选择重要特征。在这一步中,RFE使用线性支持向量机和五重交叉验证,使用主队列确定最优特征量,这与建立辐射组学模型时的RFE设置一致。最后选取了11个特征,包括8个深度学习特征和3个辐射特征。这表明,深度学习特征与EGFR突变状态的相关性比辐射特征更强。此外,我们计算了所有深度学习特征和辐射特征的单变量AUC。如补充图S5,许多深度学习特征具有比辐射特征更高的auc。
讨论
在本研究中,我们提出了一种使用无创CT图像预测肺腺癌患者EGFR突变状态的深度学习模型。我们在来自主要队列(603例患者)的14926张CT图像中训练深度学习模型,并在来自另一家医院(241例患者)的独立验证队列中验证其性能。深度学习模型在主要队列中显示出令人鼓舞的结果(AUC 0.85, 95% CI 0.83-0.88),在独立验证队列中表现良好(AUC 0.81, 95% CI 0.79-0.83)。深度学习模型显示,高维CT图像特征与EGFR基因型之间存在显著相关性。我们的分析提供了一种非侵入性评估患者EGFR信息的替代方法,并为活检提供了很好的补充。同时,我们的模型可以发现主导EGFR突变状态预测的可疑肿瘤区域。该分析为临床医生了解CT数据的预测结果提供了直观的解释。此外,深度学习模型只需要原始肿瘤图像作为输入,直接预测EGFR突变状态,无需进一步的人工辅助,易于使用,速度非常快。
以往的研究采用临床因素[8]和基于特征工程的放射组学[9,17,18]来预测EGFR突变状态。例如,使用年龄、性别、肿瘤分期和主要亚型等临床因素构建EGFR突变状态预测的nomogram [8].在本研究中,在包括464名亚洲患者的验证队列中,临床因素达到AUC 0.64。临床模型是可解释的,因为临床因素被广泛使用,nomogram代表了一个直观的线性模型。但是,分期、主要亚型等临床特征需要进行有创活检。此外,临床特征仅能在病理层面反映少量肿瘤信息。相比之下,放射组学方法利用CT图像在宏观层面量化肿瘤信息,建立肿瘤图像与EGFR突变状态之间的关系。与临床因素相比,放射组学分析提供了定量特征,可以挖掘EGFR基因型相关的高维信息。在包括353例患者的队列中,通过使用手工制作的CT图像特征,放射组学方法达到AUC 0.69 [9].尽管放射组学方法具有优势,但手工制作的特征需要耗时的肿瘤边界分割,并且可能对EGFR基因型缺乏特异性。因此,我们提出了一种深度学习方法来自动学习egfr相关肿瘤特征,避免复杂的肿瘤边界分割。此外,深度学习方法只需要用户定义肿瘤的ROI,而不是基于特征工程的放射组学中的四个复杂步骤(肿瘤边界分割、特征提取、特征选择和模型构建)。
深度学习的优势
之前的研究表明,基于ct的语义特征[18,19]和定量放射特征[9,17]反映了EGFR突变状态。但它们只能反映低阶视觉特征或简单的高阶特征。有一些抽象的特征可能与EGFR突变状态有关;然而,它们很难用手工制作的特征工程来表示。在这些情况下,深度学习显示出它的优势,因为它可以挖掘难以形式化但对识别EGFR突变状态很重要的抽象特征。
与之前报道的手工制作特征相比,深度学习模型具有以下优势。1)深度学习模型通过层次神经网络结构,从视觉特征中提取多层次特征,形成与EGFR信息直接相关的抽象映射;2)深度学习模型不需要耗时的肿瘤边界标注,这是手工特征工程的一大优势。此外,肿瘤的微环境以及肿瘤与附着组织之间的关系(胸膜牵引,等.)在深度学习模型中被考虑;3)深度学习模型快速易用,只需原始CT图像作为输入,直接预测EGFR突变状态,无需人工进一步输入。
深度学习模型的临床应用
深度学习模型从以下几个方面提供了潜在的临床应用。1)本文提出的深度学习模型提供了一种无创预测EGFR突变状态的方法,可方便地用于常规CT诊断。2)如果肿瘤的活检结果显示EGFR-wild型,由于肿瘤内部的异质性,结果可能包括假阴性。此时,深度学习模型可以被视为另一种验证工具。如果深度学习模型预测肿瘤是egfr突变,临床医生可能需要重新活检组织[38].3)深度学习模型只需要常规使用的CT图像,不增加成本。因此,该模型可在整个治疗过程中多次使用[9].4)最重要的是,尽管我们只研究了腺癌,但深度学习模型在其他组织学类型中也具有预测价值。这使得深度学习模型可以直接用于肺癌的CT扫描,而无需识别组织学类型。为了验证这一假设,我们在2013年1月至2014年7月期间在上海肺科医院收集了125例其他组织学类型的肺癌患者补充表S2).定量结果补充表S3表明深度学习模型在其他组织学类型肺癌中的AUC可达0.77 (95% CI 0.73-0.81)。因此,即使不知道肺癌的组织学类型,深度学习模型也可以在腺癌中达到AUC 0.81,在其他组织学类型中达到AUC 0.77。
尽管深度学习模型的表现令人鼓舞,但这项研究有几个局限性。首先,我们只检查了亚洲人群中的患者。然而,EGFR突变率会受到种族的影响。在未来的工作中,将需要来自多个来源的人群来测试深度学习模型是否可以推广到其他人群。其次,尽管深度学习模型表现出比临床、语义和放射组学模型更好的性能,但这些模型的组合尚不清楚。如果将这些模型结合在一起,预测性能可能会得到提高。第三,我们的研究只关注EGFR突变状态。EGFR突变与其他基因突变的关系(如。ROS-1, ALK)可以在未来的工作中进行探索。
补充材料
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:Dong D., Shi J., Liu Y., Z. Ye收集临床数据。刘震、王凯、朱毅对数据进行了处理和分析。H. Zhou提供了统计分析。S. Wang, D. Yu和M. Zhou构建了深度学习模型并撰写了文章。O. Gevaert和J. Tian构思了这个项目并编辑了文章。
利益冲突:S. Wang没有什么可透露的。
利益冲突:J. Shi没有什么可透露的。
利益冲突:Z. Ye没有什么可透露的。
利益冲突:董没有什么可透露的。
利益冲突:D. Yu没有什么可透露的。
利益冲突:周先生没有什么可透露的。
利益冲突:刘宇军没有什么可透露的。
利益冲突:O. Gevaert没有什么可透露的。
利益冲突:王凯没有什么可透露的。
利益冲突:朱洋没有什么可透露的。
利益冲突:周鸿祎没有什么可透露的。
利益冲突:Z. Liu没有什么可透露的。
利益冲突:J. Tian没有什么可透露的。
支持声明:国家重点研发计划项目(2017YFA0205200, 2017YFC1308700, 2017YFC1309100, 2016YFC010380),国家自然科学基金(81227901,81771924,81501616,61231004,81671851,81527805),北京市科委(Z171100000117023, Z161100002616022),北京市自然科学基金(L182061),中国科学院国际合作局(173211KYSB20160053),中国科学院仪器研制项目(YZ201502)、中国科学院青年创新促进会项目(2017175)。O. Gevaert由美国国立卫生研究院国家生物医学成像和生物工程研究所资助,资助编号为R01EB020527。本文的资助信息已存入交叉参考基金注册.
- 收到了2018年5月30日。
- 接受2018年12月31日。
- 版权所有©ERS 2019
本版本根据知识共享署名非商业许可4.0的条款发布。