文摘
表皮生长因子受体(表皮生长因子受体)肿瘤基因分型指导治疗决策是至关重要的关于使用表皮生长因子受体酪氨酸激酶抑制剂在nonsmall细胞性肺癌(NSCLC)。然而,一些患者可能无法获得肿瘤测试,因为组织是有限的和/或不定期提供测试。在这里,我们旨在建立一个基于模型的计算图表,以便预测的存在表皮生长因子受体突变在非小细胞肺癌。
我们回顾性收集与非小细胞肺癌患者的临床和病理数据在3006年的肿瘤基因分型表皮生长因子受体5点突变全球机构。感兴趣的变量被集成在一个多元逻辑回归模型。
在2392年的非亚洲患者肺腺癌,窝藏的最重要的预测因子表皮生长因子受体突变是:降低吸烟暴露(或0.41,95%可信区间0.37 - -0.46),戒烟和诊断时间间隔(或2.19,95%可信区间1.71 - -2.80),高级阶段(或1.58,95%可信区间1.18 - -2.13),和乳头状(或4.57,95% CI 3.14 - -6.66)或支气管肺泡(-4.06或2.84,95% CI 1.98)组织学检查主要亚型。建立了计算图表,显示良好的识别精度:一致性指数在一个独立的验证数据集是0.84。
临床实践过渡到基因分型结果将作为日常保健的一部分,这个列线图可以是非常有用的预测的存在表皮生长因子受体突变在非亚洲患者的肺腺癌突变分析或可能不可用。
Nonsmall细胞性肺癌(NSCLC)是全球最常见的癌症相关死因,占>每年100万人死亡(1]。非小细胞肺癌主要是由三种不同的类型:鳞状细胞癌,大细胞癌和腺癌。腺癌现在由> 50%的肺癌病例在美国和西欧(2,3]。
体细胞突变的表皮生长因子受体(表皮生长因子受体)基因存在于肺腺癌的一个子集。生物数据有关表皮生长因子受体突变已经广泛地查阅其他地方(4]。简单地说,表皮生长因子受体突变主要发生在酪氨酸激酶域,主要涉及删除外显子19和复发点突变(L858R) 21外显子(5,6]。这些突变导致本构激活受体,独立于配体结合,增加对特定的表皮生长因子受体酪氨酸激酶抑制剂的敏感性(TKIs)吉非替尼和埃罗替尼5]。临床上,响应率这些药物在肿瘤窝藏> 70%表皮生长因子受体激活突变(7- - - - - -9]。最近的随机III期试验(艾瑞莎泛亚研究(IPASS)、西日本胸肿瘤组织3405年和日本东北部研究小组)发现,患者表皮生长因子受体突变的肿瘤,一线吉非替尼会导致更长的无进展生存与标准以铂为基础的化疗紧身上衣(7- - - - - -9]。因此,基因分型的表皮生长因子受体指导治疗决策是至关重要的关于使用EGFR TKIs和正在成为一个标准推荐的预处理检查肺腺癌患者(10- - - - - -12]。
不幸的是,在许多国家,常规获得突变检测一直受限于缺乏完善的分子诊断实验室或经济和/或监管问题。例如,从2008年到2009年,只有16%和11%的转移性腺癌病例的基因表皮生长因子受体分别在法国和西班牙激活突变。此外,许多转移性非小细胞肺癌患者被诊断为针活检,组织用于变异测试的限制。IPASS,只有66%的患者的肿瘤标本收集表皮生长因子受体突变状态可能最终只有64%的情况下进行评估(7]。在这些设置,准确预测工具的价值的存在表皮生长因子受体突变患者的肿瘤,基于临床特点,是毋庸置疑的。
统计预测模型被广泛用于癌症的结果预测。其中,计算图表创建用户友好的图形化表达复杂的模型来生成一个事件的概率根据每个病人的个人简介(13]。在这里,我们从大集成多个临床和病理因素,好的注释国际群基因分型肺肿瘤发展多元逻辑回归模型和一个关联的诺模图预测的存在表皮生长因子受体激活突变。
患者和方法
病人
我们回顾性收集与非小细胞肺癌患者的临床和病理数据3006,其中包括2856与腺癌的肿瘤基因分型表皮生长因子受体激活突变在全球五个机构:1990腺癌患者从纪念斯隆-凯特琳癌症中心(MSKCC)(美国纽约);297人从丹娜-法伯癌症研究所(DFCI)(美国波士顿);269年来自马萨诸塞州总医院癌症中心(MGH)(波士顿,MA);213年复旦大学肿瘤医院的(CHFU)(中国上海);和87年的国立台湾大学医院(台大医院)(台北,台湾)14]。医院流行病学研究所(CIO)(德国人我Pujol三叠系,巴达洛纳,西班牙)也造成217名患者(198腺癌)的数据没有包含在最终的分析,因为缺少关键变量的数据,如吸烟史。
在台大医院从2004年开始,DFCI, MGH MSKCC, CIO, 2005和2007年在CHFU,表皮生长因子受体基因分型是对所有连续执行系统性和前瞻性,正常值或腺癌肿瘤经病理组织切片证实可用的材料测试,没有任何选择基于额外的临床或病理条件。因此,病人在我们的分析中是代表所有病人治疗五个机构包括在内。
数据收集2009年7月在当地机构审查委员会(IRB)批准的协议。本研究通过IRB每个机构。
突变分析
对于这一分析,我们认为只有非耐表皮生长因子受体激活突变,即。对EGFR激酶结构域突变与敏感TKIs:外显子19删除,21外显子突变(即。L858R)和其他点突变(G719A / C / S和L861Q)。其他肿瘤窝藏表皮生长因子受体突变被排除在外。直接测序的标准方法表皮生长因子受体基因分型(第18 - 21外显子)在DFCI, MGH, CIO, CHFU和台大医院。在MSKCC,表皮生长因子受体突变分析使用直接测序和pcr检测两种最常见的突变特异化验表皮生长因子受体突变,即。外显子19删除和L858R点突变(15]。我们也检索喀斯特非小细胞肺癌肿瘤的突变状态,如果可用。喀斯特突变是评估使用直接测序(16]。
临床和病理数据
临床和病理感兴趣的变量包括:年龄、性别、种族/民族,组织学类型(腺癌、鳞状细胞癌和大细胞癌),腺癌肿瘤,组织学上主要的亚型(17),肿瘤阶段根据美国癌症联合委员会6日TNM(肿瘤、转移和节点)系统标准时间(生成的数据18变量),和吸烟(吸烟状态,吸烟对吸烟者和数量(以pack-yrs)前吸烟者戒烟以来时间间隔)。病人被归类为不吸烟者(< 100一生香烟),前吸烟者(诊断之前退出> 1年)或吸烟者(诊断后1年内继续吸烟)。病理检查在每个执行机构。我们也从常规免疫组织化学研究检索结果与抗体对甲状腺转录因子1 (TTF),终端呼吸单元腺癌的一个标志,它更有可能港口表皮生长因子受体突变(19]。然而,由于缺乏数据,我们可以不包括这决赛中协变量模型。
统计分析
分析诊断为非小细胞肺癌病人进行腺癌,分别对非亚洲和亚洲病人,导致一个模型的两个群体。卡方和两个示例配对t用于比较的临床参数和存在的单变量之间的联系表皮生长因子受体或喀斯特突变,分别为分类和连续变量。方法用于开发预测列线图以前描述(13,20.]。短暂,我们对于每个模型,随机分为病人诊断为肺腺癌的可用数据为训练集(包括三分之二的患者),用于开发一个预测模型,验证集(包括剩下的三分之一)。模型的运动进行开发多元逻辑回归模型,使用可用的临床和病理因素预测的可能性表皮生长因子受体突变。所有变量都是单变量联系在一起表皮生长因子受体地位的水平α< 0.2是包含在多变量模型中,并保留在模型中,如果他们继续显著相关的结果。这些变量与一个明显偏态分布对数转换;连续的线性假设进一步检查和序数变量,如果与结果的关系的函数形式的建议,他们用二次多项式模型。分类变量的水平组合,如果他们有类似的效果。所有组合的两个变量之间的相互作用进行了测试,但不包括在最终的模型,因为他们的影响没有达到显著性水准的α< 0.05,将它们添加到模型没有提高模型的预测精度,> 1%。
的歧视性的能力模型量化使用一致性指数,即数值相当于接受者操作特征曲线下的面积。一致性指数表示的概率,在一对随机选择一个病人,另一个病人没有表皮生长因子受体突变,突变的模型是否正确预测更高的概率第一个病人。在实践中,一致性指数范围从0.5(无歧视性的能力,相当于一个抛硬币)到1.0(完美的歧视)21]。
校准是评估通过绘制物流预测的概率模型与实际的概率。自个人实际概率是1或0(对患者和没有表皮生长因子受体分别为突变),标定块建成使用本地回归,一种常用的数据平滑,依靠近似每个数据点与低度使用邻近值多项式。阴谋在45°线将对应于一个模型的预测概率一致,实际的概率,因此表明完美的校准。歧视和校准的预测模型计算独立验证数据集。
来防止初始随机分割的影响,分析了重复10随机分割训练和验证数据集,使用10倍交叉验证,改装模型忽略十分之一的观测获得预测省略第十。使用SAS 9.2版本进行了统计计算(SAS研究所Inc .卡里,数控,美国),和设计和locfit包R (R统计计算的基础,维也纳,奥地利)。
结果
表皮生长因子受体肺腺癌的非亚洲患者的突变
人口特征
我们我们的分析集中在最大的人口群体,即非亚洲患者(包括白人和黑人,西班牙裔和非西班牙裔),肺腺癌。最大化的机会建立一个有效的模型,我们只包括吸烟情况下的所有变量(n = 2392)。1579名(66%)患者被随机纳入一个训练数据集,剩下的813名(34%)患者形成一个验证数据集。人口、患者的临床和病理特点提出了表1。总的来说,604例(25%)肿瘤包庇表皮生长因子受体激活突变,对应于外显子19删除在54%的情况下,L858R替换在37%的情况下。
患者表皮生长因子受体突变的肿瘤更容易被女性(72%与62%的患者;p < 0.001)和被诊断出患有晚期疾病(55%与45%;与患者相比p < 0.001)表皮生长因子受体野生型肿瘤。两组之间没有显著性差异对年龄(64±12与65±11岁;p = 0.370)或种族/民族(两组94%的患者是白人)。55%的患者表皮生长因子受体突变的肿瘤是不吸烟者,相比之下,19%的表皮生长因子受体野生型肿瘤(p < 0.001)。前吸烟者戒烟以来平均时间间隔是27岁之间表皮生长因子受体突变和20岁之间表皮生长因子受体野生型患者。
肿瘤与表皮生长因子受体突变更容易港口乳头状(30%与12%的患者;p < 0.001)和支气管肺泡主要组织学亚型(25%与17%;p < 0.001),表现出腺泡的(18%的可能性较小与39%;p < 0.001)或固体架构(9%与14%;p = 0.002)。TTF-1表达更频繁表皮生长因子受体突变的肿瘤(97%与检测肿瘤的84%;p < 0.001)。组织学亚型不是另有规定(NOS)或无法评估腺癌的18%,因为诊断是在小型肿瘤组织样本(NOS病例的22%)或细胞学标本(NOS病例的78%)。
预测列线图
多变量模型预测结果的概率表皮生长因子受体突变在非亚洲肺腺癌患者中给出表2。窝藏的最重要的预测因子表皮生长因子受体激活突变是:吸烟史,以降低总吸烟暴露(对数转换pack-yrs;或0.41,95% CI 0.37 - -0.46)和时间间隔烟草戒烟和非小细胞肺癌诊断(或2.19,95%可信区间1.71 - -2.80);在诊断晚期(或1.58,95% CI 1.18 - -2.13),和乳头状(或4.57,95% CI 3.14 - -6.66)或支气管肺泡(-4.06或2.84,95% CI 1.98)主要亚型。这些预测不是不同L858R突变和外显子19删除。
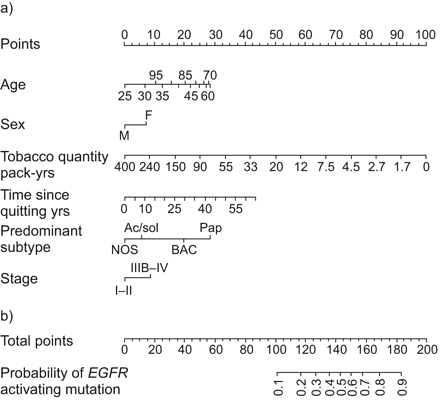
基于这种分析,我们生成的预测存在激活的诺模图表皮生长因子受体肿瘤的突变(图1)。独立的验证数据集的一致性指数计算为0.84 (95% CI 0.80 - -0.86),表明优秀的识别精度表皮生长因子受体突变体与表皮生长因子受体野生型病例组患者。此外,标定图(图2)表明,nomogram-predicted概率将很好地与实际的概率。此外,额外的内部验证表明之间没有改变原来的和谐指数,基于10倍交叉验证。
列线图包括临床和病理变量预测的表皮生长因子受体(表皮生长因子受体)从非亚洲激活突变腺癌患者。)定位总pack-year吸烟的病人数量的烟草量轴。画一条线直向上点轴来决定多少分表皮生长因子受体突变的病人接受烟草消费。重复这个过程对于其他轴(年龄、性别、戒烟以来,主要组织学亚型和舞台),每次画一条直线向上点轴。b)和每个预测和定位的点了这个和分轴。画一条线直下到底线找到的概率表皮生长因子受体突变的肿瘤。M:男性;F:女性;号:不是另有规定;Ac /溶胶:腺泡的或固体;BAC:支气管肺泡癌;人民行动党:乳头状。
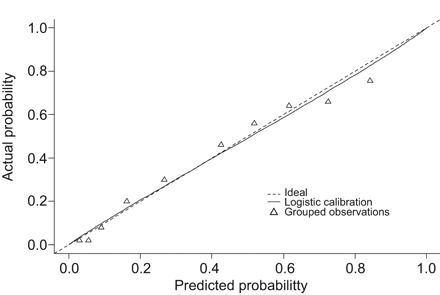
校准曲线的验证数据集。校准被策划的预测评估与实际概率窝藏表皮生长因子受体(表皮生长因子受体)在肺腺癌肿瘤突变验证群813名非亚洲患者。预测的概率表皮生长因子受体变异是绘制的x设在。观察到的频率表皮生长因子受体变异上绘制y设在。虚线表示引用的一个理想的诺模图。实线表示列线图的实际表现。一致性指数为0.84。
的影响喀斯特突变的诺模图
我们测试的影响喀斯特突变状态列线图。喀斯特突变是互斥的表皮生长因子受体在肺腺癌和突变喀斯特突变的肿瘤代表的一个子集表皮生长因子受体野生型肿瘤不应对EGFR TKIs [16,22]。给定的频率就越高喀斯特突变在非小细胞肺癌肿瘤的非亚洲病人和技术问题喀斯特更容易做基因分型,喀斯特突变已经被一些机构是一种消极使用代理的存在的标志表皮生长因子受体突变。喀斯特突变状态是用于82%的病例;17%的基因分型的肿瘤包庇喀斯特突变。在我们的群体中,我们没有确定临床或病理的存在显著相关的变量喀斯特突变。多变量模型局限于患者喀斯特野生型肿瘤产生了非常相似的结果,上述模型。该模型的预测精度独立验证数据集是0.83。
表皮生长因子受体东亚的肺腺癌患者的突变
我们分别分析了一组464年东亚肺腺癌患者来说,吸烟不都是可用的(表3)。变量与激活的存在显著相关表皮生长因子受体突变的肿瘤是:女性(66%与46%的患者;p < 0.001), never-smoker状态(79%与57%;p < 0.001),降低烟草数量前/吸烟者(24±21与39±24 pack-yrs;p < 0.001)。类似于非亚洲患者的组中观察到,表皮生长因子受体突变的肿瘤更容易港口乳头状(20%与8%的患者;p < 0.001)或支气管肺泡(22%与12%;p = 0.01)为主要的亚型,港口腺泡的(43%的可能性较小与54%;p = 0.02)和固体(1%与7%;p = 0.010)的特性。
多元模型给出的结果表4。因为患者在每个子群,我们结合组织学主要亚型的分类如下:支气管肺泡癌/乳头状与腺泡的/固体/ NOS。低pack-year吸烟史(或0.63,95%可信区间0.53 - -0.75),早期阶段(或2.27,95%可信区间1.32 - -3.85)和支气管肺泡癌/乳头状主要组织学(-4.95或2.73,95% CI 1.51)仍然具有更高的概率显著相关表皮生长因子受体突变。该模型的预测精度0.75训练数据集;然而,其准确性是令人不满意的验证在一个独立的数据集(一致性指数为0.64,95%可信区间0.55 - -0.73)。值得注意的是,在我们的数据集,只有29%的亚洲患者吸烟,导致缺乏权力吸烟的变量估计突变的风险,特别是在低风险组。
讨论
肿瘤表皮生长因子受体基因型已经成为一个重要的变量的评价肺癌患者。然而,在许多国家,组织和测试的可访问性等障碍仍然存在,禁止患者获得肿瘤表皮生长因子受体突变状态。这里,我们综合临床和病理因素从成千上万的病人来自美国和东亚,建立一个逻辑回归模型来更好地预测的存在表皮生长因子受体突变在非小细胞肺癌,应该突变测试不可用。列线图有优秀的歧视性质的非亚洲患者和谐指数> 80%。据我们所知,这群代表了迄今为止最大的数据集分析综合与临床特征表皮生长因子受体突变。
其他研究已经确定的临床和病理特征的存在表皮生长因子受体激活突变在肺癌6,17,23- - - - - -27]。与以前的结果一致,我们发现,通过多变量分析,吸烟史,包括never-smoker状态、烟草消费降低吸烟者和再停药在非小细胞肺癌诊断前吸烟者吸烟,都与的存在有关表皮生长因子受体激活突变(17,23- - - - - -27]。我们还观察到支气管肺泡之间的关联和乳头状组织学亚型(5,17,27]。与我们的分析,以往的研究没有确定先进的肿瘤分期的一个重要预测包庇表皮生长因子受体突变。不明身份的选择或技术可能存在偏差,我们分析的数据集,表皮生长因子受体突变是已知的,而发生在肺部致癌过程的早期(28]。
总的来说,与之前的报告相比,本研究是第一个,据我们所知,将多个临床变量,包括吸烟史和组织学亚型,以及性别、疾病和年龄阶段,用户友好的预测计算图表表皮生长因子受体突变。额外变量允许精度高,测试和验证集的使用进一步具体化模型的有效性。
我们的诺模图有一些限制。首先,我们的分析集中于腺癌肿瘤,限制我们的其他组织学分析。然而,大多数的表皮生长因子受体突变被发现在腺癌(24]。其次,该诺模图并不适用于亚洲患者,不同分布的预测变量(吸烟史和阶段)和相当高的患病率表皮生长因子受体突变在非亚洲病人(61%相比25%)在我们的数据集。可能由于这些问题,尝试构建一种常见的诺模图,同时适用于非亚洲和亚洲患者导致预测仪器不令人满意的预测精度。第三,任何预测仪器本身包含了一定程度的不确定性(21)和个人的预测仍不完善。我们的数据来自大型学术中心,和病人的人口在这些机构可能不同于观察其他医疗设置;一般来说,应该小心谨慎,如果诺模图是用来预测的可能性表皮生长因子受体突变的患者来自人口不同的病例组合和不同的突变患病率比研究。
IPASS的入选标准是基于临床特点与存在相关表皮生长因子受体突变的肿瘤,包括从来没有——或者光吸烟者地位和腺癌组织学(7]。在整个intent-to-treat人口,因为后续的基因显示率为59.7%表皮生长因子受体肿瘤的突变,无进展生存期更长了吉非替尼的手臂比化疗手臂(风险比为0.74,95%可信区间0.65 - -0.85;p < 0.0001) (7]。基于这些数据,考虑的门槛的机会表皮生长因子受体突变,所预测的列线图,为推荐EGFR TKI是临床上重要的,可能是60%。患者使用EGFR TKIs温和的可能性表皮生长因子受体突变的肿瘤根据诺模图可能不是推荐,如表皮生长因子受体TKI治疗导致贫穷的结果表皮生长因子受体野生型肿瘤与标准化疗的试验报告(7,29日]。最后,潜在的独立数据集必须进行验证;加入更多的亚洲病人和non-adenocarcinoma肿瘤,以及应对EGFR TKI治疗,会增加我们的结果的临床意义。
最终,尽管统计准确值的诺模图预测的存在表皮生长因子受体激活突变在非亚洲患者肺腺癌,表皮生长因子受体肿瘤的基因应该在可能的情况下获得的。临床试验,包括“丰富”人群,即。患者更容易出现表皮生长因子受体突变的肿瘤,没有达到改善结果intent-to-treat人群(7,30.),试验研究了已知的患者表皮生长因子受体突变是肿瘤(8,9]。然而,肿瘤的基因不是也不会在所有情况下都是可行的。在这种情况下,我们的诺模图可以用于优先使用EGFR TKIs在肺腺癌患者。
确认
我们感谢M.G.克丽丝(纽约纪念斯隆-凯特琳癌症中心,纽约,美国)有用的评论,m . Butaney(美国,波士顿丹娜-法伯癌症研究所,MA) DFCI数据组装和Y.L.林(国立台湾大学医院、台北、台湾)台大医院数据检索。
脚注
感兴趣的语句
语句对h .霁,m . Ladanyi和g rie可以找到www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年1月19日。
- 接受2011年6月16日。
- ©2012人队