文摘
Nintedanib和pirfenidone批准治疗特发性肺纤维化(IPF)。这个非盲、双官能团试验调查了药代动力学的药物之间相互作用这两个药物IPF患者。
受试者没有接受antifibrotics筛查(组1,n = 20)收到一个nintedanib剂量(150毫克)pirfenidone紧随其后(801毫克每日三次滴定)3周,只有进一步nintedanib剂量(150毫克)的最后一天(天23)。受试者接受pirfenidone在筛查(组2 n = 17)继续接收pirfenidone仅为7天(801毫克每日三次),然后用nintedanib流行性流感减毒活疫苗(150毫克每日两次)7天,之前单剂量治疗16天。
在组1,调整几何平均数(gMean)比率(有/没有pirfenidone)分别为88.6%和80.6%的血浆浓度时间曲线下nintedanib面积(AUC)和最大血浆浓度(C马克斯),分别。在组2,gMean比率(有/没有nintedanib) pirfenidone AUC和C的分别为97.2%和99.5%马克斯,分别。所有参数的90%置信区间包含100%,表明类似的暴露政府仅当流行性流感减毒活疫苗。两个治疗耐受良好。
这些数据显示没有相关的药代动力学nintedanib药物之间相互作用和pirfenidone流行性流感减毒活疫苗在IPF患者。
文摘
没有药代动力学相互作用nintedanib和pirfenidone IPF患者http://ow.ly/utJD30msHeU
介绍
特发性肺纤维化(IPF)是一种慢性、进行性、fibrosing形成原因不明的间质性肺病导致进行性呼吸困难,肺功能恶化1,2]。IPF预后很差,直到最近,没有被证明是有效的治疗IPF或批准临床使用1,3]。
在过去的几年中,两个小说antifibrotic治疗,nintedanib pirfenidone,在多个国家获得监管部门的批准后关键试验显示每个IPF患者有效地减缓疾病进展(4,5]。随后,两治疗收到积极的建议在国际循证指南(6]。鉴于nintedanib和pirfenidone都有效的延缓疾病进展,但最终停止和逆转这种致命的疾病,还有一个未满足的治疗需要得到进一步的发展7]。
两个antifibrotic药物的可获得性,存在多个信号通路参与IPF的发病机制,预计联合治疗可能是未来的IPF治疗发展的重点,类似于其他几个管理慢性进行性肺动脉高血压等疾病(2,7- - - - - -11]。尽管pirfenidone的作用机制尚未完全阐明,它被认为行动几个目标包括glioma-associated致癌基因同系物2-mediated转变增长factor-β-triggered事件(12- - - - - -14]。相反,nintedanib作用于血小板源、成纤维细胞和血管生长因子受体酪氨酸激酶抑制细胞内信号(15,16]。这表明,治疗与化合物可能提供添加剂或协同效应,导致更大的临床好处比单独处理(7,9]。然而,有一些重叠的耐受性pirfenidone概要文件和nintedanib IPF患者的肝酶的增加和胃肠道事件(5,17,18]。联合治疗是一个潜在的选择对于临床医生和患者,因此,潜在的药物之间的相互作用和数据相结合的整体效益/风险nintedanib pirfenidone治疗迫切需要以通知临床决策(7]。
Pirfenidone和nintedanib有不同的代谢。Pirfenidone是由各种细胞色素P450 (CYP)代谢酶,主要从CYP2C9 CYP1A2和微小的贡献,CYP2C19、CYP2D6和CYP2E1,主要分泌通过尿液的代谢物5-carboxy-pirfenidone [12,19]。合并施打抗抑郁药氟伏沙明、强有力的抑制剂CYP1A2和其他CYP同功酶,与显著增加有关pirfenidone曝光,和pirfenidone禁忌患者伴随的使用氟伏沙明[12,19]。相比之下,nintedanib的新陈代谢通过水解酯乳沟,导致游离酸的形成一部分随后glucuronidated和排泄的粪便(20.]。Nintedanib潜力很低,药物之间的相互作用通过CYP酶(21]。
这个试验计划的时候,nintedanib pirfenidone联合治疗只有经过测试在二期试验中在日本IPF患者(18]。这是一个双盲,随机,安慰剂对照试验,其中50例治疗nintedanib之上根据pirfenidone使用分层的标准医疗护理。结果显示低趋势nintedanib暴露在稳态pirfenidone和提出了一个潜在的药代动力学药物之间相互作用的问题。然而,固体结论的研究不能作为研究设计服务于不同的目的,接触患者组之间相比nintedanib只能(inter-individually)和可评价的药代动力学观察每个治疗组(< 12)并不认为足以评估药代动力学药物之间的相互作用。
提供进一步说明,本研究旨在调查nintedanib的药代动力学药物之间的相互作用和pirfenidone流行性流感减毒活疫苗在IPF患者。的主要目的是探讨影响稳态pirfenidone单个nintedanib剂量的药物动力学,并调查的影响稳态nintedanib pirfenidone药物动力学的稳态IPF患者。第二个目标是评估联合治疗的安全性。
材料和方法
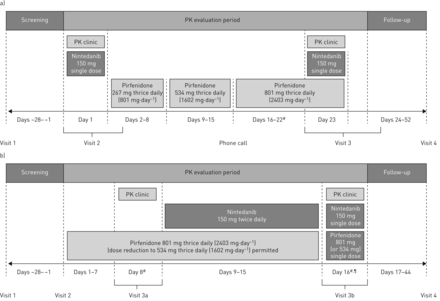
这是一个非盲、多剂量,在IPF患者群审判(EudraCT 2015-000732-15;NCT02606877)。受试者被随机。合格的人不是nintedanib或pirfenidone治疗研究中条目被分配给组1,而目前接受最大剂量pirfenidone进入组2。每组有一个固定程序设计(图1)。研究协议是一个独立的伦理委员会批准(London-Surrey边界研究伦理委员会,伦敦,英国)和主管机关(药物和保健产品监管机构,伦敦,英国)。研究符合赫尔辛基宣言的原则和国际会议上协调好临床实践指南。书面知情同意了之前所有科目学习条目。审判是在九医院在英国在2016年5月和2017年3月之间。
研究设计。一群)1;2 b)组。PK:药代动力学。#:时间窗口被允许达到或保持完整的pirfenidone剂量(组1:日时间窗;组2:两个为期3天的时间窗口),确保稳定的7天治疗期(组1和2:足量pirfenidone;组2:联合治疗与nintedanib pirfenidone);¶:16天(访问3 b),受试者单剂量pirfenidone 801毫克和150毫克nintedanib只在早上。PK抽样开始前1小时单剂量pirfenidone nintedanib总局和持续了6 h post-drug管理。在组1,PK样本收集和0.5之前,1,2,3,4,6,8,10∼剂量后24 h 1天(仅nintedanib)和23个。2组PK样本收集和0.5之前,1,2,3,4,∼6 h后剂量8天(仅pirfenidone)和16。
主题
主体资格列入≥40岁的男性和女性,与IPF诊断根据当前国际指南(1)和胸高分辨率计算机断层扫描筛查之前执行。合适的人需要有一个用力肺活量≥50%预测和扩散能力的pred肺一氧化碳30 - 79%。关键的排除标准包括肝酶升高(> 1.5倍正常范围的上限);增加出血风险(如。需要抗凝治疗或大剂量抗血小板治疗);目前的吸烟;血栓性的历史事件在12个月内的筛选;和严重肾功能损害。个人曾收到nintedanib过去2周,以前pirfenidone治疗在过去的3个月(组1)或之前停止nintedanib或pirfenidone由于不良事件被排除在外。完全排除标准中提供的补充材料。
研究设计和治疗
图1显示了研究设计和治疗两组。组1收到nintedanib的单剂量150毫克1天,pirfenidone (uptitrated三次每日三次,每次267毫克到801毫克每天)从天2到23日的单剂量150毫克nintedanib最后一天(天23)。第二组仅接受pirfenidone(每日三次,每次801毫克)连续7天(从1到8天),然后用nintedanib流行性流感减毒活疫苗150毫克每日两次连续七天(从9到15天),单剂量pirfenidone 801毫克和150毫克nintedanib 16天。安全安排了后续访问至少28天之后最后药物摄入量。
Nintedanib是提供150毫克软明胶胶囊(Ofev;勃林格殷格翰集团制药、Biberach、德国),pirfenidone 267毫克硬胶囊(Esbriet;罗氏制药、Grenzach-Wyhlen、德国)。在两组中,口服剂量的nintedanib和pirfenidone与食品管理。治疗中断和被允许剂量减少不良事件的管理。
药代动力学评价
在组1,静脉血样测量nintedanib收集和pirfenidone血浆浓度在potassium-EDTA-anticoagulant管给药后24小时天1(仅nintedanib)和23岁(图1)。在组2,血液样本测量nintedanib收集pirfenidone血浆浓度和给药后6小时8天(仅pirfenidone)和16。等离子体浓度nintedanib和pirfenidone(自由基地)的形式分析了使用验证液体色谱-光谱法测定(Nuvisan, Neu-Ulm,德国)。nintedanib校正曲线和pirfenidone等离子体未稀释的样本覆盖范围0.05 - -50.0 ng·毫升−1和100 - 50 000 ng·毫升−1,分别。
安全性评价
nintedanib的安全性和pirfenidone被12导心电图评估,生命体征(脉搏、血压),肺量测定法,常规实验室评估、体格检查、不良事件报告和评估耐受性的调查员。提供的细节补充材料。
统计和药代动力学分析
样本容量的确定不是基于功率计算。≥12个受试者的样本容量与可评价的药代动力学评估每组被认为足以达到目的的探索性试验,符合监管指导(22]。占可能辍学是计划招募到34主题,目的是进入16个学科组1和18组2。
标准noncompartmental方法被用来计算等离子体药代动力学参数。血浆浓度时间曲线下面积(AUC)是计算使用对数线性梯形法则从时间零(pre-dose)到最后一个可量化的浓度(AUC的时间0-tz)和外推到正无穷(AUC0 -∞)。
这项研究的目的是评估1)的相对生物利用度nintedanib当单独或与pirfenidone流行性流感减毒活疫苗接种组1;和2)的相对生物利用度pirfenidone当单独或与nintedanib流行性流感减毒活疫苗接种组2。药物动力学评估使用一个个体内部比较,治疗之间的比较是在对象而不是主题,避免inter-subject可变性(23]。的主要终端nintedanib AUC组10-tz和最大血浆浓度(C马克斯);AUC0 -∞是一个次要终点。在组2,主终端稳态pirfenidone AUC剂量间隔τ(AUCτ,党卫军)和C马克斯在稳态(C马克斯,党卫军)。自然对数转换AUC和C马克斯nintedanib值和pirfenidone组间比较采用方差分析模型。主要分析测试相比治疗(nintedanib和流行性流感减毒活疫苗pirfenidone)和参考(mono-treatment nintedanib或pirfenidone)使用方差分析模型来评估治疗的效果(固定效应)和主体(随机效应)的变异来源。这意味着人药代动力学数据测试和/或参考时间被用于测试/引用率估计。团体之间的两两比较,预期之间的差异意味着在相应的最小二乘估计的差异意味着(点估计);90%的双侧置信区间基于t分布的计算。这些值被back-transformed原规模提供点估计(几何平均数)和区间估计的比率测试和参照群体。这项研究的主要焦点是估计影响的大小;因此,没有假说进行了测试和等价指定范围。敏感性分析进行了基于方差分析模型与治疗和科目固定效果。这意味着只有科目可评价的数据在两个治疗周期(测试和引用)被用于测试/引用率估计和90%的CIs,尽管所有的观察都是进入模型。
其他参数给出了描述性统计(算术和几何方法(gMean),标准偏差和几何变异系数(gCV))。Noncompartmental分析血浆浓度时间数据进行了使用凤凰WinNonlin(美国NC Pharsight公司卡里)。使用SAS统计分析(SAS研究所卡里,数控,美国)。
结果
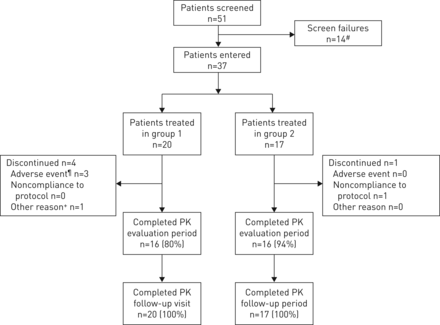
51筛选受试者中,37都有资格进入试验(图2)。其中,20进入第1组,17日进入组2 (表1)。正如预期的那样,男性比女性有更多的研究中,大多数人是白人,> 60岁。超过一半的受试者吸烟。在组1和2,18(90.0%)和15(88.2%)的患者在基线,一个或多个伴随诊断。大部分患者在1组(90.0%),组2(100.0%)花了至少一个伴随的疗法治疗。进一步的细节,同时给出的诊断和治疗补充材料。所有受试者进入试验治疗。每组16个受试者完成试验药物和所有这些完成了后续访问。
参与者的性格。药代动力学(PK)浓度或参数收集从一个病人被认为是nonevaluable如果,例如,一个病人经历了呕吐,发生在前两次中值t马克斯(时间达到最大血浆浓度(C马克斯)各自的治疗这种治疗期间,患者的pre-dose浓度> 5%的C马克斯价值的病人,服用剂量(药物)不符合临床试验协议,或限制使用药物。在组1,数据从17个学科被认为可评价的PK的分析参考治疗,其中12名可为PK的分析测试组23天。2组数据来自15个受试者可评价的PK的分析参考治疗,其中13可评价的PK的分析测试组23天。在两个治疗组,12例可评价的PK的数据参考和测试治疗(包括在灵敏度分析),分别。#:14例(27.5%)受试者不登记,因为它们不符合入选标准或他们满足排除标准;¶:不是因为疾病的恶化正在研究;+:病人误解pirfenidone政府的指令。
药物动力学的nintedanib
组1,3科目过早停止试验药物不良事件和1其他原因。17个受试者可评价的药代动力学数据分析参考治疗,其中12可评价的药代动力学分析测试组23天。总结了药代动力学参数给出表2。
在两个治疗周期,nintedanib吸收较快,平均C马克斯值达到26.1 ng·mL−1和30.3 ng·毫升−1∼2 h后政府有无pirfenidone,分别。峰值吸收后,血浆浓度nintedanib适度下降快,直到∼6 - 10 h,紧随其后的是较慢的终端阶段(数据未显示)。nintedanib gMean终端半衰期的影响与pirfenidone合并施打。Inter-individual变化暴露是中度到高C马克斯(gCV 65 - 103%)和温和的AUC (gCV 59 - 70%)治疗期。
个人的图形表示和gMean值的主要终端显示没有明确的趋势当nintedanib被单独或与pirfenidone流行性流感减毒活疫苗(图3)。比较个体暴露估计在两个治疗周期,两个受试者更明显减少从参考测试,三个显示更明显增加从参考测试,和所有其他的个人显示类似的风险估计。个人最高的三个主题马克斯值参考时期没有值在测试期。这些课程没有任何值得注意的人口学特征基线相比其他个人。
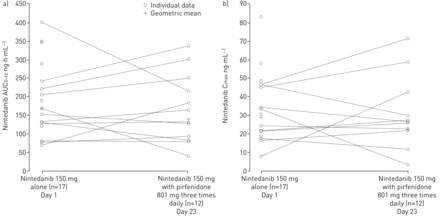
比较个人和几何平均nintedanib)血浆浓度时间曲线下的面积从0到最后一个可量化的数据点(AUC的时代0-tz在等离子体)和b)最大浓度(C马克斯后单口服nintedanib仅150毫克,和一起pirfenidone 81毫克每日三次。
点估计调整gMean nintedanib暴露与pirfenidone流行性流感减毒活疫苗时的比率与政府仅分别为80.6%、88.6%和89.5%的C马克斯,AUC0-tz和AUC0 -∞分别为(表2)。所有参数的90%置信区间包含100%,表明类似的暴露与pirfenidone独自管理,当流行性流感减毒活疫苗。自身内在的变异是中度到高(gCV 44 - 75%),这反映了广泛的90%置信区间。
敏感性分析,认为只有12个受试者在治疗期间可评价的药代动力学数据显示点估计gMean nintedanib暴露的比率为92.8%,95.9%和97.5%的C马克斯,AUC0-tz和AUC0 -∞,分别。
药物动力学的pirfenidone
在组2中,一个病人过早停止试验药物和一个没有可评价的参考治疗期间由于不遵守协议。受试者的数据包含了15个的药代动力学分析参考治疗13对象包含在测试组。总结了药代动力学参数给出表3。
pirfenidone后的药代动力学参数的多个口服801毫克每日三次,每次pirfenidone独自(参考),并与稳态nintedanib 150毫克每天两次(测试)#
稳态gMean血浆浓度时间的pirfenidone在多次给药前后相伴与nintedanib多次给药治疗组之间的可比性(数据没有显示)。Pirfenidone等离子体水平达到峰值∼1 h,然后稳步下降迅速,整个剂量间隔。
pirfenidone暴露的程度,由C表示马克斯,党卫军和AUCτ,党卫军相当pirfenidone是否单独或在nintedanib管理。符合这一点,没有增加或减少暴露的趋势可以从个人和的比较划定gMean C马克斯,党卫军或AUCτ,党卫军值(图4)。
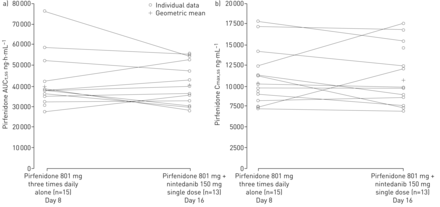
个人和几何平均数的比较(gMean) pirfenidone)曲线下的面积在稳态等离子体在一个统一的给药间隔τ(AUCτ,党卫军在等离子体)和b)最大浓度稳态(C马克斯,党卫军口服后)pirfenidone仅801毫克每日三次,和一起nintedanib 150毫克每日两次。
gMean调整比率的点估计pirfenidone暴露与nintedanib流行性流感减毒活疫苗(稳态)与AUC pirfenidone仅是97.2%τ,党卫军C和99.5%马克斯,党卫军(表3)。相应的CIs 90% 100%,标准的80 - 125%生物等效性AUC的可接受范围τ,党卫军(88 - 108%)和C马克斯,党卫军(88 - 113%)。个体内变异很低(gCV值在14.1%至17.4%之间)。敏感性分析,认为只有12个科目可评价的两组药代动力学数据显示类似的结果。
安全
在两组29例(78.4%)受试者报告说一个或多个不良事件(表4)。最常见的不良事件是腹泻、恶心、下呼吸道感染、呕吐、头痛和消化不良。腹泻是最常报道的不良事件在两组(组1 30.0%;组2 23.5%)。报告了恶心和呕吐,频率在每组> 10%。所有报告的不良事件是被研究者认为是轻度或中度除了两例严重的强度在组1。其中一个科目处理pirfenidone 267毫克每日三次感到虚弱和头晕。患者中断治疗时的事件,后来永久pirfenidone停止。另一话题pirfenidone对待每天267毫克三次报告了一颗牙齿感染严重的强度。这两个事件都被认为是与毒品有关的调查员,主题从他们的事件中恢复过来。 All diarrhoea, nausea and vomiting events were National Cancer Institute (NCI) Common Terminology Criteria for Adverse Events (CTCAE) grade 1. A total of 19 (51.4%) subjects had possible drug-related adverse events. Eight of these individuals experienced diarrhoea and seven subjects had nausea. Dyspepsia, headache and fatigue were experienced by a further four subjects each, and three individuals reported vomiting. Three subjects permanently discontinued pirfenidone treatment due to adverse events (diarrhoea n=2; vomiting n=1; asthenia n=1 subject). No serious adverse events were reported.
讨论
两种新型antifibrotic药物的批准,pirfenidone nintedanib,改变了IPF近年来的管理。当我们寻找进一步改善临床结果在这种患者人群,nintedanib pirfenidone联合治疗是一个有吸引力的治疗选择考虑针对他们的可用性和不同的作用机制7),但到目前为止对潜在的或意外的药物之间的相互反应添加剂/协同功效或不良事件。
本研究的结果表明,没有相关的药代动力学nintedanib药物之间相互作用和pirfenidone IPF患者。在组1的主要分析,gMean nintedanib曝光(基于AUC值0-tz和C马克斯)减少了12 - 19%当nintedanib与pirfenidone流行性流感减毒活疫苗。然而,主要分析使用数据从所有17个学科可评价的药代动力学观测估计gMean比率,和包括五人高曝光值参考治疗期(没有值得注意的人口学特征),但没有治疗价值测试。敏感性分析,只有包括12个受试者的数据可评价的药代动力学观察治疗时期导致gMean总额的比率和峰值接触接近100%。这表明nintedanib观察的轻微减少暴露的主要分析主要是由于不平衡的药代动力学比较结合已知高inter-patient药代动力学变化(24,25]。
个人目测nintedanib暴露(AUC值0-tz和C马克斯)提供了进一步支持缺乏药代动力学的药物之间的相互作用。之间没有明显的模式改变曝光测试和参考治疗,和可变性(包括内部,特别是inter-individual)两组高。明显inter-individual变异性也观察到在其他nintedanib研究[24,25),包括试验前日本IPF患者(18]。招收日本病人的研究中,药代动力学评价,由于与这些相应平行的组织设计,被inter-patient可变性和阻碍,因此,没有提供一个明确的结论的影响pirfenidone co-treatment nintedanib曝光。
在组2,pirfenidone(基于AUC的敞口τ,党卫军和C马克斯,党卫军)是类似pirfenidone是否有或没有稳态nintedanib管理。90%置信区间内的标准80 - 125%生物等效性可接受范围和灵敏度分析支持主要的分析结果。pirfenidone的结果与之前的结果一致描述试验在日本IPF患者(18]。
支持nintedanib药物之间的信息交互和pirfenidone IPF患者最近12周中生成INJOURNEY审判。这个试验集中在安全性和耐受性,只有包括稀疏采样(药代动力学9]。类似nintedanib槽等离子体浓度观察时单独或与附加pirfenidone管理。
因为nintedanib的不良反应概况和pirfenidone部分重叠,尤其是胃肠道事件和肝酶海拔(12,15),有一个潜在的添加剂副作用当结合治疗。Nintedanib pirfenidone和良好的耐受性研究中当独自管理,当流行性流感减毒活疫苗。胃肠活动大多数是轻微到中等强度和分布式两治疗组之间的类似。总的来说,23(62.2%)的37人在两组报告腹泻、恶心或呕吐事件(所有的列为NCI-CTCAE 1级),这是类似于以前的研究报告(9,18]。
虽然目前的数据和先前的研究9,18)表明,没有相关的药代动力学nintedanib药物之间相互作用和pirfenidone IPF患者流行性流感减毒活疫苗时,建议进一步研究解决的一些现有研究的局限性。首先,它可能是信息检查的活动pirfenidone主要代谢物5-carboxy-pirfenidone,可用在体外数据显示一些药物相关活动的这种化合物浓度超过IPF患者的血浆浓度峰值(12]。其次,本研究调查了在组1 pirfenidone作为罪犯的影响药物在稳态nintedanib的药物代谢动力学情况,受害人药物单剂量后,而不是在稳态。然而,正如没有临床相关的药物之间的相互作用在这个“最坏情况”,强烈认为,这一发现同样适用于稳态剂量nintedanib(受害者的药物),从INJOURNEY药代动力学研究结果支持的研究(9]。第三,尽管数据的长期使用nintedanib和IPF患者pirfenidone单药治疗(26,27),目前只有非常有限的数据联合治疗的长期使用。小二期研究20日本IPF患者报告了成功的长期治疗nintedanib pirfenidone在一起;均值±sd曝光时间的延长是27.0±15.8个月,安全性和耐受性方面更好仍符合每个药物不良事件的概要文件,没有新的安全信号识别(28]。此外,伴随治疗nintedanib和pirfenidone INJOURNEY 12周的试验是可行的,没有新的安全信号新兴(9]。但是,没有明确的结论在联合治疗的安全性和耐受性可以根据患者在这些研究中,和更大的和更长的试验调查的长期安全性和耐受性nintedanib给除了pirfenidone是必需的。
总之,这些数据表明,没有相关的药代动力学药物之间相互作用nintedanib pirfenidone当管理是IPF患者联合治疗。两种药物的血浆浓度时类似管理单独或结合在一起。安全这个试验的结果也符合已知的个别药物不良事件概要文件。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
在线补充材料Nintedanib_Pirfenidone_DDI_Study_Journal_Response_2_25Sep2018_SI
确认
这项研究是由勃林格殷格翰集团(英国布拉克内尔)和在英国是由九个中心。协调调查员l . Richeldi,南安普顿,英国南安普顿大学(2017年3月以来,意大利Cattolica del Sacro库雷,罗马,意大利)。美国弗莱彻:乔杜里的支持和T.M.马赫承认英国国家卫生研究所(NIHR)转化研究协作为炎症性呼吸道疾病。勃林格殷格翰集团负责这项研究的设计和实施,以及数据的收集和管理。医疗援助,写作形式的准备和修改的手稿,勃林格殷格翰集团财务支持,并提供了乔纳森·布伦南(我公司媒体,曼彻斯特,英国)作者的概念方向,基于作者的反馈。作者负责研究设计、分析和解释数据和准备的手稿。支持T.M.马赫NIHR临床科学家奖学金(NIHR Ref: cs - 2013 - 13 - 017)和英国肺脏基金会主席呼吸研究(C17-3)。
脚注
可以从本文的补充材料www.qdcxjkg.com
这项研究是在注册ClinicalTrials.gov标识号NCT02606877。研究人员可以使用链接http://trials.boehringer-ingelheim.com查找信息以请求访问临床研究数据,和其他上市的研究,提交研究计划后,根据条款中列出的网站。
利益冲突:l . Richeldi报告赠款和个人费用从InterMune(顾问委员会的成员),个人费用咨询公司赛诺菲-安万特(sanofi - aventis) ImmuneWorks, Celgene公司,日本日东和百时美施贵宝公司,个人费用从罗氏公司顾问委员会的成员,Fibrogen Promedior,个人费用从赢家,个人费用从勃林格殷格翰集团指导委员会成员,个人费用编辑活动从力学,在提交工作。
利益冲突:美国弗莱彻没有披露。
利益冲突:h . Adamali没有披露。
利益冲突:n·乔杜里报告资助(项目)从勃林格殷格翰的发言,勃林格殷格翰集团的个人费用(用于扬声器费用),其他教育经费赞助罗氏,勃林格殷格翰集团和个人费用(从罗氏公司顾问委员会),在提交工作。
利益冲突:美国Wiebe勃林格殷格翰集团制药公司的一名雇员GmbH & Co .公斤。
利益冲突:美国风勃林格殷格翰集团制药公司的一名雇员GmbH & Co KG。
利益冲突:k Hohl没有披露。
利益冲突:贝克是勃林格殷格翰集团的一名员工。
利益冲突:r . Schlenker-Herceg没有披露。
利益冲突:美国Stowasser国际GmbH是勃林格殷格翰集团的员工。
利益冲突:T.M.马赫,通过他的机构,收到葛兰素史克研发和产学资助UCB收到Apellis咨询或扬声器的费用,阿斯利康,拜耳,Idec,勃林格殷格翰的发言,Cipla公司,葛兰素史克研发、ProMetic,罗氏,Sanumed和联合银行。
支持声明:本研究从勃林格殷格翰集团资金支持。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年3月1日。
- 接受2018年的10月28日。
- 版权©2019人队