摘要
本研究的目的是比较基于放射学的类风湿关节炎相关间质性肺病(RAILD)的预测模型,以确定进行性纤维化表型的患者。
RAILD患者进行计算机断层扫描(CT)评分,并使用卡钳(CALIPER)和肺活量(FVC)测量。采用以下三种方法对结果进行评估。1)硬皮病系统评估视觉间质性肺病的范围和FVC值;2) Fleischner Society特发性肺纤维化(IPF)诊断指南在RAILD中的应用;3)与船舶相关结构(VRS)的CALIPER评分。结果与IPF患者进行比较。
在单变量Cox分析中,所有三种分期系统都能强烈预测结果(硬皮病系统风险比(HR) 3.78, p=9×10−5;Fleischner系统HR 1.98, p=2×10−3;4.4% VRS阈值HR 3.10, p=4×10−4).当硬皮病和Fleischner系统合并,称为进行性纤维化系统(C-statistic 0.71)时,他们确定了一个患者亚群(n=36)具有进行性纤维化表型,4年生存率与IPF相似。在多变量分析中,调整患者的年龄、性别和吸烟状况,并与进展性纤维化系统进行分析时,VRS阈值为4.4%,独立预测结果(模型c -统计量0.77)。
结合两种基于ct的视觉分期系统确定了23%的RAILD队列具有ipf样进行性纤维化表型。计算机导出的VRS阈值的添加进一步改善了结果预测和模型拟合,超出了疾病严重程度和程度的RAILD测量所包含的范围。
摘要
结合RAILD的硬皮病和Fleischner分期系统可以识别ipf样进行性纤维化表型的患者。CALIPER VRS评分进一步改善了模型拟合,超出了疾病严重程度和程度的RAILD度量所包含的范围。http://ow.ly/SUcV30mmeYI
介绍
2-8%的患者发现类风湿性关节炎发生肺纤维化[1,2,但与死亡风险增加3倍有关[2].由于类风湿关节炎相关的间质性肺疾病(RAILD)接受手术肺活检的患者数量有限,人们的注意力集中在通过计算机断层扫描(CT)成像评估疾病模式以预测患者预后。一些研究使用特发性肺纤维化(IPF) CT诊断指南对RAILD患者的CT扫描进行了分析[3.],并证实了RAILD与通常的间质性肺炎(UIP)模式相关的不良结局[4- - - - - -11].然而,尽管有两项研究表明RAILD和IPF患者的结果相似[4,5], CT UIP模式的RAILD患者的中位生存期在3.2 - 10.2年之间变化[4- - - - - -6,8,10在不同的报告中。
将CT上的IPF模式推断到Raild上的IPF模式的潜在限制是,由于蜂窝囊肿和网状物可以在肺的中间或上部区域或上部区域中浓缩时,术中疾病的分布可能不是基础的。12].因此,ipf样明确的UIP模式在CT上的基础优势可能只能捕获一部分真正蜂窝的RAILD患者。然而,识别那些疾病行为持续恶化或ipf样的RAILD患者的重要性越来越重要。RAILD和IPF之间的机制联系越来越被认识到[13]并且出现了抗灰度术中疾病修饰潜在作用的临床前证据[14].此外,正如最近的一个观点所强调的那样[15],在间质性肺疾病(ILD)群体中,越来越多的人认识到IPF的主要焦点可能限制了非特发性条件下快速进展纤维化表型的识别。
因此,我们的主要研究目的是通过CT成像在RAILD人群中识别进行性纤维化表型的患者,使用两种分期系统:一种源自硬皮病的评估疾病程度的系统[16]而且对Fleischner社会的修改IPF诊断指南[17].为了避免评估就诊于单一三级转诊中心的患者的固有偏见,我们分析了在英国两个国家就诊于三级转诊中心的独立RAILD队列。作为第二个目标,我们比较了RAILD患者的生存率和IPF患者的生存率,再次为了保持我们评估多中心国际IPF人群的结论的稳健性。我们的最终目的是研究在评估两种RAILD CT分期系统时,使用计算机分析CT成像的预后是否可以独立预测死亡率。
方法
临床数据
ILD数据库的回顾性分析确定了从2007年1月到2014年1月到2014年7月到2014年7月到2014年7月的两个Terital Ind Centers,以及2005年1月至2015年12月的爱丁堡皇家医院(Edinburgh,英国)。根据美国风湿病学院/欧洲联盟对风湿主义标准进行了类风湿性关节炎的诊断[18由两家机构的风湿病专家提出。肺纤维化最初是由多学科小组(包括肺科医生、放射科医生和活检样本可用的组织病理学家)复查后确诊的。在CT扫描的详细评分中证实了ILD的存在。根据临床记录的评估,如果患者一生中烟草接触量小于100支,则被定义为不吸烟者[19].
将RAILD人群与284例在Royal Brompton医院(n=179)和St Antonius医院(乌得勒支,荷兰)就诊的IPF患者(n=105)进行比较,采用共识指南对这些患者进行多学科团队诊断评估[3.].皇家布朗普顿医院IPF患者包括2011年7月至2014年12月连续转诊的患者,他们接受了基线容积非对比CT扫描。St Antonius医院就诊的IPF患者包括2004年至2015年间接受基线容积非对比CT扫描的新转诊患者。
批准本研究临床表明的CT和肺功能数据是从皇家Brompton医院,圣安东尼医院和爱丁堡皇家医务室的制度伦理委员会获得的,并且不需要知情的患者同意。
视觉CT评估
CT方案在在线补充材料.每个CT扫描分别由两名有3年和4年影像学经验的放射科医生(GC和JB)独立评估,不考虑所有临床信息。最接近5%的叶状CT模式包括磨玻璃混浊、网状模式和蜂房样(总结为ILD范围)[20.].肺气肿的程度和牵引性支气管扩张的严重程度在大叶基础上进行量化,如前所述[21].最偏差的5%的视觉评分(等于两个标准偏差)和在蜂窝或肺气肿的存在/不存在的任何分歧都是由第三次得分手(JJ)进行了10年的成像经验,蒙蔽了所有临床信息。
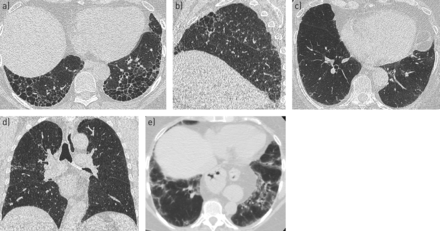
此外,根据Fleischner学会IPF诊断指南的修改,将所有的CT扫描分为五组[17]允许应用于RAILD填充(图1).第一个修改涉及从禁止UIP诊断的不一致特征列表中避免马赛克衰减模式。第二种改变是将疾病分布分为典型的IPF(周围、基底或胸膜下为主)和非典型的IPF(中、上部为主)。CT扫描分为以下五组。第1组:IPF分布下UIP模式明确;第2组:明确UIP模式,不属于IPF分布;组3:指规数分布下的可能UIP;第4组:不属于IPF分布的可能UIP模式;第5组:特征与UIP不一致(不包括疾病分布和马赛克衰减模式)(图1).CT扫描由放射科医生(JJ)和专业ILD(GM)专注的肺病学评分。将分数的任何差异与第三分钟(JB)的读数进行比较,以及拍摄的大多数视图。在17(11%)中,在157例中,在所有三个评分器之间存在分歧的情况下,裁决由原始得分手(JJ和GM)进行。
计算断层扫描(CT)图像演示了五组修改的Fleischner分期系统。a)在55岁的男性出吸烟者中,蜂窝在轴向CT图像上典型的典型常用肺炎(UIP)模式的外围,基底底部分布(第1组);b)一名58岁的男性出吸烟者有蜂窝囊肿,蜂窝状囊肿,在矢状CT图像上侧面侧面,下叶外周没有基础封闭蜂窝囊肿(第2组);c)在57岁的男性Neml-Smoker中,在轴向CT图像(第3组)的下叶片的外周基底副区中可见牵引力支气管扩张;d)一名61岁的男性出吸烟者演示了右中部区域主要牵引支气管扩张,并在冠状CT图像上施加肺部基地(第4组);e)一位70岁的女性出吸烟者有左下角的支气管或支气管或支气管监测分布的证据,该孢子拱弧可让人在轴向CT图像上的右下角中的纤维化组织组织肺炎图案。对纤维化的支气管扩张和组织肺炎模式使CT对UIP模式(第5组)不一致。
卡尺CT评估
如前所述,所有ct均使用CALIPER进行评估[21].用CALIPER进行容积评分的模式包括磨玻璃混浊、网状模式和蜂窝(概括为ILD范围)、肺气肿、正常肺和血管相关结构(VRS)。校正CALIPER计算的肺总容积后,所有实质模式体积均以肺的百分比表示。
肺功能测试
肺功能测试方案在在线补充材料.本研究中检测的肺功能包括1秒用力呼气量(FEV)1)、肺活量(FVC)、肺对一氧化碳的扩散能力(DLCO)和综合生理指标。
统计分析
数据以平均值±表示sd,或n(%)。使用连续变量的单决定标准差和顺序分类变量的加权κ-统计量评估视觉评分的观察者间变异。使用参数连续变量的双样本t检验和中位数的Mann-Whitney u检验来评估组间的平均差异。使用卡方检验评估两个分类变量之间的差异。以p<0.05评价差异有统计学意义。
本研究的主要目的是识别RAILD中的一种进行性纤维化表型,为此,使用单变量Cox比例风险分析来评估我们的RAILD人群的死亡率预测,使用两种之前在其他疾病中验证过的分期系统。第一个系统是硬皮病的复合分期系统(硬皮病系统)[16],根据CT间质分化程度(不良结局≥肺总容积的20%)将患者分为好结局组和坏结局组。对于可能被认为是不确定的病例(15-25%的ILD,占当前研究人群的30%),依据FVC测量(不良结果≤70%预测)作出裁决。
第二个系统是美国胸科学会(ATS)/欧洲呼吸学会(ERS)/日本呼吸学会(JRS)/拉丁美洲胸科学会(ALAT)对U188bet官网地址IP型的CT共识诊断[3.]由弗莱施纳协会修订(弗莱施纳制度)[17].当使用Fleischner系统时,患者被分为五组之一,如前所述(图1).此外,Fleischner系统作为三组模型进行分析,结合明确和可能的UIP组(不考虑疾病分布作为鉴别器)。
作为一个单独的分析,我们评估了自动计算机衍生CT分析软件产生的肺VRS阈值为4.4% (图2).由CALIPER得出的4.4%阈值已被证明可以区分好结果和坏结果IPF组(VRS阈值)。
轴向计算机断层扫描(CT)图像彩色地图显示的卡尺派生的血管相关结构(VRS;红色)。VRS代表肺动静脉(不包括肺门血管)和连通的管状结构,后者主要反映毗邻区域的纤维化。a - c)轴切面:71岁女性,30包年吸烟,上肺叶肺气肿,下肺叶可见纤维化(VRS 2.1%);d-f)一62岁女性,从不吸烟,上肺叶为主纤维化(VRS 7.0%)。VRS信号捕获的非血管区域可见于上叶(d)和右侧半膈(f)附近。
分别在单变量Cox比例风险分析中评估三个系统(硬皮病、Fleischner和VRS),并在多变量Cox比例风险分析中评估这三个系统,以确定每个系统对死亡率预测的贡献。多变量模型根据患者年龄(年)、男性、吸烟状况(从未与)和预测植被覆盖度的基准百分比,除非另有说明。采用Harrell’s c统计量评价模型拟合。进行生存评估通过kaplan meier方法。通过目测鞅残差和缩放Schoenfeld残差检验线性和比例危险的假设,得到了满意的结果。统计分析使用SPSS (IBM SPSS Statistics for Macintosh, version 20.0;IBM, Armonk, NY, USA)和R Studio Team (2015;RStudio:综合开发的R, RStudio,波士顿,MA,美国)。
结果
基线数据
最终的类风湿关节炎研究人群包括90名在皇家布朗普顿医院就诊的患者和67名在爱丁堡皇家医院就诊的多学科团队诊断为RAILD的患者(在线补充图S1).患者接受了最长6年的随访,其中一名患者在随访期结束前接受了审查。两所机构人口的基线差异显示在联机补充表S1,以及综合人口的基线测量方法见表1.爱丁堡皇家医院的患者比皇家布朗普顿医院的患者年龄稍大(p=0.03),并且使用功能指标测量的严重/广泛疾病较少(爱丁堡队列FVC 97.0%)与布朗普顿队列FVC 76.0%, p<0.0001)和视觉和CALIPER CT评分(爱丁堡队列视觉ILD范围16.7%与bronmpton队列视间质性病变范围31.3%,p<0.0001)。
IPF人口包括179名到皇家布朗普顿医院就诊的患者和105名到圣安东尼斯医院就诊的患者。观察者间变异得分见联机补充表S2RAILD和IPF人群之间的基线差异显示在在线补充表S3.综合IPF人群年龄较大(中位年龄为69岁与RAILD患者年龄为65岁,p=0.0004),多为男性(79%)与(45%, p<0.0001)。以功能指数衡量,IPF患者有更严重/广泛的疾病(FVC 74.2%与RAILD FVC 84.4%, p<0.0001)和视觉和CALIPER CT评分(IPF视觉ILD范围29.1%与Raild Visual ILD范围25.1%,P = 0.01)。
RAILD的单变量预后预测
在单变量分析中,视觉(纤维化和蜂窝程度,牵引性支气管扩张的严重程度)和CALIPER(纤维化和蜂窝程度,VRS)间质损伤的测量有力地预测了结果。功能指标对基线结果的预测作用较弱。阳性吸烟史不能预测结果(表2.).
使用分期系统预测结果
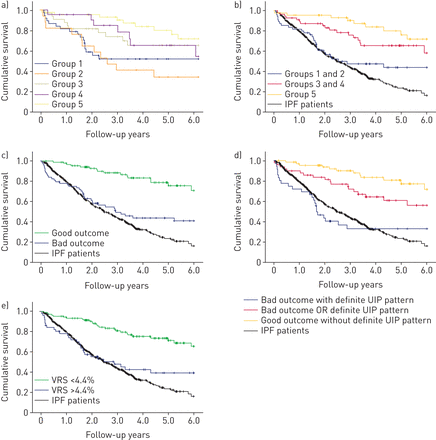
当在RAILD中检测五组Fleischner系统时,具有明确UIP型的患者,无论其分布是否类似ipf,均表现出相似的结果(图3一).同样,可能存在UIP模式的患者,无论其分布情况如何,3年和6年生存率相似。五组Fleischner评分的权重κ为0.65。
a)基于Fleischner社会特发性肺纤维化(IPF)诊断指南,根据纤维化的纤维化模式,Kaplan-Meier曲线展示了类风湿性关节炎相关间质性肺病(轨道)的患者的死亡率。第1组(IPF的蜂窝状,IPF的分布发生):53%3年和6年生存,n = 38;第2组(在非IPF的分布中发生蜂窝状):40%3年和35%的6年生存,n = 17;第3组(没有蜂窝状的纤维化,在IPF样的分布中发生):75%3年和69%的6年生存,n = 33;第4组(没有蜂窝状的纤维化,在非IPF样的分布中发生):85%3年和68%的68%存活,n = 23;第5组(CT患者具有普遍的间质肺炎(UIP)诊断的功能不一致;疾病分布和马赛克衰减的分布不被认为是该轨道研究目的的不一致功能):92%3年和75%6-年生存,n = 46。b)组合来自组1和2的患者图1一个3年生存率48%,6年生存率45%,n=55图1一个:76%3年和58%的6年生存,n = 56,而CT功能不一致的患者图1一个保持不变。将所有三组患者与IPF患者进行比较:3年生存率42%,6年生存率18%,n=284。c) Kaplan-Meier曲线显示了按照硬皮病系统分为好结局组和坏结局组的RAILD患者的死亡率,并与IPF队列进行比较。CT上肺间质病变(ILD)程度为25%的患者评分为1分(预后不良),CT上肺间质病变程度<15%的患者评分为0分(预后良好);CT上肺间质分化程度为15-25%的患者以肺活量(FVC)判定,FVC >70%的预测值为0分,FVC <70%的预测值为1分。结果良好的硬皮病系统3年生存率88%,6年生存率70%,n=88;不良结果硬皮病系统3年生存率50%,6年生存率40%,n=68。IPF患者:3年生存率42%,6年生存率18%,n=284。d) Kaplan-Meier曲线显示了用硬皮病系统分类的RAILD患者的死亡率和在CT上明确的通常间质性肺炎(UIP)模式(疾病分布和嵌合不被认为是一个明确的UIP模式的不一致特征)。在CT上有明确UIP模式的患者在硬皮病系统评分上加1分。 Scleroderma system bad outcome with a definite UIP pattern: 35% 3-year and 35% 6-year survival, n=36; either scleroderma system bad outcome or definite UIP pattern: 78% 3-year and 58% 6-year survival, n=50; scleroderma system good outcome without definite UIP: 90% 3-year and 78% 6-year survival, n=70. IPF patients: 42% 3-year and 18% 6-year survival, n=284. e) Kaplan–Meier curves demonstrating mortality for patients with RAILD categorised using a CALIPER vessel-related structure (VRS) score of 4.4%. VRS score >4.4%: 45% 3-year and 40% 6-year survival, n=51; VRS score <4.4% 82% 3-year and 70% 6-year survival, n=106. IPF patients: 42% 3-year and 18% 6-year survival, n=284.
当疾病分布被忽略时,将Fleischner系统记录为三组评分(明确的、可能的和不一致的UIP模式),明确UIP模式的患者的结局与IPF患者相似,但比可能UIP模式的患者更糟糕(图3 b).在单变性Cox回归分析中,三组粪便系统强烈预测结果(危险比(HR)1.98,95%CI 1.38-2.85; P = 2×10−3;C-statistic 0.67);本文的其余部分将使用三分量表进行分析。在多变量分析中,明确UIP模式的RAILD患者(无论分布)和IPF患者之间的预后没有差异。
在单变量分析中,硬皮病系统强烈预测结果(HR 3.78, 95% CI 2.10-6.81, p=9×10−5;C-statistic 0.69) (图3 c).在多变量模型中,IPF患者和预后差的RAILD患者(使用硬皮病系统进行分类)之间的结果没有差异。在检查两种分期系统的所有多变量模型中,当目视或CALIPER ILD范围取代FVC作为基线疾病严重程度的衡量标准时,结果保持不变。
结合真实的分段系统
为了识别显示进行性纤维化表型的RAILD患者,我们在硬皮病不良结局组中识别出CT上具有明确UIP模式(不考虑疾病分布)的患者,并与IPF人群(进行性纤维化系统)进行比较(图3 d;表3).在单变量Cox死亡率分析中,三点进行性纤维化系统强烈预测预后(HR 2.46, 95% CI 1.73-3.50;p = 1×10−5;C-statistic 0.71)。当使用FVC、目视或CALIPER ILD范围作为基线疾病严重程度的衡量标准时,多变量分析结果得到维持。
VRS阈值的附加影响
当CALIPER VRS阈值为4.4%时,预后预测是强的(HR 3.10, 95% CI 1.81-5.29;p = 4×10−4;C统计0.66)(图3 e).在多变量分析中,VRS≥4.4%的RAILD患者与IPF患者有相似的结果,当目视或CALIPER ILD范围取代FVC作为基线疾病严重程度的衡量标准时,结果维持不变。
在多变量模型中进行评估时,根据患者年龄、男性性别和吸烟状况(从未与),当硬皮病系统(C-statistic 0.78)、Fleischner系统(C-statistic 0.75)和进展性纤维化系统(C-statistic 0.77)分别检测时,VRS阈值独立预测结果(C-statistic 0.78)。联机补充表S4).结果表明,除了CT影像的视觉分析外,定量CT测量在纤维化肺疾病中提供了额外的预后信息。
讨论
我们的研究结合了两种简单的分期系统,可供临床医生使用,以前在硬皮病和IPF中得到验证。在将这些分期系统应用于RAILD患者时,我们发现157例RAILD患者中有36例(23%)表现出进行性纤维化表型,其4年生存率与IPF患者难以区分。此外,我们还显示了自动CT分析对RAILD患者的额外预后价值。
对K即时通讯et al。[4是第一个直接比较RAILD和IPF患者的结果。我们的发现与那项研究一致[4]作为一种明确的UIP模式,牵引性支气管扩张和蜂窝状支气管扩张均与生存恶化、女性和增加DLCO都与更好的结果有关。然而,在K即时通讯et al。[4,这可能与RAILD中的UIP模式是根据IPF条款评估的事实有关。疾病的基本分布是确定UIP模式的先决条件。然而,正如之前在RAILD中所记载的,CT上的蜂房状蜂窝,提示组织学上的UIP,在RAILD中叶和上叶占优势[12或表现为支气管中心[7],与指规数相比,导致分类不一致。
在本研究中,当采用严格的IPF诊断标准时,157例RAILD患者中有38例(24%)在CT上有明确的UIP型。然而,如果不考虑疾病的分布和镶嵌衰减模式(在RAILD中可继发于同时存在的小气道疾病),那么在157例RAILD患者中有55例(35%)被归类为具有明确的UIP模式。UIP定义(严格或广泛)的患者表现出与控制组IPF人群相匹配的相似结果。重要的是,与根据Fleischner学会IPF诊断指南分类为可能UIP(使用严格和广泛的定义)的患者相比,两种定义均显示出不同的结果[17].通过轻微修改IPF诊断标准,以更好地适应RAILD患者,我们有更全面的捕获患者显示一个坏的结果,这样做证实了这一概念,即是蜂窝的存在,而不是它的位置,最好地决定了患者的结果。改良Fleischner系统的临床适用性也明显体现在可接受的评分之间的κ,高于2011年ATS/ERS/JRS/ALAT诊断指南[3.].
在我们的研究中,硬皮病分期系统的预后强度强化了疾病程度作为RAILD预后预测指标的重要性,S强调了这一发现olomonet al。[5),其中纤维化程度是RAILD存活的独立预测因子。事实上,一旦疾病的范围被考虑进去,尽管Fleischner系统仍然可以独立预测结果,但它只略微增加了模型的拟合性。然而,当有明确UIP模式的不良结果硬皮病患者进行亚分析时,他们模仿了一种进行性纤维化表型,类似于IPF,更一致(表3).
几乎四分之一的铁路研究人口,CT上具有广泛而严重的(UIP模式)疾病,表现得像IPF一样。作为识别疾病机制和轨道患者亚群之间的表型的相似性以及IPF的增长[13],显示进行性纤维化表型的RAILD患者可能被认为是未来抗纤维化药物的潜在接受者。在其余部分中,根据ATS/ERS专家小组的规定,对可分类的ILD进行纵向疾病行为监测[22可能是确定可能的进行性纤维化表型的最好方法。
除了硬皮病分期系统和Fleischner协会诊断指南的修改外,我们还评估了自动化软件在预测RAILD预后方面的实用性。具体来说,我们评估了肺的VRS(肺动脉和静脉的容积,以及周围纤维化,不包括肺门的血管),这已被证明可以预测IPF的结果,阈值为肺容积的4.4% [23].在VRS≥4.4%的患者中,3年生存率几乎与IPF患者相同。当与其他分期系统一起分析时,VRS阈值不仅可以独立预测结果,还提高了硬皮病和Fleischner系统的适合度,这表明除了疾病严重程度和程度的简单测量外,VRS阈值还提供了关于结果的额外信息。几乎三分之一的RAILD人群(157例患者中的51例(32%))超过了4.4%的阈值,这表明了对VRS测量的一定程度的敏感性,这可能在大型多中心RAILD人群的分析中有实用价值,正如最近RAILD的一篇社论所设想的那样[24,而ct的视觉评分是不切实际的。
目前的研究有局限性。虽然自动分析的明显效益包括其客观性和再现性,但极其优先增强的CT算法可能导致错误分类,例如蜂窝状。出于这个原因,在目前的研究中,没有分析与西门子B60F算法重建的三个Raild CTS患者的CTS。为避免排除这种情况,应鼓励常规获取计算机友好的重建算法,并且随着定量CT分析变得更加普遍,将变得越来越重要。此外,算法的标准化将提高串行CT检查识别模式范围内的微妙变化的可能性。两项研究中心的铁路患者发生了不同的疾病严重程度,在皇家布朗普顿医院人口中看到了更先进的疾病。然而,我们认为这种异质性是潜在的力量而不是一个主要限制,因为它更好地反映了一个现实世界的铁路患者队列,而不是选择的先进,复杂的轨道患者,提到了单一的伦敦中心。因此,我们还选择将铁路患者与来自两个第三个中心的IPF患者进行比较,而不是单一的,均匀的,潜在偏见的IPF队列。
总之,我们已经证明,通过结合两种分期系统,我们能够识别出CT UIP模式的RAILD患者,显示出进行性纤维化表型。该队列占我们RAILD人群的23%,其4年生存率与IPF患者难以区分。我们还展示了CT图像计算机分析的额外预后强度,它提供了RAILD患者预后的信息,除了视觉评分的CT模式范围所描述的信息。
补充材料
脚注
这篇文章的补充材料可从www.qdcxjkg.com
作者的贡献:j .雅各F.T. van发现C.H.M. van Moorsel M.H.L. Struik,·范,n . Hirani g .交叉j . Barnett G.A.斯图尔特,m . Kokosi r . Egashira A.L.布朗,j.t Murchison, T.M.马赫,a . Devaraj g . Margaritopoulos大肠Renzoni和运算器井参与收购,或研究数据分析或解释。雅各布(J. Jacob)和A.U.威尔斯(A.U. Wells)也参与了这项研究的构思和设计。B.J. Bartholmai, R. Karwoski和S. Rajagopalan发明并发展了卡尺。他们参与处理原始CT扫描和生成数据,但不参与分析或解释研究中的数据。所有作者都对重要的知识内容进行了修改,并最终批准了将要出版的版本。所有作者同意对作品的所有方面负责,以确保有关作品任何部分的准确性或完整性的问题得到适当的调查和解决。
利益冲突:J. Jacob报告来自勃林格殷格翰的顾名费,在提交的工作之外。
利益冲突:Hirani报告了勃林格殷格翰(Boehringer Ingelheim)、Intermune、罗氏(Roche)、Galecto和UCB在提交工作之外的个人费用。
利益冲突:chh . m . van Moorsel没有什么可透露的。
利益冲突:S. Rajagopalan报告了在研究进行期间,皇家布朗普顿医院的拨款(提供给梅奥诊所以支持研究中使用的CT数据集的处理和处理);梅奥诊所已经从Imbio、LCC收取了专利使用费,用于在提交的作品之外授权CALIPER;此外,S. Rajagopalan拥有一项专利,授权给Imbio, LLC,用于使用医学成像数据分析体内组织体积的系统和方法。
利益冲突:j。t。默奇森没什么可透露的。
利益冲突:H.W. van Es没有什么可透露的。
利益冲突:B.J. Bartholmai报告了在研究进行期间皇家布朗普顿医院的拨款(提供给梅奥诊所以支持研究中使用的CT数据集的处理和处理);梅奥诊所已经从Imbio、LCC收取了专利使用费,用于在提交的作品之外授权CALIPER;此外,B.J. Bartholmai拥有一项由Imbio, LLC授权的使用医学成像数据分析体内组织体积的系统和方法专利。
利益冲突:范·比克没有什么可透露的。
利益冲突:斯特瑞克没有什么可透露的。
利益冲突:G.A. Stewart没有什么可透露的。
利益冲突:M. Kokosi没有什么可透露的。
利益冲突:R. Egashira没有什么可透露的。
利益冲突:A.L.布朗没有什么可透露的。
利益冲突:克罗斯没有什么可披露的。
利益冲突:J. Barnett没有什么可透露的。
利益冲突:A. Devaraj报告了罗氏和勃林格殷格翰提交的工作之外的个人费用。
利益冲突:G. Margaritopoulos没有什么可透露的。
利益冲突:R. Karwoski报告,在研究进行期间,皇家布朗普顿医院(Royal Brompton Hospital)向梅奥诊所(Mayo Clinic)提供资金,用于支持研究中使用的CT数据集的处理和处理;梅奥诊所已经从Imbio、LCC收取了专利使用费,用于在提交的作品之外授权CALIPER;此外,R. Karwoski拥有一项由Imbio, LLC授权的使用医学成像数据分析体内组织体积的系统和方法专利。
利益冲突:E. Renzoni报告了来自罗氏和武田的演讲费用,以及来自勃林格的演讲费用和顾委会费用。
利益冲突:T.M. Maher,通过他的机构获得了来自葛兰素史克研发、UCB和诺华的行业-学术资助,并获得了来自Apellis、Astra Zeneca、Bayer、Biogen Idec、Boehringer Ingelheim、Cipla、葛兰素史克研发、Lanthio、InterMune、ProMetic、罗氏、赛诺菲-安万特、武田和UCB的咨询或演讲费。
利益冲突:A.U. Wells报告了来自Intermune、勃林格殷格翰(Boehringer Ingelheim)、罗氏(Roche)和拜耳(Bayer)的顾问费和演讲者费,来自吉利德(Gilead)和MSD的顾问费,以及来自基耶西(Chiesi)的演讲者费,这些费用不包括提交的研究成果。
支持声明:这项工作是由国家卫生研究所呼吸疾病生物医学研究单位在皇家布朗普顿和哈里菲尔德NHS基金会信托基金和帝国理工学院伦敦。J. Jacob得到了威康信托临床研究职业发展奖学金209553/Z/17/Z的支持。
- 收到了2018年5月10日。
- 接受2018年10月17日。
- 版权©2019人队
本文在知识共享署名许可4.0条款188滚球软件下开放访问和发布。