文摘
DNA修复是不足与慢性阻塞性肺疾病(COPD)的发病机制。然而,慢性阻塞性肺病的基础不足的DNA修复机制知之甚少。我们应用一个综合基因组的方法来识别DNA修复基因和通路与慢性阻塞性肺病严重程度有关。
我们测量了419个基因的转录组变化参与DNA修复和DNA损伤发生的宽容与严重的慢性阻塞性肺病三个独立组(n = 1129)。差异表达基因被证实与RNA序列和用于病人集群。临床和全基因组转录组差异集群识别后进行评估。我们补充分析通过执行基因集富集分析,z分数和加权网络分析来识别转录组基因相关性模式与临床相关的DNA修复途径测量COPD的严重性。
我们发现15个基因参与DNA修复和DNA损伤耐受性差异表达在严重的慢性阻塞性肺病。慢性阻塞性肺病的k - means聚类情况下基于15-gene签名确认三个病人显著差异在临床特色集群和全球转录组的概要文件。增加慢性阻塞性肺病严重程度的差别,对这些基因的核苷酸切除修复途径。
系统分析严重COPD患者的肺组织转录组识别DNA修复反应与疾病严重程度相关,可能是COPD发病的基础。
文摘
严重的慢性阻塞性肺病与减少转录基因的核苷酸切除修复途径http://ow.ly/TNoa30l9j2y
介绍
慢性阻塞性肺疾病(COPD)是全球死亡率的主要原因1]。慢性暴露于香烟烟雾中(CS)是慢性阻塞性肺病的主要可改变的危险因素,但慢性阻塞性肺病是一种复杂和异构的疾病,慢性CS暴露的临床和病理的后果在吸烟者之间差别很大。慢性阻塞性肺病的因素构成的异质性不清楚,但可能包括细胞DNA损伤反应(2- - - - - -6]。CS是特征明显genotoxin, CS-mediated DNA损伤导致COPD发病机理(7,8]。COPD患者肺细胞和外周血细胞证明增加全球和端粒的DNA损伤,和细胞反应CS-mediated DNA损伤可以导致致病事件参与疾病进展,包括细胞凋亡、细胞衰老、炎症和诱变(9- - - - - -11]。
DNA损伤是感觉和修复多样化,综合网络细胞信号通路统称为DNA损伤反应,涉及多个DNA修复和DNA损伤耐受性通路(12- - - - - -14]。直接修复(博士)核苷酸逆转共价修改通过单一酶反应,基本切除修复错误或损坏(BER)维修基地、错配修复(MMR)维修异常核苷酸插入或删除,和核苷酸切除修复(尼珥)维修“笨重”病变通过的切除和修复multi-base寡核苷酸所感觉到的停滞的RNA聚合酶或螺旋扭曲。DNA双链断裂是有效的诱导细胞功能障碍和修理通过同源重组(人力资源)或异源end-joining (NHEJ)。人力资源需要模板姐妹染色单体和主要发生在复制,而NHEJ发生在整个细胞周期,但更容易出错。Fanconi贫血(FA)通路整合多个DNA修复途径修复interstrand交联,而某些酶需要修理或拉长缩短端粒和/或损坏。Translesion合成(TLS)指的是使用专门的聚合酶,使DNA复制过去的DNA损伤。此外,许多酶是参与染色质的重塑应对DNA损伤。总的来说,这些通路构成机制通过真核细胞修复或容忍DNA损伤。
DNA修复不足一直是制约观察慢性阻塞性肺病的上下文中。CS抑制DNA修复在体外和细胞从慢性阻塞性肺病患者获得证明的DNA修复能力较低(15,16]。几个DNA修复基因的多态性与慢性阻塞性肺病易感性有关,和减少特定的DNA修复基因的表达已经证明在肺部的主题与慢性阻塞性肺病(2,16,17]。然而,一个系统的描述慢性阻塞性肺病是DNA修复机制的缺乏。我们提出严重的慢性阻塞性肺病与受损应对DNA损伤有关。评估这一假设,我们分析了参与DNA修复基因的表达和DNA损伤宽容从COPD患者肺组织识别差异表达基因(度)和通路与严重的慢性阻塞性肺病。
方法
我们从肺组织微阵列mRNA表达数据分析三个独立样本病人军团:肺癌基因组研究财团(LGRC)、俄亥俄州立大学(俄勒冈州立大学)和肺表达数量性状位点财团(肺eQTL)。提供了基本的汇总数据表1。正常基因表达值调整年龄、吸烟状态(现任、前任,从不)和性在LGRC和肺部eQTL研究中,但不是在俄勒冈州立大学的研究由于样本量(18]。细节描述组织采购、群体特征、基因表达正常化和坚持机构审查委员会的指导方针已经先前描述,并提供进一步的细节补充的方法(19- - - - - -22]。显示了研究设计的大纲图1。我们确定了419个基因构成10通路参与DNA修复和DNA损伤公差(DDRT) (补充表E1)[23,24]。使用数据从LGRC,俄勒冈州立大学和肺eQTL研究中,我们比较这些基因的表达在严重慢性阻塞性肺病患者(慢性阻塞性肺疾病的全球倡议(黄金)(四)与不重的疾病(黄金I, II)和严重的慢性阻塞性肺病(黄金(四)与控制(黄金0)使用意义分析微阵列(25,26]。DDRT基因包括进行进一步分析,如果他们在所有三个组差异表达和共享同一个方向的效果(错误发现率(罗斯福)< 0.1)(补充表E2)。DDRT基因验证基于RNA序列(RNAseq)肺组织从57 LGRC病人样本的一个子集。完整的细节对于这个队列之前描述(补充表E3)[27]。我们集中所有LGRC COPD患者(黄金I-IV)基于使用k - means 15 DDRT共识的基因。集群识别后,我们确定了与每个集群相关的临床特点,我们进行了全基因组转录组分析来识别特定通路与每个集群相关联。基因集富集分析(GSEA) (28),z分数(29日)和加权基因相关网络分析(WGCNA) [30.,31日从LGRC]应用全基因组转录组数据队列来识别转录DDRT通路的变化知道与疾病严重程度相关。的详细方法,请参考补充的方法。
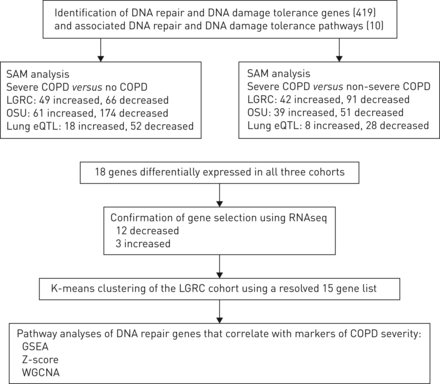
研究工作流程。慢性阻塞性肺病:慢性阻塞性肺疾病;山姆:微阵列的意义分析;LGRC:肺癌基因组研究财团;俄勒冈州立大学:俄亥俄州立大学;肺eQTL:肺表达数量性状位点;GSEA:基因集富集分析;WGCNA:加权网络分析基因相关性。
结果
15个基因的DNA修复签名与严重的慢性阻塞性肺病
我们分析了419个DDRT基因在三个群体:LGRC,俄勒冈州立大学和肺eQTL。这些被选出的军团克服潜在的混杂效应共存的恶性肿瘤可能发生如果我们研究了LGRC队列。我们选择一个COPD患病率高的群体共存的恶性肿瘤(肺eQTL)和一个COPD组没有共存的恶性肿瘤(俄勒冈州立大学)。黄金三世患者不包括在俄勒冈州立大学的研究中,因此并不包括在这些分析。我们确定了18个差异表达DDRT基因出现在比较严重的慢性阻塞性肺病,不重的慢性阻塞性肺病和控制三组(补充表E2)。第二个过滤步骤是实现测试这些18 DDRT基因病人的一个子集LGRC使用RNAseq队列,一个非数组方法,证实基因表达变化的COPD患者的肺。18基因识别的基于数组的军团,15 DDRT基因被证实RNAseq子群(图2)。
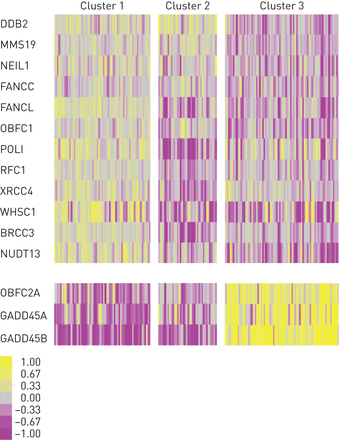
基于15 k - means聚类的患者基因一致的签名。黄色表示增加样本均值,样本均值和紫色表示减少。
慢性阻塞性肺病识别三个集群使用15-DDRT基因签名
描述不同的DNA修复病人集群在慢性阻塞性肺病,我们进行k - means聚类使用15-DDRT LGRC群签名。我们确定了三个不同的慢性阻塞性肺病的使用这种方法(图2相比),临床差异在集群。临床疾病的测量包括肺气肿的比例目前基于高分辨率计算机断层扫描,用力呼气量在1 s (FEV1)%预测,一氧化碳扩散能力(DLCO(6)%预计,6分钟步行距离随钻测量),圣乔治呼吸问卷(SGRQ),波德指数(身体质量指数,气流阻塞,呼吸困难和运动能力),和12项的短小精悍的健康调查。病人在集群1 (n = 65)温和的疾病,患者在集群2和集群3中,以少肺气肿,障碍DLCO和增加FEV1(图3)。同样,病人在集群2和集群3相比,病人在集群1最好功能状态和更高的生活质量以6随钻测量,预示指数和SGRQ分数。没有统计上显著的差异在集群严重疾病的患者的临床特征2和严重疾病集群3。没有性别的差异、久、种族或平均年龄在三个集群(补充表E4)。没有利率的差异共存集群集群2和3之间的恶性肿瘤,但也有集群1中共存的恶性肿瘤发生率增加。这些数据表明,慢性阻塞性肺病的集群情况下基于DNA修复基因签名识别三个集群,集群与集群2和3的特点是疾病严重程度增加。
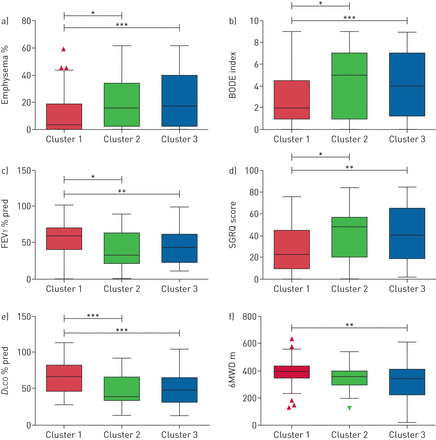
慢性阻塞性肺疾病的临床特点集群。)框和胡须百分比肺气肿的集群。b)盒子和胡须预示指数(身体质量指数,气流阻塞,呼吸困难和运动能力)集群。c)盒须在1 s (FEV用力呼气量1集群)%的预测。d)框和胡须的圣乔治呼吸问卷(SGRQ)得分集群。e)框和胡须的肺一氧化碳扩散能力(DLCO集群)%的预测。f)框和胡须的6分钟步行距离(6随钻测量)集群。*:p < 0.05;* *:p < 0.005;* * *:p < 0.0005。
全球DNA修复基因表达分析集群在慢性阻塞性肺病
全球基因表达模式的描述这三个集群,我们比较了全球转录组的患者在三个集群控制样本LGRC队列。集群1有361度,集群2有3109度和集群3有2219度。73度是在所有三个集群,特异表达和22%的这些常见度(n = 16)三组人群中都有相同的变化方向。与这些集群相关识别非dna修复途径,通路富集分析(补充表E5)。前丰富通路集群集群1和3都与细胞因子信号有关。在集群1中,几个白介素通路(il - 1、IL-3 IL-5, il - 6, IL-17和地震)是在前十名丰富通路。同样,在集群3,白介素通路(IL-3 IL-5, il - 10和IL-17)是在前10名丰富通路。最丰富的途径在两个集群1和集群3 IL-5但方向相反的效果:集群和集群3显示差别1显示对这些upregulation IL-5通路中的基因。集群与集群1和3,集群2被upregulation特征的几个途径参与细胞粘附和细胞骨架改建计划,包括转变增长factor-β(TGF-β)和WNT通路。最重要度排名前50的信号通路中2集群和集群3所示图4。这些途径浓缩数据表明,集群2是增加组织改造,相关基因的表达和集群3是与炎症相关基因的表达增加有关。
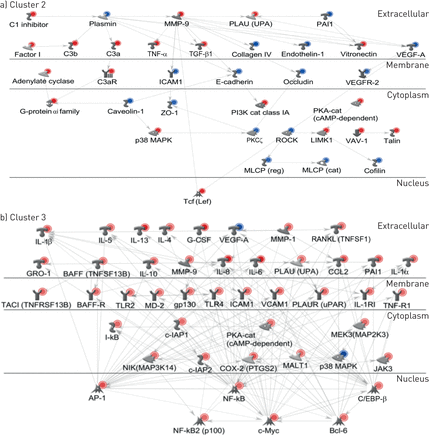
过多的基因在前50名丰富通路。2)对比集群和控制。集群3 b)比较和控制。红色表示调节基因。蓝色表示表达下调的基因。行代表策划之间的关联基因。
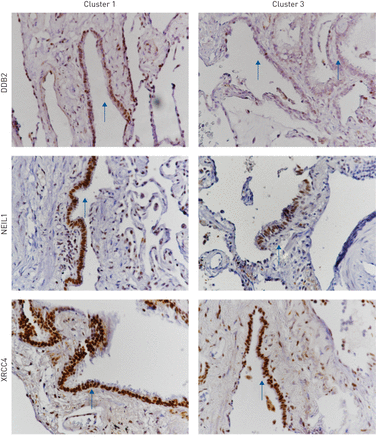
确认的位置选择DNA修复蛋白,我们对肺组织样本进行免疫组织化学酶8-like 1 (NEIL1), x射线修复cross-complementing蛋白4 (XRCC4)和DNA damage-binding蛋白质2 (DDB2)。核染色发现上皮细胞、内皮细胞和巨噬细胞。细支气管上皮细胞表现最突出的三个蛋白质染色强度(图5)。之间有明显异质性染色强度对所有三种蛋白质样品。我们没有确定集群在评估XRCC4之间有着明显的差别;然而,我们识别降低上皮染色DDB2和NEIL1样本严重疾病的患者相比集群3样本病人轻度集群1。值得注意的是,有更多DDB2染色样品的吸烟史的患者比那些从不吸烟。这些数据表明,转录改变在整个肺组织样本也与细胞相关蛋白水平的差异严重的慢性阻塞性肺病患者。
免疫组织化学,DDB2 NEIL1 XRCC4。免疫组织化学显示本地化和DDB2染色强度,NEIL1和XRCC4(被棕色的发色体)患者肺组织样本进行集群1和集群3。核染色出现特别局部细支气管上皮细胞(箭头),尽管其他细胞还演示了核染色。图像获得使用40×物镜。
DDRT通路在慢性阻塞性肺病患者
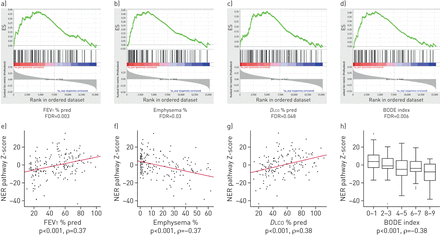
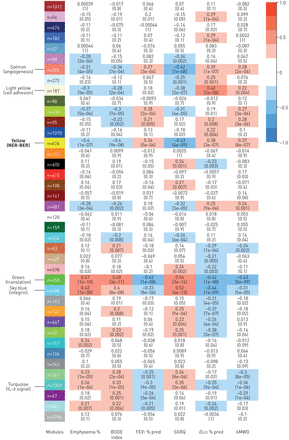
而我们初步分析确定单个基因与严重的慢性阻塞性肺病,我们试图确定如果DDRT途径差异表达严重慢性阻塞性肺病患者使用三种不同的方法。首先,我们进行了全基因组分析来确定基因与临床相关的测量慢性阻塞性肺病严重程度,然后用GSEA识别DDRT通路显著富集在最相关的基因。我们发现TLS,尼珥和FA途径是负相关性(即。与多个测量COPD的严重性(保护)图6- d和补充表E6A)。第二,z分数分析使用COPD患者肺组织的转录组的概要文件。我们生成DDRT路径系数(z分数)为每个单独的慢性阻塞性肺病,这些系数及相关疾病的临床特点。尼珥、tl、FA、麻疹和人力资源途径与多个措施严重的慢性阻塞性肺病(呈负相关图6 e- h和补充表E6B)。博士在这两种方法,途径是唯一一个显示与慢性阻塞性肺病的临床测量严重程度正相关。然而,这个途径是最小的(n = 8基因),使它更容易受到的影响权重系数用于生成。最后,我们执行WGCNA使用全转录组数据来确定DDRT通路中的,与疾病严重程度的指标。我们确定了40模块中的基因,多个模块与疾病严重程度相关图7)。以确保我们的DNA修复途径基因的组成列表不是偏置我们的结果,我们使用Metacore识别基因集富集在完整的细胞通路(补充表E7)。测量模块与最强的负相关疾病的严重性,黄色,NER-BER通路也最丰富。黄色的模块与肺气肿的百分比(相关= −0.4,p = 1×10−7),波德指数相关性= −0.4,p = 4×10−8),FEV1% pred(相关= 0.34,p = 5×10−6),SGRQ(相关= −0.43,p = 4×10−9),DLCO% pred(相关= 0.38,p = 3×10−76)和随钻测量(相关= 0.37,p = 8×10−7)。有多个规范尼珥基因在黄色模块演示了高模块加入慢性阻塞性肺病的临床指标和基因的重要性程度,包括着色性干皮病集团a-complementing蛋白质(XPA)和切除修复cross-complementation集团5 (ERCC5) (补充图E8)。这三种方法的组合尼珥的差别表明,对这些通路与慢性阻塞性肺病严重程度相关。
核苷酸切除修复(尼珥)途径是严重的慢性阻塞性肺疾病中表达下调。模拟)浓缩情节从基因集富集分析。浓缩情节包含配置文件运行的浓缩分数(ES)和条形码情节表明基因在每个基因的位置设置;红色代表斯皮尔曼相关系数与更严重的疾病,蓝色代表斯皮尔曼相关系数较低的严重的疾病。错误发现率(罗斯福)尼珥报告基因集富集在1 s)用力呼气量(FEV1肺气肿比例),b), c)的肺一氧化碳扩散能力(DLCO)% pred和d)预示指数(身体质量指数,气流阻塞,呼吸困难和运动能力)。超高频)尼珥通路z分数为每个病人谋害e) FEV系数1% pred, f)百分比肺气肿,g)DLCO% pred和h)预示指数。
加权基因co-expression网络分析(WGCNA)。WGCNA发现40个基因模块WGCNA的热图中说明。n代表基因在每个模块的数量。积极的相关性是红色的,和负相关性是蓝色的。绿色、天蓝色和绿松石是三个模块大部分与指数降低了疾病的严重程度呈正相关,和黄、鲑鱼和淡黄色的三个模块大部分指数增加了疾病的严重程度呈负相关。最高度浓缩的过程表示为每个六大模块,包括核苷酸切除修复(尼珥)基地切除修复(BER)过程的黄色模块。il - 6:白介素6;波德:身体质量指数,气流阻塞,呼吸困难和运动能力;FEV1:在1 s用力呼气量;SGRQ:圣乔治呼吸问卷;DLCO:肺的一氧化碳扩散能力;6随钻测量:6分钟步行距离。
讨论
在这项研究中,我们确定了15度,是很常见的三个独立军团迄今为止最大的DDRT评估基因。这15个基因的转录变化是异构在慢性阻塞性肺病患者。然而,随后的集群的患者根据这些15个基因识别三个集群与不同的临床特点和相关基因表达谱与疾病发病的重要机制,表明DNA修复之间的潜在关系,炎症和组织改造。我们的数据也表明,多个DDRT通路下调在COPD患者中,最有力的证据是证明尼珥通路。综上所述,这些数据支持的假设减少DNA修复基础的复杂和异构表现慢性阻塞性肺病。
严重的慢性阻塞性肺病与upregulation三15 DDRT基因,GADD45A,GADD45B和OBFC2A。这三个COPD发病相关的基因,因为它们涉及细胞周期阻滞,细胞凋亡和细胞衰老。我们也发现严重的慢性阻塞性肺病12 DDRT差别和对这些基因。在这12个DDRT基因两个足总基因(FANCC和芳珂),两种尼珥基因(DDB2和MMS19)和三个基因参与人力资源和NHEJ通路(WHSC1, BRCC3和XRCC4)。此外,我们确认OBFC1,这是与端粒长度的维护;波里,这有一个核酸外切酶功能;和NEIL1规范化的误码率基因也与尼珥。先前的研究的NEIL1和波里表明,基因毒性压力增加这些基因的表达;然而,我们的数据显示,这些基因的表达减少严重的慢性阻塞性肺病(32]。有许多潜在的原因这种差异与COPD的发病机制,包括组蛋白修饰、稳态信号由于氧化应激失调,干扰DNA损伤的基因转录。例如,NEIL1一直在频繁发现hypermethylated头颈癌(33]。因此,我们的数据支持的假设不适应的反应基因毒性压力有助于在慢性阻塞性肺病疾病进展。
15-DDRT基因签名确认三个病人慢性阻塞性肺病的集群分化疾病严重程度和不同的非dna修复途径表达谱。集群1被轻微的临床疾病的特征,而集群2和3有严重的疾病。集群2显示浓缩通路与细胞骨架改建计划,包括TGF-β和WNT信号。集群3显示浓缩NF-κB, IL-5 IL-17通路。过度的炎症和异常的改造是很好的描述COPD发病机制。DNA损伤和慢性炎症之间的关系描述,因为DNA修复缺陷导致自身免疫,慢性炎症和组织改造(34,35]。基于这些发现我们建议未来的研究的COPD发病机理认为DNA损伤反应结合评估这些炎症和组织改造的途径。
我们应用多种方法描述转录DDRT途径的变化,并确定转录尼珥通路的变化是最稳定与疾病严重度增加有关跨多个临床特征分析方法。有趣的是,某些基因集群集群2和3之间出现差异表达,包括NEIL1,DDB2和MMS19与尼珥。此外,免疫组织化学证实DDB2和NEIL1都减少严重疾病集群3。这是慢性阻塞性肺病的重要病机,因为尼珥通路主要负责检测和去除粗大DNA加合物引起的CS,并因此防止tobacco-induced致癌作用的关键。先前的研究已经证明与CS尼珥能力受损,和减少尼珥能力已经涉及作为肺癌的风险(36,37]。尼珥不足也会导致多余的DNA损伤和随后的对细胞死亡,组织破坏和/或炎症,和肺气肿(38]。很可能其他DDRT通路在COPD提供给我们的发现。重要的是,几乎所有观察慢性阻塞性肺病严重程度之间的关联和DDRT通路基因的差别表明对这些参与DNA修复和DNA损伤耐受发生在严重的慢性阻塞性肺病。
对我们的研究有一定的局限性。共存的影响恶性肿瘤DDRT基因的转录组剖面在COPD患者是一个重要的混杂变量。当组织样本取自良性组织,变化已确定在“正常”从COPD患者肺组织和共存的恶性肿瘤39,40]。这是一个具有挑战性的问题,因为肺组织不是一般从肺功能正常的患者,除非有怀疑的癌症。占的潜在影响“cancerisation领域”,我们包括俄勒冈州立大学的队列,排除患者共存恶性肿瘤DNA修复签名生成我们的共识。其他潜在的局限性,许多DDRT基因不是主要在转录水平调节,因此我们异形全肺组织和基因表达差异可能是由于不同的组织组成不同的细胞类型。要解决这个问题,我们进行了各种DNA修复蛋白和免疫组织化学鉴定DDB2下降和严重疾病集群3 NEIL1肺组织样本。我们没有看到深刻分析XRCC4时集群之间的差异;然而,有显著的异质性在样品和我们的研究可能是检测不同动力不足。未来的研究将需要分析与其他分子读数包括蛋白质浓度、修饰符(即。磷酸化、泛素化),细胞类型和核co-localisation。
我们使用多步,补充分析方法研究DDRT基因和通路及其与疾病严重程度在三个独立的军团。在个体基因水平上,我们发现15-DDRT基因签名启用三种疾病的识别集群的特点是临床严重程度的差异和不同的非dna修复基因通路增加炎症和组织改造。尼珥的差别我们也发现了一致的对这些通路在严重的慢性阻塞性肺病。这些发现表明,转录DDRT基因的变化导致疾病异质性和可能构成不同的致病反应在慢性阻塞性肺病。
补充材料
确认
作者要感谢工作人员的呼吸健康网络组织银行昏聩de矫揉造作的魁北克-桑特提供的宝贵援助与肺eQTL拉瓦尔大学的数据集。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:w·华报道无限制的机构资助从默克公司在进行研究;从辉瑞支付给机构咨询公司的费用,费用支付给机构从葛兰素史克讲课,基耶西,莉莉肿瘤学和勃林格殷格翰的发言,费用支付给机构咨询和讲课,和旅行费用,从罗氏诊断/ Ventana,从荷兰哮喘基金拨款,旅行费用支付给生物监测的机构,和费用支付给咨询的机构,从默克公司大幅Dohme讲课,阿斯利康和诺华公司在提交工作。
利益冲突:n·卡明斯基报道赠款和个人费用咨询Idec,个人费用从勃林格殷格翰集团咨询公司,第三个岩石和MMI,非金融支持Actelion股价和Miragen从顺从个人费用咨询委员会工作,无偿为Samumed顾问工作,从Numedii和个人费用,在提交工作;此外,n·卡明斯基在肺纤维化许可专利新疗法,和专利外周血基因表达,并科学顾问委员会的一员,研究咨询论坛和肺纤维化基金会的董事会,并担任副主编胸腔。以上与慢性阻塞性肺病。
支持声明:作者要感谢授予m .扫罗(K08HL135402-01;FAMRI YCSA 142017)和评论戈麦斯(K01HL125474-03;FAMRI YCSA 113393)。m . Lamontagne是收件人的博士奖学金昏聩de矫揉造作的魁北克-桑特(FRQS)。y博斯持有加拿大研究主席心脏和肺部疾病的基因组。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2017年9月29日。
- 接受2018年7月25日。
- 版权©2018人队