摘要
晚期非小细胞肺癌(NSCLC)不同抗癌治疗方案的最佳生存效益需要保护肾功能。我们评估了培美曲塞维持期间肾损害的发展。
在一项前瞻性多中心队列研究中,我们评估了接受培美曲塞维持治疗的IIIB/IV期NSCLC患者的急性/慢性肾脏疾病(AKD/CKD)发生率、相关停药频率以及与AKD相关的临床变量。我们在一个独立的队列中验证了这些发现。
190例患者接受培美曲塞治疗。在主要队列中,149例患者开始诱导,其中44例患者(30%)继续维持。在独立队列中,41例患者接受维持治疗。在维持期间,13例患者(30%)发生AKD,在主要队列中,8例患者(62%)发生CKD并停止治疗。较高的估计肾小球滤过率(eGFR)(每单位5 mL·min)−1每1.73米2(OR 0.70, 95% CI 0.54-0.90和OR 0.78, 95% CI 0.62-0.98)和诱导期间eGFR的相对下降(每10%)(OR 2.54, 95% CI 1.36-4.74)与维持期间的AKD相关。在独立队列中,20例患者(49%)发生AKD, 11例患者(55%)发生CKD, 6例患者(30%)停止治疗。
患者在培美曲塞维持期间有肾损害的风险,这可能危及进一步的抗癌治疗。
摘要
培美曲塞维持期间存在肾损害的显著风险,这可能危及进一步治疗http://ow.ly/q8r830lnNZR
简介
培美曲塞被广泛用于非鳞状非小细胞肺癌(NSCLC)的一线和二线治疗,没有可操作的驱动突变或高程序性死亡配体1 (PD-L1)表达[1].最近,与化疗相比,一线铂基治疗培美曲塞联合派姆单抗延长了总生存期,而不管PD-L1表达如何[2].在铂类诱导治疗后无疾病进展的患者,推荐培美曲塞作为维持治疗[3.- - - - - -6].免疫疗法和多西他赛联合抗血管生成药物均已证明其优于常规化疗的疗效,并已被批准用于二线治疗[7,8].然而,为了从所有这些药物中获得最佳的生存益处,患者应能够开始并继续需要维持足够肾功能的多种治疗方案[9,10].
肺癌患者发生急性肾损伤(AKI)的风险增加[11].除了暴露于肾毒性化疗药物外,这些患者肾功能下降的原因还包括癌症或化疗引起的真容量或有效容量耗损、患者年龄大以及肾毒性伴随药物[12].培美曲塞的肾损伤机制被认为主要是小管间质性的,因为培美曲塞通过减少的叶酸载体进入基底外侧膜的近端小管细胞,并通过其顶端的叶酸受体运输。一旦进入管状细胞,培美曲塞发生聚谷氨酰化,导致细胞内滞留,并增加与叶酸代谢有关的酶的亲和力,导致DNA合成受损而导致管状损伤[12,13].尽管肌酸酐清除率<45 mL·min的患者不建议使用培美曲塞−1每1.73米2[14],研究表明,即使是较轻微的预先存在的肾损害也是药物性肾毒性的危险因素[15,16].
无论其性质如何,AKI是即时和长期不利结果的预测因子[17- - - - - -19].此外,AKI是发生慢性肾脏疾病(CKD)的重要危险因素[20.]并可能危及进一步的癌症治疗[21].中止培美曲塞维持治疗后肾功能持续损害已在几个病例报告中被描述[22,23].派拉蒙研究(一项关于晚期非鳞NSCLC诱导和维持治疗的研究)报告了培美曲塞维持治疗的患者中<10%的肾损害,以及<5%的患者因肾毒性而停止治疗[24].然而,该试验人群被高度选择,在日常临床实践中可能低估了肾毒性的风险和后果。
因此,我们的目标是描述在培美曲塞维持治疗期间急性和慢性肾损害的发展,以及它对现实环境中治疗决策的影响。
材料与方法
前瞻性多中心队列(主要队列)
PERSONAL(培美曲塞和生物标志物:一项观察性研究)是一项前瞻性多中心队列研究,研究对象为局部晚期或转移(IIIB/IV期)非鳞NSCLC和不可切除间皮瘤的成年患者,接受铂联合培美曲塞作为一线治疗,培美曲塞单药治疗作为二线治疗。患者在2012年10月至2014年11月期间从荷兰的一所大学医院(鹿特丹伊拉斯姆斯大学医学中心)、两家专门从事肺癌护理的大型教学医院(Amphia医院,Breda和Franciscus Gasthuis & Vlietland,鹿特丹)和一家地区医院(Bravis医院,Roosendaal)招募。接受培美曲塞作为二线治疗的患者和不可切除间皮瘤患者被排除在本研究的分析之外。在本文中,PERSONAL队列将被表示为“主要队列”。所有患者均提供书面知情同意书。这项研究得到了伊拉斯谟大学医学中心机构审查委员会的批准。
根据护理标准,铂联合培美曲塞化疗每3周静脉输注一次,最多4个周期。根据体表面积(500、75 mg·m)计算培美曲塞和顺铂给药剂量−2,分别)[14].根据Calvert公式,根据估计的肾小球滤过率(eGFR)和曲线下靶面积值5或6计算卡铂剂量[25].如果化疗方案涉及顺铂,则按照方案给予水合前和水合后治疗。如果患者没有进展性疾病,没有不可耐受的毒性,没有连续放疗或手术,则建议他们继续培美曲塞维持治疗。
基线血清肌酐(μmol·L−1)是在初始化疗周期之前获得的。随后,在诱导治疗期间每次化疗前和化疗后每周检测血清肌酐。在维持治疗期间,血液样本仅在培美曲塞给药前和每个周期的第14天提取。通过计算eGFR (mL·min−1每1.73米2)使用慢性肾脏疾病流行病学合作方程[26].肾不良事件按照《不良事件通用术语标准》(CTCAE) 3.0版进行登记,与培美曲塞维持期登记试验进行比较[24],更新后的版本为4.03 (表1).
独立的群体
为了验证主要队列的研究结果,我们选择了2014年11月至2016年12月在一家医院(安菲阿医院)开始使用培美曲塞维持治疗的所有晚期NSCLC患者。我们使用该中心的药房数据库构建了第二个接受培美曲塞维持治疗的患者的独立队列,这些患者在个人研究的患者登记结束后接受了培美曲塞维持治疗。在维持治疗之前,这些患者在开始诱导和维持前,以及每次培美曲塞给药前的维持期间,根据护理标准(见前一节),接受一线铂联合诱导治疗培美曲塞和水合治疗。由于该队列的数据是回顾性收集的,根据荷兰指南,不需要医学研究和伦理委员会的批准。
急性和慢性肾脏疾病的定义
在两个队列中,急性肾脏疾病(AKD)和CKD患者在诱导和维持治疗期间根据肾脏疾病:改善全球结果(KDIGO)临床实践指南(表2) [27,28].
除了CKD的发展,我们还记录了与肾功能下降相关的临床后果,包括停止治疗、住院治疗、剂量调整和延期。
统计分析
描述了纳入两个队列的所有患者的社会人口学和临床变量。接受维持治疗的主要队列患者分为两组(eGFR <90)与≥90毫升·分钟−1每1.73米2)根据他们在基线(诱导治疗开始)和维持治疗开始时的肾功能。对于这些组,我们报告了AKD、CKD患者的百分比以及使用Wilson评分法计算的95%置信区间的临床后果。使用卡方检验或Fisher精确检验这些组之间AKD发生率的差异。通过logistic回归,我们确定了诱导和维持前肾功能的单变量相关性(每单位eGFR为5 mL·min−1每1.73米2),诱导期间肾功能变化(相对于基线每10%),以及维持期间与AKD发生率相关的其他患者和治疗相关因素。为了验证前瞻性队列研究的结果,我们在第二个独立队列中重复了这些分析。
所有统计分析均使用SPSS 22.0版(IBM, Armonk, NY, USA)进行。P <0.05为差异有统计学意义。
结果
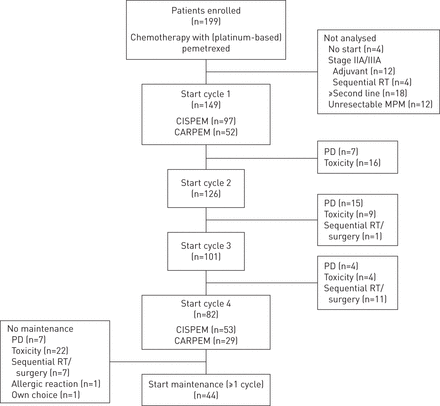
目前的研究共纳入190例接受培美曲塞治疗的患者。在主要队列中,149例晚期NSCLC患者开始使用培美曲塞进行一线诱导治疗。其中44例患者(29.5%)最终接受了一个或多个周期的培美曲塞维持治疗(图1).第二个独立队列包括41例晚期NSCLC患者,他们在一线诱导治疗后接受了一个或多个周期培美曲塞维持治疗。
主要队列患者的流程图。RT:放射治疗;MPM:恶性胸膜间皮瘤;CISPEM:顺铂和培美曲塞联合用药;CARPEM:卡铂和培美曲塞联合用药;PD:进展性疾病。
两组患者的所有患者和治疗特征概述在表3.在主要队列中,维持培美曲塞的患者(n=44)比仅接受诱导治疗的患者(n=105)有更高比例的转移性疾病(p=0.003),并且他们有更高的血清白蛋白(p=0.001)。在两个队列中进行维持的患者之间,没有显著差异,铂联合治疗相似。第二独立队列中接受培美曲塞维持的女性患者略多于第一队列(65.9%)与50.0%;p = 0.188)。第二独立队列中位随访时间(四分位数范围(IQR))为3.2(1.9-6.1)个月,第一队列为3.5(1.4-8.3)个月。
主要队列中的肾损害
诱导治疗
顺铂-培美曲塞联合治疗(CISPEM)与卡铂-培美曲塞联合治疗(CARPEM)患者基线时计算的eGFR值有显著差异(98.1±16.0与88.7±15.9毫升·分钟−1每1.73米2;p = 0.001)。在4个周期的总诱导治疗中,CISPEM患者(n=53)的平均eGFR下降,而CARPEM患者(n=29)的平均eGFR下降(−9.1±9.5)与−2.0±11.0毫升·分钟−1每1.73米2;p = 0.003)。接受联合铂诱导治疗的患者每周eGFR中位数在文献中描述补充材料.
维护
培美曲塞维持周期的中位数(IQR)为5(2-12),第一个维持周期给药前的eGFR为86.3 (71.6-97.2)mL·min−1每1.73米2.在使用培美曲塞维持治疗期间,44例患者中有13例(29.5%)发生了KDIGO定义的AKD。在这13例患者中,根据CTCAE 4.03, 10例患者(77%)发生了全级别的肾不良事件,而使用CTCAE 3.0的患者只有7例(54%)发生了肾不良事件。因此,使用CTCAE 3.0,我们发现只有16%的患者经历了肾脏不良事件。
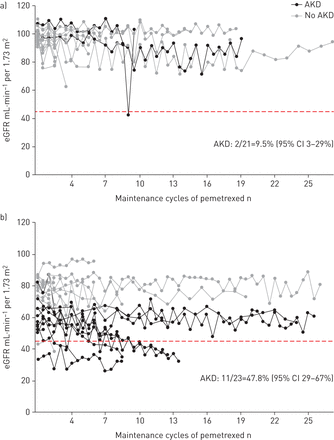
患者肾脏功能的个别病程显示在图2.与eGFR≥90 mL·min患者比较−1每1.73米2维持开始时,肾功能轻度下降的患者(eGFR <90 mL·min−1每1.73米2)更容易发展为AKD (11 / 23)与21人中有2人;p=0.005),肾功能更常低于培美曲塞的推荐阈值(eGFR <45 mL·min)−1每1.73米2在21个国家中,美国有6个与21分之一;p = 0.017)。2例eGFR <45 mL·min−1每1.73米2在维修之前已经被排除在这个分析之外。
在主要队列研究中,培美曲塞维持治疗期间肾功能和急性肾脏疾病(AKD)的发展(n=44)。eGFR:估计肾小球滤过率。a) eGFR≥90 mL·min−1每1.73米2(n=21)和b) eGFR <90 mL·min−1每1.73米2(n = 23)。数据显示为发生AKD和未发生AKD的个体在维持治疗期间的肾功能测量值和肾功能病程。红色虚线表示eGFR=45 mL·min−1每1.73米2,低于该值不建议使用培美曲塞。
每单位5 mL·min−1每1.73米2,维持治疗前和诱导治疗前较高的eGFR值与较低的AKD风险相关(OR 0.70, 95% CI 0.54-0.90和OR 0.78, 95% CI 0.62-0.98) (表4).相比之下,诱导期间eGFR相对基线下降10%与AKD概率增加相关(OR 2.54, 95% CI 1.36-4.74)。AKD患者的平均±sd诱导期间eGFR下降为−12.2±8.9 mL·min−1每1.73米2与−2.1±8.4 mL·min相比−1每1.73米2没有AKD的患者。
临床意义
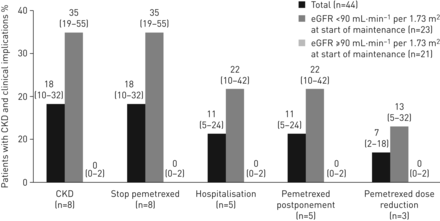
CKD的发展和维持治疗期间肾损害的临床后果概述在图3.在维持治疗期间发生AKD的13例患者(30%)中,8例患者(62%)最终发生CKD。13例AKD患者中有8例(62%)因肾损害而被迫停止维持治疗。重要的是,所有这些发生CKD并停止治疗的患者已经有轻度肾功能受损(<90 mL·min−1每1.73米2),方可开始维修。此外,在诱导前肾功能已经轻度受损的患者(<90 mL·min−1每1.73米2)不得不停止治疗的患者比例高于eGFR正常的患者(6 / 11)与33人中有2人;p = 0.001)。相应地,患者更容易发展为AKD (6 / 11)与33人中有7人;p=0.057)和CKD (5 / 11)与33人中有3人;如果诱导前肾功能轻度受损,P =0.016)。
慢性肾病(CKD)和培美曲塞维持治疗期间肾损害的临床意义eGFR:估计肾小球滤过率。数据以% (95% CI)表示。
第二个独立队列的肾损害
在第二个独立队列中,培美曲塞维持周期的中位数(IQR)为4(3-8),第一个维持周期给药前的eGFR为80.6 (63.4-93.3)mL·min−1每1.73米2.20例患者(49%)发展为AKD,其中11例患者(55%)最终发展为CKD, 6例患者(30%)停止培美曲塞维持。与主要队列相似,所有发生CKD并停止维持治疗的患者eGFR均<90 mL·min−1每1.73米2在开始维护之前。
我们测试了与主要队列中相同的患者和治疗相关变量,以确定它们在维持期间与AKD发展的关系(表4).同样,每单位5 mL·min−1每1.73米2,维持前和诱导治疗前较高的eGFR值与维持期间较低的AKD概率单变量相关(OR 0.64, 95% CI 0.48-0.84和OR 0.78, 95% CI 0.62-0.98)。此外,与基线相比,诱导期间eGFR下降10%与AKD风险增加有关(OR 1.56, 95% CI 1.03-2.36)。
讨论
在晚期NSCLC患者的生存受益的新药物加速开发和适应的时代,确定哪些患者能够开始并继续多个治疗线变得越来越重要。我们的研究表明,在培美曲塞维持治疗期间,人们对保持足够的肾功能存在严重的担忧,这可能会使患者接受次优的肿瘤治疗。在现实环境中,三分之一的转移性NSCLC患者在培美曲塞维持治疗期间发生AKD,其中一半患者被迫停止维持治疗。此外,大多数AKD患者的肾功能没有恢复(或仅部分恢复),这些患者发展为CKD。重要的是,这些结果在接受培美曲塞维持治疗的晚期NSCLC患者的独立队列中得到了验证。
在培美曲塞维持治疗期间,观察到患者每5 mL·min发生AKD的风险降低约20%−1每1.73米2诱导治疗开始前eGFR升高。发生AKD、CKD和停止维持治疗的患者比例在肾功能受损患者中显著增高(eGFR <90 mL·min)−1每1.73米2)在维修开始和入职前。已经认识到,肾功能下降,即使是轻度下降,也可导致化疗诱导的肾毒性[15,29].年代装配等.[30.]还报道了维持治疗前肾损害与停用培美曲塞和贝伐单抗双重维持治疗的更高概率之间的联系。与我们的研究相反,他们没有发现诱导前肾功能与治疗停止之间的关联。此外,诱导前肾功能数据缺失近20%,eGFR <60 mL·min的患者较少−1每1.73米2在该研究的基线时,贝伐单抗导致肾损害的不同病理生理可能解释了这种差异。
在培美曲塞维持期间,诱导治疗期间eGFR每下降10%,患者发生AKD的风险比基线高2倍。接受CISPEM治疗的患者eGFR下降了~ 10 mL·min−1每1.73米2,这与近期接受顺铂治疗多种肿瘤类型患者的研究结果相当[13].在整个维持期,诱导治疗期间使用CISPEM治疗与AKD无关,因此维持期间的肾毒性不太可能仅仅是一种延迟性顺铂效应。这得到了对包括肺癌在内的各种癌症类型患者的随访研究结果的支持,这些研究表明,在停止顺铂治疗后,eGFR的下降并没有恶化[13,31].虽然没有统计学意义(p=0.06),但接受培美曲塞维持周期较多的患者更容易发生AKD。培美曲塞的累积系统剂量可能在这些患者肾毒性的发展中发挥作用,最近也由L愤怒et al。[32].
培美曲塞的肾毒性潜能已在先前的临床研究中描述过。在关键的派拉蒙审判中[3.], Pujol等.[24]根据CTCAE 3.0, 7.8%的患者出现了全等级的肾毒性,4.5%的患者在培美曲塞维持期间因肾损害而停止治疗。考虑到患者数量较少,我们的研究注意到使用CTCAE 3.0与AKD (KDIGO)相比可能低估了肾毒性。考虑到肌酐的绝对增加和相对基线的增加,更新的CTCAE 4.03的结果与AKD的结果更吻合。此外,与我们的现实生活人群相比,PARAMOUNT试验中的患者群体是根据东方肿瘤合作组的表现状况、基线时的肾功能和伴随药物进行高度选择的。因此,该试验可能低估了日常实践中肾功能不全的风险。虽然培美曲塞维持与贝伐单抗联合使用,因此结果不能完全归因于培美曲塞,S装配等.[30.]报告了导致17%患者停止治疗的肾不良事件。
由于在主要和独立队列中,每个亚组的事件率较低,我们无法进行多变量分析,以确定维持治疗期间与AKD发展相关的患者和治疗相关变量。由于两个队列在肾功能数据收集的频率和时间上存在设计上的差异,我们认为不适合对这些队列进行联合分析。我们不能排除铂化合物的影响,因为所有患者在诱导治疗期间都接受了CISPEM或CARPEM,没有培美曲塞单药治疗比较臂。
总之,这项在现实生活环境中的研究结果表明,晚期NSCLC患者在培美曲塞维持治疗期间有发生肾损害的风险。这具有重要的临床后果,因为这些患者中的大多数会发展为CKD,约15-20%被迫停止维持治疗,进一步的抗癌治疗可能会受到危害。提高对高危患者肾脏保护策略的认识和进一步探索可能是有益的,例如在培美曲塞维持期间继续水化。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充附件erj - 00884 - 2018 - _supplement
图S1。在主要队列中,诱导治疗期间肾功能和AKD的发展(N=149)。A)平方:高危患者每周测量的中位eGFR四分位数范围。线:培美曲塞联合顺铂(实线)和卡铂(虚线)诱导时肾功能的变化。B)列:培美曲塞联合顺铂(填充)和卡铂(模式)诱导期间发生急性肾脏疾病的危险患者每周百分比。AKD:急性肾脏疾病;eGFR:估计肾小球滤过率;CISPEM:顺铂联合培美曲塞;CARPEM:卡铂联合培美曲塞;PD:进行性疾病; RT: radiotherapy.erj - 00884 - 2018 - _figure
确认
我们感谢Hans in ' t Veen (Franciscus Gasthuis & Vlietland,鹿特丹,荷兰)提供的数据。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:S. Visser报告了ZonMw(资助号152001017)在研究进行期间的资助。
利益冲突:J. Huisbrink没有什么可透露的。
利益冲突:N.E. van ' t Veer没有什么可透露的。
利益冲突:j·j·范·图尔没什么可透露的。
利益冲突:a。j。m。范。波塞姆没什么可透露的。
利益冲突:N.C. van Walree没什么可透露的。
利益冲突:B.H. Stricker报告了ZonMw(资助号152001017)在研究进行期间的资助。
利益冲突:在研究进行期间,J.G.J.V. Aerts报告了来自ZonMw的资助(资助号152001017);在提交的工作之外,他还担任礼来公司、罗氏、百时美施贵宝、默沙丹和勃林格殷格翰的顾问/顾问职位。
支持声明:这项工作得到了荷兰卫生研究与发展组织(ZonMw)的支持(资助号152001017)。本文的资助信息已存入交叉参考基金注册.
- 收到了2018年5月12日。
- 接受2018年8月8日。
- 版权所有©ERS 2018