摘要
虽然一些全基因组关联研究(GWAS)已经调查了肺通气功能的遗传,但对影响气体交换的遗传因素知之甚少。本研究的目的是调查遗传的可能性,和遗传变异与肺扩散能力。
GWAS是通过测量肺的一氧化碳吸收能力(dLCO)和每肺泡容量(V一个)使用单次呼吸技术,在8372个人从两个人口为基础的队列研究,鹿特丹研究和弗雷明汉心脏研究。遗传相关估计(N = 6246)和不相关的(N = 3286)的个体。
遗传的dLCO和dLCO/V一个23%和在无关个体28%之间和45%,而在相关个体49%之间。Meta分析鉴定基因变体中ADGRG6即显著关联dLCO/V一个。基因表达分析ADGRG6在人肺组织显示在慢性阻塞性肺疾病(COPD)和受试者降低的表达具有降低的dLCO/V一个。
dLCO和dLCO/V一个是可遗传的性状,方差的相当大的比例是由遗传解释。在功能变体ADGRG6基因区域与dLCO/V一个。肺ADGRG6慢性阻塞性肺病患者的表达降低。
摘要
这是第一个基于种群遗传力和GWAS的气体交换研究。我们鉴定了ADGRG6的一种功能性变异,并证实慢性阻塞性肺病患者的肺组织中存在表达差异和扩散能力下降。http://ow.ly/Rvy430kHIT4
介绍
呼吸系统功能上可以分为两个区域。第一个是导电区,其中包括气管,支气管,细支气管和终末细支气管和其在通风功能,即引导空气进出肺部。第二个区域是呼吸区,它由呼吸性细支气管、肺泡管和肺泡组成,是肺和血液之间交换氧气和二氧化碳的地方。
不同的肺功能测试可用于测量这些不同的通气和气体交换功能。这些测试有助于评估和管理有呼吸道症状和疾病的病人,包括肺活量测定、肺容积测量和肺一氧化碳扩散能力(dLCO)。后者,也被称为肺一氧化碳的转移因子,提供了在肺气体转移的定量量度[1,2],反映在肺泡隔和肺部微循环过程。
该dLCO提供临床见解互补通过肺活量测定和肺容积的测量所获得的那些,例如,在判别从慢性阻塞性肺病(COPD)哮喘,以识别低氧血症或呼吸困难的原因,并监测患者的间质性肺病[3]。dLCO在肺气肿患者中,由于肺总表面积的减少和毛细血管床的损失[1,4]。与此相反的丰度全基因组关联研究(GWAS)调查的肺功能检查措施的遗传变异[五-8],的遗传力,和遗传影响dLCO在很大程度上是未知。
因此,我们首先研究的遗传dLCO来理解方差的比例dLCO可以用遗传学来解释。接下来,我们进行了GWAS,以确定影响变异的遗传变异dLCO该研究使用了来自鹿特丹研究和弗雷明汉心脏研究这两个前瞻性人群的数据。最后,我们研究了慢性阻塞性肺病(COPD)和(非吸烟和吸烟)对照个体肺组织中铅- GWAS相关性的表达。
方法
这里简要地描述了这些方法;指的是补充材料更详细的信息。
设置
本荟萃分析相结合,从两个基于人口的研究结果,即鹿特丹研究和弗雷明汉心脏研究。在这两个队列中,只有欧洲血统的个体被纳入分析。鹿特丹研究[9] is an ongoing prospective population-based cohort study that includes three cohorts encompassing 14 926 participants aged ≥45 years, living in the Netherlands.dLCO是在2009年到2013年之间测量的。鹿特丹研究已经获得伊拉斯谟医学伦理委员会和荷兰卫生、福利和体育部的批准,实施了Wet Bevolkingsonderzoek: ERGO(人口研究法案:鹿特丹研究)。
弗雷明汉心脏研究是一项基于人口的家庭研究,从1948年开始招募弗雷明汉(马萨诸塞州,美国)的居民。dLCO在后代世代(2005-2008和2011-2014)和第三代队列(2002-2005和2008-2011)的第一和第二检查的第八和第九检查测量。对于参与者在两个时间点的测量,我们分析了以后测量。弗雷明汉心脏研究已获得美国波士顿大学医学校园的机构审查委员会。所有参与者都提供了书面知情同意参加研究,并获得他们的治疗医师的信息。
肺功能
dLCO(毫摩尔·分钟-1·帕-1)和肺泡体积(V一个)用单次呼吸技术按照欧洲呼吸协会/美国胸科协会指南[测量188bet官网地址2]。该dLCO每肺泡体积(dLCO/V一个;更易·敏-1·帕-1·L-1)是通过除以dLCO通过V一个。分析仅限于两种可解释和可重复测量的参与者dLCO和dLCO/V一个。
遗传分析
遗传被定义为特征方差的比率由于占变量后加性遗传效应的总表型变异。在鹿特丹研究,GCTA软件[10]被用来估算无关个体遗传。在弗雷明汉心脏研究,SOLAR(连续寡基因连锁分析程序)软件[11]用于基于家族关系估计遗传力。分析调整了年龄,性别和遗传相关的主要成分(只在GCTA)。在随后的分析中对目前和以前的吸烟情况进行了额外的调整。
GWAS分析
两种表型均行GWAS检查dLCO和dLCO/V一个使用ProbABEL(0.4.4版本)。与插补质量(R变2) <0.3和小等位基因频率(MAF) <0.01。对每个单核苷酸多态性(SNP)进行线性回归,假设有一个可加模型。所有的分析都在模型1中调整了年龄、性别和主要成分(鹿特丹研究),在模型2中调整了吸烟、体重和身高。在弗雷明汉心脏研究分析中,模型中加入了一个随机效应来解释家庭关系。使用METAL软件(www.sph.umich.edu/csg/abecasis/metal/)并且进行了调整的基因组控制。全基因组显着性阈值设置为p-值<5×10-8p值为5×10时的提示关联7。使用R软件生成分位数图、曼哈顿图和区域图。在鹿特丹研究中,血红蛋白校正后重复分析;2)额外调整1 s用力呼气量(FEV)1)/forced vital capacity (FVC) and 3) additional adjustment for quantitative emphysema (less than −950 LAA on computed tomography scan of the lungs), as measured in the Framingham Heart Study within 8 years of the lung function measurement.
后续分析
为了探索感兴趣的变异和基因的功能,并将这些新发现的位点与临床相关的疾病结果联系起来,采取了几个步骤,如下所示。1)研究遗传相关性;2)利用与COPD显著相关的snp研究了遗传重叠[12]和肺气肿[13];3)利用FINEMAP软件计算领先SNP的后验因果关系概率[14];4)铅SNP的调节功能进行了探索的Haploreg服务器上(http://archive.broadinstitute.org/mammals/haploreg/haploreg.php);5)利用基因型组织表达(GTEx portal)的肺组织数据集(expression quantitative trait loci, eQTL),检测SNP引物对mRNA表达的影响(expression quantitative trait loci, eQTL)。www.gtexportal.org/home/;GTEx门户eQTL数据,从位置的javascript获得肺组织组:portalClient.browseDatasets.downloadFile( 'Lung.allpairs.txt.gz', 'gtex_analysis_v7 / single_tissue_eqtl_data / all_snp_gene_associations / Lung.allpairs.txt.gz'));6)组织特异性基因表达在GTEx门户检查;和7)的mRNA表达ADGRG6基因在肺组织中进行分析(使用实时PCR)的92例患者具有或不COPD。
结果
研究队列和参与者的特点
研究人群的一般特性(鹿特丹研究和弗雷明汉心脏研究)显示在表1。平均±SDage was 67.3±8.0 years in the Rotterdam Study and 52.8±14.8 years in the Framingham Heart Study.图1显示参与者的研究流程。
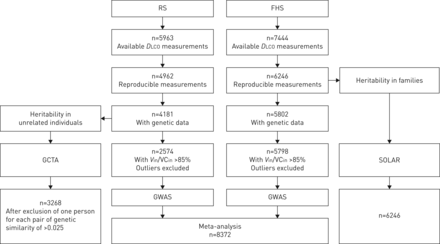
研究参与者流程图。拉尔夫-舒马赫:鹿特丹研究;FHS:弗雷明汉心脏研究;dLCO:扩散肺一氧化碳的能力;V在:吸气量;风投在:最大吸气过程中测量肺活量;GWAS:全基因组关联分析;GCTA:全基因组复合性状分析软件;太阳能:连续寡基因连锁分析程序包。
遗传
遗传估计两种方式;首先使用与个人无关的鹿特丹研究的数据,与3286名参与者与遗传数据和解释测量总数dLCO;其次,基于在6246名参与者的解释测量家庭关系使用从弗雷明汉心脏研究的数据来估计遗传dLCO(图1)。在表2遗传可能性估计dLCO和dLCO/V一个介绍。在不相关的个体,我们发现了一个年龄和性别和主成分调整遗传dLCO的23%,和28%后当前和过去的吸烟额外调节的遗传力。类似的遗传率被发现的dLCO/V一个与调整年龄,性别和主成分后24%,和之后用于吸烟附加的调整的25%。在弗雷明汉心脏研究,调查个人已知家族的关系,我们发现了一个年龄和性别调整遗传dLCO在对现在和过去的吸烟进行额外调整后,遗传率为47%。遗传可能性估计dLCO/V一个分别为45%(经年龄和性别调整后)和46%(经现时及过去吸烟情况进一步调整后)。
遗传变异体与扩散相关联的能力
我们表演了GWAS ondLCO和dLCO/V一个鹿特丹研究(N = 2574)和Framingham心脏研究中(N = 5798),并且随后的元分析两个群(N = 8372)。所有具有p值变体<5×106在荟萃分析阶段都表3。相应的位数,位数图在介绍补充图E1。单独的队列的GWAS结果与(p值<5×106),在被呈现补充表E1和E2。
对模型1中的年龄、性别和主要成分进行了调整。在模型2中,除了体重、身高、现在和过去的吸烟情况外,还对模型1中的变量进行了调整。
图2代表曼哈顿的阴谋dLCOGWAS在元分析层面。对于这两个dLCO分析(模型1和2),无变体达到全基因组显着性的阈值。在模型2中,两个在10q22.1(rs1665630,基因变体CDH23我们是0.44;p-值= 2.8×107),并在20p12.3(rs2423124,靠近基因GPCPD1,MAF 0.19;p-值= 4.2×107)显示出一种暗示的联系dLCO。
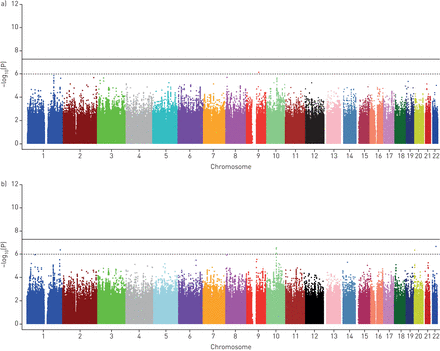
与扩散肺容量为一氧化碳(相关的常见遗传变异体dLCO)。一)常见的遗传变体和之间的关联的曲线图曼哈顿dLCO,调整后的年龄,性别和遗传相关的主成分;B)普通遗传学之间的关联曼哈顿情节和变种dLCO,调整后的年龄,性别,体重,身高,吸烟和遗传相关的主要部件。
图3代表曼哈顿的阴谋dLCO/V一个GWAS在元分析层面。在相同的基因座19点的变体在6q24.1(顶部:rs17280293,基因ADGRG6,MAF 0.03;p-值= 1.4×10-10年)显著相关dLCO/V一个在模型1中(参见区域图)图4)。其中,6q24.1位点相同的6个变异在模型2中达到全基因组显著性阈值。通过调整FEV进行敏感性分析1/FVC没有解释rs17280293与dLCO/V一个(β±SE =−0.07±0.01,p = 1.51×10-10年调整FEV后1/ FVC与β±SE= -0.07±0.01,p值= 7.9×10-11年FEV调整前1在模型2 / FVC)(补充图E2)。同样,在弗雷明汉心脏研究(n=2176)的一个亚组中,对定量肺气肿(肺部ct扫描<−950 LAA)进行调整并没有改变rs17280293和dLCO/V一个(β±SE= -0.06±0.02,p值= 0.003调整肺气肿后与β±SE= -0.06±0.02,p值= 0.002调整肺气肿之前)。此外,在这两种模式,在5q12.1一个变种(rs918606,基因IPO11我们是0.44;假定值模型1 = 5.96×108,p-value-model 2 = 7.49×108)被发现与被暗示性地相关联dLCO/V一个。通过调整血红蛋白血药浓度进行的附加敏感性分析并没有显著改变本研究的结果dLCO/V一个GWAS (补充材料)。
与扩散肺容量为一氧化碳(相关的常见遗传变异体dLCO)每肺泡容积(V一个)。一)常见的遗传变体和之间的关联的曲线图曼哈顿dLCO/V一个,调整后的年龄,性别和遗传相关的主成分;B)普通遗传学之间的关联曼哈顿情节和变种dLCO/V一个,调整后的年龄,性别,体重,身高,吸烟和遗传相关的主要部件。
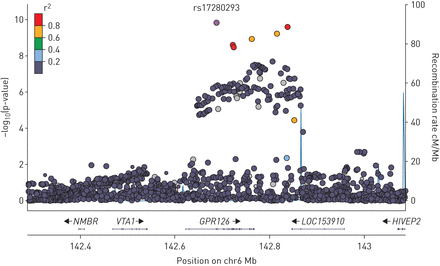
在用于扩散肺每肺泡容量一氧化碳的容量的全基因组关联研究的全基因组基因座显著区域关联曲线图。
有趣的是,一个更深入的调查ADGRG6区域(图4)显示存在两个误义变异:领先的SNP rs17280293和rs11155242 (MAF 0.19, p-value=2.1×10-06年)。显示,那些两个SNP是在连锁不平衡对方,其中r2= 0.14和d'= 1。
后续分析
后续分析的最重要的发现总结如下,包括遗传相关性和肺组织中的基因表达。对遗传相关附加结果与报道的COPD和肺气肿GWAS协会,因果关系的后验概率,功能注释和基因表达重叠在被呈现补充材料。
遗传相关
我们研究之间的遗传相关dLCO/V一个和dLCO使用年龄、性别、吸烟状况、体重、身高和主要成分调整模型。遗传相关性为59%(ρgenetic = 0.59, p = 0.04)。这与之间的表型相关是一致的dLCO和dLCO/V一个(右2Rotterdam研究和r = 0.46的2在Framingham心脏研究,p值<0.01)= 0.57。此外,我们审查了FEV的遗传相关性1/ FVC和高度(补充材料)。
ADGRG6表达
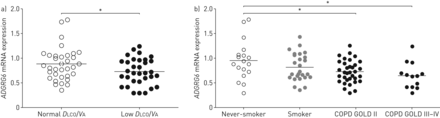
我们提取的mRNA从92例肺切除标本谁接受手术治疗孤立性肺肿瘤或肺移植,其中44例无慢性阻塞性肺病和48例慢性阻塞性肺病(表4)。mRNA的表达ADGRG6患者肺组织中显著降低与降低dLCO/V一个与正常的患者相比,dLCO/V一个(图5a)和COPD患者(根据相对于从不吸烟控制全球慢性阻塞性肺疾病肺功能分类)包含不同种类COPD严重度的(图5b)。该ADGRG6mRNA水平与dLCO/V一个在模型1(N = 67,β= 0.85(95%CI 0.06-1.64))和之后对体重,身高附加调整和模型2(N = 66吸烟,β= 0.75(95%调整年龄和性别之后CI 0.03-1.47))。
肺组织mRNA表达ADGRG6在人类主题。a) mRNA水平ADGRG6在有正常肺一氧化碳扩散能力的人的肺组织中(dLCO)每肺泡容积(V一个)(N = 38)和低dLCO/V一个(N = 39)。使用基于三个参考基因mRNA表达(计算的归一化因子的mRNA水平进行校正GAPDH,SDHA,HPRT-1);b) mRNA水平ADGRG6在不吸烟者(n=18)、无气流限制吸烟者(n=26)、慢性阻塞性肺病全球计划慢性阻塞性肺病II期(GOLD)患者(n=34)和慢性阻塞性肺病III-IV期(n=14)患者的肺组织中,使用定量逆转录酶- pcr进行测量。统计分析采用Kruskal-Wallis检验和Mann-Whitney u检验,COPD采用独立样本t检验dLCO/V一个后级改造。*:P <0.05。
讨论
这是第一个利用基于人群的队列研究来调查肺的遗传力和全基因组关联的研究。我们发现肺部扩散能力的很大一部分差异是由遗传因素造成的。我们还确定了6号染色体上的一个基因座,包括ADGRG6基因,与dLCO/V一个与同一区域的其他snp相比,其前导变异具有较高的后验概率。最后,我们能够连接的肺表达ADGRG6直接到慢性阻塞性肺病和低dLCO/V一个(适用于一般人群的肺气肿)。在这里,我们展示了一个差异的mRNA表达ADGRG6COPD患者和患者的肺组织中具有降低的dLCO/V一个。
遗传和遗传重叠
研究的遗传dLCO在一般人群和无关个体缺乏,到目前为止,dLCO遗传力只在双胞胎中研究过[15,16],其中44%的最高的报告估计。在我们的研究中,我们估计的最大限制基于可能性遗传dLCO使用在鹿特丹研究[无关个体的GCTA工具17],和观察到的年龄和性别调整后的遗传dLCO和dLCO/V一个的分别为23%和24%。基于弗雷明汉心脏研究中已知的家族关系,我们还研究遗传。在这里,我们发现的年龄和性别调整遗传dLCO和dLCO/V一个的分别为49%和45%。家族相关的个体间的遗传后者估计是在双胞胎研究的遗传率线和突出我们的数据的可靠性。重要的是,我们的研究第一次调查下界遗传的dLCO通过家庭和双生子研究[估计18]。估计的优势遗传无关个体使用GCTA除了方法基于家庭和双生子的研究,GCTA计算遗传的比例,涵盖了下议院的添加剂影响单核苷酸多态性,并且不受偏见由于上位相互作用或共享环境。后一种效应可能确实存在于家庭和双胞胎研究中,导致对遗传可能性的高估[18-20]。
尽管他们对遗传可能性的估计相似,dLCO和dLCO/V一个似乎有不同的遗传决定因素,这是由于59%的人的两种性状的遗传重叠,这解释了为什么我们在两种分析中没有观察到相同的铅关联。
的变化ADGRG6
遗传变异的元分析dLCO/V一个产生一个全基因组关联显著,有一个数字,没有达到全基因组显着性暗示协会一起。在这项研究中铅变种(rs17280293)是一个错义SNPADGRG6,其MAF值为0.03,与公共数据集(0.03 ExAC、0.02 TOPMED和0.03 in 1000个基因组)中的MAF值相当。该SNP的突变导致了氨基酸的变化(S123G),根据SIFT [21]和Polyphen2 [22]。因此,很可能这是SNP在功能ADGRG6。在这项研究中,我们发现这种变体具有很高的后验概率因果关系比其他单核苷酸多态性在同一地区,这SNP与不同监管染色质标记,催化剂在不同组织细胞组蛋白标记和增强器组蛋白标记线包括胎儿肺纤维母细胞细胞系和肺癌细胞株。此外,rs17280293始终与该区域的另一个功能SNP (rs11155242, D ' =1)同时发生,是一个eQTLADGRG6在人类肺组织中。
以前的研究也表明,在ADGRG6与肺功能的肺功能措施[相关联五,7]。小号奥立一个rtigas等。[7]观察到肺活量之间有很强的相关,特别是FEV1/FVC,另一个SNP rs148274477,与rs17280293存在强连锁不平衡。然而,由于气流的限制(即低FEV1/ FVC比)可能具有低扩散能力由于与肺气肿受试者弹性回缩的损失相关,我们评估的可能性,rs17280293和之间的观察到的关联dLCO/V一个可能由FEV驱动1/ FVC。然而,这一敏感性分析表明rs17280293和之间的独立联系dLCO/V一个因为FEV的额外调整1/植被覆盖度不影响估计数,也不能证明两者之间存在遗传重叠dLCO/V一个和FEV1/ FVC。其他研究也发现了基因变异ADGRG6与高度。在我们的研究中,身高的调整并不影响两者之间的联系dLCO/V一个和rs17280293,这表明我们的GWAS领先协会是独立的高度。此外,遗传重叠后在模型中高度附加调整消失,表明通过高度在我们的分析没有残余混杂。
此外,Eichstaedt等。[23来自19个阿根廷高地最近使用的全基因组序列数据相比,16个美国本土平地,并表明,rs17280293可能有助于生理适应于低压缺氧。
基因功能和表达
该ADGRG6基因(粘附g蛋白偶联受体G6)属于g蛋白偶联受体(GPCR)超家族,是人类基因组中已知最大的受体家族。它在血管生成中已经被证明是必不可少的[24]。ADGRG6,一个相对较新的粘附性GPCR,已经被证明可以通过调节内皮生长因子受体2 (VEGFR2)的表达来促进血管内皮生长因子(VEGF)信号传递。自ADGRG6是否参与血管生成,这对胎儿时期肺毛细血管床的发育至关重要ADGRG6导致妊娠中期胚胎致死因心血管发育失败。的气流受限的肺功能措施GWAS(FEV1/植被覆盖度比)表明了几个基因和通路参与了分支的形态形成和肺的发育,暗示了复杂的成人呼吸系统疾病(如COPD)的早期生命起源。有趣的是,这个GWAS的肺扩散能力(dLCO和dLCO/V一个)也表示一个基因(ADGRG6),其在胎儿期心肺发展中有牵连。
的调制效应ADGRG6上VEGFR2表达被证明是通过转录激活的STAT5和GATA2[24]。有趣的是,GATA2最近被链接到肺泡蛋白沉积症[25],是一种罕见的肺部疾病,其特征是肺泡内的肺表面活性物质异常积聚,导致气体交换改变。
此外,敲下来ADGRG6在小鼠视网膜显示导致缺氧诱导的血管发生的抑制[24]。这个信息是在两个方面有趣的:首先,它链接ADGRG6对缺氧,这是非常相关的气体交换;第二,视网膜上的过程可能提供对肺微血管系统的独特见解,因为视网膜和肺泡中的血管变化反映了非常相同的过程,即微血管病。
尽管有大量的证据表明ADGRG6在肺发育和微血管病,mRNA的表达是重要的ADGRG6尚未研究在肺病如COPD和降低的扩散能力。因此,我们进行的表达分析ADGRG6在人肺组织,并表明的mRNA表达ADGRG6慢性阻塞性肺病患者和a型糖尿病患者是否有显著下降dLCO/V一个。
优点和局限性
我们使用了两个基于人口的研究的数据进行分析;鹿特丹研究和弗雷明汉心脏研究。这些研究的优势在于以人群为基础的设置,包括来自吸烟者和非吸烟者的数据,以及标准化的前瞻性数据收集。我们不知道其他基于人群的队列研究dLCO基因型个体的数据可用。因此,在其他基于人群的群组中复制是不可能的。然而,鹿特丹研究和弗雷明汉心脏研究的独立分析结果表明,rs17280293在弗雷明汉心脏研究中已经达到全基因组意义,并在鹿特丹研究中进行了重复。最后,在我们的实验室中对肺组织进行了基因表达分析。
这项研究有一定的局限性。首先,用于扩散能力的测量,使用单次呼吸技术。这种技术是已知的的低估测量V一个在患有阻塞性疾病或空气滞留的个体中,因为扩散能力无法在肺的不通风区域测量。人们也知道,对……的低估V一个将更大更严重的慢性阻塞性肺病,少在温和的慢性阻塞性肺病。然而,在我们的人口为基础的队列中,有重度COPD少数人,从而降低了低估的影响V一个在我们的研究。其次,血红蛋白校正dLCO措施只适用鹿特丹研究进展。然而,有或无修正血红蛋白没有实质性改变鹿特丹研究中的结果进行敏感性分析。三,rs17280293和rs11155242之间的高d'可能意味着联变种出现。然而,高d'的那些变体之间,使用从1000基因组参考板的数据估计,可能会导致从d的充气估计'由于SNP的低频。对于这一点,这将是有帮助的估计d'在一个更大的参考板,如单倍型参考财团当该信息变得可用。最后,在这项研究中,我们控制了FEV1/ FVC在我们的模型。此外,我们研究了气体交换和FEV之间的遗传相关1/ FVC。同时控制FEV1/FVC在我们的分析中提出了令人信服的证据,表明rs17280293与dLCO/V一个在全基因组中,扩散能力与FEV之间缺乏遗传相关性1/FVC不排除该位点的多效性,因为遗传相关分析受功率影响,且我们的GWAS样本量相对较小。因此,在解释这些结果时需要谨慎。
结论,dLCO和dLCO/V一个是遗传性状,在肺扩散能力上有相当大的差异,可用遗传学来解释。我们发现了一个功能性变异ADGRG6,该基因参与气体交换和缺氧,在COPD患者和扩散能力下降的受试者肺组织中差异表达。因此,需要通过实验研究来探讨其病理生理机制及其治疗意义。
补充材料
确认
作者感谢研究参与者,从鹿特丹研究人员和参与全科医生和药剂师。鹿特丹研究GWAS基因型数据的生成和管理(RS I,II RS,RS III)由内科,伊拉斯谟MC,鹿特丹,荷兰系的遗传实验室的基因分型人执行基金。我们感谢Pascal ARP,米拉Jhamai,Marijn沃克,Lizbeth埃雷拉,Marjolein彼得斯,和北卡罗来纳州梅迪纳 - 戈麦斯为他们在创建GWAS数据库的帮助下,和卡罗尔埃斯特拉达,尤里Aulchenko和北卡罗来纳州梅迪纳 - 戈麦斯为创建和估算数据的分析。数据可以根据要求而得到。申请应朝鹿特丹研究(secretariat.epi@erasmusmc.nl),其中有审批数据请求的协议的管理团队为目标。因为基于隐私法规和参与者的知情同意限制的,数据不能在公共库中免费提供。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
作者投稿:N. Terzikhan,F. Sun和J.杜普伊斯遗传分析和全基因组关联分析的数据。L. Lahousse促成了数据质量控制。N. Terzikhan,H.H.H.亚当斯,L. Lahousse和G.G.Brusselle设计研究。L. Lahousse,J.杜普伊斯,G.G.Brusselle和G.T.奥康纳监督研究。调频。Verhamme和K.R. Bracke performed and analysed the gene expression study. K.R. Bracke supervised the gene expression study. N. Terzikhan, F. Sun and F.M. Verhamme wrote the manuscript. All authors contributed equally to revising the manuscript.
利益冲突:l . Lahousse报告个人费用从勃林格殷格翰集团GmbH是一家咨询公司,住宿支持和个人费用咨询公司从诺华,从阿斯利康赠款,差旅补助和住宿欧洲呼吸协会的支持,赠款和住宿比利时呼吸社会的支持,从基耶西和赠款,在提交工作。188bet官网地址
利益冲突:G.T. O’connor报告了从阿斯利康公司获得的关于哮喘和慢性阻塞性肺病药物的个人咨询费,以及从詹森制药公司获得的波士顿大学研究慢性阻塞性肺病基因组学的拨款。
支持声明:这项工作得到了科学研究基金Flanders (FWO)项目(G035014N)的资助。Verhamme是佛兰德斯科学研究基金(FWO)的博士后研究员。鹿特丹研究由鹿特丹伊拉斯谟学院和伊拉斯谟大学资助;荷兰卫生研究与发展组织(ZonMw);老年疾病研究所(RIDE);教育、文化和科学部;卫生、福利和体育部;欧洲委员会(DG XII);以及鹿特丹市政府。GWAS的数据集由荷兰科研组织NWO投资支持(编号175.010.2005.011,911-03-012),内医学系遗传实验室,伊拉兹马斯医学中心,老年疾病研究所(014-93-015; RIDE2), the Netherlands Genomics Initiative (NGI)/Netherlands Organisation for Scientific Research (NWO) Netherlands Consortium for Healthy Aging (NCHA), project number 050-060-810. The Framingham Heart Study was supported by the National Heart, Lung, and Blood Institute's Framingham Heart Study (contract number N01-HC-25195 and HHSN268201500001I) and its contract with Affymetrix, Inc., for genotyping services (contract number N02-HL-6-4278). Also supported by NIH P01 AI050516. Research from the Laboratory for Translational Research in Obstructive Pulmonary Diseases in Gent is supported by the Concerted Research Action of the Ghent University (BOF/GOA, 01G02714).
- 收到了2018年4月4日。
- 公认2018年6月22日。
- 版权©2018人队