抽象的
背景慢性早产儿肺疾病(Chronic lung disease of prematurity, CLD),又称支气管肺发育不良,是早产的主要后果,但微生物组在其发展中的作用尚不清楚。因此,我们评估了通气早产儿上、下气道细菌群落随时间的进展,并通过比较上、下气道细菌群落与粪便发现来评估肠-肺轴。最后,我们评估了细菌群落是否与肺部炎症相关,以提示生态失调。
方法我们连续采样通气早产,出生的婴儿多的解剖部位,包括上呼吸道(鼻咽抽吸),下呼吸道(气管吸液和支气管肺泡灌洗液)和肠道(粪便)。细菌DNA负荷所有样品中测量和使用16S rRNA基因的V3-V4区测序。
结果从1102(539鼻咽抽吸,276气管吸出流体,89支气管肺泡灌洗,198粪便)的样品从16S RNA基因测序适当扩增55名早产儿,352(32%)。细菌负荷是在出生时低,并用时间迅速增加,但在所有样品类型主要操作分类单元(的OTU)相关联。有相异在上和下呼吸道和肠道细菌之间社区,在婴幼儿的下气道中产生的单独的dysbiotic炎症过程。个人的OTU用增加炎症标志物相关。
结论综上所述,这些发现表明对主要生物体进行靶向治疗,包括那些不常规治疗的生物体,例如Ureaplasma可降低早产儿慢性肝病的发展。
抽象的
出生后获得呼吸殖民化并与促炎症反应相关,表明婴儿出现过早产儿(CLD)的慢性肺病风险的传染性过程,从而提供减少CLD的靶标http://bit.ly/31C27iX
介绍
早产儿慢性肺疾病(Chronic lung disease of prematurity, CLD),也称为支气管肺发育不良,是早产儿受到许多早期生命因素影响的主要后果,包括在肺发育的早期阶段分娩、需要呼吸支持和补充氧治疗[1].我们以前已经证明优势细菌的存在可能与慢性肝病的发展有关通过肺部炎症通路[2,3.].此外,特定生物如Ureaplasma与慢性肝病的发病机制密切相关[4,5],有一些证据表明消除了Ureaplasma可能会降低CLD的率[6].在足月出生的婴儿中,上呼吸道的早期细菌定植似乎在出生后几分钟内就出现了[7,但早产儿肺上、下气道的自然定植史尚不清楚[8].最近的系统评论[9选择早产婴儿的气道微生物组的发展提出了关于早产肺的细菌定植的问题,而不是随着现有研究的回答;没有研究调查了上航通道和胃肠道之间的联系,即。所提出的肠肺轴线,与早产儿的下气道。这六个研究包括[10- - - - - -15.]显示可变结果,例如一个报告从变形菌门进展到厚壁菌门,但另一个显示相反的进展。提供一个更全面的评估细菌社区在早产儿的风险开发CLD,我们研究1)连续多个解剖网站,包括获得气管吸入液体(TAF)和支气管肺泡灌洗(BAL)流体从通风早产儿评估气管和更低的航空公司,分别;和鼻咽部吸入物(NPA)和粪便样本,以评估通气早产儿上、下呼吸道细菌群落随时间的进展;2)评估粪便与上/下呼吸道的微生物关系;即。肠肺轴,目前没有学习的学习或早产婴儿;3)评估细菌群落与临床因素之间的关系,包括递送模式,性别,临床部位的采样和抗生素的影响;4)在所有样品类型中测量的促炎细胞因子白细胞介素(IL)-6和-8,并将研究结果与观察到的细菌社区相关。
方法
样品收集
从英国两个三级区域新生儿重症监护病房招募妊娠≤32周的早产儿。在常规气管插管(ETT)抽吸时采集TAF和NPA。根据我们之前的研究收集BAL样本[2,16.],并根据欧洲呼吸学会特别工作组的指导方针[188bet官网地址17.进行常规ETT抽吸时,如补充材料.在第一周期间,TAF,BAL和NPA样品在每周两次或直到拔管时收集,或直到拔管,以至于先发药。每周收集粪便样本直至生命的28天。道德批准(REF 14 / WA / 0190)是从威尔士研究伦理委员会2获得的,并从父母获得书面知情同意书。
DNA提取,细菌负荷和测序
DNA提取,细菌负荷和16S测序将在补充材料.根据已发表的方案,使用定量PCR方法对总细菌负荷进行定量[18.扩增16S rRNA基因的V3-V4区。对纯化的PCR产物进行定量,并将扩增充分的样品汇集到一起,建立扩增文库。分别为TAF、BAL、NPA和粪便样品准备了单独的库。每个文库在Illumina MiSeq (San Diego, CA, USA)设备上测序[19.].
数据分析
mothur v1.39.5 [20.]对测序数据进行处理,剔除嵌合序列和低质量reads,并以3%的差异将DNA序列数据分组为操作分类单元(OTUs)。小于1000 reads的样本被排除在外。核糖体数据库计划的参考数据库[21.]用于从王国到属族的每个OTU的系统发育鉴定。在进一步分析之前,每种样品稀释到1000读数的样品。统计学分析在R V3.4.2中进行(www.r-project.org)使用Phyloseq v1.20.0 [22.]和素食主义者(https://cran.r-project.org/web/packages/vegan/index.html).邮票v2.13 [23.]用来比较不同组之间的细菌谱。数据集在属水平合并,以比较不同解剖部位的微生物组概况。单个OTU代表>50% reads的样品被认为含有优势生物。
结果
在前28天内,从出生于≤32周的妊娠(中位数26.0周,24.7-27.5周24.7-27.5周)中出生的55个早产儿。包括539 NPA,276 TAF,89 BAL和198凳样品。人口统计数据显示在表格1,包括比较两个招聘中心(威尔士大学医院和北布里斯托尔信托基金)之间的数据。NBT招募的未成熟婴儿略多,尽管差异没有统计学意义(26.8与25..9 weeks, p=0.07). More patent ductus arteriosus were identified at NBT, since they screen for this condition. As expected with recruitment of only ventilated preterm infants, most infants developed CLD defined using the National Institute of Child Health and Human Development definitions [24.],84%发育中度至严重的CLD。
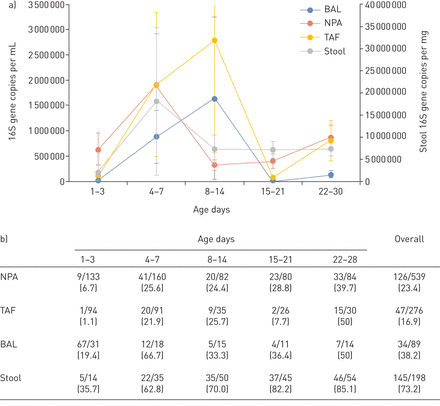
352(32%)1102个样品的16S rRNA基因对粪便(73%)样品的最大成功率和TAF(17%)样品(17%)(图1).在第1-3天,细菌载量较低,只有1.1%的TAF和6.7%的NPA样本成功测序了细菌16S rRNA基因。我们获得的粪便样本的成功率为35.7%,表明出生时的细菌载量较低,特别是在上呼吸道。尽管19.4%的BAL样本可用于DNA测序,但对这些样本使用较低的细菌DNA测序阈值(pcr后DNA扩增浓度为0.3 ng·µL−1TAF和NPA, 0.1 ng·µL−1对于BAL和0.5 ng·μl−1对于凳子)。在第4-7天的细菌载量达到BAL和TAF样品的第4-7天,并且在8-14天用于NPA和粪便样品。有趣的是,对于TAF和BAL样品,观察到类似的增加模式,如粪便和NPA样品(图1).
早产儿肠道和呼吸道的总细菌负荷。a)四个解剖部位的总细菌负荷随时间的变化:支气管肺泡灌洗(BAL)、鼻咽吸液(NPA)、气管吸液(TAF)和粪便样本。每mL上清液中测定16S RNA基因拷贝数中的BAL、TAF和NPA样本。每毫克粪便样本中检测16S DNA基因的拷贝数。数据以平均值±表示SE..b)显示每个样本类型的每个时间点的样品数量的表,以及在每个样品类型的每个时间点在每个时间点中成功扩增的样本的百分比。数据显示为n / n(%)。
去除低质量reads和嵌合序列后,TAF样本的平均(范围)reads为109 457 (8665-426 696);BAL样品44 548 (27-177 875);NPA样品60 295 (5951-222 539);粪便样本为59 329(1-481 757),读取值<1000的样本分别为0、2、0和39。阴性对照的最大reads分别为7558、588、580和206,其中1份TAF样本与阴性对照样本共聚而被丢弃。
所有样品中大部分的门,如图所示图2和总结补充图S1,为变形菌门和厚壁菌门;在TAF和BAL样本中也存在Tenericutes,在NPA样本中较少;在粪便样本中发现拟杆菌门,在NPA、TAF和BAL样本中较少出现。门TAF和BAL的模式样本在第一个月的生活保持静态,平均相对丰富∼变形菌门的40 - 50%,而NPA变形菌门和粪便样本的增加意味着相对丰富的NPA的15%和30%在凳子上生命第一周为46%和55%,分别到第三/第四周时(图2;汇总数据显示补充图S2).大多数样品含有单个显性门(> 50%从单门阅读)。在属的水平,葡萄球菌,如图3,是占所有样品的近30%的占主导地段(> 50%的单一属的读数)Klebsiella.,埃希氏杆菌属,未分类的肠杆菌,肠球菌和Serratia.占主导地位的是35%的TenericutesUreaplasma和支原体占所有样品的5.2%。虽然蛋白质体会增加和变压随着年龄的增长,但特别是在NPA(Proteobacteria P <0.001,Formicute P = 0.008; Kruskal-Wallis测试与Benjamini-Hochberg错误发现率)和粪便样本,Genus水平没有明显的变化模式,虽然上述属的主导地位是明显的。在Genus和Otu水平中,大多数样本中存在显性属/ otu,31个(91%)中的34只BAL样品中的31个(91%),47个TAF样品中的43(92%),122(97%)中的126个NPA如图所示图3.
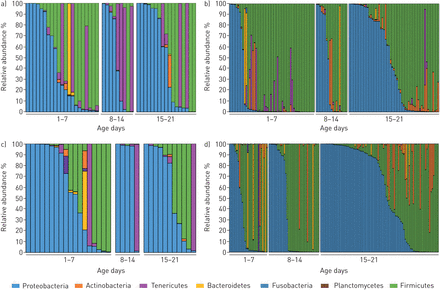
门所示每个样本部位的微生物组分析:a)气管吸液;b)支气管肺泡灌洗;c)鼻咽吸入;凳子和d)。早产儿优势门的相对丰度显示在每个时期。每个条形图代表一个样本,在将每个门的所有操作分类单元合并并平均后显示相对丰度。
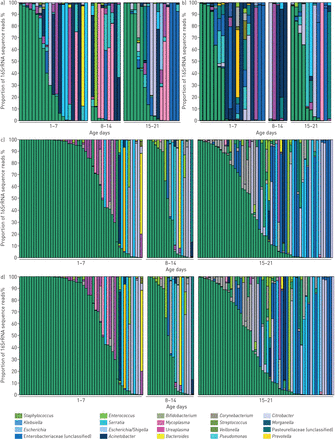
在属水平显示的每个样本点的微生物组分析:a)气管吸液;b)支气管肺泡灌洗;c)鼻咽吸入;凳子和d)。每个条形图代表一个样本,在每个属的所有操作分类单元合并后显示相对丰度。
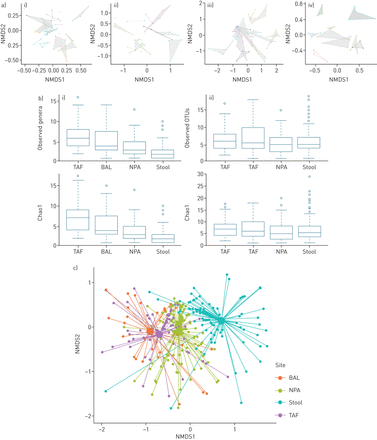
有趣的是,每个婴儿都有自己的细菌定植模式,这些模式在不同的婴儿个体和不同的解剖部位(图4一和c)。由于随着时间的推移没有整体模式,我们将来自每个解剖部位的样品整理,以进一步分析。观察到的属和Chao1指数的数量在样品类型之间不同,在BAL和TAF样品中更大(两个指数的P <0.001)(图4 b),但在Genus级别计算时,不是Shannon或Simpson的α-分集指数(数据未显示)。但是,在OTU级别计算时,观察到的OTU或Chao1没有差异(图4 b).BAL和TAF样品属和OTU水平的相似指数表明,这些样品中个体OTU占主导地位,但NPA和粪便样品属和OTU之间指数的增加表明这些样品的丰富度更高。TAF和NPA样品的β多样性分析没有显示出任何显著的随时间变化的模式(补充图S4).
样本点之间的微生物群落结构。一)非度量多维尺度(NMDS)曲线为每个样本点婴儿个体:1)气管吸出流体(TAF);ⅱ)支气管肺泡灌洗(BAL);ⅲ)鼻咽抽吸(NPA);和iv)粪便。每个有色多边形加入所有样品从单个婴儿。B)在一)属所示观察到的属/操作分类单元(的OTU)和超1和ii)操作分类单元水平的α-多样性。C)NMDS显示解剖部位的细菌群落之间的关系曲线。PERMANOVA显示BAL之间显著差异与TAF,落下帷幕与NPA,落下帷幕与凳子,TAF.与NPA, TAF与粪便和npa.与使用Bonferroni校正粪便(所有P <0.01)。
当alplenova的四种样品类型之间检查细菌社区时,彼此有显着不同,如图所示图4 c:落下帷幕与TAF;落下帷幕与NPA;落下帷幕与凳子;TAF.与NPA;TAF.与凳子;和NPA与凳子(p < 0.01)。
分娩方式影响足月新生儿在许多解剖部位的早期定植,在粪便样本中早产儿的有限数据中[7,25.,26.].分娩方式与革兰氏阴性属的增加有关(不动杆菌(p=0.04)假单胞菌(p = 0.06));支原体(p = 0.04)在TAF样品中;和Serratia.(p = 0.01)在阴道递送的婴儿的NPA中。对于剖腹产发行的婴儿,葡萄球菌在NPA中增加(p=0.02),而在TAF中则略有增加(p=0.056) (补充图S2a).但是,性别没有影响TAF或NPA细菌社区(补充图开通).各招募中心的细菌群落结构差异显著(p<0.05) (补充图S2c).这可以通过爆发部分解释不动杆菌在一个地点,导致更大不动杆菌在招聘中心观察到的。
在这两个招募中心,最初的预防性抗生素方案苄青霉素和庆大霉素是根据随后的微生物评估而改变的。276个TAF样本中有219个(79%)和539个NPA样本中有335个(62%)是在婴儿接受抗生素治疗时采集的(补充图S3).未使用抗生素的样本比使用抗生素的样本更有可能成功测序16S rRNA基因(OR 2.91, 95% CI 1.48-5.73;TAF p = 0.002;2.05和3.10,-4.67;p<0.0001的NPA样本)。在成功测序的TAF和NPA样品中,抗生素没有影响α-多样性,这表明它们在整体上抑制了细菌的生长,而不是抑制特定物种。然而,抗生素与Tenericutes的比例增加相关(p=0.03),可能是由于支原体,与无抗生素组相比,TAF样本中这一比例略有增加(p=0.059)。
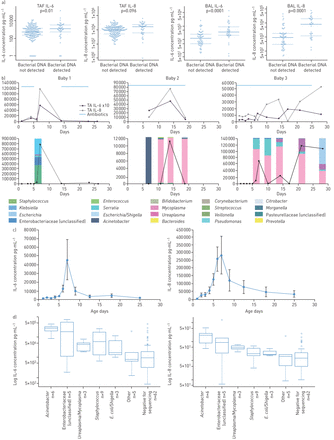
由于在大多数成功测序的样品中,单个OTU主要(> 50%的读数),因此可能是具有更大初始生物质的样本,我们在所有样品中测量IL-6和IL-8以评估样品中成功的细菌DNA检测是否是与炎症反应相关。在NPA和粪便液提取物中,IL-6和IL-8在很大程度上不可检测,但如果可以测序,则在BAL和TAF样品中以相当数量的数量指出,如图所示图5一个在TAF和BAL样本:TAF成功测序与不成功测序样品:IL-6 1222(534-3224)PG·毫升−1与539(217-1377)pg·ml−1;和IL-8 26 383(3460-51 740)PG·mL−1与9031 (2535-20 511) pg·mL−1;IL-6 3629 (2029-8538) pg·mL−1与1213(485-2459)pg·ml−1;IL-8 80 689 (12 303-196 477) pg·mL−1与9520.(3060–18 572) pg·mL−1(所有p < 0.001)。接下来,我们跟踪婴儿个体的动态变化,如图所示图5 b.每个婴儿的IL-6和IL-8都有间歇性的增加,这与细菌负荷的增加和占优势的OTUs的存在相对应。从20个断断续续的TAF IL-8峰值>50 000 pg·mL−1在19名婴儿中观察到,13名(65%)发作与细菌DNA的存在相关,在峰细胞因子浓度的24小时内。IL-6和IL-8均在7天的年龄显示峰值浓度,因为我们以前在婴儿开发CLD [2,3.,16.) (图5 c).最后,otus的主要优势如不动杆菌,未分类的肠杆菌和碎片,包括支原体和Ureaplasma与LAL中的IL-6和IL-8的最大增加强烈关联,比在无法测序的样本中的几倍图5 d).
下气道微生物群与炎症标志物的关联。)日志10在气管抽吸液(TAF)和支气管肺泡灌洗液(BAL)样本中,对细菌测序阳性或阴性的样本进行白介素(IL)-6和-8评分。b)上图中IL-6、IL-8、抗生素治疗(蓝色)与细菌载量(黑色)之间的关系,条形图显示了三个婴儿的属成分。一般情况下,尽管抗生素治疗,所有指标均观察到平行增加和减少。c)每个时间点TAF样本中IL-6和IL-8的平均值,无论细菌是否存在,如前所述,这两种细胞因子均在第7天出现峰值[2,3.,19.]数据显示为平均值±扫描电镜.d)IL-6和IL-8的BAL样品中示出的存在与特定的操作分类单元(的OTU)的关联增加了IL-6和IL-8,如果与阴性用于测序组时的OTU被确定。大肠杆菌:大肠杆菌.
讨论
在这项全面的纵向研究中,我们研究了有罹患慢性阻塞性肺病风险的早产儿的上、下气道,并将研究结果与一系列粪便样本相关联,以评估肠-肺轴。我们已经做了几个重要的观察:首先,在生命的最初几天,细菌DNA载量低,在生命的第一个月增加。其次,包括上、下气道在内的所有解剖部位都有自己独特的细菌群落模式,大多数情况下存在显性OTU,且解剖部位之间存在差异。第三,下气道的细菌群落与活跃的促炎期相关。第四,特异性OTUs与促炎细胞因子显著增加相关。
总体而言,对于细菌测序,从1102个样品中,31.9%(n = 352)令人满意地扩增。在寿命的前3天内,在所有样品中,细菌负荷低,但在Bal和TAF样品的生命中达到峰值,并且在粪便和NPA样品中的第8-14天。细菌习得最有可能来自具有阴道相关的微生物的母亲,包括在阴道递送的婴儿中占优势的十字葡萄球菌为主的,当输送是通过剖腹产。
在门水平上,NPA和粪便样品随时间变化类似,变形菌门(Proteobacteria)增加,而在BAL/TAF样品中相对静止。Tenericutes,Ureaplasma和支原体主要局限于下呼吸道样本,只有在NPA样品中的存在,但几乎没有粪便样品。相比之下,不动杆菌在粪便和NPA样品中存在,但不在下呼吸道样本中,反映了该单位的爆发。几乎所有样品都有一个主要的OTU,具有> 90%的样品,其具有> 50%的读数的主要OTU葡萄球菌,支原体和Ureaplasma尤指在较低的气道中占优势的。有趣的是,所有的婴儿都有自己的细菌模式,样本类型之间很少有重叠,这表明一个积极的感染发作过程。PERMANOVA分析表明,每个解剖部位的样本的群落结构存在显著差异。丰富度α-多样性指数显示,BAL和TAF的属数高于NPA和粪便样品,但OTU水平上的差异消失,表明NPA和粪便样品在OTU水平上具有较高的丰富度。由于均匀度(Shannon多样性指数)在样本点之间没有差异,数据表明单个OTU的优势度在解剖点之间没有差异。NPA和BAL/TAF样本之间的差异可能部分是由于存在一个未套管的气管内管,该管部分分离上、下气道。从未通气的早产儿或足月新生儿中获取下气道样本是不可能的,因此下气道微生物演化的数据有限[27.].
正如之前对足月出生婴儿的观察,分娩方式与增加的比例葡萄球菌在NPA(p = 0.022)中,在剖腹产分娩并增加的人中,在TAF(P = 0.056)中支原体(p = 0.039)不动杆菌(p = 0.042)在TAF样品中Serratia.(p = 0.008),Ureaplasma(p = 0.024)和棒子杆菌(p = 0.028)在来自阴道递送婴儿的NPA样品中。性没有影响细菌定植,但是获得样品的中心对结果影响了结果。这些结果可以通过爆发部分解释不动杆菌在一个单元中,但两个中心之间的差异在敏感性分析中仍然存在,当婴儿殖民不动杆菌被拆除,从而表明对当地环境或当地人员似乎影响定植除了母体环境。抗生素,如预期的,细菌负荷降低,以更少的样品适于细菌基因测序。然而,OTU单板的多样性和数量是相似的,当婴儿被打开或关闭抗生素。Tenericutes的存在TAF样品(P = 0.03)在增加和朝向Tenericutes趋势在NPA样品(p值= 0.059)在抗生素组增加。
最有趣的是,当细菌测序可行时,我们注意到BAL和TAF中IL-6和IL-8浓度的几倍差异。我们的数据表明,有罹患慢性阻塞性肺病风险的婴儿的肺部正在出现一种传染性的失调环境。低生物量样品可能具有较低的细胞因子浓度,这是由于返回的样品体积的变化引起的稀释。然而,根据我们之前的观察,IL-6和IL-8的整理数据显示,这两种细胞因子的浓度在出生后7天达到峰值[2,3.,16.].在每个婴儿个体中,细胞因子峰值的增加与主要OTUs相关,提示一个感染过程。个别OTUs中TAF IL-6和IL-8的显著增加进一步支持了这一观点,证实感染过程在有患慢性肝病风险的婴儿的肺部是常见的。
总之,这些数据表明,细菌群落和肺部炎症都是用抗生素,如阿奇霉素,同时具有抗感染和抗炎活性降低CLD率[潜在目标6].
本研究有几个局限性,值得注意的是存在气管管的存在,以支持婴儿的呼吸系统。最重要的是,这排除了从“健康”的早产和术语出生的婴儿的采集,这不是道德上可能的。由于许多婴儿在延长的婴幼儿中,尽管许多婴儿延长,但是,尽管许多婴儿在胃肠道和胃肠道中,但尽管延长了通风,但是,这种情况可能会分离下呼吸道和上气管。该研究的强度是来自纵向获得的多个解剖部位的大量样品,通过迄今为止最大的早产儿研究。此外,我们与招聘中心之间的调查结果与婴儿肺部发生的炎症过程有关,患有CLD的风险。
总之,出生时细菌负荷低,但很快地增加和微生物最有可能从母亲那里获得。上下呼吸道和细菌群落结构之间存在异味,细菌群落结构具有在婴幼儿的下呼吸道中发生的单独炎细胞炎症过程,提高了CLD的风险。此外,尽管婴儿在抗生素上表明微生物不容易常规使用抗生素,但肺炎炎症过程也在发生抗生素的情况下发生。Ureaplasma和支原体可能是主要的,并可能提供一个治疗靶点,以减少早产儿慢性肝病的发展[6].
补充材料
可共享的PDF
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
数据共享:所有序列已上传到EBI的ENA(https://www.ebi.ac.uk/ena).
作者贡献:S. Kotecha和J.R. Marchesi和N. Klein负责最初的设计。D. Gallacher和R. Wach负责样本采集,由S. Kotecha监督。D. Alber, D. Gallacher和E. Mitchell负责样品分析,由N. Klein和J.R. Marchesi监督。所有人都负责数据收集和数据分析。这份手稿是大家共同写的。
利益冲突:d·加拉赫没有什么可透露的。
利益冲突:E. Mitchell没有什么可以披露的。
利益冲突:D.阿尔伯没有什么可披露的。
利益冲突:沃什没有什么可披露的。
利益冲突:N. Klein没有什么可披露的。
利益冲突:J.R. Marchesi没有什么可披露的。
利益冲突:S. Kotecha没有什么可披露的。
支持声明:S. Kotecha从医学研究委员会(MRC)(MRC / M022552 / 1)和国家卫生研究所(NIHR)/健康技术评估(HTA)(16/111/106)获得资金。对于J.R. Marchesi,伦敦帝国学院综合体系医学和消化系统疾病的划分收到了NIHR帝国生物医学研究中心(BRC)的财政支持,基于帝国学院医疗保健NHS信托和伦敦帝国学院。本文是由NIHR BRC资助的独立研究,本出版物中表达的观点是作者的观点,而不是NHS,NIHR或健康部的观点。卡迪夫大学为博士学位为米切尔提供了博士学位。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2019年9月26日。
- 接受2020年2月1日。
- 版权所有©ers 2020
这个版本是在知识共享署名许可证4.0的条款下发布的。