文摘
人类间充质干细胞/基质细胞(msc)产生M2-like报道,或者激活巨噬细胞的表型。此外,msc调解有效细菌在临床前间隙脓毒症模型。因此,msc有矛盾的抗菌和抗炎反应还不甚了解。
在这里,我们研究了monocyte-derived人类巨噬细胞的表型和功能响应MSC曝光在体外。
msc诱导两种截然不同的,同时代的表型:M2-like巨噬细胞(一般细长的形态,CD163+、急性phagosomal酸化、低NOX2表达式和有限phagosomal超氧化物生产)和M1-like巨噬细胞的特点是高水平的phagosomal过氧化物生产。增强phagosomal活性氧产量也从啮齿动物模型中观察到肺泡巨噬细胞pneumonia-induced脓毒症。生产M1-like巨噬细胞是依赖前列腺素E2和磷脂酰肌醇3-kinase。msc增强的人类unopsonised细菌和增强巨噬细胞吞噬细菌杀死而未经处理的巨噬细胞。细菌杀死被封锁NOX2使用diphenyleneiodonium显著降低,表明M1-like细胞主要是负责这种效果。msc还增强巨噬细胞吞噬作用和分化M1-like来自严重脓毒症患者。
增强抗菌能力(M1-like)和炎症解决表型(M2-like)可能占矛盾影响这些细胞在脓毒症在活的有机体内。
文摘
间充质干细胞促进细菌杀死通过生产phagosomal巨噬细胞的活性氧http://ow.ly/tigl30iGFPG
介绍
脓毒症是危重病人死亡的最大原因,可能导致一半的医院死亡(1,2]。改善治疗脓毒症可以提供有意义的人口死亡率的改善。
间充质干细胞/基质细胞(msc)基质细胞,形成一个支持血管周的利基在骨髓造血干细胞(hsc)、协调贩卖肝星状细胞和单核细胞3,4]。尽管最初确定骨髓(5),msc也存在血管周的细胞在其他组织,包括肌肉、脐带和脂肪组织(6,很容易孤立和扩大在文化。msc在临床前模型证明承诺(7- - - - - -9),这样他们在早期阶段的临床试验正在测试在危重患者脓毒症(10,11]。
的关键交互msc治疗的好处是msc和单核细胞/巨噬细胞。msc已被证明改变行为的单核吞噬细胞诱导抗炎(M2)或宽容的表型(12]。msc促进monocyte-to-macrophage过渡,减弱M1激活巨噬细胞,增强M2激活(13]。这MSC-mediated调制单核细胞/巨噬细胞的免疫反应被认为扮演关键角色在他们的治疗效果(14]。M2巨噬细胞抑制炎症,促进创面修复,但有限的细胞机制能够有效杀菌剂的反应,包括强大的氧化系统组成的NADPH氧化酶(15]。白介素(IL) 10-secreting M2巨噬细胞尤其善于抑制抗菌免疫,并能提高一些微生物的生存和传播(16,17]。然而,这种抗炎表型不一致,几项研究证明msc可有效改善细菌清除率和生存在脓毒症动物模型,在一定程度上依赖出现的巨噬细胞产生影响(14,18- - - - - -20.]。
因此,目前尚不清楚msc如何既能提高细菌清除率和诱导抗炎巨噬细胞表型。
为了更好地定义MSC对巨噬细胞的影响,我们研究人类巨噬细胞表型和功能,以应对人类骨骨髓来源MSC曝光。具体来说,我们希望定义如何接触msc改变巨噬细胞分化和关键功能,如超氧化物生产和吞噬作用。最后,我们还旨在识别一些介质通过msc改变巨噬细胞功能和信号通路。
材料和方法
所有的工作都是人类伦理委员会批准的基南和动物保健和使用委员会生物医学研究中心的圣迈克尔医院(多伦多,加拿大),和在加拿大卫生部的许可下进行的。详细介绍了方法补充材料。
msc、成纤维细胞和单核细胞/巨噬细胞隔离和文化
人类骨髓msc得到中心的成人干细胞的制备和分布(medicine.tamhsc.edu/irm/msc-distribution.html医学)德州A&M大学健康科学中心大学再生医学研究所(美国TX庙)。人脐带msc是提供组织再生疗法(多伦多,加拿大)。细胞达到国际标准。人类正常皮肤成纤维细胞从Lonza购买(加拿大在米西索加)。人类外周血单核细胞从血液中分离的健康成人捐助者或脓毒症患者使用右旋糖酐/聚蔗糖或Lympholyte H细胞分离媒体(CL5015;Cedarlane,伯灵顿,加拿大)。详细的协议提供了补充材料。短暂,隔离后,人类血液单核细胞与媒体含血清培养8天(定义为M0巨噬细胞)或5天后骨骨髓来源的细胞培养的msc transwell或coculture表示在图3天传奇。生产的定义M1和M2巨噬细胞,单核细胞与巨噬细胞集落刺激因子治疗(ng·25毫升−1)6天然后il - 4 (10 ng·毫升−1)2天(M2)或粒细胞−巨噬细胞集落刺激因子(ng·25毫升−1)6天然后interferon-γ(10 ng·毫升−1ng)和脂多糖(500毫升−1)2天(M1),如前面描述的(15]。
血清opsonised酵母聚糖和氮蓝四唑试验
乾酵母聚糖(酿酒酵母)Bioparticles(生命技术、伯灵顿,加拿大)标记了荧光团(alexa - 555或异硫氰酸荧光素(FITC))如前所述[15]。氮蓝四唑(电视台)化验进行如前所述[15]。简而言之,alexa - 555共轭血清opsonised酵母聚糖(但他)和电视台(N5514-25TAB;σ,奥克维尔、加拿大)被添加到细胞浓度表示在图中传说的30分钟,洗净,然后固定在4%多聚甲醛在PBS 15分钟。细胞被微分干涉差显微镜观想。黑甲瓒存款是phagosomal超氧化物生产的象征。在一些实验中,电视台化验后,细胞被固定在冰冷的甲醇在−2分钟20°C处理和免疫荧光显微镜。
细菌吞噬,phagosomal pH值测量,分析死亡
文化的红色荧光蛋白(RFP)表达大肠杆菌(DH5a)或RFP-expressing伯克cenocepacia被添加到巨噬细胞细胞浓度表示在图中传说,清洗和固定在4%多聚甲醛/牛血清白蛋白,持续15分钟。细菌吞噬作用被旋转的圆盘共焦显微镜监控。Phagosomal pH值测量使用比率成像(15]。对于细菌杀死,庆大霉素排斥试验,所描述的补充材料。
啮齿动物大肠杆菌全身的伤
特定的无菌成年男性的雄性sd大鼠中(查尔斯河实验室、魁北克、QC、加拿大)重350 - 450克被用于实验。动物犀牛和气管插管14 g静脉导管(BD Insyte;正欲,英国牛津大学)。2×109CFU的大肠杆菌在300年μL PBS悬挂被灌输到气管使用1毫升注射器,和动物允许恢复,治疗10×106msc·公斤−1或PBS (21]。48小时后麻醉下的动物被放血。心肺块切割从胸腔,支气管肺泡灌洗进行使用Lympholyte R细胞和肺泡巨噬细胞被孤立分离媒体(CL5041;Cedarlane)。
统计分析
所有值平均值与标准偏差或标准错误报告如上所述图中传说。一个未配对t检验假设等于方差用于双态比较。方差分析图基的紧随其后事后测试是用于多个条件的比较。p < 0.05被认为是显著的。
结果
msc促进巨噬细胞phagosomal活性氧的生产在体外和在活的有机体内
msc增强细菌间隙已报告在一些感染的动物模型在活的有机体内,尽管的确切机制尚不清楚14,18- - - - - -20.,22]。线粒体转移(22,23)和生产抗菌肽(LL-37 [24)和lipocalin 2 (25)已被证明参与细菌通过msc间隙。此外,M1特别是巨噬细胞被认为是强有力的抗菌能力在一定程度上由于高水平和phagosomal NADPH氧化酶的活性,促进细菌杀死(15]。检查msc对巨噬细胞phagosomal氧化酶活动的影响,人类骨骨髓来源msc与人类monocyte-derived巨噬细胞和cocultured phagosomal超氧化物被暴露监测巨噬细胞,但他在电视台的存在。电视台与过氧化物反应的产物是甲瓒,黑暗的存款容易通过光学显微镜(视觉效果15]。
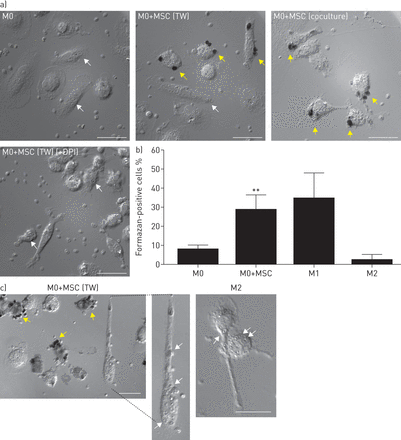
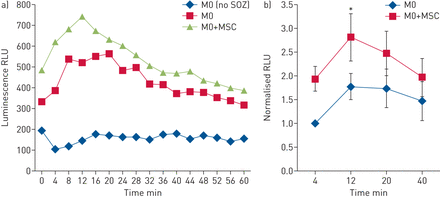
值得注意的是,所示图1一个和b,在有限的条件下或没有phagosomal过氧化物检测控制M0细胞(白色箭头),许多formazan-positive细胞明显M0细胞暴露在msc (图1一个,黄色箭头)。这M1-like表型观察transwell和coculture条件。M0细胞暴露于成纤维细胞而不是msc证明没有改变在生产超氧化物(补充图S1)。甲瓒生产依赖NADPH氧化酶活动没有细胞phagosomal甲瓒存款观察M0 + MSC细胞治疗NADPH氧化酶抑制剂diphenyleneiodonium (DPI) (图1一个),这并不影响细胞吞噬但他的能力。总的来说,实验条件下,∼formazan-positive三倍增加巨噬细胞暴露于msc与M0相比,transwell控制(图1 b)。另外,我们观察到电视台浓度很高,现在大部分的圆形细胞产生phagosomal甲瓒(图1 c,黄色箭头),主要是细长的巨噬细胞的一个子集M0 + MSC条件是完全缺乏phagosomal甲瓒(图1 c,插图,白色箭头)。这是非常有限的象征phagosomal过氧化物生产,这是一个功能的M2巨噬细胞(图1 c,右面板)15]。验证巨噬细胞phagosomal氧化酶活动确实增强了MSC暴露我们执行一个发光氨测定巨噬细胞(图2一个和b)。分析多个实验显示显著增加phagosomal活性氧(ROS)生产早期跨度为巨噬细胞细胞暴露于msc (图2 b)。
人类间充质干细胞的影响/基质细胞(msc) phagosomal活性氧的生产在人类巨噬细胞(氮蓝四唑(电视台)测定)。人类血液单核细胞)与媒体含血清培养8天(M0)或5天后骨骨髓来源的细胞培养的msc在transwell (TW)或coculture 3天。细胞培养与0.01 mg·毫升−1血清opsonised酵母聚糖(但他)和0.125 mg·毫升−1电视台没有或存在10µM diphenyleneiodonium (DPI),表示。这些细胞被固定和成像(DIC)微分干涉对比显微镜。白色箭头表示细胞吞噬但他没有甲瓒的存款。与MSC接触众多细胞有明显证据phagosomal甲瓒,表明高phagosomal超氧化物生产(黄色箭头)。代表图像所示的各种条件。酒吧规模:20µm。b) formazan-positive细胞的定量。数据意味着±sd。n = 4个独立的实验。* *:p < 0.01, M0与M0 + MSC (TW)。c) M0细胞暴露于msc (TW)或M2孵化,但他和2 mg·毫升−1电视台30分钟。细胞被洗,固定,DIC显微镜成像。酒吧规模:20µm。两个表型观察:大多数圆细胞吞噬但他黑甲瓒存款在左面板(黄色箭头),而细长的细胞吞噬但他有限或没有甲瓒存款时间在插图(白色箭头),类似于M2细胞(右面板)。
人类间充质干细胞的影响/基质细胞(msc) phagosomal活性氧(ROS)生产在人类巨噬细胞(鲁米诺试验)。人类血液单核细胞被播种在96孔板,与媒体含血清培养8天(M0)或5天后骨骨髓来源的细胞被cocultured msc为3天。鲁米诺试验进行监控phagosomal ROS生产中描述的材料和方法。相对发光的发光单元(RLU)监控。但他:血清opsonised酵母聚糖。)代表单一实验显示控制巨噬细胞不暴露但他,或控制或MSC-exposed巨噬细胞但他对待。发光的增加只是观察到巨噬细胞暴露于但他。b)数据正常化RLU价值在t = 4分钟。n = 5个独立的实验。*:p < 0.05。
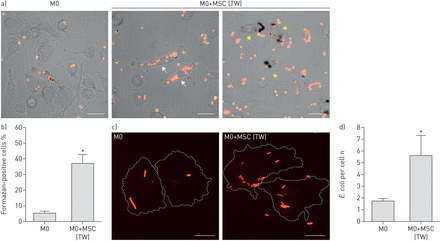
为了确定增强phagosomal过氧化物生产在msc在活的有机体内,我们孤立巨噬细胞从一种啮齿动物模型大肠杆菌pneumonia-induced败血症。肺泡巨噬细胞被隔离治疗后大鼠msc或PBS,和一个电视台试验后进行隔离和文化。formazan-positive细胞的数量(表明高phagosomal过氧化物生产)是显著增加MSC-treated条件(图3)。
人类间充质干细胞的影响/基质细胞(msc) phagosomal活性氧(ROS)在隔离大鼠肺泡巨噬细胞从一个生产大肠杆菌肺炎模型。肺泡巨噬细胞从老鼠暴露在被孤立大肠杆菌肺炎,然后用PBS或msc治疗48 h中描述的材料和方法。一个血清opsonised zymosan-nitroblue四唑试验执行。)代表图像。Phagosomal甲瓒存款表明Phagosomal ROS出现黑色。酒吧规模:20µm。b) formazan-positive细胞的定量。数据意味着±sd。n = 4实验。*:p < 0.05。
MSC-induced phagosomal巨噬细胞活性氧产量取决于NOX2激活
鉴于phagosomal过氧化物生产依赖于NADPH氧化酶酶,我们检查了gp91的表达和本地化phox的膜结合催化亚基NOX2同种型,这已被证明是表示上级M1与M2巨噬细胞(15]。gp91phox表达式是容易控制M0细胞中发现,以及巨噬细胞细胞M0 + MSC条件(补充图S2,白色箭头)。相比之下,细长M2-like细胞观察只在M0 + MSC gp91较低phox表达式(补充图S2,黄色箭头)。gp91phox染色后巨噬细胞细胞但他吞噬的电视台化验显示表达式是最高的细胞产生phagosomal超氧化物被甲瓒生产(补充图S2白色箭头),而M2-like细胞gp91水平较低phox。然而,总gp91phox水平圆M0巨噬细胞细胞+ MSC条件没有显著不同于控制M0细胞(补充图S2d和e)。
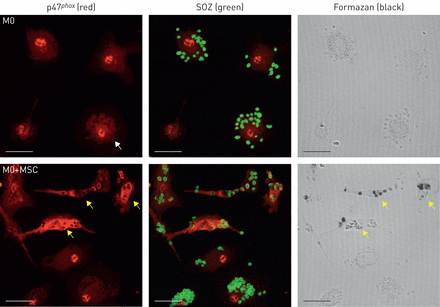
因此,增强phagocytosis-induced NADPH氧化酶激活,而不是水平的提高催化NOX2单元,是更有可能MSC-induced ROS生产巨噬细胞的机制。Phagocytosis-induced氧化酶的活化是一个复杂的和高度管制过程,涉及装配功能multisubunit酶复杂新形成的吞噬体通过招聘几个胞质膜结合组件gp91子单元phox和第22位phox(26,27]。我们检查了本地化的胞质单元之一,p47phox。的电视台进行化验M0细胞或M0暴露于msc、其次是p47疣状phox。所示图4,大多数M0细胞吞噬但他没有产生甲瓒在试验条件下使用,而大多数p47phox胞质或隐藏在细胞核周围的位置。M0细胞暴露于msc、phagosomal活性氧产量明显透露的黑暗phagosomal甲瓒存款(图4右下角的面板,黄色箭头)。在这些细胞的许多酵母聚糖颗粒被明亮的p47包围phox疣状(图4左面板、底,黄色箭头)。因此,细胞产生phagosomal超氧化物增强能力,更为普遍的M0 + MSC条件,总体水平的提高活跃氧化酶。
M1-like巨噬细胞增加了phagosomal NADPH氧化酶亚基p47的水平phox。人类巨噬细胞接触或不骨骨髓来源间充质干细胞/基质细胞(msc) transwell 3天。细胞被孵化与血清opsonised酵母聚糖一起0.125 mg·毫升−1氮蓝四唑30分钟。这些细胞被固定和p47应用phox。在控制细胞M0没有检测到phagosomal超氧化物生产、p47phox疣是明显在集群细胞核周围的地区一些细胞的胞质和疲软的染色观察周围性酵母聚糖颗粒(白色箭头)。M0暴露于MSC (M0 + MSC)许多细胞产生丰富的phagosomal超氧化物,当检测到黑甲瓒存款,很明显在右下角的面板(黄色箭头)。一般来说这些细胞有较高的p47phox疣状周围性酵母聚糖颗粒在左面板底部(黄色箭头)。但他:血清opsonised酵母聚糖。比例尺:10µm。
MSC-induced phagosomal ROS生产依赖前列腺素E2和磷脂酰肌醇3-kinase
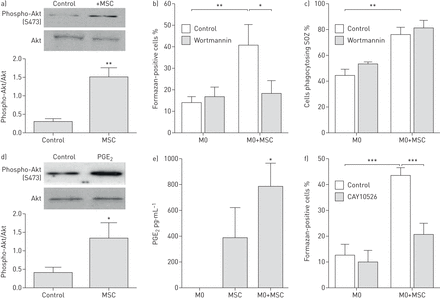
接下来,我们希望了解的机制,msc增强氧化酶活动。吞噬作用,胞质亚基p47phox和p40phox被雇来的吞噬体结合磷脂酰肌醇3 4-bisphosphate和磷脂酰肌醇3 -磷酸,分别,这是由不同的磷脂酰肌醇生成3-kinase (PI3K) [26- - - - - -28]。因此,我们假设,PI3K活动可能会增加一些M0细胞暴露于msc,这在一定程度上可能导致招募胞质氧化酶亚基增强的能力,从而增强能力吞噬刺激激活的氧化酶反应。分析phospho-Akt PI3K通路的下游目标,显示增加M0细胞暴露于msc与M0独自一人(图5一个)。此外,抑制PI3K活动与加强phagosomal渥曼青霉素预防细胞的增加超氧化物生产(图5 b)而不影响但他吞噬作用(图5 c),这表明PI3K活动需要这种效果。类似的结果PI3K抑制剂LY294002(结果未显示)。
全身的间充质干细胞/基质细胞(MSC)生产M1-like巨噬细胞需要前列腺素E2(铂族元素2)和磷脂酰肌醇3-kinase (PI3K)。人类血液单核细胞与媒体含血清培养8天(M0)或5天后骨骨髓来源的细胞培养的msc transwell 3天。)监测PI3K激活的巨噬细胞暴露于msc、总细胞溶解产物受到西方墨点法与anti-phospho-Akt (S473)。为蛋白质加载正常化,膜与anti-total探测一种蛋白激酶。数据意味着±sd。n = 3。* *:p < 0.01。b, c)确认PI3K激活的作用,M0细胞培养与msc transwell没有或存在1µM渥曼青霉素PI3K抑制剂。细胞培养与0.01 mg·毫升−1血清opsonised酵母聚糖(但他)和0.125 mg·毫升−1氮蓝四唑(电视台)30分钟。细胞被洗和固定。b) formazan-positive细胞的百分比和c)细胞吞噬但他使用旋转阀瓣共焦显微镜进行分析。数据意味着±sd。n = 3。*:p < 0.05,控制与渥曼青霉素;* *:p < 0.01, M0与M0 + MSC。d)人类血液单核细胞培养5天,之后与刺激的车辆或100纳米铂族元素224 h。水平的phospho-Akt (S473)和总Akt蛋白免疫印迹分析。数据意味着±sd。n = 3。*:p < 0.05。e)铂族元素的含量2在文化上层清液M0, msc和M0暴露于msc在transwell铂族元素进行分析2酶联免疫试剂盒。数据意味着±sd。n = 3。*:p < 0.05。f)人类血液单核细胞培养5天,然后用msc在transwell cocultured 3天没有或存在10µM铂族元素2合酶抑制剂CAY10526。电视台进行化验,formazan-positive细胞的百分比量化。数据意味着±sd。n = 3。* * *:p < 0.001, M0与M0 + MSC和控制与CAY10526。
PI3K可以激活的因素包括前列腺素E2(铂族元素2),它是由msc (14]。事实上,铂族元素2仅提高phospho-Akt水平在人类M0巨噬细胞(图5 d)和铂族元素2水平明显增强当msc cocultured与巨噬细胞(图5 e)。测试是否铂族元素2需要增加细胞的数量与增强phagosomal ROS,抑制铂族元素呢2与CAY10526生产,防止ROS-positive巨噬细胞对MSC的增加接触(图5 f)。因此,MSC铂族元素的生产2可能导致增强PI3K激活巨噬细胞的一个子集,允许增强(NOX2) NADPH氧化酶组装吞噬作用,导致增强phagosomal ROS生产。
msc促进M2-like巨噬细胞的某些特性
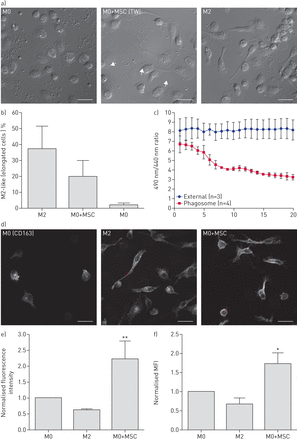
先前的研究已经确定了,msc分化的巨噬细胞像一个M2-like表型(29日]。我们的研究结果支持和扩展这些发现。细胞形态学分析显示,一些巨噬细胞细胞培养的msc在transwell有一个细长的外观,是典型的多平方米细胞(图6)。量化显示msc引起∼20%的人口采取这种形态(图6 b)。M2细胞的一个重要功能特性是,M1细胞相比,他们迅速酸化新成立的时间15]。来确定MSC-induced表现得像“M2-like”细胞善意的M2细胞,我们监控phagosomal pH值的比率成像在巨噬细胞细胞暴露于FITC-labelled但他。细长的巨噬细胞细胞在受到MSC接触迅速酸化新成立的时间所观察到的下降在490 nm / 444 nm激发波长比(图6 c),类似于M2细胞(15]。
间充质干细胞/基质细胞(msc)会导致一些人类巨噬细胞采用M2-like形态和表型。人类血液单核细胞)与媒体含血清培养8天(M0)或5天后骨骨髓来源的细胞培养的msc在transwell (TW) 3天。M2细胞生成的所述材料和方法。这些细胞被固定和微分干涉差显微镜观察到。许多M2细胞采用细长的形态,明显M0 + MSC条件(白色箭头),而不是M0条件。酒吧规模:20µm。b)的细长细胞比例量化。数据意味着±sd。n = 7实验。c)人类血液单核细胞培养5天然后用msc在TW培养3天。Phagosomal pH值在M2-like细胞监测490海里/ 440 nm激发波长比率成像用异硫氰酸荧光素(FITC)血清opsonised酵母聚糖(但他)中列出的材料和方法。在一些实验中外部nonphagocytosed FITC-SOZ粒子成像作为一种控制。数据意味着±sd。n = 3 - 4个独立的实验。d)巨噬细胞准备如(a)所述,然后固定CD163应用。代表共焦图像。酒吧规模:20µm。使用ImageJ (e)细胞荧光强度测量https://imagej.nih.gov/ij/M0)和值正常化水平细胞。数据意味着±sd。n = 3实验。* *:p < 0.01平方米与M0 + MSC。f)流式细胞术CD163在各种条件下的分析。阳性细胞的平均荧光强度(MFI)人口。数据意味着±sd。n = 4。*:p < 0.05平方米与M0 + MSC。
M2巨噬细胞也区分某些细胞表面表达的蛋白质(30.,31日),如CD163在人类细胞(31日,32]。我们本地化和监测水平的CD163免疫荧光显微镜使用特定的抗体(33]。细胞的数量与CD163疣状(圆和细长的)高M0细胞暴露于msc与控制M0细胞(图6 d)。量化的总荧光(图6 e通过流式细胞术()和表面水平图6 f)表明,MSC-treated巨噬细胞表达CD163水平高于M0细胞或定义M2细胞。
鉴于phagosomal ROS生产是M1巨噬细胞的功能,我们决定是否M0细胞暴露于msc,特别是增强活性氧产量,提高水平的M1-specific蛋白质如CD40 [30.]。免疫荧光显微镜证实CD40在M1巨噬细胞产生phagosomal超氧化物表面染色电视台试验(检测到的补充图S3)。然而,巨噬细胞暴露于msc没有CD40染色(补充图S3)。因此,尽管M1-like细胞M1细胞的一些特性,如高phagosomal过氧化物生产,他们缺乏的标记善意的炎症细胞M1。
msc加强细菌的吞噬作用,杀死健康的人类巨噬细胞和巨噬细胞的脓毒症患者
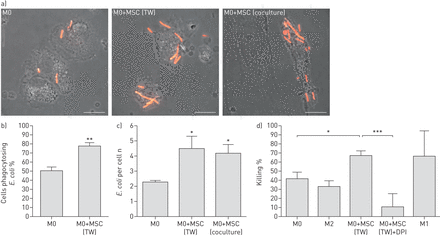
鉴于NADPH氧化酶在杀菌剂的能力有重要作用(27),我们观察细胞与加强氧化酶活动的增加,我们假定的msc可以促进细菌杀死通过这种机制。吞噬作用的unopsonised大肠杆菌(图7- c)和b . cenocepacia(补充图S4)是显著增加巨噬细胞的细胞已经暴露于msc在transwell或coculture。我们接下来研究msc对细菌造成的影响。所示图7 d,巨噬细胞细胞暴露于msc杀死有更大的能力大肠杆菌相比之下,控制细胞M0和M2。细菌杀死明显降低与DPI NADPH氧化酶的抑制作用,表明M1-like细胞可能会主要负责增强细菌杀死。
间充质干细胞/基质细胞(MSC)曝光增强大肠杆菌吞噬作用和杀戮。人类血液单核细胞)与媒体含血清培养8天(M0)或5天后骨骨髓来源的细胞培养的msc在transwell (TW)或coculture 3天。活的细胞培养红色荧光蛋白(RFP)表达大肠杆菌旋转下来到巨噬细胞细胞。这些细胞被洗20分钟后用PBS,固定,然后通过光和荧光显微镜成像。代表扩展重点结合相衬和RFP的荧光图像。比例尺:10µm。b)的比例的细胞吞噬细菌和c)的数量大肠杆菌细胞腹腔巨噬细胞吞噬或绑定/。数据意味着±se。n = 4 - 5个独立的实验。*:p < 0.05;* *:p < 0.01, M0与M0 + MSC (TW或coculture)。d)巨噬细胞细胞准备如(a)所述,吞噬和评估大肠杆菌杀死在材料与方法中执行。数据意味着±se。n = 6个独立的实验。* p < 0.05, M0与M0 + MSC (TW);* * *:p < 0.001, M0 + MSC (TW)与M0 + MSC (TW) + diphenyleneiodonium (DPI)。
考虑到临床前证据msc小说兼职抗生素治疗,我们还检查了msc对monocyte-derived巨噬细胞的影响与脓毒症患者。msc增强吞噬phagosomal ROS的但他和生产(图8和b),以及吞噬作用大肠杆菌(图8 c和d)。这表明,msc能增强巨噬细胞吞噬作用和败血症的细菌杀死。
间充质干细胞/基质细胞(msc)诱导M1-like M2-like表型和加强巨噬细胞的吞噬作用来源于脓毒症患者。人类血液单核细胞)对脓毒症患者中分离的培养与媒体包含8天血清(M0)或5天后骨骨髓来源的细胞培养的msc在transwell (TW) 3天。在执行一个血清opsonised zymosan-nitroblue四唑试验图1一个。共焦显微镜的细胞被固定和成像。M2-like细胞(白色箭头)和M1-like细胞检测phagosomal甲瓒(黄色箭头)被观察到。结果是代表n = 4例。酒吧规模:20µm。b)的量化phagosomal formazan-positive细胞。数据意味着±sd。n = 4。*:p < 0.05。c)细胞准备在(a),和大肠杆菌吞噬作用是监控中描述的材料和方法。MSC-exposed巨噬细胞增加了细胞内或绑定大肠杆菌。代表图像。比例尺:10µm。d)的数量大肠杆菌腹腔巨噬细胞吞噬细胞或绑定/量化。数据意味着±sd。n = 3例。*:p < 0.05。
讨论
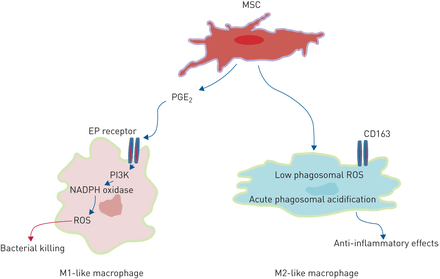
在这项研究中我们发现了骨头的能力来源于msc影响巨噬细胞的分化和功能,在体外和在活的有机体内诱导一个异构的人口。我们的研究表明铂族元素2作为一个重要的中介效应(图9)。我们所知,我们是第一个报告里这样一个显著的异质性monocyte-derived巨噬细胞暴露于msc。出人意料地,我们发现msc诱导同时共存的M1-like M2-like巨噬细胞表型。巨噬细胞可以指向一个表型具有增强抗菌能力(M1-like),以及解决炎症和组织修复的表现型(M2-like),可能占矛盾影响这些细胞的致病条件如败血症在活的有机体内。
示意图的机制的间充质干细胞/基质细胞(msc)改变巨噬细胞功能。铂族元素2:前列腺素E2;EP: E-prostanoid;PI3K:磷脂酰肌醇3-kinase;ROS:活性氧。
之前的工作在这一领域的K即时通讯和Hematti(29日)和其他(14,34,35)描述了人口M2-like人类巨噬细胞生成在体外与人类msc coculture之后,定义为CD206+,il - 10高可以,il - 12低,il - 6高和肿瘤坏死因子(TNF) -α低。这里,我们发现M2-like巨噬细胞表型诱导msc在一小部分的人口确实有很多特性与M2巨噬细胞细胞,包括细长的形状(36),表面标记(CD163+),急性phagosomal酸化和低NOX2表达有限phagosomal过氧化物生产(15]。
还值得注意的是,msc诱导M1-like巨噬细胞表型的巨噬细胞的一部分人口,以增强phagosomal过氧化物生产。但是,与定义M1巨噬细胞,MSC-induced M1-like细胞较低或CD40检测不到M1巨噬细胞水平的标志。重要的是,这个M1-like表型也从一个孤立的肺泡巨噬细胞中观察到在活的有机体内啮齿动物模型大肠杆菌肺炎在回应注射。MSC治疗。
我们发现,msc诱导PI3K和铂族元素2端依赖NADPH氧化酶活性的增加。我们还演示了一个增强的能力杀死大肠杆菌在巨噬细胞暴露于msc、明显受损的NADPH氧化酶的抑制作用。这已是不争的激活吞噬细胞NADPH氧化酶(NOX2)是一种重要的先天免疫机制27]。事实上,许多酸性吞噬溶酶体,即能茁壮生长的细胞内病原体等利什曼虫ROS-mediated杀死(spp。尤其敏感37,38]。NADPH氧化酶的催化作用的形成高度不稳定的超氧化物阴离子,它可以转化为过氧化氢。这两种活性氧能破坏蛋白质,脂类和DNA,导致杀菌剂的活动(39]。我们的数据支持的关键作用增强NADPH氧化酶(NOX2)诱导msc在MSC-induced增强细菌杀死。msc还加强巨噬细胞的吞噬作用和phagosomal ROS生成严重脓毒症患者。单核细胞无力和免疫抑制导致不良事件的风险增加在脓毒症40]。恢复与msc单核/巨噬细胞抗菌功能代表了一种有前途的治疗策略。我们的研究结果为此提供了强有力的支持,msc确实可以促进改善微生物间隙。我们建议增强吞噬作用和oxidase-mediated杀死可能的机制之一msc的有益的治疗效果。
ROS起到至关重要的作用在许多细胞过程中,包括吞噬细菌的破坏(41]。鉴于小说M1-like表型发现,我们我们的努力集中在识别msc如何调解增强phagosomal巨噬细胞的活性氧产量。噬细胞NADPH氧化酶(gp91复杂的由膜结合型子单位phox和第22位phox(NOX2))和胞质因素(p40数组phox,p47phox,p67phox和Rac)把膜,导致形成的影射和活跃NADPH氧化酶复杂。我们发现氧化酶大会增加和增强巨噬细胞产生phagosomal超氧化物的能力,所监控的p47的分布phox在电视台化验,PI3K M1-like增加细胞活动是至关重要的。基底PI3K活动增强巨噬细胞的人口暴露于msc。大概这将提高能力招募胞质氧化酶组件的子集巨噬细胞吞噬作用,这取决于磷酸肌醇的生产促进胞质氧化酶的招聘在形成吞噬体(子单位的膜结合型子单位26- - - - - -28]。
NOX2激活通过msc在我们的研究中铂族元素2相关的。然而,前列腺素类,包括铂族元素2传统上被认为在巨噬细胞发挥抗炎作用。铂族元素2已被证实能抑制炎性分子如TNF-α的生产(42等)和增加抗炎细胞因子的分泌il - 10 (43]。关于MSC-mediated M2表型分化的巨噬细胞,一个主要的角色已被归因于铂族元素2(14]。然而,研究前列腺素类受体的小鼠,在辅助细胞和树突细胞(Th),显示不同的前列腺素类受体调节免疫反应在各个步骤的发挥往往反对行动(44,45]。特别是,尽管铂族元素2抑制炎性巨噬细胞和Th1分化通过提高细胞内环腺苷酸的浓度,铂族元素2也便于Th1细胞分化通过PI3K。此外,铂族元素2肥大细胞中诱导活性氧的生产PI3K-dependent方式(46]。在这里,我们表明,抑制MSC-derived铂族元素2预防MSC-induced phagosomal ROS生产,而coculture msc和巨噬细胞诱导增强铂族元素的生产2msc。铂族元素2单独激活PI3K和巨噬细胞的活性氧产量。不同功能的铂族元素2可能是取决于几个因素,包括微分表达式E-prostanoid (EP)巨噬细胞受体(47),EP受体表达的动力学过程中巨噬细胞激活(48),不同的配体的亲和力EP受体和受体的脱敏,动力学和最后的具体下游通路每个受体(49]。
同样重要的是要指出,尽管NADPH氧化酶是一个关键组成部分抗菌反应,其他因素也可能有助于增强细菌杀死。事实上,虽然M2细胞NOX2有限表达他们仍然能够杀死大肠杆菌,虽然不如M1或M1-like细胞有效。据推测,这是由于在低pH值环境中降解能力的吞噬溶酶体50]。此外,线粒体ROS也被卷入造成病原体杀死(51),最近的研究表明,线粒体msc可以交付巨噬细胞细胞通过细胞外囊泡(52),通过隧道nanotubules [22]。
msc如何产生不同的巨噬细胞表型相同的血液单核细胞?至少存在三种不同类型的血液单核细胞(53),大概至少有一个这些种群产生巨噬细胞对铂族元素2生产M1-like表型观察。当我们和其他人也表明,msc诱导单核细胞的M2-like表型(12,14]。这个导演成熟部分监管通过细胞直接接触,而且MSC分泌的铂族元素2il - 6,吲哚胺2,3-dioxygenase和TNF-stimulated基因6 (14,34,35,54]。然而,其他因素也可能导致MSC-induced效果。其他研究者最近表明,巨噬细胞吞噬mitochondria-containing微泡和microRNA-containing液从msc、从而提高巨噬细胞生物能学而抑制巨噬细胞激活(23,52]。李和他的同事们展示了一些抗菌作用的MSC-secreted角质细胞生长因子和微泡对人类单核细胞(55,56]。很明显从这些和我们自己的研究MSC免疫调制的单核细胞和巨噬细胞是复杂的,可能不是通过单个分泌的因素,代表了一个平衡的职业,抗炎症刺激。
这些实验有很多的局限性。msc调节巨噬细胞功能和细菌杀死通过多种机制不是检查在这些研究中,包括线粒体转移和监管小分子核糖核酸(52),分泌的抗菌肽(24]。我们专注于铂族元素2,因为它有一个重要的角色在脓毒症MSC的影响,以及巨噬细胞分化[14]。我们没有增加铂族元素2分泌在我们的研究中,它可以作为一种机制来提高MSC效力,虽然这种方法可能是脱靶效应。效果还需要进一步评估的时间:我们在体外巨噬细胞实验涉及48 - 72 h接触msc、不能反映在活的有机体内MSC-macrophage交互。虽然我们的研究调查了从健康志愿者msc对巨噬细胞的影响,以及败血症的病人,我们没有隔离危重患者巨噬细胞没有脓毒症。但是很有可能,msc改变吞噬作用和ROS生成类似的方式健康对照组。最后,利用RNA单细胞测序和生物信息学方法未来的研究可以提供更详细的描述我们所观察到的异构巨噬细胞的数量。
MSC治疗的未来取决于有效的发展,一致的细胞治疗。虽然颗粒的方法,使用MSC-derived细胞外囊泡,成为一个有前途的治疗策略,我们观察到msc和巨噬细胞之间的协同和相声,指向细胞本身需要达到最大疗效。因素限制了潜在的MSC治疗脓毒症包括有限MSC持久性、多变的免疫调节能力不足,依赖在活的有机体内由宿主炎症介质激活(57]。详细了解宿主应对msc,在这个研究和其他(22,52),是必要的为了发展一个一致的治疗和识别患者最有可能受益。以前的msc对其他疾病的临床试验适应症演示需要开发在体外和在活的有机体内模型可以预测成功的主机响应MSC治疗(58]。我们的研究确定了吞噬作用和ROS生产宿主因素在MSC治疗脓毒症可以获救。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
Supplementarymaterialerj - 02021 - 2017 - _supplementarymaterial
补充图1erj - 02021 - 2017 - _supplemental_fig1
补充图2erj - 02021 - 2017 - _supplemental_fig2
确认
我们要感谢Chris弹簧(圣迈克尔医院,多伦多,加拿大)与流式细胞术分析,寻求帮助和约翰·e·戴维斯和组织再生疗法(多伦多,加拿大)提供脐带间充质干细胞。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:G.F.科里和J.G. Laffey加拿大卫生研究院资助的研究(cihr - 312714)和举行绩效奖和临床科学家过渡奖,分别从麻醉的部门,多伦多大学。G.F.科里国际麻醉研究社会和拥有一个奖项是由安大略省政府的研究和创新,早期研究奖。G.F.科里和k . Szaszi由一个从圣迈克尔医院转化创新基金奖。kc塔是由美国国家卫生研究所资助(英国),欧洲创新和技术研究所和医学科学院(英国)。资金信息,本文已沉积的Crossref资助者注册表。
利益冲突:G.F.科里报告赠款从安大略政府支付给他的机构,研究和创新部(早期研究者奖),加拿大健康研究所(操作格兰特cihr - 312714)和圣迈克尔医院转化创新基金(TIF奖2015),在进行这项研究的。J.G. Laffey赠款从加拿大卫生研究院的研究报告和薪水支持部门的麻醉,多伦多大学,在进行这项研究的。
- 收到了2017年10月3日。
- 接受2018年2月21日。
- 版权©2018人队