摘要
目前尚不讨论烟雾诱导的气道重塑如何影响高表达呼吸上皮防御蛋白质,从而影响粘膜主体防御。
在分化良好的原代支气管上皮细胞(PBEC)培养物中评估一组高表达的呼吸上皮宿主防御蛋白的定位。接下来,PBEC在气液界面培养,并在分化过程中培养2-3天 每天暴露于整支香烟烟雾中数周。随后评估基因表达、蛋白质水平和上皮细胞标记物。此外,测定戒烟后功能活动和香烟烟雾诱导效应的持续性。
聚合免疫球蛋白受体、分泌性白细胞蛋白酶抑制剂和长、短PLUNC (palate,肺和鼻上皮克隆蛋白(肺和鼻上皮克隆蛋白)局限于管腔细胞,与对照组相比,将分化的PBECs暴露于香烟烟雾中,导致这些管腔细胞受限的呼吸道宿主防御蛋白的选择性表达减少。这种表达减少是吸烟损害上皮细胞末期分化的结果,并伴随着IgA经上皮转运的显著减少和细菌杀灭。
这些调查结果阐述了气道上皮细胞分化在呼吸道主体防御中的重要性,并可为吸烟者和慢性阻塞性肺病患者增加呼吸道感染的易感性提供了额外的解释。
摘要
香烟烟雾诱导的气道上皮重塑导致宿主防御蛋白的高表达丢失http://ow.ly/Q6Jr30iR6Jg
介绍
呼吸道感染和微生物定植是吸烟者的主要健康负担,并导致慢性阻塞性肺病(COPD)的恶化和发展葱头[1])。对有或没有COPD的吸烟者的这种易感性增加的机制是不完全理解的,但可以部分地归因于上皮损伤和重塑,导致破坏的粘膜清除率[2].除了清除粘液纤毛外,气道上皮还通过各种各样的额外活动帮助宿主防御[3.包括作为内源性抗生素或调节重要的抗菌免疫反应的抗菌肽的分泌通过各种机制[4].此外,上皮细胞产生细胞因子和趋化因子,启动免疫反应,以对抗微生物入侵。最后,通过聚合免疫球蛋白受体(pIgR)将聚合IgA和IgM运输到腔内,通过抑制粘附和促进病原体清除,促进肺内适应性免疫,这一过程称为免疫排斥[5].在气道中,这些呼吸道宿主防御蛋白(HDPs)在上皮细胞稳态时高度表达,表明它们对气道上皮屏障功能的重要性。高表达的蛋白和多肽包括但不限于抗菌肽如人β防御素(hBD)-1和脂钙素2 (LCN2),分泌性白细胞蛋白酶抑制剂(SLPI), pIgR和上皮钠通道调节短、长腭,肺和鼻上皮克隆蛋白(s/lPLUNC或BPIFA1 / BPIFB1) [6- - - - - -8].其他参与气道宿主防御的多肽如核糖核酸酶(RNase)7、LL-37和hBD-2在稳态时表达较低,但可被炎症介质、微生物产物和上皮细胞损伤诱导,从而有助于病原体的清除和由此产生的炎症过程[4].假复层气道上皮由多种细胞类型组成,包括杯状细胞、棒状细胞和纤毛细胞,这些细胞伸向气道管腔,而在完整的上皮层中,基底细胞不到达管腔[9].基于它们不同的解剖定位,这些不同的细胞类型也会产生不同类型的介质也就不足为奇了。例如,pIgR的表达仅限于假分层气道上皮的管腔细胞,因此在很大程度上受气道上皮细胞分化的调节[10,类似于杯状细胞产生的粘蛋白。相反,抗菌蛋白RNase 7的表达仅限于基底细胞[11].
众所周知,吸烟可诱导吸烟者和慢性阻塞性肺病患者的气道上皮重塑,其特征是杯状细胞增多和纤毛细胞减少[2].结果,上皮细胞产生更高水平的黏液,而黏液运输受损,从而影响管腔气道上皮细胞的黏液纤毛清除活动。目前尚不清楚对气道上皮防御重要的蛋白表达是否在上皮中极化,如果是,香烟诱导的气道上皮重塑如何影响它们的表达。我们假设,吸烟引起的上皮细胞分化改变导致导致呼吸HDPs的蛋白表达减少,这可能使宿主更容易受到感染。
方法
细胞培养
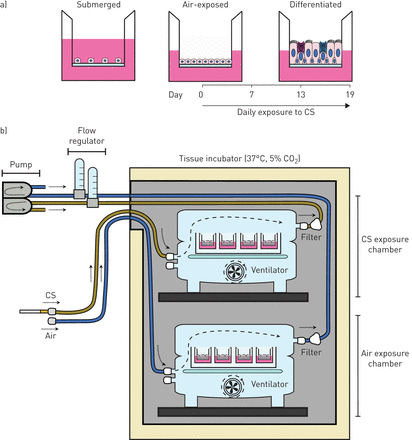
原发性支气管上皮细胞(PBECs)是在Leiden大学医学中心(Leiden,荷兰)从无肿瘤切除的肺组织中获得的在线补充材料,并如所述有文化[11].PBECs在气液界面(ALI)培养13-19天(图1一个).每天进行根尖冲洗;中号每隔一天刷新一次。
细胞培养和烟熏暴露在气液界面分化的原代支气管上皮细胞(PBECs)。a)将PBECs种在包被的transwell上,在淹没条件下培养至融合。第0天,将培养物暴露在空气中,再培养13-19天,使粘液纤毛分化。b)每天,从第0天开始,将培养物置于暴露室中,分别注入CS或空气4-5分钟。接下来,将来自培养箱的空气注入培养箱,以消除室内的残留烟雾10分钟。每次CS暴露前约4小时,将培养物顶端表面冲洗以去除粘液。每隔一天更换基础培养基。有限公司2:二氧化碳。
气道上皮培养物的分离
如前所述,从3-4周分化的ALI-PBEC培养物中获得腔内和基底细胞富集组分[11]。将管腔细胞部分向下旋转并在RNA裂解缓冲液中裂解或在PBS中用1%多聚甲醛(荷兰阿姆斯特丹Millipore)固定10分钟 将transwell嵌件上剩余的基底上皮细胞部分在RNA裂解缓冲液(Promega,Leiden)中裂解或在PBS中用1%多聚甲醛(微孔)固定10分钟 然后用冰冷的PBS清洗。接下来,细胞按照图中所述进行染色在线补充材料使用抗体,如在线补充表S2.
长期接触香烟烟雾
当聚合后,PBECs通过从transwell插入的顶端去除培养基暴露在空气中(第0天),4小时后使用3R4F参考香烟暴露于新鲜产生的全香烟烟雾中(肯塔基大学,列克星敦,KY,美国)。每日重复接触香烟烟雾,详情见[11],在图中的图中图1和在线补充图S1和说明图1 b和在线补充图S1.简单地说,将细胞暴露在改良的低氧室中4-5分钟,吸入来自一支香烟的烟雾或室内空气,之后通过通风10分钟以上的空气来消除烟雾,随后将细胞放回培养箱过夜。至18-20小时后,用PBS清洗ALI-PBEC, 4小时后暴露在香烟烟雾中。这个循环每天重复,直到第13-19天。在最后一次卷烟烟雾暴露后18-20小时采集细胞进行分析。
共聚焦显微镜
细胞用1%的多聚甲醛(Millipore)在PBS中冰冻固定在transwell插片上10分钟,然后用冰水PBS清洗。接着,按图中所示对细胞进行染色在线补充材料使用抗体,如在线补充表S2.
Transcytosis实验
方法在在线补充材料.
抗菌活性试验
方法在在线补充材料
酶联免疫吸附试验和经上皮电阻测定
方法在在线补充材料.
DAPT抑制分化
第0天,通过去除插入物中的培养基,将pbec暴露在空气中,并用添加5µM DAPT (Notch信号通路抑制剂;Sigma Aldrich, Zwijndrecht,荷兰)或溶剂控制。每隔一天,以类似的方式改变基础培养基,直到第13天,当细胞被收获。
统计
采用GraphPad Prism 7 (GraphPad Software, La Jolla, CA, USA)进行统计分析。数据以平均值±表示扫描电镜和显著性使用配对t检验或双向方差分析与bonferroni校正事后测试。p<0.05时认为差异显著。
结果
呼吸道宿主防御蛋白在气道上皮细胞培养中呈极化分布
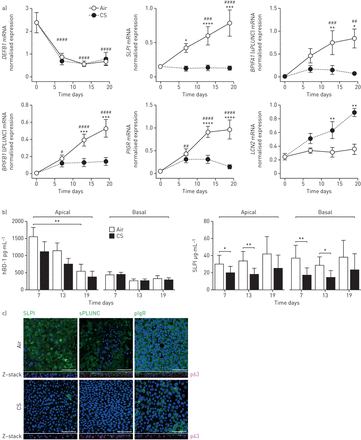
在这项研究中,我们重点研究了一组对呼吸道宿主防御很重要的蛋白质和多肽。这些HDPs是根据它们的组成和/或气道上皮细胞在稳态期间的高表达而选择的,即。SLPI, s/lPLUNC, pIgR, hBD-1和LCN2。首先,我们研究了在气道上皮培养中这些蛋白的表达是否极化。为此,我们制备了分化良好的PBECs的管腔和基底上皮细胞富集部分,在ALI (图2a).通过确定典型基底细胞标记物的基因表达,我们证实了腔细胞和基底细胞的成功富集TP63和KRT5和管腔上皮细胞标记物FOXJ1(纤毛细胞),SCGB1A1(俱乐部牢房),MUC5AC和MUC5B(两个杯状细胞)(图2a), p63(基底细胞)、CC16(球杆细胞)和乙酰化α-微管蛋白(纤毛细胞)免疫荧光染色(在线补充图S2).进一步分析表明,腔细胞富集的部分表达了显著高水平的BPIFA1(sPLUNC),BPIFB1(lPLUNC)和SLPI(图2a).相比之下,LCN2和DEFB1腔内和基底细胞富集部分的表达无差异(图2a).通过共聚焦成像进一步证实了SLPI和sPLUNC的管腔细胞特异性表达,这两种蛋白的染色均未与p63共定位+基底细胞,但在PBEC培养的根尖侧和管腔细胞富集部分高度存在(图2b和在线补充图S2).
呼吸宿主防御蛋白在原代支气管上皮细胞(PBEC)的气液界面(ALI)培养物中呈极性分布。a)PBEC接种在包被的转孔上,在浸没条件下培养直至融合。第0天,培养物暴露在空气中,并在ALI处培养。3-4之后 分离分化周的管腔和基底细胞富集部分,然后进行RNA分离、互补DNA合成和定量(q)PCR分析。数据显示为参考基因ATP合成酶、氢转运、线粒体F1复合物、β-多肽几何平均表达的标准化目标基因表达(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A);n = 5 - 7不同的捐赠者。采用配对t检验进行统计学意义检验。*: p<0.05, **: p<0.01, ***: p<0.001。b)共聚焦图像显示在分化的ALI-PBEC培养细胞中分泌白细胞蛋白酶抑制剂(SLPI)和短腭、肺和鼻上皮克隆蛋白(sPLUNC)的极化分布。经过3周的分化,细胞被固定在1%多聚甲醛,用免疫荧光染色主要抗体p63(基底细胞标记,红色)结合主要抗体SLPI和/或sPLUNC(绿色)和4”,6-diamidino-2-phenylindole (DAPI)核染色(蓝色)。共聚焦成像成像染色细胞顶端和基底侧的z堆和图像。显示的图像代表了从四个不同的捐赠者获得的细胞的结果。规模酒吧= 50µm。
慢性吸烟暴露气道上皮细胞培养减少呼吸道HDPs的表达
接下来,我们研究了香烟烟雾暴露是否影响这组呼吸HDPs的表达。为此,ALI-PBEC培养物在2-3周的分化过程中每天暴露于全烟烟雾(图1和在线补充图S1).基因表达分析表明DEFB1(hBD-1) mRNA水平在分化过程中降低,但不受卷烟暴露的影响(图3一).相反,的表达SLPI,BPIFA1(sPLUNC),BPIFB1(lPLUNC)和PIGR在分化过程中显著增加,而吸烟显著地阻止了这种增加(图3一).相反,基因表达LCN2(脂钙素2)在分化过程中因暴露于卷烟而增加(图3一).通过评估来自ALI-PBEC培养的根尖洗涤和基础培养基中的hBD-1和SLPI蛋白水平,进一步证实了这些发现(图3 b)事实上,hBD-1水平在根尖洗涤液中随分化时间而降低,但不受慢性吸烟暴露的显著影响,而SLPI水平在慢性吸烟暴露的细胞培养物中显著降低(图3 b).接下来,我们对气道上皮细胞培养进行免疫荧光染色,发现与空气对照相比,慢性吸烟暴露上皮细胞中SLPI-、sPLUNC-和pigr阳性细胞的存在显著减少(图3 c).这些结果证实了在气道上皮细胞分化过程中,慢性香烟烟雾暴露可选择性损害特定的呼吸HDPs。
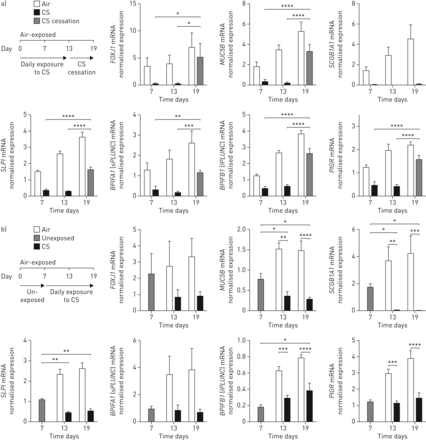
原代支气管上皮细胞(PBECs)培养物长期暴露于卷烟空气-液体界面(ALI)可降低管腔细胞受限宿主防御蛋白的表达。a) ALI-PBECs在分化过程中每天暴露在全烟烟雾(CS)或空气中作为对照(air),连续13-19天。在这一过程中,细胞在几个点被裂解,RNA被分离,然后互补DNA合成,以评估基因表达DEFB1(人类β-defensin-1 (hBD-1)),SLPI(分泌性白细胞蛋白酶抑制剂)BPIFA1短腭、肺和鼻上皮克隆蛋白(sPLUNC)),BPIFB1(长腭,肺和鼻上皮克隆蛋白(lPLUNC)),PIGR(聚合免疫球蛋白受体)和LCN2(lipocalin 2).数据以靶基因表达为标准,内参基因ATP合酶、氢转运、线粒体F1复合物、β多肽(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A).第0、7和13天n=8个不同的供体;第19天n=4个不同的供体。使用双向方差分析和Bonferroni评估统计差异事后测试。* *: *: p < 0.05, p < 0.01, * * *: p < 0.001, * * * *:空气和CS之间p < 0.0001。#: p < 0.05,##: p < 0.01,###: p < 0.001,####:第7、13和19天空气和第0天未暴露培养之间的p<0.0001。b)在这些培养物的顶端洗涤液和基础培养基上进行hBD-1和SLPI的ELISA检测。第7天和第13天,n=8个不同的捐赠者,第19天n=4个不同的捐赠者。第7天和第13天(而不是第19天)的统计差异使用成对双向方差分析来比较空气和CS。*: p<0.05, **: p<0.01。c) ALI-PBECs分化2-3周,每天暴露于CS或空气中作为对照。随后,细胞在1%多聚甲醛中固定,使用抗SLPI、sPLUNC和pIgR的一抗染色(均为绿色),结合4',6-二氨基-2-苯基吲哚(DAPI)染色细胞核(蓝色)。所示图像代表了从四种不同供体获得的细胞培养结果。规模酒吧= 50µm。
慢性烟雾暴露通过减少顶端分泌IgA的释放和细菌的杀死来降低宿主对气道上皮细胞培养的防御莫拉克斯氏菌属复活和Klebsiella肺炎
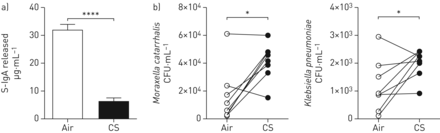
接下来,我们评估了是否大幅减少SLPI,BPIFA1(sPLUNC),BPIFB1(lPLUNC)和PIGR在吸烟暴露的气道上皮培养中表达水平对宿主防御具有功能后果。我们选择了pigr介导的二聚体(d)IgA穿过上皮细胞的转移,作为免疫调节宿主防御功能后果的原理证明,并发现在长期暴露于香烟烟雾的培养中这一结果显著降低(图4一).此外,我们还分析了慢性暴露在香烟烟雾中的革兰氏阴性菌的细胞培养对细菌的杀灭作用莫拉克斯氏菌属复活和Klebsiella肺炎,发现COPD稳定或急性加重患者肺部的病原体增多[12].与暴露在空气中的PBEC培养物相比,我们观察到慢性吸烟暴露的PBEC培养物的细菌计数显著升高(表明抑菌活性较低)(图4 b).这些数据表明,在吸烟暴露的上皮细胞培养中,多种宿主防御机制功能受损,这与呼吸防御蛋白表达受损相对应。
原代支气管上皮细胞(PBECs)培养物的慢性烟雾暴露损害宿主的防御活动。a) ALI-PBECs在分化期间每天暴露于全烟烟雾(CS)或空气中作为对照(air),连续13天。在13天的慢性CS暴露后,通过ELISA测定顶端冲洗的分泌(S)-IgA水平来评估上皮培养物的二聚体(d)IgA转运能力(在基础培养基中不能检测到S-IgA,作为只识别S-IgA而不识别d-IgA的对照)。n = 10个不同的捐赠者。b)慢性CS暴露13天后,ALI-PBECs在无抗生素细胞培养基中培养48 h,然后暴露2 h莫拉克斯氏菌属复活或Klebsiella肺炎在ALI-PBEC的顶端。存活的细菌为CFU·mL-1.n = 8种不同的捐赠者。采用配对t检验确定显著性。*: p<0.05, ****: p<0.0001。
吸烟影响气道上皮细胞的终末期分化
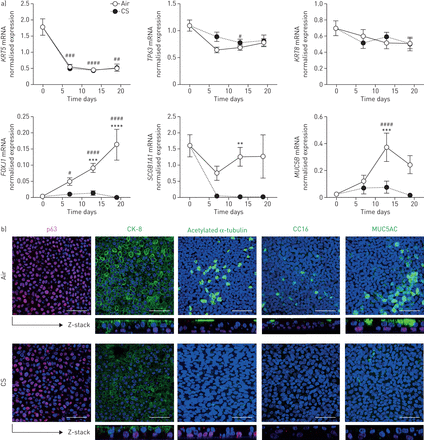
接下来,我们通过测量上皮细胞特异性标记物的基因表达来评估慢性卷烟暴露是否会影响ALI-PBECs的分化。基底细胞标志物细胞角蛋白-5 (KRT5),TP63和细胞角蛋白8 (KRT8),由中间/委托祖细胞上皮细胞表达[13],没有受到香烟烟雾的影响(图5a).相反,腔上皮细胞特异性基因的表达FOXJ1(纤毛细胞),SCGB1A1(俱乐部细胞)MUC5B(杯状细胞)在分化过程中增加,吸烟显著地阻止了这种增加(图5a).共聚焦成像证实了香烟暴露培养中异常的上皮分化,在慢性吸烟暴露培养中,纤毛标记物乙酰化α-微管蛋白、球杆细胞标记物CC16和杯状细胞标记物MUC5AC阳性细胞减少,而细胞角蛋白8 (CK-8)。+和p63+暴露在空气和香烟烟雾中的培养细胞保持不变(图5b).
慢性卷烟烟雾(CS)风液界面(ALI)培养物的初级支气管上皮细胞(PBEC)改变细胞组合物。a)在分化期间暴露Ali-PBEC以连续13-19天暴露于整个CS。在几个时间点裂解细胞,并分离RNA,然后互补DNA合成,评估基础细胞标志物细胞角蛋白-5的基因表达(KRT5),TP63,早期祖细胞标志物细胞角蛋白-8 (KRT8)和专用细胞标志物FOXJ1(纤毛细胞),SCGB1A1(俱乐部细胞)MUC5B(杯状细胞)。参考基因ATP合酶、氢转运、线粒体F1复合物、β-多肽(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A).第0,7和13天= 8个捐助者;第19天= 4个捐助者。使用双向Anova和Bonferroni确定了意义事后测试。* * * * *: p < 0.01, p < 0.001, * * * *:空气和CS之间p < 0.0001。#: p < 0.05,##: p < 0.01,###: p < 0.001,####:在第7,13和19天之间的空气之间的P <0.0001和时刻0.b)ali-pbecs分化为2-3周并每天暴露于Cs。随后,将细胞固定在1%多聚甲醛中,并使用对基底细胞(P63)(红色)的一抗染色,与抗细胞角蛋白-8(CK-8),乙酰化α-微管蛋白(纤维化细胞),CC16组合。(俱乐部细胞)和MUC5Ac(脚杯细胞)(绿色);4′,6-二氨基-2-苯基吲哚(DAPI)染色细胞核(蓝色)。使用共聚焦成像获得染色细胞的顶端和基底侧的Z堆叠和图像。所示的图像是具有来自四种不同供体(CK-8,N = 3个不同供体)的细胞获得的结果的代表性。规模酒吧= 50µm。
卷烟对HDP表达影响的可逆性
以评估吸烟引起的减少的持久性SLPI,BPIFA1(sPLUNC),BPIFB1(lPLUNC)和PIGR表达水平及其对细胞组成的影响,我们通过额外培养6天不暴露于卷烟烟雾的细胞,使培养细胞从暴露于卷烟烟雾的13天恢复过来。长期暴露在香烟烟雾中的培养物能够(部分)从缺乏末期分化中恢复,因为所有特化的管腔细胞标记物,除了SCGB1A1(球团细胞)的表达显著增加(图6a).此外,SLPI,BPIFA1(sPLUNC),BPIFB1(lPLUNC)和PIGR与第13天相比,表达增强(图6a).此外,KRT5(基底细胞标记物)DEFB1和LCN2戒烟后增加,反之TP63和KRT8未受影响(在线补充图S3A).这表明,卷烟暴露对上皮细胞分化和特异性呼吸防御蛋白表达的抑制作用至少部分是可逆的。此外,为了更好地模仿在活的有机体内我们进行了一个单独的实验,以确定当将已经部分分化的上皮暴露于慢性香烟烟雾时,是否可以获得慢性香烟烟雾暴露后观察到的影响。在这个实验中,我们首先让培养物分化一周,之后我们开始额外的12天慢性吸烟暴露。在这里,我们发现从第0天开始,与接触香烟烟雾相比,接触香烟烟雾对ALI-PBEC培养物的细胞类型特异性标记物和HDP表达有类似的影响(图6b和在线补充图S3B).
香烟烟雾(CS)诱导的宿主防御蛋白和分化标记的损伤在停止吸烟后部分持续。a)将原代支气管上皮细胞(PBECs)的气液界面(ALI)培养物在分化过程中暴露于全CS连续13天,之后继续培养6天不暴露于CS。在这一过程中,细胞在几个点被裂解,然后分离RNA,然后合成互补DNA,以评估细胞特异性标记物的基因表达:FOXJ1(纤毛细胞),MUC5B(杯状细胞)和SCGB1A1(俱乐部细胞)和呼吸防御蛋白:SLPI(分泌性白细胞蛋白酶抑制剂)BPIFA1(短腭、肺和鼻上皮克隆蛋白(sPLUNC)),BPIFB1(长腭、肺和鼻上皮克隆蛋白(lPLUNC))PIGR(聚合物免疫球蛋白受体)。参考基因ATP合酶、氢转运、线粒体F1复合物、β-多肽(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A).n = 8种不同的捐赠者。仅使用双向方差分析和Bonferroni来评估停止和先前CS表达之间的差异事后测试。b) ALI-PBECs在第0天暴露于空气中,在标准条件下培养7天。在第7天培养时,将细胞置于CS中连续12天,之后对细胞进行分析,类似于(a)。数据显示为靶基因表达与内参基因的几何平均表达归一化ATP5B,B2M和RPL13A。n = 6个不同的捐赠者。使用双向方差分析和Bonferroni评估统计差异事后测试:p<0.05,***:p<0.01,***:p<0.001,***:p<0.0001。
Notch信号传导抑制在分化期间损害HDP表达
到目前为止,我们的结果显示,在香烟烟雾暴露的培养物中,终末期分化为特殊管腔上皮细胞的能力受损,导致SLPI水平降低,sPLUNC, lPLUNC和pIgR。既往研究表明Notch信号参与气道上皮分化,吸烟者气道上皮显示Notch信号减弱[14].因此,我们接下来研究了在香烟暴露培养中Notch信号是否受损,以及Notch信号抑制是否在分化过程中调节HDP的表达。首先,我们评估了Notch信号级联元件的基因表达,发现在这些培养中,长期暴露在香烟烟雾中并不影响Notch配体、受体或转录共激活因子的基因表达(图7a).然而,Notch信号的靶基因,HEY1和HEY2,因长期接触香烟烟雾而显著降低,而hes1没有(图7b),表明长期暴露在香烟烟雾中会选择性地影响Notch信号通路的靶基因。
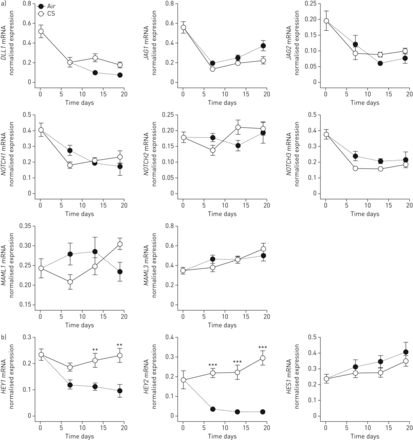
慢性香烟烟雾(CS)暴露于气液界面(ALI)培养的原代支气管上皮细胞(PBECs)可导致Notch信号的选择性损伤。a)分化2周后,每日暴露于卷烟烟雾,裂解ALI-PBECs,分离RNA,合成互补DNA。随后对notch信号配体进行定量PCR分析DLL1.,JAG1和JAG2,在陷波受体1-3和转录的共同活化剂上MAML1和MAML3;数据显示为ATP合酶、氢转运、线粒体F1复合物、β-多肽(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A).n = 8种不同的捐赠者。b)后续对Notch信号转导靶基因进行qPCR分析HEY1,HEY2和hes1.数据显示为靶基因表达归一化后的内参基因几何平均表达ATP5B,B2M和RPL13A。n = 8种不同的捐赠者。使用双向方差分析和Bonferroni检验统计学显著性事后测试。**: p<0.01, ***: p<0.001。
为了进一步研究Notch信号在宿主防御蛋白表达中的重要性,我们检测了γ分泌酶抑制剂DAPT的作用,它作为Notch信号的抑制剂(图8a).在DAPT存在的PBEC分化15天后,我们测量了HDPs的表达。DEFB1(hBD-1)和LCN2未受DAPT影响,而SLPI,BPIFA1(sPLUNC),BPIFB1(lPLUNC)和PIGR被DAPT孵育强烈降低(图8b).此外,dapt暴露培养显示出细胞分化偏离分泌表型向纤毛细胞增加的倾斜(图8c)也通过共聚焦成像确认(图8d).
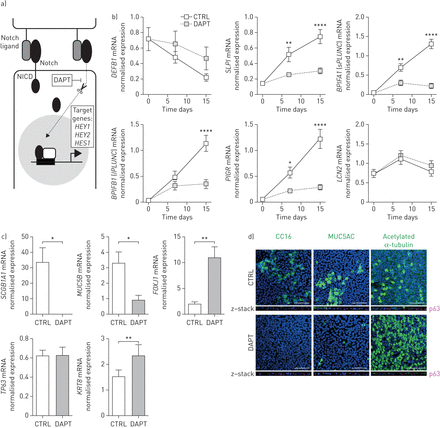
DAPT抑制原代支气管上皮细胞(PBECs)气液界面(ALI)中宿主防御蛋白的表达。a) Notch抑制剂DAPT的作用机制。DAPT是一种γ分泌酶抑制剂,可防止Notch细胞内结构域(NCID)的蛋白水解裂解。b)将PBECs种在包被的transwell上,在淹没条件下培养直到融合。第0天,在基础培养基或溶剂中加入5µM的Notch信号转导抑制剂DAPT作为对照,细胞再分化15天。分别在第0、7和15天裂解细胞,分离RNA并合成互补DNA。随后进行定量PCR分析,以评估呼吸防御蛋白和上皮细胞特异性基因的表达,如DEFB1(人类β防御素-1),SLPI(分泌性白细胞蛋白酶抑制剂)BPIFA1(短腭、肺和鼻上皮克隆蛋白),BPIFB1(长腭、肺和鼻上皮克隆蛋白)、聚合免疫球蛋白受体(PIGR),LCN2(lipocalin 2)。数据显示为靶基因表达归一化后的内参基因ATP合酶、氢转运、线粒体F1复合物、β-多肽(ATP5B),β2-microglobulin (B2M)及核糖体蛋白L13a (RPL13A).n = 7个不同的捐赠者。使用双向方差分析和Bonferroni检验统计学显著性事后测试。*: p<0.05, **: p<0.01, ****: p<0.0001之间的对照(CTRL)和DAPT。c)采用qPCR检测上皮细胞标记物的mRNA表达SCGB1A1(俱乐部牢房),MUC5B(杯状细胞),FOXJ1(纤毛细胞),TP63(基底细胞)和细胞角蛋白8 (KRT8)(中间细胞)分化15天后用DAPT或溶剂对照。n = 6个不同的捐赠者。采用配对t检验进行统计学意义检验;*: p<0.05, **: p<0.01。d)用DAPT或溶剂对照分化ALI-PBECs 15天。随后,细胞在1%多聚甲醛中固定,并使用针对CC16(球杆细胞)、MUC5AC(杯状细胞)和乙酰化α-微管蛋白(纤毛细胞)的一抗进行染色(绿色);4′,6-二氨基-2-苯基吲哚(DAPI)染色细胞核(蓝色)。所示图像代表了从三种不同供体获得的细胞的结果。规模酒吧= 50µm。
讨论
在这里,我们证明香烟烟雾对呼吸HDPs: pIgR, SLPI, lPLUNC和sPLUNC的表达有负面影响。在分化过程中,每天暴露在香烟烟雾中的上皮细胞表达明显减少,这是由于特化管腔细胞末期分化受损的结果。因此,香烟烟雾对气道上皮的重塑对呼吸道宿主的防御产生了重大影响,尤其是IgA在暴露于香烟烟雾的上皮细胞中的传输严重减少和抗菌防御受损复活的和k .肺炎.我们的数据表明,增加特定呼吸HDPs的表达(或防止其减少)可能对改善COPD患者肺部的宿主防御有治疗意义。此外,这种(选择性)损失也可能导致肺微生物组组成的变化,这越来越被认为是慢性炎症性肺病的重要因素[15,16].
ALI-PBEC培养物的细胞组成在长期暴露于香烟烟雾后发生了显著变化。中间CK-8的存在+上皮细胞(也称为早期、中期或委托祖细胞[13,17)不受长期暴露于香烟烟雾的影响,在长期暴露于香烟烟雾的培养物中特异性的腔细胞标记物减少。这些结果表明,暴露于香烟烟雾似乎会损害终末期分化。当细胞第一次在没有香烟烟雾的情况下分化一周时,也观察了长期暴露在香烟烟雾中的影响。此外,在戒烟后,大多数管腔细胞标记物的基因表达都有较强的恢复。相比之下,SCGB1A1在恢复近1周后,mRNA表达仍然缺失,表明吸烟对杆状细胞分化或调控异常有害SCGB1A1基因的表达。一项研究强调了这一点,该研究表明,俱乐部细胞蛋白CC16 (SCGB1A1)在COPD患者和暴露于香烟烟雾的小鼠中减少。CC16的缺失与疾病的严重程度增加相关,在过表达CC16的小鼠中,吸烟引起的肺部炎症较低[18].
细胞毒性不太可能对香烟烟雾对li - pbec培养物的诱导作用有主要贡献,因为我们在香烟烟雾和空气暴露对照之间的分化过程中,没有检测到作为屏障功能测量的跨上皮电阻(TEER)的差异。我们之前观察到,急性单次吸烟暴露后TEER短暂下降,24小时后恢复正常[11].在我们的慢性吸烟设置中,我们在先前吸烟暴露18-20小时后测量了TEER,这可能解释了为什么我们没有观察到空气和香烟暴露培养之间的TEER有显著差异。先前的研究表明,吸烟会降低TEER,但通常使用香烟烟雾提取物(CSE),而不是整个香烟烟雾[19,20.].CSE与我们研究中使用的整个卷烟烟雾的成分和浓度不同。此外,在一些研究中,CSE被添加到基础培养基中,导致从transwell的基础侧刺激[19].这也可能导致TEER效应的差异。在我们的烟草暴露培养中,乳酸脱氢酶释放没有增加,而在一些供体的烟草暴露培养中,细胞大小出现较大。最后,暴露在香烟烟雾中的培养物产生了更多的白细胞介素-8,并显示出更多的可诱导的抗菌肽rna - 7和LL-37(而不是hBD-2)的mRNA表达。这些结果在在线补充材料而在在线补充图S4.
出乎意料的是,我们没有观察到培养物中暴露于卷烟烟雾的培养细胞增生,以前在吸烟者中显示[21,豚鼠[22),大鼠(23]和细胞系[23,24]或暴露于CSE的PBECs [19].然而,Brekman等.[25]观察到持续暴露于CSE的PBECs杯状细胞标志物下降。因此,数据是相互矛盾的,依赖于所使用的细胞培养的类型。显然,在我们的原代分化培养中,完全暴露于卷烟烟雾不足以在19天内诱导杯状细胞增生。我们强烈认为,患者的研究结果可能是由吸烟引起的炎症的二次效应(这在我们的研究中显然不完全代表在体外模型)。例如,由于香烟诱导的炎症和后续释放蛋白酶和其他分子的中性粒细胞募集可能有助于解释患者的脚卵细胞形成。此外,除嗜中性粒细胞(例如巨噬细胞)之外的其他细胞类型的存在似乎很重要。这是在文献中提出的[26- - - - - -29].此外,一些研究表明,参与COPD发病机制的各种其他因素,包括细菌和病毒感染,在促进脚卵细胞增生方面可能具有重要作用[30.,31].
而之前的研究表明,吸烟会减少纤毛细胞的存在[19,25,32],到目前为止,香烟诱导的气道上皮重塑尚未被证实与高表达的呼吸HDPs水平的变化有关,尽管事实上这些蛋白的表达变化已经在吸烟者或COPD患者中被报道。一个arbiouet al。[33结果显示,与非COPD患者相比,COPD患者受损支气管上皮中SLPI的表达明显降低ohyet al。[10与健康对照组相比,COPD患者肺部的pIgR水平降低;然而,这在肺功能正常的吸烟者中并不常见。最后,与不吸烟者相比,在当前吸烟者的支气管刷中检测到较低的PLUNC水平[34].
我们观察到吸烟暴露的气道上皮培养物的抗菌活性受损复活的和k .肺炎.此外,我们评估了使用栅格测定的慢性卷烟烟雾暴露培养物的直接抗菌活性,并使用细菌的活/死亡染色[35,36),通过常规电镀方法铜绿假单胞菌和non-typeable流感嗜血杆菌,但无法检测到任何差异(数据未显示)。这些数据表明,所观察到的吸烟引起的抗菌活性损伤可能是病原体特异性的,因为并不是在所有被研究的病原体中都能观察到。除了抑制宿主的抗菌防御活性外,气道上皮表达HDP的缺失还会对宿主产生进一步的负面影响。例如,SLPI表达缺失(正常肺组织中高表达)可促进COPD患者肺部炎症。SLPI作为有害蛋白酶的抑制剂,如中性粒细胞弹性蛋白酶,作为核因子-κB激活的抑制剂,并调节巨噬细胞功能[37- - - - - -39].sPLUNC参与上皮钠通道的调节,从而调节气道表面液体(ASL),降低水平可导致ASL体积降低和粘液纤毛清除受损[40].
由于此前有报道称Notch信号在COPD中受损[14,我们首先分析了慢性吸烟暴露对Notch信号通路成分和Notch靶基因的影响,发现吸烟降低了选定的Notch靶基因的表达。当我们接下来使用Notch信号抑制剂DAPT来抑制气道上皮细胞分化时,我们发现与香烟烟雾暴露相比,在呼吸道HDPs的选择组表达上有类似的效果。据我们所知,这是第一个将Notch信号与一系列在分化时增加的HDPs表达联系起来的研究。尽管长期暴露在香烟烟雾中导致所有腔细胞标记物的减少,但与对照处理的细胞相比,dapt暴露的培养细胞显示出更高水平的纤毛细胞,这与之前的研究一致[41,42].这些结果表明腔细胞限制性HDPs的表达仅限于成熟的分泌上皮细胞,而不是纤毛上皮细胞。进一步的研究使用单细胞RNA测序,可能揭示是否表达局限于某种分泌细胞表型。dapt培养的培养物与暴露在香烟烟雾中的培养物之间的部分相似性表明,在香烟烟雾诱导的效应中,Notch信号的改变参与其中。然而,其他信号通路的改变也可能与吸烟的影响有关,例如涉及上皮生长因子受体[32,转化生长因子-β [25], Wnt [43和骨形成蛋白[44].很有可能,一种更系统/组学的方法有可能详细阐明慢性香烟烟雾暴露对Notch和其他信号通路的所有影响[45].
总之,这些发现通过强调呼吸道上皮细胞分化在呼吸HDPs表达中的重要性,为吸烟者和COPD患者中宿主防御失调的作用提供了新的线索。进一步研究香烟烟雾抑制上皮细胞分化如何导致微生物感染为了开发新的治疗方法来恢复COPD患者的气道上皮-宿主防御,需要对气道进行细菌定植和感染。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑的,而是由作者提供的。
在线数据补充ERJ-01009-2017在线数据补充
补充图s1图1
补充图s2sFigure 2低
补充图s3sFigure 3低
补充图s4sFigure 4低
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:概念与设计:G.D.阿马特加利姆,J.A.施伦普夫,F.迪什切肯尼安,P.S.希姆斯特拉,A.M.范德杜斯;分析与解释:G.D.阿马特加利姆,J.A.施伦普夫,F.迪什切肯尼安,D.K.尼纳伯,A.C.范德林登,C.皮莱特,P.S.希姆斯特拉,A.M.范德杜斯;起草手稿以供重要参考知识内容:G.D.阿马特加利姆、J.A.施伦普夫、C.皮莱特、C.陶贝、P.S.希姆斯特拉、A.M.范德多斯。
利益冲突:P. HIEMSTRA从欧盟(Marie Curie内欧洲奖学金)的赠款(研究奖学金)报告荷兰肺基金会,加拉帕戈斯N.V.和Boehringer Ingelheim的拨款(无限制的研究补助金),外部提交的工作。
支持声明:这项工作得到了玛丽·居里欧洲内部奖学金(#622815)和荷兰肺基金会(#5.1.13.033)和加拉帕戈斯群岛的资助Crossref资助者注册表.
- 收到了2017年5月17日。
- 接受2018年2月28日。
- 版权©2018人队