摘要
使用固定比率来定义气流限制(AFL)的假设结果是,老年人诊断过度,而年轻人诊断不足。然而,年轻个体潜在诊断不足的AFL的预后描述很差。我们假设年轻时AFL的潜在诊断不足与预后不良有关。
我们将来自哥本哈根一般人群研究的95 288名20-100岁的参与者分为以下组:没有AFL但1秒内用力呼气量(FEV)的人1)/强迫肺活量(FVC)≥0.70和≥正常下限(LLN) (n=78 779, 83%);潜在诊断不足的AFL伴FEV的个体1/FVC≥0.70 and 与没有AFL的个体相比,潜在诊断不足的AFL个体的发病率和死亡率增加,年龄和性别校正的危险比(HR)肺炎为2.7 (95% CI: 1.7-4.5),心力衰竭为2.3 (95% CI: 1.2-4.5),全因死亡率为3.1 (95% CI: 2.1-4.6)。 根据LLN(但不是固定比例),年轻和中年AFL患者的呼吸和心血管发病率和早期死亡增加。
摘要
中青年患者按LLN限流但不固定比例,预后较差http://ow.ly/QwOP30iiU11
介绍
慢性阻塞性肺疾病(COPD)的诊断不足是严重的,并与预后不良相关,即使在无症状的个体中[1].然而,气流限制(AFL)的存在与较低的1秒内用力呼气容积比(FEV)1)及强迫肺活量(FVC)可轻易用肺活量测定法测定[2,3.].尽管不推荐使用肺活量测定法筛查无症状成人,但鼓励使用肺活量测定法,以便让临床医生在高危人群中积极寻找病例,并在严重AFL出现之前及早发现COPD [4].人们对AFL的恰当定义进行了激烈的讨论。一方面,使用固定的比率(即。FEV1/FVC <0.70)在繁忙的日常临床环境中是一种简单的方法[2,3.,而另一方面,固定比例不能解释正常的年龄依赖性肺功能下降,导致FEV比例较低1/随年龄增长的植被覆盖度[5].因此,使用固定比例的假设结果将是老年人诊断过度,而年轻人诊断不足[5,6].后一种情况尤其令人担忧,因为它可能妨碍戒烟建议和早期治疗的开始。建议使用FEV预测值的较低的第5百分位,而不是固定的比例1/ FVC (即。FEV1/FVC <正常下限(LLN)),因此这种方法不会倾向于肺功能的年龄依赖性变异,也能够解释其他生物学差异,如性别和种族[7,8].以往的研究主要集中在可能过度诊断的老年AFL (FEV)患者的预后1/FVC <0.70,≥LLN)。然而,年轻的AFL (FEV)患者的预后可能不佳1/FVC≥0.70和 在本研究中,我们调查了来自一般人群的年轻个体中潜在诊断不足的AFL的预后,通过LLN而不是固定比例来定义。为此,我们使用了哥本哈根一般人口研究,包括95 288名20-100岁的随机选择的个体。我们假设年轻时AFL的潜在诊断不足与预后不良有关。
方法
研究设计和参与者
我们从哥本哈根一般人口研究中招募了95 288名年龄在20-100岁的人,这是一项丹麦基于人口的前瞻性队列研究,于2003年11月26日开始,正在进行注册[1].在本次研究中,我们获得的信息截止到2013年7月10日。在丹麦,所有个人在出生或移民时都有一个唯一的身份识别号码,并记录在丹麦国家民事登记系统中。根据年龄和性别,从该登记系统中随机选择居住在丹麦首都地区的个人,使用唯一的识别号码,以反映丹麦血统的成年丹麦白人人口。应答率约为45%,所有参与者完成了一份全面的问卷调查,进行了身体健康检查,并提供了血液进行生化分析。调查问卷在出席的当天由保健专业人员和参与者一起审查。该研究由Herlev和Gentofte医院和地区伦理委员会批准(H-KF-01-144/01),并根据《赫尔辛基宣言》进行。所有参与者均提供书面知情同意。
临床组的形成
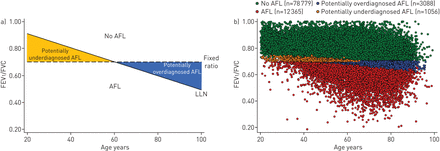
肺功能测定采用支气管扩张剂前FEV肺活量测定法1和FVC。哥本哈根普通人群研究中肺活量测定的使用经过了严格的验证过程[9].使用内部衍生参考值分别计算男性和女性的预测值,该参考值基于11 288名健康、无症状、从不吸烟的亚样本,年龄和身高为协变量[9].肺测量程序的详细描述和用于评估特征的问题可以在补充材料.LLN,定义为FEV预测值的较低的第5百分位1/植被覆盖度,以平均值减去1.645个标准差计算。根据AFL的不同标准,患者被分为4个单独的亚组(图1),如下:1)无AFL (FEV患者1/FVC≥0.70和≥LLN);2)可能诊断不足的AFL (FEV患者1/FVC≥0.70但 气流限制(AFL)的定义及正常下限与固定比率标准的区别。(a)基于AFL的两个不同标准的理论描述,固定比率和正常下限(LLN)。(b)将哥本哈根一般人口研究的个人分配到AFL的不同标准。AFL未定义为1 s内用力呼气量(FEV)1)/强迫肺活量(FVC)≥0.70和FEV1/ FVC≥LLN。潜在诊断不足的AFL定义为FEV1/FVC≥0.70和FEV1/ FVC < LLN。可能过度诊断的AFL被定义为FEV1/FVC <0.70和FEV1/ FVC≥LLN。AFL定义为FEV1/FVC <0.70和FEV1/ FVC < LLN。
结果
严重加重的阻塞性肺病,包括COPD和哮喘相关(国际疾病分类(ICD)代码ICD-8: 491-493和ICD-10: J41-J46)和肺炎(ICD-8: 480-486和ICD-10: J12-J18)被定义为具有上述初级诊断的急诊科就诊或住院。缺血性心脏病(ICD-8: 410-414和ICD-10: I20-I25)和心力衰竭(ICD-8: 427.09-427.11和ICD-10: I50)被定义为具有上述初级或二级诊断的住院和门诊患者。截至2014年11月10日的信息来自丹麦国家患者登记处,该登记处涵盖了丹麦所有公立和私立医院。丹麦在1994年1月1日之前一直使用ICD第8修订版(ICD-8),然后在这一日期之后直接使用第10修订版(ICD-10)。生命状态信息从丹麦国家民事登记系统获得,记录到2014年11月14日。由于使用登记册进行跟踪(根据每个人出生或移民时提供的唯一识别号码进行连接),没有人在跟踪中失踪,而移民的个人在移民日期被审查(n=376)。登记册中记录的所有诊断都是根据国家法律由一名医生作出的。
统计分析
比较采用Wilcoxon秩和检验和Pearson卡方检验。由于临床组之间的年龄差异很大,使用逻辑回归和线性回归模型来解释临床属性;但是,也提供了未经调整的差异。核密度估计用于说明临床组的年龄分布,Cox比例风险模型用于确定预后。对于急性加重和肺炎,采用Andersen-Gill方法进行多重失效时间分析(意味着个体有复发事件的风险);否则,使用单一故障时间分析方法。使用左截体和年龄作为潜在的时间尺度进行分析,并且,由于肺炎和心力衰竭的结果,也使用Fine和Gray提出的方法进行竞争风险分析(竞争事件是全因死亡率)。由于使用多个故障时间分析的方法不能使用Fine和Gray,因此使用单一故障时间分析的方法。对全因死亡率采用Kaplan-Meier分析,并绘制了面积比例维恩图[10].在敏感性分析中,我们纳入了其他与结果相关的潜在混杂因素,并根据相关症状的存在进行了分层(即。慢性黏液高分泌、呼吸困难、喘息和/或咳嗽),并根据FEV的四分位数限制对无AFL的个体进行分析1/ FVC。用于评估潜在混杂因素和症状的问题的详细描述可在补充材料.所有分析均使用STATA/SE 13.1 for Windows (StataCorp, College Station, Texas, US)进行,双侧p值<0.05被认为是显著的。
结果
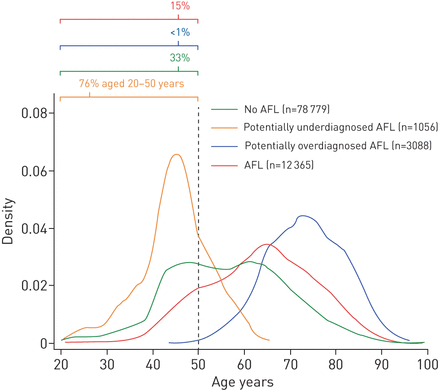
在95 288名参与者中,78 779人(83%)没有AFL, 1056人(1%)潜在诊断不足AFL, 3088人(3%)潜在诊断过度AFL, 12 365人(13%)有AFL。在潜在诊断不足的AFL个体中,76%的年龄在20-50岁,而这一比例在没有AFL的个体中为33% (图2).潜在诊断不足的AFL患者在20-50岁的年轻人中占3%,在50-100岁的老年人中占不到0.5%。中位随访时间为6.0年(范围:2天至11年),在此期间,我们观察到2073例阻塞性肺病严重加重,4487例肺炎,3859例缺血性心脏病事件,2046例心力衰竭和5260例死亡。由于主要目的是调查潜在诊断不足的AFL患者,因此包括潜在过度诊断的AFL患者和潜在诊断不足的AFL患者在内的分析在补充材料.
使用核密度估计说明了气流限制(AFL)临床组的年龄分布。AFL未定义为1 s内用力呼气量(FEV)1)/强迫肺活量(FVC)≥0.70和FEV1/FVC≥正常下限(LLN)。潜在诊断不足的AFL定义为FEV1/FVC≥0.70和FEV1/ FVC < LLN。可能过度诊断的AFL被定义为FEV1/FVC <0.70和FEV1/ FVC≥LLN。AFL定义为FEV1/FVC <0.70和FEV1/ FVC < LLN。
与没有AFL的个体相比,潜在诊断不足的AFL个体更年轻,中位年龄为45岁与56岁,目前吸烟者更多,患病率为28%与15% (表1);然而,累积烟草消费的差异很小(16包年)与14日久)。考虑到年龄和性别后,与没有AFL的个体相比,潜在诊断不足的AFL个体的哮喘患病率更高(10%)与5.2%),呼吸道症状(54%)与40%)和气道用药(8.6%)与4.2%) (表2).此外,80%有轻度AFL, %预测FEV1≥80%。与没有AFL的个体相比,在血液中炎症生物标志物的浓度和之前使用的医疗保健中,只能观察到微小的差异。结果是相似的,没有调整(见补充表S1).
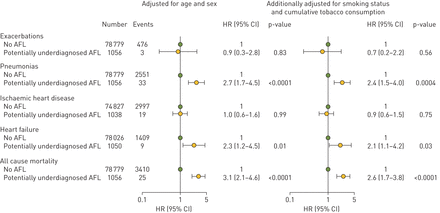
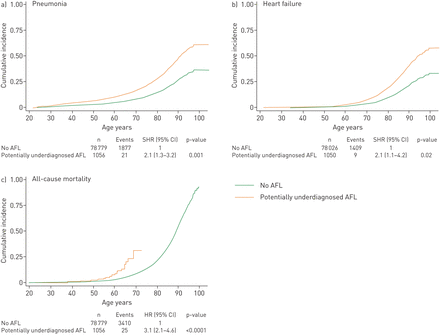
与非AFL患者相比,潜在诊断不足的AFL患者肺炎、心力衰竭和全因死亡率增加,但阻塞性肺病或缺血性心脏病加重的风险没有增加(图3和补充图S1).年龄和性别校正的危险比(HRs)肺炎为2.7 (95% CI 1.7-4.5),心力衰竭为2.3 (95% CI 1.2-4.5),全因死亡率为3.1 (95% CI 2.1-4.6)。图3左面板)。在对吸烟状况及累积吸烟量进行额外调整后,风险估计结果大致相同(图3右面板)。在一项竞争性风险分析中,肺炎和心力衰竭风险的增加持续存在,竞争性事件为全因死亡率(图4).在伴有肺炎、心力衰竭和/或死亡的潜在未确诊AFL患者中,仅观察到少量重叠(图5).在敏感性分析中,在对其他潜在混杂因素进行额外调整后,风险估计是相似的(见补充表S2和S3和补充图S1右面板)。此外,根据呼吸道症状的存在进行分层后,无症状个体的风险估计值略低,而有症状个体的风险估计值较高(见补充图S2).最后,在没有AFL的个体中,FEV的1 / 41/FVC(范围:0.70-0.76)与第4分位fv患者相比,阻塞性肺病加重和全因死亡的风险增加,但肺炎、缺血性心脏病或心力衰竭的风险没有增加1/FVC(范围:0.83-1.00)(见补充图S3).这表明,即使在肺功能正常的范围内,肺功能低下似乎与预后不良有关。
潜在诊断不足的气流受限(AFL)患者的预后。使用多重失效时间分析评估急性加重和肺炎的风险;否则,使用单一故障时间分析。p值由Wald检验得到。AFL未定义为1 s内用力呼气量(FEV)1)/强迫肺活量(FVC)≥0.70和FEV1/FVC≥正常下限(LLN)。潜在诊断不足的AFL定义为FEV1/FVC≥0.70和FEV1/ FVC < LLN。置信区间:置信区间;人力资源:风险比。
肺炎(a)和心力衰竭(b)的竞争风险分析,以及潜在诊断不足的气流受限(AFL)个体的全因死亡率Kaplan-Meier分析(c)。所有的风险估计都经过年龄和性别调整。肺炎和心力衰竭的风险估计是通过使用Fine和Gray提出的方法进行竞争风险分析获得的,竞争事件是全因死亡率。全因死亡率的风险估计来自Cox比例风险模型。值得注意的是,肺炎风险评估采用单失效时间分析,而不是多失效时间分析。p值由Wald检验得到。AFL未定义为1 s内用力呼气量(FEV)1)/强迫肺活量(FVC)≥0.70和FEV1/FVC≥正常下限(LLN)。潜在诊断不足的AFL定义为FEV1/FVC≥0.70和FEV1/ FVC < LLN。置信区间:置信区间;人力资源:风险比;月:subhazard比率。
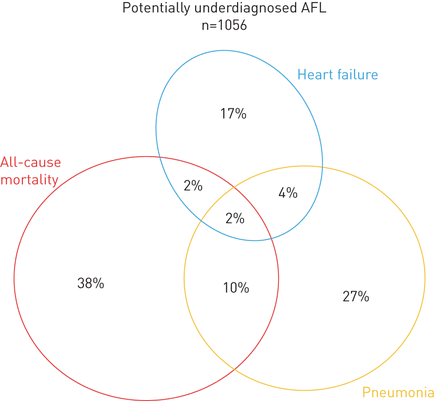
潜在诊断不足的气流受限(AFL)个体中肺炎、心力衰竭和全因死亡率的面积比例维恩图潜在诊断不足的AFL定义为1秒用力呼气量(FEV)1)/强迫肺活量(FVC)≥0.70和FEV1/FVC <正常下限(LLN)。
尽管对潜在的混杂因素进行了调整,但与没有AFL的个体相比,潜在过度诊断AFL的个体发生急性加重和肺炎的风险增加,但缺血性心脏病、心力衰竭或全因死亡的风险没有增加(见)补充图S1).年龄和性别调整后的HRs为2.6 (95% CI 1.8-3.8),肺炎为1.5 (95% CI 1.3-1.8)补充图S1左面板)。根据呼吸道症状的存在进行分层后,无症状个体的风险估计略低,而有症状个体的风险估计较高(见补充图S2).此外,有症状的个体也增加了缺血性心脏病、心力衰竭和全因死亡的风险。
讨论
在来自普通人群的大样本中,我们发现使用LLN标准而非固定比率标准定义的年轻AFL患者患肺炎的风险为2.7倍,患心力衰竭的风险为2.3倍,全因死亡的风险为3.1倍。
据报道,在潜在诊断不足的AFL患者中,只有12%患有哮喘。随访期间,与没有AFL的患者相比,这些患者COPD或哮喘相关加重的风险没有增加。一种可能的解释是,这些没有哮喘的人可能肺部发育不全。正常肺发育的特点是在儿童时期肺功能迅速增加,在成年期约20-25岁达到高峰。然后这一阶段被一个平台期所取代,在随着年龄的增长肺功能稳定下降之前,肺功能得到最大程度的保留约10年。因此,这些年轻人中的AFL可能是由于成年期肺功能峰值不足所致[11- - - - - -14].成年早期肺部发育不全,最大肺功能达到较低,这是老年时呼吸道疾病的危险因素,甚至可能通过正常肺功能下降导致晚年发展为慢性阻塞性肺病[15].
另外,患者可能诊断AFL可能是一个混合的临床组不仅组成的呼吸道疾病,或倾向发展它,但是也有心脏病,这些个体显示增加心脏衰竭的风险相比,在随访中个人没有AFL。长期以来,心力衰竭一直与AFL有关,在患有呼吸系统疾病的患者中,它通常是一个诊断挑战[16- - - - - -18].因此,通过在年轻人中使用LLN,我们可能不仅可以识别那些未来患呼吸系统疾病风险增加的人,还可能识别出未来患心脏病的人。此外,在随访期间经历肺炎、心力衰竭和/或死亡事件的个体中,维恩图仅显示相对有限的重叠,这清楚地表明结果的异质性,并提示不同的疾病实体可能是不良预后的原因。
以往的研究主要集中在可能过度诊断AFL的老年人,而不是潜在诊断不足的年轻人。总的来说,根据LLN(而非固定比例)患有AFL的个体似乎是一个未来患病风险增加的群体[19- - - - - -22].在欧洲共同体呼吸健康调查中,这些个体出现预期FEV %的风险增加19年随访后因呼吸问题而住院服务利用率<80% [20.].在第三次全国健康和营养检查调查中,在长达18年的随访期间,同一临床组的全因死亡率风险估计最高(4.0);然而,该组只有20人,并没有达到统计学意义[21].在肺健康研究中,与没有AFL的患者相比,5年随访期间的年恶化率没有总体差异;然而,在随访的最后一年,可以观察到明显的增加,可能表明早期COPD的发展或进展[19].此外,在同一队列中,肺功能下降没有差异[19],提示肺功能没有加速衰退,而这通常是慢性阻塞性肺病的特征[23].
在以往的研究中,根据固定比例而非LLN的AFL患者大多观察到copd相关加重和全因死亡率的风险增加[19,21,24,25].在目前的研究中,发现阻塞性肺病加重的风险增加,但未发现全因死亡率。这些人的临床研究结果似乎与慢性阻塞性肺病相一致[19,25- - - - - -28],使用固定比例与老年人的LLN相比,似乎也与COPD的临床诊断和预后更相关[29].因此,基于以前的研究,结合目前的发现,这些人可能患有未诊断的COPD。
本研究的优势包括从普通人群中随机选择具有肺活量测定信息的大样本,以及较长的完整随访时间和临床相关结果。此外,本研究中有大量个体根据LLN和固定比例对AFL的定义存在差异。
该研究的一个主要局限性是缺乏支气管扩张剂后测量,这使得我们无法对AFL的类型进行分类。因此,有些人可能有可逆形式的AFL(提示哮喘),有些人可能有不可逆形式的AFL(提示COPD或哮喘- COPD重叠)。然而,很明显,具有潜在的未被充分诊断和过度诊断的AFL患者有增加的呼吸结果风险,并且由于缺乏后支气管扩张剂测量而可能的误分类,这只会削弱而不是夸大我们的发现。另一个限制是,除了欧洲白人血统以外,这种结果可能不能移植到其他种族。
总之,根据LLN而不是在较年轻时的固定比率来定义AFL,似乎可以确定个体具有较高的呼吸和心血管疾病发病率和早期死亡风险。临床医生应定期对年轻患者进行肺量测定,并将LLN应用于AFL诊断,假设重点是确定具有较高发病率和死亡率的易感人群。
补充材料
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:Y. Çolak已经收到勃林格殷格翰和阿斯利康提交的作品之外的个人费用。J. Vestbo已获得葛兰素史克、Chiesi制药、勃林格殷格翰、诺华、Almirall和阿斯利康等公司COPD 2期和3期项目的个人咨询费,以及Bioxydyn公司核磁共振软件开发的个人咨询费。演讲的个人费用,包括在葛兰素史克、奇耶西制药、诺华、阿斯利康和勃林格殷格翰的演讲机构的服务,以及在提交工作之外的葛兰素史克、阿斯利康和费林的个人费用。P. Lange已获得Almirall、Boehringer Ingelheim和GSK的拨款和个人费用,以及Astra Zeneca、Novartis、Nycomed、Pfizer和Mundipharma的个人费用。
支持声明:伦德贝克基金会和丹麦肺脏协会支持这项工作。资助方在研究的设计和实施,数据的收集、管理、分析或解释,手稿的准备、审查或批准,或提交手稿发表的决定中没有作用。本文的资金信息已存入Crossref资助者注册表.
作者贡献:Y. Çolak和P. Lange可以完全访问研究中的所有数据,并对提交发表的决定负有最终责任。Y. Çolak, S. Afzal, B.G. Nordestgaard, J. Vestbo和P. Lange对研究概念和设计做出了贡献。Y. Çolak, S. Afzal, B.G. Nordestgaard, J. Vestbo和P. Lange收集、分析或解释数据。Y. Çolak撰写了初稿。Y. Çolak, S. Afzal, B.G. Nordestgaard, J. Vestbo和P. Lange为重要的知识内容对手稿进行了修订。Y. Çolak进行了统计分析。B.G. Nordestgaard和P. Lange获得了资金。B.G. Nordestgaard提供行政、技术或物资支持。兰格指导了这项研究。
- 收到了2017年12月22日。
- 接受2018年2月4日。
- 版权©2018人队