摘要
全表观基因组关联研究表明,吸烟暴露与芳烃受体阻遏物低甲基化之间存在一致的关联(AHRR基因(cg05575921)我们验证了这个假设AHRR在一般人群中,低甲基化与肺功能低下、肺功能急剧下降和呼吸道症状有关。
AHRR甲基化程度测量了1991-1994年哥本哈根城市心脏研究检查中9113人的甲基化程度,使用亚硫酸氢盐处理的白细胞DNA。所有个体在采血时均可进行肺活量测定。2001-2003年,对其中4532人的肺功能进行了再次测量。
横切面上,甲基化程度降低10%与1 s内用力呼气量(FEV)降低0.2 z评分(95% CI 0.1-0.2)相关1),经包括吸烟在内的多变量调整后。低甲基化也与强迫肺活量(FVC)和FEV的z评分较低有关1/ FVC。在前瞻性分析中,个体得分最低与甲基化程度越高,FEV下降越明显1/高3.(p对于examination×methylation相互作用=0.003)和植被覆盖度/高度3.(p=0.01), FEV除外1/ FVC (p = 0.08)。慢性支气管炎的多变量调整优势比为1.31 (95% CI为1.18-1.45),任何呼吸道症状的优势比为1.21 (95% CI为1.13-1.30)。
AHRR低甲基化与低肺功能、严重的肺功能衰退和呼吸道症状相关。
摘要
AHRR低甲基化与肺功能低下、肺功能急剧下降和呼吸道症状有关http://ow.ly/a30J30hB2dS
简介
表观遗传学是研究不引起DNA序列改变的减数分裂和有丝分裂可遗传的变化[1].有证据表明,表观遗传机制,如DNA甲基化和组蛋白修饰,与单基因和多因素疾病都有因果关系[2].一些生活方式的因素,如。酒精、吸烟和空气污染可能通过表观遗传机制影响健康和疾病[3.].芳基烃受体阻遏物的低甲基化(AHRR)基因在全表观基因组关联研究中一直与吸烟暴露相关,其中cg05575921位点的低甲基化与吸烟状态的相关性最强[4- - - - - -11].此外,AHRR低甲基化与二手烟有关[12]及母婴吸烟情况[13].
吸烟是影响肺功能、肺功能衰退和呼吸道症状的单一最重要的生活方式因素[14,15].有关吸烟的信息往往基于自我报告和不准确的数据[16].AHRR低甲基化以前与吸烟有关[4- - - - - -11,17],肺活量测定定义的慢性阻塞性肺疾病(COPD)和严重COPD加重的风险较高[17];然而,这是否是未知的AHRR低甲基化与肺功能低下、肺功能急剧下降和呼吸道症状的高风险相关。
我们假设AHRR低甲基化作为吸烟的生物标志物,提供了有关肺功能和呼吸道症状的信息,超出了有关吸烟的自我报告信息。因此,我们验证了假设AHRR在普通人群中,低甲基化与低肺功能、更严重的肺功能衰退和更高的呼吸道症状风险相关。
方法
研究人群
哥本哈根城市心脏研究(CCHS)是一项针对丹麦普通人群的前瞻性队列研究,始于1976-1978年,并于1981-1983年、1991-1994年和2001-2003年进行随访检查[17,18].从丹麦中央人员登记处随机选择20-100岁的人,代表丹麦一般人口。在每次测试中,参与者都要填写一份反映生活方式和健康状况的广泛问卷。参与者在参加研究当天与一名研究人员一起审阅问卷,然后进行身体检查和血液采样以进行生化分析和DNA提取。在本研究中,我们纳入了1991-1994年检查的9113例患者(占所有被邀请患者的61%),并进行了甲基化程度测量和肺活量测定。此外,2001-2003年,所有参加1991-1994年检查的在世参与者都被重新邀请参加检查,其中4581人(50%)参加了检查,因此可以重复测量一部分个体的肺功能。该研究得到Herlev和Gentofte医院以及丹麦伦理委员会的批准(KF100.2039/91),并根据《赫尔辛基宣言》进行。所有参与者均获得书面知情同意。
甲基化程度
使用QIAamp DNA血液迷你试剂盒(Qiagen, Hilden, Germany)从1991-1994年检查的冷冻全血样本中提取DNA。甲基化程度AHRR(对应于Illumina BeadChip 450 K阵列上的cg05575921 CpG位点)在重复样品中进行测量,使用亚硫酸氢盐处理,然后使用基于taqman的PCR法,探针设计用于检测未甲基化的因此转化的T残基,或甲基化的因此保守的C残基,如前所述[17].重复失败的测量,有效的甲基化程度测量可用于99.8%的可用DNA样本。在71%甲基化程度水平下,不同内控批次的变异系数在5% ~ 7%之间变化[17].对13个批次的测量值进行了调整,以解释分析间的差异,并使用焦磷酸测序进行验证[17].
肺量测定法
1秒内用力呼气量(FEV)1)和强迫肺活量(FVC)在1991-1994年和2001-2003年的检查中使用干楔肺活量计测定。对于每个个体,都进行了三次肺活量测定,只有当两个最佳结果之间的差异<5%时,结果才被接受。
协变量
自我报告有关吸烟状况、累计吸烟、被动吸烟、职业性粉尘和烟雾暴露以及最高完成教育水平的信息。身体质量指数(BMI)的计算方法是体重(公斤)除以身高(米)的平方。我们没有交通空气污染暴露的资料。
呼吸道症状
所有包括的呼吸道症状都是1991-1994年检查时自我报告的。方法中提供了有关方法的其他详细信息补充材料.
统计分析
我们使用Stata/SE 13.1。双尾p值<0.05被认为是显著的。我们使用Cuzick的趋势非参数检验来检验相关性AHRR不吸烟者、戒烟者和正在吸烟者甲基化程度。用按吸烟状态分层的核密度图来可视化甲基化程度的分布。此外,还绘制了戒烟后所有人群甲基化程度随时间的变化,并按性别分层。甲基化程度与性别、身高和年龄的关系在线性模型中以吸烟状况分层进行评估。缺失的协变量数据(0.2%)是根据年龄和性别使用多变量链式impu缀;然而,不加imputation的结果相似。
肺功能:横断面分析
线性回归模型用于肺功能z评分与甲基化程度之间关系的横断面分析。FEV1、FVC和FEV1/FVC z-score根据全球肺功能倡议2012年方程(GLI-2012)计算[19].我们使用残差图直观地评估了同方差与预测的值。我们通过绘制变量的分位数对正态分布的分位数来评估残差的正态性。未观察到严重违反同方差或正态性的情况。绘制二次回归线和线性回归线进行视觉评估。为了正式检验非线性,引入了二次甲基化程度项,并进行似然比检验,以检验线性模型和二次模型之间的系数相似性。我们对相关混杂因素进行了多变量调整,即。性别、年龄(连续)、BMI(五分位数,以第二个五分位数为参考)、被动吸烟(二分位数)、粉尘和烟雾暴露(二分位数)、教育水平(丹麦传统分类:<10年教育、10年教育、高等教育<1年、高等教育1 - 3年、高等教育> - 3年、学历)、吸烟状况(当前、以前或从不吸烟)和累积吸烟(连续)。此外,分析还按性别和吸烟状况进行了分层。
肺功能下降:前瞻性分析
采用以下方法评估肺功能:FEV1/基线高度的立方(高度3.)(以前由弗莱彻和皮托使用[20.)、FVC /高度3.和FEV1/ FVC。使用重复测量线性混合模型评估这些测量的下降,因为这些模型可以解释受试者内部的相关性[21].检查次数(一次或两次)规定了肺功能的重复测量次数;那些只进行了一次测量的个体被包括在内,以提高基线估计的精度。为了绘制关联图,使用了甲基化程度的百分位。我们使用非结构化协方差类型,因为它对结构没有限制。每个个体的身份作为随机效应被引入,以指定分组结构,从而解释主题内的相关性。我们通过在包含这两个因素的模型中引入双因素相互作用项(检查次数和百分位甲基化程度),采用似然比检验,检验了甲基化程度与第一次至第二次检查时间对肺功能变化的相互作用。此外,我们根据吸烟状况和性别对肺功能变化进行分层。模型根据这些变量进行了调整,即。年龄、性别、检查(1991-1994年或2001-2003年)和累积吸烟(每次检查时更新)可能会混淆甲基化程度与肺功能参数之间的关系。使用混合模型线性回归系数的线性组合计算组平均值的例子。
在敏感性分析中,我们在线性回归模型中只纳入参加两项检查的个体。为了评估排除只参加过第一次检查的个体的潜在偏倚,我们评估了参加过一次或两次检查的个体之间COPD住院发生率、死亡、呼吸道症状和肺活量的差异。
甲基化程度与测量FEV的差异1预测FEV1
甲基化程度与测量FEV之间的差异之间的关系1预测FEV1采用未调整线性回归模型进行评估。对于所有个体,我们绘制测量FEV1负预测FEV1对照1991-1994年检查的甲基化程度。对于参加两项检查的个体,我们还绘制了测量的FEV1负预测FEV1在2001-2003年检查中对照1991-1994年检查中的甲基化程度。
呼吸道症状:横断面分析
采用logistic回归的横断面设计评估呼吸道症状与吸烟状态分层的甲基化程度之间的关系。在包括FEV在内的线性回归模型中,多变量模型对相同的混杂因素进行了调整1z分数。
在敏感性分析中,我们在甲基化程度与按性别和吸烟状况分层的呼吸道症状之间进行了logistic回归。
结果
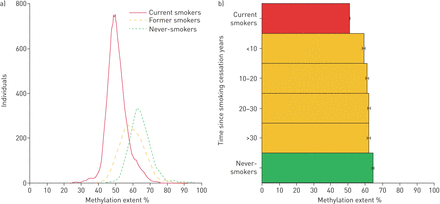
表1根据吸烟状况和甲基化程度,总结1991-1994年检查的基线特征。9113例CCHS患者的中位甲基化程度为56%(四分位数范围(IQR) 50-63)。如前所述[17的甲基化程度AHRR因吸烟情况而异(图1一个);目前吸烟者甲基化程度中位数为50% (IQR 47-54),前吸烟者为59% (IQR 54-64),从不吸烟者为64% (IQR 60-68)(趋势p <0.001)。当按性别分层时,甲基化程度的差异在男性中最为明显(补充图S1).我们发现,戒烟时间越长,甲基化程度越高AHRR(图1 b).当按照吸烟状况进行分层时,甲基化程度在所有分层中都与性别一致,男性的甲基化程度低于女性(补充表S1).在两性中,甲基化程度与戒烟时间呈正相关(趋势p值均<0.001,补充图S1).
芳基烃受体阻滞剂的分布(AHRR)甲基化程度9113人。a)甲基化程度在当前吸烟者、前吸烟者和从不吸烟者中的分布。b)戒烟后各亚组甲基化程度的平均值,置信区间为95%。目前和从不吸烟显示为参考。黑色条表示95%置信区间。在戒烟者中,使用Cuzick趋势检验计算趋势p: p<0.001。
肺功能:横断面分析
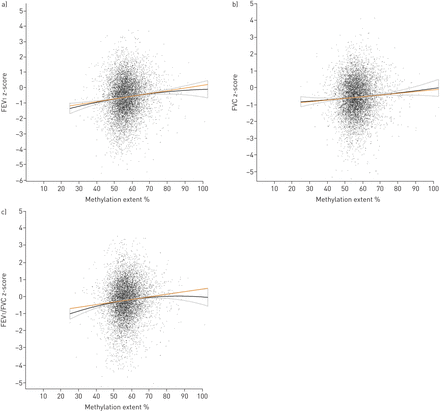
在多变量调整分析中,低甲基化程度与低FEV相关1z分数(图2).甲基化程度降低10%与FEV降低0.2 z-score (95% CI 0.1-0.2)相关1(图2一个).FVC的z评分也有类似的结果(图2 b)和FEV1/ FVC (图2 c).按吸烟状况分层的结果相似(补充图S2),尽管在从不吸烟的人群中这种现象有所减弱。在回归中加入二次项确实改善了模型对某些参数的拟合;然而,大多数偏差是在最高和最低甲基化水平观察到的(图2而且补充图S2).同样,女性和男性的结果也相似(补充数字S3和S4).
芳基烃受体阻遏物的关联(AHRR)甲基化程度与肺功能参数的关系。一)FEV1每降低10%甲基化程度,z-score (95% CI 0.1-0.2)降低0.2;b)每降低10%的甲基化程度,FVC的z评分(95% CI 0.07-0.1)降低0.1;c) FEV1/FVC每降低10%甲基化程度,z-score (95% CI 0.1-0.2)降低0.2。分析对年龄、性别、体重指数、粉尘和烟雾暴露、被动吸烟、教育程度、吸烟状况和累计吸烟进行了多变量调整。橙色的线表示一条线性回归线。黑线代表二次回归线。二次线周围的面积表示回归线的95%置信区间。黑点代表单独的测量值。单独的测量值被调整为协变量。FEV1:用力呼气量1 s;FVC:强迫肺活量。
肺功能下降:前瞻性分析
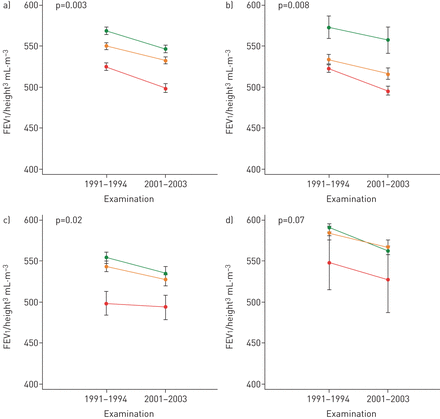
在对肺功能随时间变化的前瞻性分析中,我们发现检查(1991-1994与甲基化程度对FEV的下降具有交互作用1/高3.(交互作用p =0.003) (图3).甲基化程度最低的个体的FEV下降幅度更大1/高3.与甲基化程度最高的不育个体相比。根据纵向模型,在甲基化程度最低的不育区,男性参与者(50岁,身高1.80米,吸烟5包年)的平均FEV11991-1994年检查为3.71 L (95% CI 3.68-3.75), 2001-2003年检查为3.16 L (95% CI 3.12-3.20)。甲基化程度最高的不育粒个体的相应估计分别为3.97 L (95% CI 3.94-4.00)和3.44 L (95% CI 3.41-3.47)(数据未显示)。按性别分层时,FEV下降幅度较大1/高3.甲基化程度低的个体在男性中最为明显(补充图S5).当按吸烟状况分层时,目前吸烟者的结果相似,而FEV的下降之间没有关联1/高3.而且AHRR从不吸烟的人甲基化程度低(图3).相似的结果显示,智商最低的个体下降幅度更大与甲基化程度以FVC/height最高3.(相互作用p <0.001)和FEV1/FVC(相互作用p <0.001) (补充数字S6和S7).在对两次检查更新的包年进行额外调整后,未发现FEV检查与甲基化程度的相互作用1/FVC(相互作用p =0.08)。FVC和FEV的变化趋势相似1/男性和女性的覆盖度(补充数字S8和S9).在仅包括两次测量的个体的敏感性分析中,我们发现FEV下降13.6 mL/年(95% CI 2.2-5.0),甲基化程度降低10% (补充图S10).然而,在只参加1991-1994年检查的个体中,与参加两次检查的个体相比,15年内死亡的发生率更高,与copd相关的住院病例更多,报告的呼吸道症状也更多(补充表S2).
FEV变化之间的关系1/高3.根据芳香烃受体阻遏剂(AHRR)甲基化a)整体和分层为b)当前吸烟者,c)前吸烟者和d)从不吸烟者。分析根据每次检查、年龄、性别和检查时段更新的累积吸烟量进行调整。数据基于对9113人每人进行一到两次肺活量测定,时间跨度长达11.5年;那些只进行了一次测量的个体被包括在内,以提高基线估计的精度。每个个体的身份作为随机效应被引入,以指定分组结构,从而解释主题内的相关性。仅使用基线高度。黑色条表示95%置信区间。绿线代表最高甲基化程度;橙色线代表中间甲基化程度;红线代表最低甲基化程度。 p-values for interaction of examination (1991–1994与2001-2003),甲基化程度为百分位。FEV1: 1秒内的用力呼气量。
甲基化程度与测量FEV的差异1预测FEV1
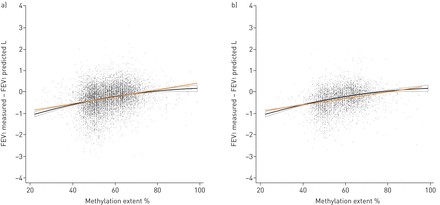
测量FEV之间的差异1和预测的FEV1与甲基化程度相关(图4一)及预期(图4 b).测量FEV之间的差异1预测FEV11991-1994年甲基化程度每降低10%,高0.16 L (95% CI 0.15-0.18)。在2001-2003年的检查中,甲基化程度与每低10%甲基化程度的0.15 L (95% CI 0.13-0.17)高差异相关。
芳基烃受体阻滞剂(AHRR)甲基化程度和测量FEV之间的差异1预测FEV1A)横截面和b)前瞻性。在a中,1991-1994年测量的甲基化程度与测量的FEV相对应1预测FEV11991-1994年考试;FEV1测量−FEV1预测=每降低10%甲基化程度降低0.16 L (95% CI 0.15-0.18)。在b中,1991-1994年测量的甲基化程度与测量的FEV相对应1预测FEV12001-2003年考试;FEV1测量−FEV1预测=每降低10%甲基化程度降低0.15 L (95% CI 0.13-0.17)。预测FEV1采用基于年龄、身高、性别和种族的2012年全球肺功能方程计算。橙色线表示未调整的线性回归线。黑线表示未调整的二次回归线。二次回归线周围的面积表示回归线的95%置信区间。黑点代表单独的测量值。FEV1: 1秒内的用力呼气量。
呼吸道症状:横断面分析
在分层分析中,经过包括FEV在内的多变量调整1在当前吸烟者中,z评分、甲基化程度与所有呼吸道症状类别相关,但只有慢性支气管炎、喘息和任何呼吸道症状在前吸烟者中显著(图5).在所有吸烟层中,只有慢性支气管炎与甲基化程度显著相关。在所有个体中,包括吸烟状况和累积吸烟在内的多变量调整分析显示,甲基化程度与除呼吸困难外的所有呼吸道症状相关(补充图S11).慢性支气管炎与甲基化程度的相关性最强,每降低10%甲基化程度的多变量调整优势比为1.31 (95% CI 1.18-1.45),任何呼吸道症状的多变量调整优势比为1.21 (95% CI 1.13-1.30)。
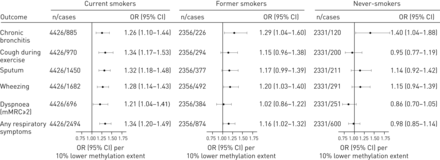
每10%低芳烃受体阻滞剂的呼吸道症状优势比(AHRR)在1991-1994年的检查中,甲基化程度按吸烟状况分层。所有分析均根据年龄、性别、体重指数、粉尘和烟雾暴露、被动吸烟、教育程度、1秒的用力呼气量和累积吸烟(仅限以前和现在的吸烟者)进行了调整。mMRC:改良医学研究委员会呼吸困难量表。
在进一步按性别分层后,男性和女性的结果相似,尽管戒烟者之间的联系在男性中最为明显(补充图S12).
讨论
在这项对普通人群中9113人的研究中,我们发现AHRR低甲基化与肺功能低下、肺功能急剧下降和呼吸道症状的高风险相关。这些都是新颖的发现。
虽然目前尚不清楚AHRR在肺功能损害中的作用,但这些发现具有几个意义。首先,他们认为甲基化程度的测量可以提供吸烟的信息,而不是自我报告的吸烟行为。其次,由于低甲基化也与从不吸烟的人肺功能低下和慢性支气管炎风险增加有关,低甲基化可能会捕获未报告的烟草暴露。第三,低甲基化可以作为对吸烟有害后果易感性的标志,并有助于识别更容易受到烟草诱导的肺损伤的吸烟者。第四,尽管像我们这样的研究无法推断因果关系,AHRR低甲基化可能是吸烟与肺功能损害、肺功能下降和呼吸道症状之间的因果关系。这些考虑是基于吸烟对健康影响的唯一假设AHRR甲基化;然而,从不吸烟者的结果,以及香烟烟雾含有许多有毒物质的事实,意味着我们不能排除其他环境暴露的影响,如。空气污染。
AHRR低甲基化是一种潜在的吸烟史生物标志物,即使在戒烟35年后也能捕捉到以前的吸烟情况[22].自我报告的吸烟状况和累积吸烟情况往往报告不足,而后者可能会受到回忆偏差的影响[16,23].因此,需要更客观的吸烟行为标记。目前,血液或尿液中的可替宁浓度,或呼出CO浓度的测量,两者的生物半衰期<24小时,是验证吸烟状态的主要生物标志物[10].虽然这些方法可能能够区分真正的吸烟者和不吸烟者,但它们并不适合反映长期吸烟史[10,22].的概念AHRR甲基化程度作为长期吸烟史的生物标志物[17我们的研究结果支持AHRR前吸烟者甲基化程度与戒烟时间及呼吸道症状有关。然而,这些关联是否可以归因于低甲基化是吸烟有害影响的一个更好的指标,还是由于吸烟习惯报告不充分造成的残留混杂仍有待澄清。同样,之间的联系AHRR不吸烟者的低甲基化、低肺功能和慢性支气管炎可能是由于残留混杂,或反映了其他未测量的环境暴露,如空气污染。低甲基化与测量到的FEV之间的较大差异有关1预测FEV1无论是横截面的还是10年后的。我们推测,CpG等网站AHRR可以解释这种差异的部分原因,从而改善肺功能和肺功能衰退的预测模型。
另外,AHRR低甲基化可能是烟草诱导肺损伤易感性的一个代理。烟草烟雾成分引起的双链DNA断裂在机制上导致DNA修复和DNA甲基转移酶的募集[24].新创修复DNA附近的CpG二核苷酸可能发生甲基化,以通过基因沉默避免突变蛋白的表达[24].吸烟能够通过多种途径改变基因甲基化,其中一种途径是通过尼古丁诱导的DNA甲基转移酶I表达下调[24- - - - - -26].因此,如果AHRR低甲基化标志着DNA损伤和修复机制不足,它可以确定相对于甲基化水平正常的烟草暴露个体,烟草暴露的DNA损伤更大。
最后,AHRR低甲基化可能是吸烟致肺损伤的原因之一。鉴于吸烟导致肺损伤的多种机制,目前尚不清楚香烟烟雾的哪一种成分是监测的AHRRhypomethylation。我们的观察性研究无法澄清这一重要观点。AHRR低甲基化与单核细胞中AHRR的高表达有关[27]、淋巴母细胞和肺巨噬细胞[28].虽然AHRR在AHR通路中的复杂相互作用仍在研究中,但研究表明,增加AHRR表达通过负反馈抑制AHR活性[29],导致异种代谢基因的表达减少,如CYP1A1[25].反过来,这可能会损害身体代谢和清除有害物质(如多芳烃)的能力,可能导致肺功能受损[30.].或者,考虑到AHRR-缺陷小鼠在注射脂多糖后某些促炎分子表达降低[31], AHRR可能参与调节炎症反应,而炎症反应也出现在肺功能下降中。然而,我们不能排除基因内甲基化改变的可能性,例如AHRRCg05575921可能是基因表达变化的结果[32].因此,AHRR低甲基化可能是继发于吸烟引起的AHRR表达,因此不仅仅是一个因果因素。
在我们的研究中,我们发现了一些性别差异。首先,在所有吸烟层中,根据年龄和身高调整后的模型中,男性的甲基化程度低于女性。这可能是由于男性和女性在吸烟行为和一般环境暴露方面的差异,也可能反映出男性更容易受到烟草引起的DNA改变的影响。其次,在女性中,甲基化程度在戒烟者和不吸烟者之间没有很好的区别,并且与戒烟者的呼吸道症状无关。最后,在对女性的前瞻性分析中,低甲基化程度与任何吸烟阶层的肺功能下降都不相关。对此的一种解释可能是男性和女性在报告吸烟行为方面的差异,或者这些发现可能反映了实际的生物学差异,这些差异可以在未来的研究中解决。
以往的研究AHRR低甲基化和呼吸道疾病主要集中在肺癌;AHRR低甲基化与肺癌发病率、肺癌死亡率和全因死亡率相关[5,7,17].此外,来自CCHS的数据显示了两者之间的联系AHRR在横断面分析中,低甲基化和肺活量测定法定义的COPD,以及未来严重COPD加重的更高风险[17].现在,我们来证明一下AHRR低甲基化与肺功能低下、肺功能急剧下降和呼吸道症状的高风险相关。
我们研究的优势包括来自同质人群的大样本量和肺功能的重复测量。尽管如此,还是应该考虑一些潜在的限制。首先,使用重复的肺量测定法可能引入了偏倚;因为AHRR低甲基化与肺功能和全因死亡率相关[17],甲基化程度低的个体可能由于发病率或死亡而没有参加两次检查,如我们的研究所示。然而,这种优先去除甲基化程度低的个体很可能会使我们的结果偏向零假设,因此不能解释我们的发现。其次,由于我们的研究人群仅由丹麦人组成,我们的发现可能并不一定适用于不同种族的个体,尽管目前还没有证据支持这一点。
总之,AHRR在普通人群中,低甲基化与肺功能低、肺功能下降更严重和呼吸道症状风险更高有关。我们的结果扩展了与吸烟相关的表型的数量AHRR低甲基化和强化的证据AHRR低甲基化是吸烟史和/或其有害影响的潜在生物标志物。AHRR和AHR在肺功能损害、肺功能下降和呼吸道症状发展中的作用及其复杂的相互作用尚不清楚。
补充材料
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究由丹麦首都大区和哥本哈根大学医院Herlev和Gentofte医院临床生物化学系资助。本文的资助信息已存入交叉参考基金注册.
利益冲突:没有声明。
- 收到了2017年1月26日。
- 接受2017年12月31日。
- 版权所有©ERS 2018