文摘
Interleukin-1受体1(IL1RL1)是一个重要的哮喘基因。(Epi)基因的监管IL1RL1蛋白表达尚未建立。我们评估之间的关系IL1RL1单核苷酸多态性(snp),IL1RL1甲基化和血清IL1RL1-a蛋白质含量,旨在识别因果通路在哮喘。
协会IL1RL1单核苷酸多态性与荷兰哮喘哮喘测定全基因组关联研究队列和三个欧洲同期出生的,BAMSE(儿童/谷仓,过敏,环境,斯德哥尔摩,流行病学调查),INMA (Infancia y五分镍币环境)和PIAMA(预防和哮喘的发病率和螨虫过敏),参与机制过敏研究的发展。我们进行了血液DNAIL1RL1甲基化数量性状位点(QTL)定位分析(n = 496)和(epi)全基因组蛋白质QTL分析血清IL1RL1-a水平(n = 1462)。我们协会的调查IL1RL1CpG甲基化与哮喘(n = 632)和IL1RL1-a水平(n = 548),与随后的因果推理测试。最后,我们决定协会IL1RL1-a水平与哮喘及其临床特征(n = 1101)。
IL1RL1患哮喘的危险snp密切相关IL1RL1甲基化(rs1420101;p = 3.7×10−16)和血清IL1RL1-a水平(p = 2.8×10−56)。IL1RL1甲基化与哮喘或IL1RL1-a水平无关。与血液嗜酸性粒细胞计数IL1RL1-a水平负相关,而没有IL1RL1-a水平和哮喘之间的联系。
总之,asthma-associatedIL1RL1snp强烈规范IL1RL1甲基化和血清IL1RL1-a水平,然而,无论这些IL1RL1 -甲基化CpG网站也IL1RL1-a水平与哮喘有关。
文摘
Interleukin-1受体1(IL1RL1)单核苷酸多态性调节IL1RL1甲基化和血清IL1RL1-a水平,然而,这些影响哮喘并不相关http://ow.ly/AStC30hSvGy
介绍
哮喘的遗传已被估计为60%左右(1)和大规模的全基因组关联研究(GWAS)已经确定了多个易感性位点(2,3]。一个基因发现哮喘GWAS的interleukin-1受体1(IL1RL1),编码toll样/ il - 1受体超家族的成员表达对炎症和居民肺癌细胞(4- - - - - -7]。单核苷酸多态性(SNPs)IL1RL1与(开始时间)有关哮喘和过敏性特征(2,3,8- - - - - -16]。IL1RL1编码三个蛋白亚型:IL1RL1-a(可溶性ST2),血清中可测量;跨膜受体,IL1RL1-b (S2TL);和两个特征明显少亚型,同种型3和IL1RL1-c (ST2V) [17]。IL1RL1-a, IL1RL1-b和IL1RL1-c都表示在肺18,19]。绑定的IL-33 heterodimeric受体组成的复杂IL1RL1-b IL1RAcP Th2细胞,先天免疫细胞(如。嗜碱性粒细胞和肥大细胞)和2型先天淋巴细胞激活一个MYD88-mediated炎症信号级联,导致气道炎症通过释放促炎Th2细胞因子il - 4、IL-5和IL-1320.]。IL1RL1-a被认为作为诱饵受体,隔绝IL-33和抑制其功能21- - - - - -23]。
精确的单核苷酸多态性和甲基化作用IL1RL1在调节的表达IL1RL1仍然知之甚少。单核苷酸多态性在IL1RL1与DNA甲基化在5′-C-phosphate-G-3′(CpG)网站(甲基化(meQTL)数量性状)和影响蛋白质水平(蛋白质(pQTL)数量性状)和功能(24]。单核苷酸多态性在IL1RL1以前被发现与IL1RL1-a血清和支气管肺泡灌洗(BAL)液25,26]。然而,它是未知的IL1RL1单核苷酸多态性与甲基化或如何与IL1RL1蛋白表达和哮喘的发展。
在这项研究中,我们分析了之间的关系IL1RL1单核苷酸多态性,IL1RL1基因甲基化和血清IL1RL1-a蛋白质水平。我们旨在通过整合这些多层次的数据揭示的基因组机制IL1RL1在哮喘。
方法
详细描述中提供的方法补充材料。
研究人群
表型和遗传分析,我们使用样本荷兰哮喘GWAS (DAG)组(n = 1885) (27)和三个不同的欧洲同期出生的,导致了MeDALL(过敏)的发展机制项目(28]:PIAMA(预防和哮喘的发病率和螨虫过敏)(n = 1913) (29日),BAMSE(儿童/谷仓,过敏,环境,斯德哥尔摩,流行病学调查)(n = 385) (30.)和INMA (Infancia y五分镍币环境)(n = 320) (31日]。表观遗传分析的三个MeDALL组(n = 632)。所有的研究是医学伦理委员会批准,通知(父母)从所有参与者同意了。
哮喘的诊断
在DAG人群中,哮喘被定义为医生的诊断哮喘,哮喘症状和(AHR)气道高反应的存在。在控制,无论是哮喘气道高反应性也在场。在PIAMA BAMSE INMA群组,哮喘是基于出版古典哮喘的定义MeDALL [32),两个以下三个标准必须是积极的:1)医生的诊断哮喘,2)哮喘药物的使用在过去12个月中,3)喘息/呼吸困难在过去的12个月。
的选择IL1RL1区单核苷酸多态性
候选基因分析,我们定义了IL1RL1地区所有IL1RL1其实和intronic序列以及并列基因组区域200 kb 5′的转录起始站点和200 kb的3′最后一个外显子。我们验证了连锁不平衡(LD)的模式与未成年人snp等位基因频率(加)> 0.01在本地区使用数据从1000基因组CEU面板(版本3,2012年3月)33]。
(Epi)基因数据和血清IL1RL1-a水平
基因型和归责细节提供的补充材料。在MeDALL研究中,IL1RL1DNA甲基化的全血DNA收集四年岁的测量使用Illumina公司450 k甲基化Beadchips (Illumina公司Inc .)、圣地亚哥、钙、美国)。
血清IL1RL1-a DAG的蛋白质含量,BAMSE INMA军团测量使用ST2 / il - 1 R4 Quantikine ELISA试剂盒(研发系统,Inc .,明尼阿波利斯,美国),和以前报道PIAMA使用ST2酶联免疫试剂盒(医学和生物实验室有限公司沃本,妈,美国)(25]。
统计分析
我们检查协会IL1RL1基因变异与哮喘和IL1RL1-a表达与哮喘有关的特征在DAG MeDALL军团。我们进行全基因组SNP和epigenome-wide CpG协会分析血清IL1RL1-a水平DAG PIAMA, BAMSE和INMA复制。评估如果snp在不同的LD块有独立影响IL1RL1-a血清水平,我们执行条件分析DAG队列使用SPSS 22.0(美国纽约伊本,阿蒙克)。我们执行的候选人IL1RL1CpG荟萃分析在哮喘和IL1RL1-a MeDALL群体水平。PIAMA因果推理测试执行,队列的最大样本量完整的数据(单核苷酸多态性、甲基化、蛋白质)(详情,请参考补充材料)。我们定义了一个(epi)遗传协会作为重要的假定值Bonferroni-corrected阈值以下时。
结果
研究人群
临床特征的参与者DAG和MeDALL群组是总结补充表S1和S2a−c。DAG队列组成主要是成人中度到更严重的哮喘和配偶控制,而PIAMA, BAMSE INMA同期出生的评估患有轻度哮喘儿童从一般人群和控制。所有的分析提供了概述表1。
IL1RL1基因组区域
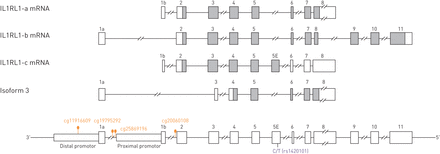
基因组区域跨越200 kb,下游IL1RL1基因(GRCh37 / hg19;chr2:102,728,004 - 103168041)包含了IL1R1,IL1RL2,IL18R1,IL18RAP和SLC9A4基因。总共有2229重叠snp在所有人群。高度复杂的LD的模式识别,LD块扩展到邻近的基因(r2> 0.7;33 LD块)(补充图S1)。的概述IL1RL1提供了成绩单图1。
的interleukin-1受体1(IL1RL1)基因(GRCh37 / hg19;chr2:102,927,962 - 102968497)的文本注释IL1RL1-a (ENST00000311734.6) IL1RL1-b (ENST00000233954.5) IL1RL1-c (ENST00000427077.1)和同种型3 (ENST00000404917.6)。研究的位置5′-C-phosphate-G-3′网站(cg11916609、cg19795292 cg25869196, cg20060108)和IL1RL1甲基化和相关蛋白单核苷酸多态性rs1420101。外显子已经屈指可数了。灰色区域是转录的部分外显子。
协会IL1RL1单核苷酸多态性与哮喘
在DAG队列,名义上被发现之间的重要关联IL1RL1单核苷酸多态性和哮喘(如。rs6543119,β= 0.14,p = 0.03)。PIAMA队列和MeDALL荟萃分析,名义上重要的结果还发现哮喘4岁之间和snp位于旁边的基因IL1RL1(如。rs7572871 (IL1R2):PIAMAβ= 0.35,p = 0.008;MeDALL荟萃分析β= 0.27,p = 0.01) (表2)。
甲基化的IL1RL1地区与cis-meQTLs相关联
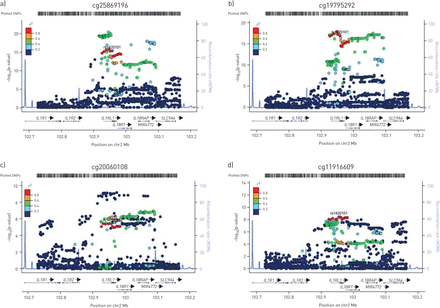
所选的IL1RL1地区包括47 CpG 9基因体内CpG网站的网站IL1RL1。单核苷酸多态性在五个不同的LD块明显与四CpG甲基化相关网站IL1RL1基因体在4岁(点击率最高:rs76886731 / cg25869196, p = 2.91×10−21;rs1420104 / cg19795292, p = 1.20×10−18;rs56179005 / cg20060108, p = 5.08×10−13;rs1420101 / cg11916609, p = 6.88×10−7)(图2所示模拟)。这四个CpG位点位于远端启动子(cg11916609),基因内区1 (cg19795292和cg25869196)和基因内区1 b (cg20060108)。rs1420101显著降低T等位基因的甲基化水平在所有四个IL1RL1CpG网站(cg25869196, p = 3.73×10−16;cg20060108, p = 5.18×10−8;cg11916609, p = 6.88×10−7;cg19795292, p = 1.20×10−17),并且也与CpG甲基化有关IL1RL2,IL18RAP和SLC9A4(补充表S3)。我们还发现了强大的IL1RL1meQTLs在IL1R1,IL1RL2,IL18R1,IL18RAP和SLC9A4(补充表S4),但是没有发现trans-meQTLs。
区域协会情节显示cell-type-corrected−log10假定值之间的联系单核苷酸多态性(snp)interleukin-1受体1(IL1RL1)基因组区域和IL1RL15′-C-phosphate-G-3′(CpG)网站)cg25869196, b) cg19795292, c) cg20060108和d) cg11916609 MeDALL荟萃分析。snp的颜色代表的连锁不平衡rs1420101(紫色圆圈)r2范围从0到1。
IL1RL1单核苷酸多态性强烈调节血清IL1RL1-a水平
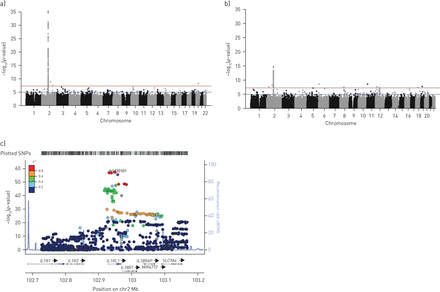
GWAS DAG IL1RL1-a血清水平和PIAMA军团显示IL1RL1SNP是强cis-pQTLs(上相关的SNP rs13020553: DAGβ= −0.33,p = 5.2×10−36;PIAMAβ= −0.12,p = 1.45×10−15)(图3 a - c)。在PIAMA八个重要trans-pQTLs被确定,但不复制在DAG (补充表S5)和荟萃分析trans-pQTLs不显著。荟萃分析的IL1RL1单核苷酸多态性在DAG MeDALL军团为高度显著cis-pQTLs甚至提供了有力的证据。联合军团,rs142010的T等位基因与IL1RL1-a血清水平较低(p = 2.83×10−56)。
联系单核苷酸多态性(snp)和血清interleukin-1受体1 (IL1RL1)——的水平。曼哈顿的情节显示结果的全基因组关联研究在DAG)组和b) PIAMA队列。红线表明全基因组意义的假定值阈值5×10−8;蓝线表示1×10的严格的假定值较小−5。c)区域协会图显示的结果IL1RL1基因组区域荟萃分析在DAG MeDALL军团。snp的颜色代表的连锁不平衡rs1420101(紫色圆圈)r2范围从0到1。
DAG条件的分析表明,三个独立的单核苷酸多态性(rs1420101, rs11685424和rs13015714)有关,与年龄和性别,解释42%的变异IL1RL1-a血清水平(表3)。LD snp标记之间的价值观不同的LD块了补充表S6。
协会IL1RL1甲基化与哮喘或IL1RL1-a水平
候选人CpG的荟萃分析九之间的联系IL1RL1CpG位点和哮喘透露一个名义上重要的CpG站点位于远端启动子,cg17738684(β= −0.006,p = 0.02),但这一发现失去了意义当纠正血液细胞成分和多个测试(补充表S7)。epigenome-wide协会研究IL1RL1-a水平显示两个trans-CpG网站,cg26748568(基因间区域所对应16日,p = 2.70×10−08年)和cg08889789(4,从而向外显子2巨噬细胞成红血球细胞连接器(MAEA),p = 8.93×10−08年),与IL1RL1-a水平显著相关(补充图S2)。
IL1RL1单核苷酸多态性不调节IL1RL1-a水平通过甲基化
我们下一个因果推理测试34)IL1RL1甲基化和相关蛋白SNP与cg11916609 rs1420101 cg19795292, cg25869196 cg20060108和血清IL1RL1-a水平PIAMA 4岁。有独立的苏格兰民族党和甲基化之间的关系,和苏格兰民族党和IL1RL1-a之间的水平,这表明我们pQTL最强IL1RL1rs1420101 SNP,不是通过甲基化调节蛋白质含量的选择CpG网站(补充表S8)。
讨论
单核苷酸多态性之间的复杂关系的综合分析,甲基化和蛋白质水平的网站IL1RL1表明asthma-associatedIL1RL1snp基因甲基化和血清蛋白质含量IL1RL1-a强烈影响。IL1RL1甲基化与IL1RL1-a水平无关。此外,我们没有观察到一个强烈的联系IL1RL1甲基化和IL1RL1蛋白表达与哮喘。
我们的研究是第一次讯问的角色IL1RL1基因甲基化在哮喘。我们发现在四甲基化水平IL1RL1在全血DNA与CpG网站IL1RL1单核苷酸多态性在五个不同的LD块,无论细胞类型组成。这是相关的,因为IL1RL1snp以前报道与外周血嗜酸性粒细胞计数(10]。我们提出,IL1RL1甲基化或全基因组CpG甲基化可能与哮喘和/或血清IL1RL1-a水平。我们发现没有证据表明哮喘有一定的联系但是我们识别两个trans-CpG网站,cg26748568 cg08889789, IL1RL1-a水平显著相关。后者CpG位点位于MAEA一个基因编码一种蛋白质,这种蛋白质介导的依恋成红血球细胞巨噬细胞。它的作用在调节IL1RL1-a还不知道,应该进一步研究。
在四LD在snpIL1RL1有非常重要的强烈影响血清IL1RL1-a蛋白质水平。PIAMA队列trans-pQTLs我们还观察到,但是考虑到相关的单核苷酸多态性低加器(0.01),没有在DAG复制,我们怀疑这些是假阳性结果。在我们成人群体识别多个独立基因信号调节蛋白的表达,有三个单核苷酸多态性(rs1420101, rs11685424和rs13015714)从不同的LD块解释血清IL1RL1-a变异的40%以上。这增加了越来越多的证据IL1RL1轨迹港口不同,独立的遗传信号(15]。
更深入的了解复杂的扩展IL1RL1地区,我们将讨论LD块大部分与基因甲基化和IL1RL1-a水平密切相关。
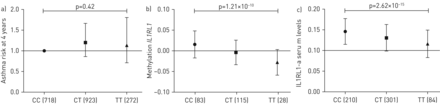
第一个LD块,围绕rs1420101,是密切相关的IL1RL1CpG甲基化在4岁和血清IL1RL1-a水平(图4 a - c)。首次报道Rs1420101调节血液嗜酸性粒细胞数量和血清IgE, T等位基因导致高嗜酸性粒细胞计数和更高的IgE水平。T等位基因也被发现是哮喘的危险变体在候选基因研究10,15]。rs1420101 (T)也降低IL1RL1信使rna表达水平在气道上皮细胞35和肺组织35,36),和更低的IL1RL1-a BAL液蛋白质含量。SNP与rs950880完全LD,最重要的SNP发现在之前的大GWAS IL1RL1-a水平(37]。我们发现rs1420101的T等位基因与更少IL1RL1甲基化和降低血清IL1RL1-a水平(表2和图4一- c), rs1420101仅仅解释18%的蛋白质含量的变化。鉴于IL1RL1-a作为IL-33拮抗剂,IL1RL1-a水平较低可能导致更明显过敏炎症,这是同意发表发现T等位基因与哮喘的风险更高(10]。此外,协会也已发现T等位基因与2型哮喘病人高表型(35]。Rs1420101位于内含子5 IL1RL1-a和- b和外显子5 e IL1RL1-c成绩单的变体。这IL1RL1变异在人类辅助细胞克隆和表达在人类白血病细胞系,UT-7 [17]。IL1RL1-c局部等离子体膜的研究在COS7细胞中过度表达,说明一个可能的函数作为一个跨膜受体(18]。然而,IL1RL1-c缺乏胞内信号域存在于IL1RL1-b由于过早终止密码子;因此,它可能不会作为功能性IL-33受体。我们建议更多的研究应该关注这一问题IL1RL1同种型。
关联分析结果的rs1420101) 4年岁哮喘的风险,b) cell-correctedinterleukin-1受体1(IL1RL1)甲基化的5′-C-phosphate-G-3′站点cg19795292和c)血清IL1RL1-a水平PIAMA队列。结果显示每rs1420101的基因型。数据在提出或(95% CI)。数据在b和c均值±sd。每个协会的假定值的分析计算模型使用添加剂。
第二个LD块被snp标记在远端(rs11685424)和近端启动子(rs12712141) 5′地区,1基因内区IL1RL1。这段与远端启动子的甲基化(cg11916609)和基因内区1 (cg19795292和cg25869196)和蛋白质IL1RL1水平(表2)。协会的LD块血嗜酸性粒细胞(25[],IL1RL1-a BAL水平26)和血清水平(25,37),但不与哮喘,曾被报告过。
第三个LD块包含两个远端启动子单核苷酸多态性,rs6543115 rs6543116。单核苷酸多态性在这个街区与远端启动子的甲基化(密切相关表2)。值得注意的是,这些snp少与IL1RL1-a水平密切相关。因此它应该有趣的调查这些单核苷酸多态性的影响,比上述rs1420101, IL1RL1-b跨膜受体同种型。
单核苷酸多态性位于下游的基因IL1RL1第四LD块过多,不包含最显著相关snp meQTL和pQTL分析。
大多数之前报道asthma-associated snp是位于LD块5,包括三个IL1RL1-b在第11外显子编码非同义单核苷酸多态性(2,9,10]。asthma-protective等位基因的单核苷酸多态性在LD块显示一个相对温和的协会IL1RL1甲基化和IL1RL1-a血清水平(表2)。这些协会的数据显示,LD阻止患有哮喘可能改变蛋白质功能(26,37)而不是从监管(epi)基因信号,尽管后者不能排除给定观察到的关联。在补充表S9我们报告其他之前报道的结果IL1RL1asthma-associated snp。有趣的是,一些asthma-associated信号并不位于LD块大部分与甲基化或蛋白质水平密切相关。这表明替代机制的存在不是由监管研究CpG或网站IL1RL1蛋白质同种型。
使用数据从GTEx财团(38),我们发现IL1RL1snp位于五LD块占最独立的协会与基因甲基化和IL1RL1-a水平信号在该地区被认为也强烈表达数量性状基因座(eQTLs)全血及肺组织基因位于IL1RL1区域(补充表S10)。SNP等位基因相关的军团IL1RL1-a水平较低的蛋白质,如。rs1420101,也降低IL1RL1表达的肺部组织。此外,使用GTEx数据,我们发现没有trans-eQTLsIL1RL1在肺部,凸显了多态性的重要性IL1RL1轨迹在调节2 12号染色体上IL1RL1基因的表达。
我们没有找到一个血清IL1RL1-a水平之间的联系和哮喘的儿童或成人well-powered分析。这与早些时候,较小规模的研究报告在成人过敏性哮喘患者血清IL1RL1-a水平高于健康对照组(39)或在儿童急性哮喘发作(14]。然而,我们的研究结果与之前的报道相一致PIAMA队列(25和严重的哮喘患者26]。因为我们的分析使用的数据不稳定的哮喘患者出现了恶化或最近的恶化,我们推测,哮喘与血清IL1RL1-a水平无关,但这可能会改变在急性加重。哮喘患者我们的数据证实,增加血清IL1RL1-a水平可以降低外周血嗜酸性粒细胞数量(14,25),符合保护IL1RL1-a对嗜酸性粒细胞的炎症反应的影响。封锁的IL-33-IL1RL1通路可能因此被认为是未来可能的哮喘患者的治疗选择嗜酸性Th2-associated炎症。
我们确定了名义IL1RL1地区单核苷酸多态性与哮喘的重要遗传协会在我们的成人和儿童的同伴的影响大小和方向符合之前报道发现在大型GWAS [2,3,8- - - - - -16]。这种温和协会在我们的队列可能导致有限的功率检测甲基化之间的关联IL1RL1轨迹或IL1RL1蛋白质含量和哮喘。IL1RL1 SNPs和哮喘之间的关系这一事实后失去了意义修正多个测试可能是由于我们研究的样本量相对较低,相比大规模GWAS [15]。然而,另一个重要因素,可以发挥作用的大型异构性哮喘。有多个sub-phenotypes哮喘的我们不能正确区分我们的军团。如前所述,多项研究表明,IL-33-IL1RL1通路中重要的2型炎症(4,5,26,35]。我们调查了一般哮喘表型,常用以人群为基础的流行病学研究,可以解释为什么我们没有发现一个强大的协会之间IL1RL1 IL1RL1之间的甲基化和哮喘和蛋白质含量和哮喘。这个假设是由最近的一项研究支持在2 - 3岁儿童喘息,这表明,血清IL1RL1-a水平没有与医生诊断哮喘在6岁,但是预测哮喘FeNO水平增加,嗜酸性气道炎症的标志(40]。最后,单核苷酸多态性可以解释大部分甲基化和基因表达,但只有很少的变化最终疾病表型。基于最近估计的哮喘的遗传异质性,数以百计的基因可能是重要的哮喘。因此很难进行因果推论功能snp哮喘使用这种方法。
我们的研究需要解决的一些限制。首先,我们发现单独的块的单核苷酸多态性通过检查LD在该地区,但意识到一些相关性在不同的LD块仍然存在单核苷酸多态性(补充表S7)。条件分析IL1RL1-a水平,然而,确认单核苷酸多态性的影响在三个独立LD块。第二,在我们的中介分析调查了四个IL1RL1CpG位点,但其他CpG网站,没有量化或分析可能也很重要。第三,我们的研究主要集中在IL1RL1-a蛋白质,但要完全理解的作用IL1RL1基因在哮喘、其他受体变异,如。IL1RL1-b - c,还应该调查。因为我们没有找到一个强大的协会之间的snp / IL1RL1-a和哮喘,因果通路分析不能被执行。
总之,我们的研究发现高度重要的关联IL1RL1单核苷酸多态性基因甲基化和蛋白表达,以及识别多个独立、功能基因在基因和基因区域的信号。然而,我们的分析表明,IL1RL1甲基化对蛋白表达不重要,确定asthma-associated snp对甲基化的影响和IL1RL1-a水平与哮喘(补充图S3)。未来的研究还应该关注IL1RL1亚型,在其他功能蛋白质编码变异的影响IL1RL1基因(地区),在确定具体的哮喘的表型IL1RL1是很重要的,这将导致哮喘诊断和个人治疗干预措施。
补充材料
确认
我们感谢DAG的参与者群体的孩子和家长MeDALL军团的参与。我们也要感谢现场工人、经理和数据科学合作者致力于这些军团。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:j . Bousquet已收到个人费用从Almirall作用于科学顾问委员会,梅达,默克公司默沙东公司,诺华公司,赛诺菲-安万特,武田,Teva Uriach;和个人费用从Almirall讲课,阿斯利康,基耶西,葛兰素史克,梅达,Menarini,默克公司默沙东公司,诺华公司,赛诺菲-安万特,武田,Teva, Uriach外提交的工作。
利益冲突:R.J.P. van der Valk收到荷兰肺脏基金会资助的行为研究;和荷兰医疗事务的员工葛兰素史克(2015年6月以来),但不持有股票,而不是参与对葛兰素史克公司进行任何研发活动。
利益冲突:贝拉Nawijn先生收到提交的支持给予他的机构从荷兰肺脏基金会工作期间进行的研究。
利益冲突:美国Guerra接到欧盟第七框架计划的拨款的行为研究。
利益冲突:科学博士Postma:格罗宁根大学接受资助的研究从阿斯利康,基耶西,Genentec、葛兰素史克和罗氏。费用咨询公司给格罗宁根大学的阿斯利康,勃林格殷格翰的发言,基耶西,葛兰素史克,武田和梯瓦。
利益冲突:G.H. Koppelman已收到机构从荷兰肺脏基金会赠款,Ubbo Emmius基金会和欧盟委员会(European Commission)在进行研究;从荷兰肺脏基金会和赠款,TEVA(荷兰)和左Astma Bestrijding外提交的工作。
资金的支持声明:本研究我们感谢荷兰肺脏基金会(格兰特数字AF 95.05, 98.48和AF3.2.09.081JU AF);格罗宁根大学医学中心;Ubbo Emmius基金;欧盟第七框架计划(批准号261357);荷兰卫生研究与发展组织;荷兰科学研究组织;荷兰的空间规划、住房和环境;荷兰卫生、福利和体育运动;皇家研究院祝您健康卡洛斯三世(红色INMA G03/176, CB06/02/0041);西班牙卫生部(FIS-PI041436 FIS-PI081151); Generalitat de Catalunya-CIRIT (1999SGR 00241); Fundació La marató de TV3 (090430); Swedish Research Council; Swedish Heart-Lung Foundation; Stockholm County Council (ALF); Strategic Research Programme (SFO) in Epidemiology; The Swedish Research Council Formas and the Swedish Environment Protection Agency. Funding information for this article has been deposited with theCrossref资助者注册表。
- 收到了2017年7月9日。
- 接受2018年1月13日。
- 版权©2018人队