摘要
放射诱导肺纤维化(RIF)是胸部放疗的延迟副作用,常与巨噬细胞浸润有关。
我们的目的是通过接受胸部恶性肿瘤放射治疗的患者的肺活检和16 gy胸部照射后C57BL/6小鼠的RIF模型来描述肺巨噬细胞在RIF中的作用。
在临床和临床前RIF中检测到大量的巨噬细胞(包括间质和肺泡)。在临床前模型中,检测到RIF组织裂解液中t辅助剂(Th)2细胞因子上调,而Th1细胞因子下调。支气管肺泡灌洗显示两种细胞因子的上调。在稳定状态下,组织浸润性巨噬细胞(IMs)表达的Arg-1是肺泡巨噬细胞(AMs)的10倍,而从RIF分离的IMs中Arg-1表达上调了40倍。im,而非AMs,能够诱导肌成纤维细胞激活在体外.此外,虽然使用Clodrosome消耗am不会影响RIF评分,但使用临床可用的集落刺激因子受体-1 (CSF1R)中和抗体消耗im具有抗纤维化作用。
这些结果提示肺泡的作用不同与RIF中的间质巨噬细胞,突出了im的成纤维作用。CSF1/CSF1R通路被认为是抑制RIF的新的治疗靶点。
摘要
一种改进辐射引起的肺部并发症管理的新方法通过CSF1R抑制http://ow.ly/dfWA30h6jxW
简介
纤维化是放疗的严重副作用[1],导致细胞外基质(ECM)的积累和器官功能的丧失。人们早就知道,肌成纤维细胞通过分泌胶原蛋白在维持纤维化过程中起着关键作用[2转化生长因子(TGF)-β1/Smad通路的激活,使PAI-1等下游纤维化因子的表达得以延续[3.].然而,最近的研究报道了巨噬细胞作为纤维化的关键调节因子的作用[4m2极化巨噬细胞参与各种纤维化模型[5,6已经被描述过。巨噬细胞极化受多种因素控制,其中包括CSF1R信号,该信号被证明对形成M1/M2巨噬细胞表型至关重要[7,8].巨噬细胞极化在辐照实体肿瘤中的作用已被研究过[9],而高辐射剂量(>8 Gy)已被证明可促进M2极化[10],而低剂量(<2 Gy)则能够对巨噬细胞进行重编程,使其朝着有利于消除肿瘤的M1表型方向发展[11].最近的数据表明这个数字很高与低剂量的放疗可引起肿瘤中巨噬细胞的分化激活。然而,巨噬细胞在辐射诱导肺纤维化(RIF)中的作用尚不明确。因此,我们的目的是利用一个特征良好的肺纤维化实验模型来研究肺巨噬细胞的作用[12]由单一的高剂量胸部照射引起,其剂量与目前在立体定向身体放射治疗中使用的剂量相当。由于正常肺对辐照的耐受性至关重要,因此选择肺作为巨噬细胞作用至关重要的参考器官[13].事实上,巨噬细胞肺泡炎一直与RIF相关。我们的结果显示,临床和临床前RIF被巨噬细胞高度浸润。RIF组织裂解液的细胞因子分析显示T辅助(Th)2细胞因子上调,而Th1细胞因子下调。然而,支气管肺泡灌洗(BAL)显示两种细胞因子的上调。间质巨噬细胞(IMs)降低促炎标志物Icam1的膜表达,增加抗炎标志物CD206的膜表达,而肺泡巨噬细胞(AMs)的膜上Icam1和CD206均升高。巨噬细胞激活相关基因的表达分析支持了im和AMs之间的表型差异。在稳态下,im的arginase -1表达量是AMs的10倍。此外,从RIF肺分离的im中检测到Arg-1的40倍上调。最后,通过损耗实验,我们强调了im的不同贡献与使用抗集落刺激因子受体-1 (CSF1R)中和抗体消耗的IMs显示出抗纤维化作用,而使用氯膦酸酯脂质体(Clodrosome;Interchim, Montluçon, France)没有效果。
材料和方法
更多材料和方法,请参见在线补充材料.
人类组织样本
经法国研究部(AC-2016-2844)批准,从当地肿瘤库中采集样本。这项研究得到了当地科学和伦理委员会的批准,并免去了具体同意的需要。样本收集自2012年至2016年在我科手术的10例胸部恶性肿瘤患者。4例患者术前接受放疗,在左肺切除术前接受35 - 60 Gy的放疗。此外,6例未接受放疗的患者纳入研究;他们接受了手术并被用于控制目的。
动物与辐照程序
雌性12周龄C57BL/6J小鼠购自法国查尔斯河实验室(Saint-Germain-Nuelles, France)。小鼠通过麻醉(2%异氟醚)固定,并使用瓦里安管NDI 226 (x光机;250 Kev,管电流:15 mA,束滤:0.2 mm Cu),剂量率1.08 Gy·min−1.局部给整个胸腔注射单剂量16戈瑞。
流式细胞术和荧光激活细胞分选
F4/80-FITC (eBioscience, Paris, France)、Gr1- pe (eBioscience)、CD11c-PE-Cy7 (Biolegend, Ozyme, Montigny-le-Bretonneux, France)和CD11b-APC-Cy7 (Biolegend)被用于鉴定中性粒细胞(Gr1高(Ly6G+Ly6C−))、单核细胞(Gr1一起+(Ly6G−Ly6C+)), AMs (CD11c+CD11b−F4/80+) [14和即时通讯(Gr1−CD11b+CD11c−/ +F4/80+) [15].Gr1一起−单核吞噬细胞(MPs)被鉴定为Gr1−CD11b+CD11c+F4/80−.Icam1-Pacific blue (Biolegend)用于识别m1极化的巨噬细胞,CD206-PerCpCy5.5 (Biolegend)用于识别m2极化的巨噬细胞。使用CD115-PE (eBioscience)检测AMs和im中CSF1R的表达。使用FlowJo 10.0.7 (FlowJo, Ashland, OR, USA)对样本进行分析。利用荧光激活细胞分选技术对im和AMs进行分选,并将其转移到培养基中。
胶囊氯膦酸酯脂质体(Clodrosome)给药
大约60 μ L的Clodrosome经鼻内给药[16胸椎照射后15周,5周内每3-4天进行一次。
使用CSF1R单克隆抗体抑制肺巨噬细胞
胸部照射15周后,照射组和对照组动物分别用中和性抗csf1r单克隆抗体(mAb) (CS7;Eli Lilly, Indianapolis, IN, USA)为40毫克·公斤−1(i.p。)每周三次,持续五周。
统计分析
使用GraphPad Prism 7 (GraphPad Software, San Diego, CA, USA)进行统计分析。双向方差分析用于检测辐照和未辐照小鼠随时间变化的差异,随后进行Sidak多重比较试验。采用单因素方差分析(One-way ANOVA)检测各组间差异,随后进行Tukey多重比较检验。p值≤0.05被认为是显著的。数据以平均值±表示扫描电镜.
结果
RIF与肺巨噬细胞的积累有关
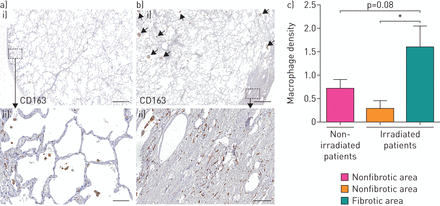
辐照肺实质取自1981年至1998年间接受治疗的4例患者的手术样本。他们接受了术前放疗;治疗他们的胸部恶性肿瘤的总剂量为35 ~ 60戈瑞。未放疗的肺实质来自6例未接受任何放疗的患者。与对照样本相比(图1一个),来自RIF患者的样本显示肺泡壁增厚,肺泡空气空间减少,导致肺泡结构消失(图1 b).为了表征RIF区域的肺巨噬细胞浸润,对辐照和未辐照的人肺组织进行CD163染色。我们展示了CD163+肺巨噬细胞在辐射患者肺组织肺泡内形成簇状(图1 b箭头)。有趣的是,CD163在辐射后的人肺纤维化区高表达(图1 bc)对照肺组织(图1一个c). CD163标记被描述为在m2样巨噬细胞中上调[17],提示人类RIF可能与m2样肺巨噬细胞相关。鉴于人类纤维化和对照肺组织的可及性非常有限,我们旨在通过使用小鼠RIF模型来验证这一假设,以便深入描述RIF发展过程中的肺髓样亚群浸润。
人类辐射诱导的肺纤维化与高CD163相关+巨噬细胞浸润。a)和b)使用DAB(3′,3-二氨基联苯胺)抗cd163标记在25 - 60 Gy之间的未辐照和辐照人肺实质石蜡吸收切片中巨噬细胞浸润的组织学评估。人体活组织切片取自1981年至2012年间接受胸部放射治疗的患者。i)比例尺=1 mm;Ii)比例尺=100 μm。箭头表示巨噬细胞簇。c)辐射患者(n=5)和对照组(n=5)巨噬细胞密度定量。数据代表一次实验,用平均值±表示扫描电镜.*: p<0.05(单向方差分析,Tukey检验)。
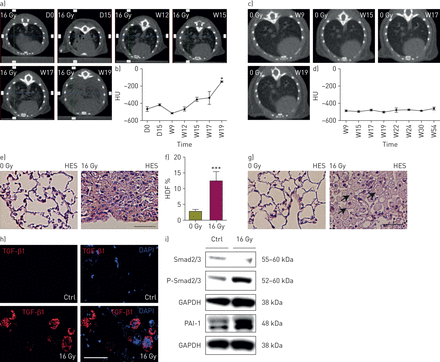
我们首先在文献中描述的RIF小鼠模型中验证了肺纤维化的发展[12].圆锥束计算机断层扫描在照射后的几个时间点进行,显示照射后第15天肺密度增加的趋势(图2一个第二,这表明肺部有早期炎症反应。有趣的是,肺密度在照射后第9周恢复到基础率,在照射后第12周至第19周第二次增加(图2一个(2)建议RIF的发展。对未辐照小鼠的监测显示,随着时间的推移,肺密度是稳定的(图2 c和2 d)。照射后20周的肺组织病理学检查显示胶原蛋白沉积,通过藏红花(黄色)染色(图2 e)和天狼星红染色(在线)补充图S1a)。利用自动组织学图像分析软件定量评估实质纤维化[18]显示放射肺的高组织密度频率(HDF)指数显著升高与年龄组(图2 f).此外,照射后胶原沉积的天狼星红染色明显增加(在线补充图S1b).纤维形成模式与重要的细胞浸润相关(图2 g),特异性积累TGF-β1表达细胞(图2 h).最后,通过Western blot分析,RIF导致PAI-1表达和Smad2/3磷酸化的增加(图2我).
临床前放射诱导肺纤维化模型及纤维化定量。a)辐照C57BL/6小鼠在辐照后第(D) 0、15天和第(W) 12、15、17、19周时肺密度的锥形束计算机断层扫描(CBCT);b)辐照C57BL/6小鼠肺密度定量(n=4);*: p<0.05(单因素方差分析,Dunnett检验);c)未照射C57BL/6小鼠肺密度随时间变化的CBCT扫描;d)未照射C57BL/6小鼠肺密度定量(n=5);e)辐照C57BL/6小鼠肺纤维化代表性图像(苏木精-伊红-藏红花(HES)染色)(n= 3-6)与年龄匹配的对照组,照射后20周;f)在照射后20周,通过评估未照射(n=10)和照射(n=8)的C57BL/6小鼠的高组织密度频率(HDF)指数来量化实质纤维化。数据来自三次实验,并以均数±表示扫描电镜.* * *: p < 0.001 (t);G)照射后20周肺间隙巨噬细胞浸润的代表性图像。箭头表明巨噬细胞。比例尺= 200μm;h)照射后20周肺组织转化生长因子(TGF)-β1免疫荧光(红色)和DAPI(4',6-二胺基-2-苯林多)染色(蓝色)。比例尺= 15μm;i) Western blot检测照射后20周肺组织中Smad2/3 Ser465/467磷酸化(p-Smad2/3)和Smad2/3、PAI-1和GAPDH的表达。b)和d)数据来自一次实验,并以平均值±表示扫描电镜.控制:控制。
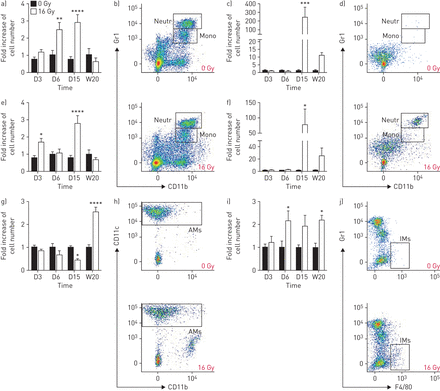
接下来,我们描述了照射后不同时间点BAL和肺间质中的细胞浸润(在线补充图S2).中性粒细胞Gr1一起高(Ly6G+)数目在照射后6和15天显著增加,并在照射后20周恢复到基础比率(图3一b).在肺泡间隙(BAL)中,仅在第15天检测到中性粒细胞浸润,并在照射后20周保持高浸润水平(图3 cd).瞬时Gr1+照射后第3天薄壁内可见单核细胞浸润(图3 e和b).第15天检测到第二个浸润峰值,与肺泡间隙的浸润有关,如观察到的中性粒细胞(图3 fd)和Gr1+20周后,单核细胞在牙槽间隙进一步积累。Gr1的个数−在薄壁组织或BAL中,MPs没有随时间变化(数据未显示)。
胸部辐射损伤时的炎症细胞特征。a)未辐照和辐照C57BL/6小鼠在辐射损伤过程中实质内的间质中性粒细胞数量增加一倍;b)鉴别中性粒细胞的门控策略(Neutr;Gr1一起+CD11b+)和单核细胞(Mono;Gr1一起国际米兰CD11b+)在照射后20周未照射和照射小鼠的实质内;c)辐照和非辐照小鼠在辐射损伤过程中支气管肺泡灌洗液(BAL)中中性粒细胞数量增加一倍;d)门控策略识别中性粒细胞(Gr1高CD11b+)和单核细胞(Gr1+CD11b+)在照射后20周,未辐照和辐照小鼠的BAL;E)辐照和非辐照小鼠在辐射损伤过程中实质内的间质单核细胞数量增加了一倍;f)辐照和非辐照小鼠在辐射损伤过程中BAL单核细胞数量增加一倍;g)辐照和非辐照小鼠在辐射损伤过程中肺泡巨噬细胞(AMs)数量增加一倍;h)鉴别AMs的门控策略(CD11c+CD11b−)在照射后20周未照射和照射的小鼠;i)辐照和非辐照小鼠在辐射损伤过程中,组织浸润性巨噬细胞(IMs)数量增加一倍;j)鉴别im的门控策略(F4/80+Gr1一起−)在照射后20周,未照射和照射的小鼠。用固定数量的10 μm聚羧酸酯微球计算绝对数值,用与同一时间点的平均值相比增加一倍表示。数据来自两个独立的实验,并以均数±表示扫描电镜.D:一天;W:一周;*: p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。D3: 0 Gy, n= 7-8;16 Gy, n = 8 - 9;D6: 0 Gy, n= 7-8; 16 Gy, n=7; D15: 0 Gy, n=7–8; 16 Gy, n=8; week 20: 0 Gy, n=7; 16 Gy, n=8–10 (two-way ANOVA, Sidak test).
辐射诱导AMs (CD11b)的数量逐渐减少−CD11c+F4/80+)直到第15天(图3 g).广泛灌洗支气管肺泡间隙后,从消化的肺中获得的AMs很少,这表明AMs与肺泡上皮的粘附性更强。AMs的整体积累与表达cd11b的AMs比例的增加有关。照射后20周,AMs恢复,数量超过(图3 gh),此时高达30%的AMs为CD11b+(在线补充图S3).
最后,IMs (CD11c−/ +CD11b+F4/80+)在照射后6天和20周肺实质内显著增加(图3我和j),从未在BAL中检测到(数据未显示),表明该子集仅存在于肺间质中。
我们的结论是,RIF与RIF发展早期炎症细胞(单核细胞和中性粒细胞)渐进式浸润和积累到肺泡间隙有关,并与肺纤维化和晚期肺AMs和im的积累增加有关。
RIF与AMs和im的差异表型相关
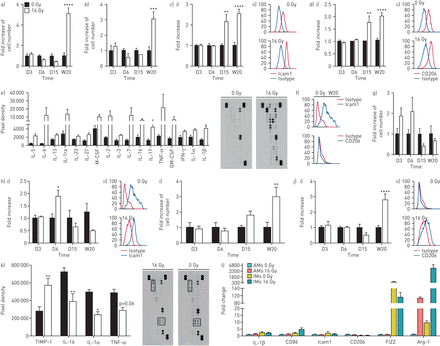
研究了Icam1(促炎标记物)和CD206(抗炎标记物)的膜表达,以及im和AMs中的基因谱。Icam1的编号+和CD206+照射后第20周AMs增加(图4一和b)两种标记物在RIF肺的AMs上均上调(图4 c通过对BAL的脱细胞部分进行细胞因子分析的微环境分析是一致的,并表明促炎Th1-和抗炎th2相关细胞因子(白介素(IL)-2, IL-7,肿瘤坏死因子-α, IL-6和IL-5)在照射后均被诱导(图4 e).
胸部照射后肺泡巨噬细胞(AMs)和组织浸润性巨噬细胞(IMs)的表型特征。a) Icam1的数量倍增+AMs和b) CD206+辐射损伤时的AMs;c) i) AMs在辐射损伤过程中,Icam1膜ΔMFI(抗体平均荧光强度/同型对照平均荧光强度)成倍增加;ii)辐照后第20周,未辐照小鼠和辐照小鼠体内经Icam1标记染色的AMs单参数代表性直方图;d) i) AMs在辐射损伤过程中CD206的ΔMFI膜成倍增加;ii)照射后第20周,未照射和照射小鼠的AMs染色CD206标记的代表性单参数直方图;e)在照射后第20周使用细胞因子阵列分析支气管肺泡灌洗液(BAL)的脱细胞部分,并对信号和代表性印迹进行密度分析;f)辐照后第20周(0 Gy),未辐照小鼠体内Icam1和CD206标记的组织浸润性巨噬细胞(IMs)代表性单参数直方图;g) Icam1增加1倍+辐射损伤时IM值;h) i) im中Icam1的ΔMFI膜在辐射损伤过程中成倍增加;ii)辐照后第20周,未辐照和辐照小鼠体内Icam1标记染色的具有代表性的单参数im直方图;i) CD206增加一倍+辐射损伤时IM值;j) i)辐射损伤时im中CD206的ΔMFI膜增加了一倍;ii)照射后第20周,未照射和照射小鼠体内CD206标记染色的具有代表性的单参数im直方图;K)肺组织消化,在照射后第20周使用细胞因子阵列进行蛋白质组分析,并进行信号的密度分析,有代表性的印迹。用固定数量的10 μm聚羧酸酯微球计算绝对数值,用与对照平均值相比增加的倍数表示。数据来自两个独立的实验,并以均数±表示扫描电镜.D:一天;W:一周;IL:白介素;M-CSF:巨噬细胞集落刺激因子;TNF:肿瘤坏死因子;GM-CSF:粒细胞-巨噬细胞集落刺激因子;干扰素:干扰素。D3: 0 Gy, n=8;16 Gy, n = 8 - 9; D6: 0 Gy, n=7–9; 16 Gy, n=7; D15: 0 Gy, n=8; 16 Gy, n=8; W20: 0 Gy, n=7; 16 Gy, n=8–10. In e and k) n=3 in each group. *: p<0.05; **: p<0.01; ***: p<0.001; ****: p<0.0001 (two-way ANOVA, Sidak test). l) Fold change of mRNA of M1 and M2 markers in AMs and IMs at 20 weeks after irradiation. Data were obtained from one experiment and presented as mean±sd技术复制。0 Gy:汇集9只小鼠样本;16戈瑞:来自7只小鼠的混合样本。
稳定状态下,im中Icam1表达亮,CD206表达低(图4 f).Icam1的编号+即时消息瞬时增加(图4 g), Icam1表达水平在辐照后第6天升高,并在第20周逐渐恢复到基础值(图4 h).在晚期(第20周),CD206数目增加+观察到表达更高水平CD206的im (图4我和4 j)。IM微环境的细胞因子分析显示th1相关细胞因子(如IL-1α和IL-16)下调,th2相关介质TIMP-1 (图4 k).随后,我们对选定的激活标记进行基因表达分析。其中最显著的结果之一是Arg-1 mRNA水平:稳态时,im中Arg-1的表达量是AMs的10倍,而在rif分离的im中是40倍与RIF-isolated AMs (图4 l).此外,与健康肺分离的im相比,RIF分离的im诱导了400倍的Arg-1 mRNA水平。我们的结果表明,辐射对AMs和im表型的影响是不同的,RIF的发展与组织和BAL中不同的局部细胞因子和趋化因子微环境有关。
激活的im能够诱导肌成纤维细胞的激活和ECM的产生体外
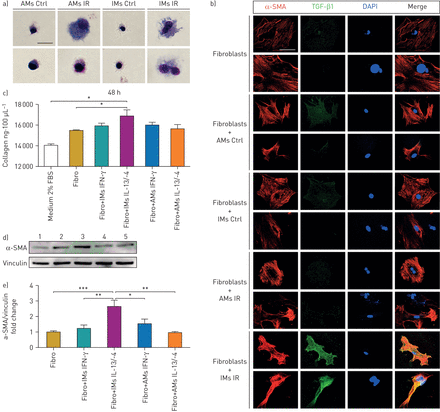
AMs和im各自参与纤维发生的机制被探讨体外实验。首先,从辐照后15周的RIF组织中筛选出im和AMs。Giemsa染色显示辐照小鼠的im和AMs与正常巨噬细胞相比表现出泡沫表型(图5一个).rif分离的im显示CD206标记的表达增强,AMs显示CD206和Icam1标记的表达增强(在线补充图S4),说明自动辅助系统和即时通讯系统在此阶段已被激活。将筛选好的im和AMs用转孔与正常成纤维细胞共培养,用α-平滑肌肌动蛋白(SMA)和TGF-β1的表达检测肌成纤维细胞的分化。当成纤维细胞与rif分离的im共培养时,观察到TGF-β1在成纤维细胞中的诱导作用(图5 b),但与rif孤立的AMs无关。
正常成纤维细胞和活化的肺巨噬细胞共培养。a) May-Grünwald照射后第15周,流式细胞仪对活化和非活化肺巨噬细胞进行吉氏染色。比例尺= 50μm。b)成纤维细胞和巨噬细胞共培养(三份)24 h后,α-平滑肌肌动蛋白(SMA)(红色)和转化生长因子(TGF)-β1免疫荧光(绿色)和DAPI染色(蓝色)。比例尺= 20μm。数据来自一次实验。c)用Sircol法在100 μL成纤维细胞上清中定量胶原生成在体外激活的肺泡巨噬细胞(AMs)/组织浸润性巨噬细胞(IMs)。d)共培养48 h后,Western blot检测全成纤维细胞裂解液中α-SMA的表达;1)成纤维细胞;2)成纤维细胞+ IMs IFN -γ;3)成纤维细胞+ IMs IL-13 / 4;4)成纤维细胞+ AMs IFN -γ;5)成纤维细胞+ AMs IL-13 / 4。e)共培养48小时后,全成纤维细胞裂解液中α-SMA表达/vinculin表达的折叠变化定量。数据来自两个独立的实验,并以均数±表示扫描电镜.n = 6 - 7。控制:控制;红外光谱:辐照;干扰素:干扰素;IL:白介素。*: p < 0.05;* *: p < 0.01;***: p<0.001(单向方差分析,Dunnett检验)。
此外,从正常小鼠肺中筛选出im和AMs并激活在体外用重组干扰素-γ诱导经典激活和重组IL-13/-4诱导替代激活24小时。然后将激活的AMs和im与正常肺成纤维细胞在没有激活介质的情况下共培养。与IL-13/-4激活的im共培养的成纤维细胞产生过多的ECM成分(图5 c增加α-SMA的表达(图5 de),而激活的AMs对正常成纤维细胞产生的ECM、α-SMA无影响。这些结果证实了激活im的不同参与程度与AMs对肺成纤维细胞表型的调节作用。
使用Clodrosome对AMs的特异性消耗对RIF没有影响
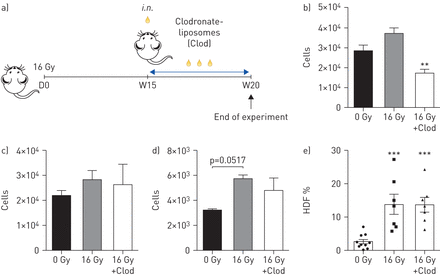
Clodrosome经鼻给药会消耗AMs,但不会消耗im [16],并在照射后15周用于选择性消耗AMs (图6).选择这个时间点是因为Icam1的数量增加了+/ CD206+照射后15周观察AMs (在线补充图S4).最初的流式细胞术分析证实了通过Clodrosome治疗选择性消耗AMs (图6 b).相比之下,单核细胞(图6 c)、IMs (图6 d)和Gr1一起−Clodrosome治疗对MPs(数据未显示)无影响.在照射后20周,氯drosome介导的AMs耗损与高HDF纤维化指数相关,在未使用氯drosome治疗的辐照小鼠中也是如此(图6 e).
胸部照射后氯膦酸酯脂质体(Clod)对肺泡巨噬细胞(AMs)的特异性靶向作用a)鼻内AM耗竭(i.n。)给C57BL/6小鼠照射15周后(16 Gy)给予60 μL的Clod。照射20周后,处死小鼠,取右肺一半分离消化。随后,用流式细胞术对肺组织源性细胞进行染色和分析。b) AM, c)单核细胞和d)流式细胞术定量检测不同处理组动物的组织浸润性巨噬细胞数量。e)在照射后20周,通过评估治疗和非治疗小鼠的高组织密度频率(HDF)指数来量化实质纤维化。采用固定数量的非荧光10 μm聚羧酸酯微球计算绝对数。数据来自两个独立的实验,并以均数±表示扫描电镜.0 Gy: n = 7;16 Gy: n = 7;16 Gy+Clod: n=7。In e) 0 Gy: n=10;16 Gy: n = 7;16 Gy +笨蛋:n = 7。*: p < 0.05;* *: p < 0.01;***: p<0.001(单向方差分析,Tukey检验)。
使用CSF1R单抗时,im的特异性耗竭而非AMs的特异性耗竭阻断了RIF的发展
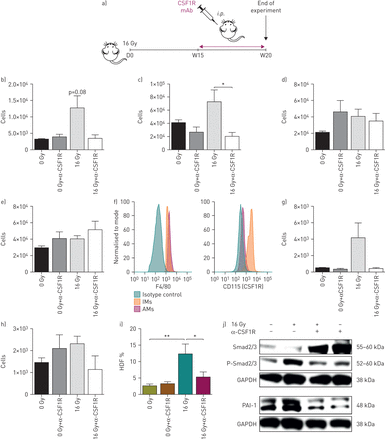
接下来,我们尝试使用抗csf1r抗体(CS7)更广泛地清除肺巨噬细胞亚群。小鼠在胸部照射后第15周开始,每周治疗3次,持续5周(图7).因此,在照射后20周,我们发现CSF1R单抗治疗特异性地降低了im (图7 b)和Gr1一起−议员(图7 c).Gr1的数量没有减少+此时观察到单核细胞和AMs (图7 de)。随后,我们分析了CSF1R在AMs上的表达,发现与im相比,AMs表达的CSF1R水平较低(图7 f),从而解释了该种群缺乏CS7的调制。有趣的是,抗csf1r治疗更大幅度地减少了CD206的数量+与Icam1相比+IMs (图7 g和h)。这种降低与RIF的急剧下降相关(图7我而且联机补充图S5PAI-1表达和Smad2/3磷酸化水平显著降低(图7 j).
胸部照射后抗csf1r靶向组织浸润性巨噬细胞(IMs)。C57BL/6小鼠(n= 4-6)胸部照射。a)小鼠给药CSF1R mAb (i.p。)在照射后15周(16 Gy)。照射后20周处死小鼠。分离右肺并消化,用流式细胞仪检测肺巨噬细胞特征。b) IM, c) Gr1−单核吞噬细胞,d)单核细胞和e)肺泡巨噬细胞(AM)数量定量。f)用F4/80和CD115染色的im和AMs的代表性单参数直方图(CSF1R)。g) CD206+IM和h) Icam1+我数字量化。i)照射后20周,通过测定治疗和非治疗小鼠的高肺组织密度频率(HDF),对纤维化评分进行组织学评估。数据来自三个实验,0 Gy: n=10;0 Gy +α-CSF1R: n = 9;16 Gy: n = 8;16 g +α-CSF1R: n = 12。j) Western blot分析照射后20周消化后肺组织中Smad2/3 Ser465/467磷酸化(p-Smad2/3)和Smad2/3、PAI-1和GAPDH的表达。采用固定数量的非荧光10 μm聚羧酸酯微球计算绝对数。数据来自一次实验,以均数±表示扫描电镜.*: p < 0.05;**: p<0.01(单向方差分析,Tukey检验)。
最后,我们探索了肺成纤维细胞在辐射小鼠中触发肺巨噬细胞激活的可能性。从辐照和未辐照小鼠中分离的原代肺成纤维细胞与正常AMs或正常im共培养,共培养24 h后收集上清(在线补充图S6a).从辐射肺+ im分离的成纤维细胞产生的上清中,CSF1和单核细胞趋化蛋白-1的含量高于辐照成纤维细胞+ AMs或未辐照成纤维细胞+ im产生的上清(在线补充图S6b和c).这些结果表明,受辐照的成纤维细胞可以激活驻留/招募的巨噬细胞,以促进炎症细胞的招募和不同亚群的极化走向成纤维原型。
我们得出的结论是,CSF1R单克隆抗体可阻断肺内RIF的发展,但可减少im,而不是AMs。
讨论
巨噬细胞在肿瘤放疗反应中的关键作用最近被发现[19],其可能作用于交替激活的巨噬细胞释放促血管生成因子,有助于肿瘤抵抗和/或辐射后的再生[10].在本研究中,我们以肺为模型,研究了正常组织对放疗的反应,并广泛描述了肺巨噬细胞的作用。结论如下:1)人及临床前RIF均与巨噬细胞浸润相关,提示肺巨噬细胞在RIF中发挥重要作用;2)纤维源性照射剂量既可诱导急性促炎反应先发生在实质,后发生在肺泡,也可诱导晚期炎症反应,其特征为表型差异的AMs和im;3) rif分离的im可能通过诱导肌成纤维细胞分化诱导成纤维过程;这些结果得到了证实在体外使用IL-13/-4激活的im;4)利用CSF1R单抗特异性消耗RIF中的im,而不是消耗AMs,可发挥抗纤维化作用,CSF1R被认为是一个有效的抗纤维化靶点。
肺对辐射高度敏感,是放射治疗中剂量限制的主要器官。急性和迟发性辐射引起的肺毒性已在病理生理和细胞水平上被描述过[20.,21].临床急性肺毒性在近30年前就有描述,命名为“急性放射性肺炎”[21].这种急性综合征的特征是空气间隙中的巨噬细胞浸润和肺泡壁中的单核炎症细胞[12].一致地,我们的临床前模型重复了这些旧的结果,显示了薄壁组织和肺泡间隙之间炎症细胞浸润的不同时间。延迟性肺毒性的临床特征为慢性进行性肺RIF [21].慢性期主要表现为弥漫性胸膜下纤维化、肺泡塌陷或消失,并被无功能结缔组织所取代[21如所示图1.在小鼠模型中,巨噬细胞肺泡炎被描述为肺部RIF的标志[12].总之,人类和小鼠RIF都与巨噬细胞的高浸润有关,我们的假设是肺巨噬细胞能够触发RIF的发生和维持。
我们的研究结果支持了这一假设,并为AMs和im在纤维形成过程中的不同作用提供了第一个证据。大量证据表明AMs和im代表不同的细胞群[22].因此,我们在AMs和im之间显示了稳定状态下的基因表达差异,并首次描述了AMs中CSF1R膜表达低于im。此外,与rif分离的AMs不同,rif分离的IMs失去了Icam1,但增强了CD206膜表达和过表达的Arg-1 mRNA。此外,来自患者的RIF活检显示CD163高浸润+被描述为交替激活的巨噬细胞[17].这种巨噬细胞亚型也被描述在博莱霉素诱导的肺纤维化中[23]和特发性肺纤维化[23],由微环境中存在的特定细胞因子模式驱动[24,25].此外,我们提供的证据表明,受辐射的肺成纤维细胞本身可以通过细胞因子(如CSF)的分泌促进巨噬细胞的激活。因为rif分离和IL-13/-4激活的im刺激成纤维细胞分化为肌成纤维细胞。因此,信号似乎是双向的,RIF中证实了成纤维细胞和im之间的功能性串扰,正如前列腺癌进展过程中所描述的那样[26].我们的研究发现了一种新的纤维形成环,它涉及并维持间质巨噬细胞和成纤维细胞的激活,如图8.
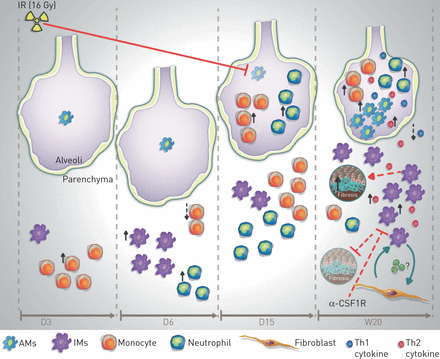
提出了肺巨噬细胞对辐射诱导肺纤维化(RIF)的贡献模型。在对高剂量辐射(IR;16 Gy),照射后第(D)3天,软组织内出现以单核细胞数量增加为代表的炎症反应,随后在照射后第6天,中性粒细胞和促炎组织浸润性巨噬细胞(IMs)数量增加。在D15时,单核细胞、中性粒细胞和im的数量恢复到基础速率。此时肺泡间隙内单核细胞和中性粒细胞数量增加,伴有肺泡巨噬细胞(AMs)的大量减少。在晚期(至W)20周),肺泡面积减少,间质RIF评分增加。在肺泡间隙,AM数量的增加与t辅助细胞1 (Th1)和Th2细胞因子分泌的增加以及中性粒细胞和单核细胞数量的增加有关。在间质空间中,Th2细胞因子如TIMP-1的分泌与IM数量的增加有关,它能够诱导成纤维细胞的直接激活和反之亦然.这种im和成纤维细胞之间的相互作用有助于RIF的发病机制,并指出了激活im的促纤维化作用,而激活AMs似乎是非促纤维化的。抗csf1r对im的特异性消耗可诱导激活im的显著消耗,而非AMs,并降低纤维化评分。
该方案与其他类型纤维化的结果一致[13,27],并首次证明了im有可能触发RIF的特定功能。因此,这些结果支持了抗噬细胞策略作为抗纤维化治疗的相关性。我们确定并证明CSF1R是一个治疗靶点。事实上,鉴于CSF1R在im上的优先表达,使用抗CSF1R中和抗体导致了原纤维性im的特定消耗,而不影响AMs的种群(见模型)图8)和反向RIF。CSF1R抑制联合放疗的临床应用超出了正常组织毒性,因为在小鼠前列腺癌模型中,当联合放疗时,CSF1R抑制被描述为肿瘤生长的有效抑制因子[28].这表明使用CSF1R抑制剂靶向CSF1/CSF1R轴可以提高放疗的治疗指数,但需要进一步的研究在肺模型中验证这一假设。许多制药公司正在开发靶向巨噬细胞的治疗工具,早期临床研究表明CSF1R抑制剂[29具有临床应用价值。我们研究中使用的抗csf1r抗体(CS7)是目前在前列腺癌和乳腺癌临床试验中的人类CS4抗体的小鼠对应物[30.].因此,我们的结果打开了有趣的治疗视角,可以很快在早期临床试验中进行评估。
总之,尽管近期放射肿瘤学在治疗计划和图像引导放射治疗方面取得了进展,但正常组织毒性仍然是局部肿瘤最佳控制的剂量限制因素。此外,随着长期癌症幸存者数量的增加,严重的并发症会出现,并极大地损害患者的生活质量。在此,我们提出了一种新的方法来改善放射诱发并发症的临床管理通过CSF1R的抑制和激活间质巨噬细胞的消耗。
补充材料
披露的信息
补充材料
e·多伊奇erj - 02120 - 2017 - _deutsch
m . Mondonierj - 02120 - 2017 - _mondoni
b .小erj - 02120 - 2017 - _petit
mc。Vozeninerj - 02120 - 2017 - _vozenin
确认
作者要感谢Yann Lécluse、Philippe Rameau、Sophie salme - desnoulez(成像和细胞检测平台(PFIC))和Olivia Bawa(临床前评估平台(PFEP))对Gustave Roussy (Villejuif, France)的技术支持;David Schaer (Eli Lilly, New York, NY, USA)提供有益的讨论。作者也希望感谢Y. Julé和J.C. Gilhodes (Biocellvia, Marseille, France)对肺纤维化的自动组织学图像分析和有益的讨论。
作者贡献:L. Meziani设计并执行实验,进行数据/统计分析并撰写稿件;M. Mondini设计了抗csf1r实验,监督了实验并撰写了手稿;B. Petit进行实验;A. Boissonnas分析和解释数据;O. Mercier和V. Thomas de Montpreville收集人体样本并审查工作;mc。Vozenin和E. Deutsch设计并监督了实验,提供了资金并撰写了手稿。
脚注
本文的补充资料可从www.qdcxjkg.com
支持声明:本研究已获得美国国立癌症研究所(INCa)和礼来公司的资助。本文的资助信息已存入Crossref资助者注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2017年3月10日。
- 接受2017年12月4日。
- 版权©2018人队