摘要
小气道是慢性阻塞性肺疾病(COPD)的主要阻塞部位。本研究使用多排计算机断层扫描(MDCT)、微计算机断层扫描(microCT)和组织学的新组合检查小气道病理。
上试样MDCT可见气道分支进行计数和三阶到第五代气道的尺寸被计算,而末端细支气管(指定TB),细支气管preterminal(TB-1)和预preterminal细支气管(TB-2)分别为在终末期慢性阻塞性肺病8个移植的肺和作为对照七个未供体肺与显微CT和组织学检查。
On MDCT, COPD lungs showed a decrease in the number of 2–2.5 mm diameter airways and the lumen area of fifth-generation airways, while on microCT there was a reduction in the number of terminal bronchioles as well as a decrease in the luminal areas, wall volumes and alveolar attachments to the walls of TB, TB-1 and TB-2 bronchioles. The combination of microCT and histology showed increased B-cell infiltration into the walls of TB-1 and TB-2 bronchioles, and this change was correlated with a reduced number of alveolar attachments in COPD.
在COPD中,小气道疾病从直径2mm的气道扩展到终末细支气管。肺泡附着体的破坏可能是由终末前细支气管中b细胞介导的免疫反应驱动的。
摘要
慢性阻塞性肺病患者末梢前细支气管B细胞浸润与肺泡附着物破坏有关http://ow.ly/htxe30hMFoE
介绍
20世纪60年代的一系列报告[1- - - - - -4] established that the small conducting airways <2 mm in diameter offer <10% of the total resistance to airflow in health but become the major site of increased resistance in chronic obstructive pulmonary disease (COPD). Based on these and other data, M含铅[5] postulated that the small conducting airways <2 mm in diameter are a “quiet” zone within normal lungs where disease can accumulate over many years without being noticed. Since then, numerous reports have shown that disease in the small conducting airways in patients with COPD is characterised by chronic inflammation, lumen narrowing, wall thickening and loss of alveolar attachment to the outer walls of these airways [6- - - - - -12.].此外,20世纪90年代多探测器行计算机断层扫描(MDCT)的引入使得在MDCT上可见的直径2-3毫米的气道异常与COPD中的气流阻塞密切相关[13.].使用MDCT和微计算机断层(微CT)更多最近的报告表明,末端细支气管(指定TB)变窄,广泛患者终末期COPD与肺移植治疗肺破坏[14.].此外,microCT研究显示,慢性阻塞性肺病小叶中央型肺气肿的终末前细支气管(TB-1)内腔狭窄、壁增厚和肺泡附着体缺失[15.].
本报告的目的是用一个非常最近开发的方法能够准确地从组织的相同样本连接MDCT和显微CT扫描,组织学切片的[16.]为了确定小气道疾病延伸的小支气管和细支气管(2 - 2.5毫米直径)定义开始的肺的安静区(pre -) preterminal (TB-1和TB 2)和终端细支气管(结核病)中最后一个纯粹的开展航空肺安静的区域。
方法
知情同意
与极重度COPD等待肺移植和捐赠者的近亲,允许被认为不适合移植的器官被释放的研究条件下直接获得患者的知情同意。
多层螺旋ct和微螺旋ct扫描
在本研究中,所有标本均为右肺。为多层螺旋ct和显微ct成像准备肺组织的程序以及随后的组织学已在其他地方详细描述[14.- - - - - -16.].简单地说,接受COPD肺移植的患者捐献了8个受COPD影响的肺;所有患者均患有全球慢性阻塞性肺病倡议(GOLD) 4期疾病。7个未使用的捐赠肺(3个从不吸烟,4个以前吸烟)作为对照。肺完全充气至30厘米每小时正压2O, then deflated and held at constant pressure (10 cmH2O)而将肺用液氮蒸气和冷冻固体包围。The inflated lung specimen was kept frozen while MDCT scans were obtained using a CT scanner (either a Siemens Sensation 16 (Siemens Medical Solutions, Munich, Germany; 120 kVp, 250 mA, pitch: 1.25, 1 mm contiguous images) or a GE Discovery CT750 HD (GE Healthcare, Milwaukee, USA; 120 kVp, 250 mA, pitch: 1.375, 0.625 mm contiguous images)) and reconstructed using a high spatial frequency reconstruction algorithm (Siemens: B60f, GE: Bone). The frozen specimen was then cut into 20 mm-thick transverse slices from lung apex to base, and regions of mild to moderate emphysema were specifically identified by visually inspecting photographs of the slices from the COPD lungs. Frozen tissue cores 14 mm in diameter and 20 mm in length were removed from the selected lung regions of COPD lungs and from randomly selected regions of control lungs. The cores were imaged on a Nikon HMX 225ST micro CT scanner (Nikon Metrology, Leuven, Belgium) with 11 μm isotropic voxel resolution at −30C, using a technique recently described in detail by Vasilescuet al。[16.].
MDCT分析
采用Apollo 2.0软件(VIDA Diagnostic Inc., Coralville, IA, USA)分析多层螺旋ct标本扫描中的气管支气管树。基于区域生长算法,对气道树进行了自动分割。根据最近报告的一种方法,人工设置了一个新的种子点,以便在必要时进一步进行区域生长[17.].使用分段气道树自动计算每一代气道的分支数。测量了RB1和RB10路径的第三代、第四代和第五代气道的管腔和壁面积,并取每代的平均值。< - 950 Hounsfield单位(LAA%)的低衰减肺组织百分比[18.,19.,以评估整个右肺肺气肿的严重程度。
MicroCT分析
平均线性截距(LM)和每毫升肺终末细支气管的数目中的每个组织核心测定如先前所述[14.]. 在每个组织核心随机选择一个末端细支气管,定义为最后一个纯传导气道,然后是末端前细支气管[15.]和预preterminal细支气管通过从所选择的终末细支气管[跟踪回识别14.].被重建每个气道的横截面显微CT图像垂直于它们的管腔的中心线上,和细支气管长度(二分支点之间的距离),管腔和壁区域,壁厚和体积,内径,肺泡附件的数目它们的壁,以及由外周调节肺泡附件的数量,使用先前报道的方法[所得15.].
组织学
冷冻组织芯检查通过显微CT的部分是在固定过夜醇基福尔马林保持在-20℃,升温至室温,处理和包埋在石蜡中,并切成4微米厚的切片[16.].使用光学显微镜检查苏木精和伊红染色的切片,可以将组织学切片与微ct扫描相关联,以识别TB、TB-1和TB-2。对于免疫组化,切片与一抗孵育以识别特定的细胞类型(表E1),随后通过使用碱性磷酸酶系统来放大信号的第二抗体。气道壁的体积分数通过占用免疫细胞亚型计算所有可识别的TB,TB-1并在组织学切片TB-2。另外,基底膜的周边(PBM),管腔和相对圆形的气道的壁区域(长径/短径<3)进行测定,和组织学壁厚通过根据先前报道的由PBM分隔壁面积计算手动跟踪技术[10.].由于基底膜长度不受膨胀水平或平滑肌收缩程度的影响[10.,20.],由基底膜在一个假设的所包围的区域最大限度扩张气道的圆形(A最大限度)可以计算为;一种最大限度= PBM2/(4π),管腔狭窄程度可计算为1−(测量的管腔面积/A)最大限度答案:Boskenet al。[11.].
统计分析
数据表示为平均值±SD..对照组与COPD组比较采用t检验或Wilcoxon秩和检验。Tukey的调整被用于多次比较。免疫细胞体积分数对数变换后进行Pearson相关检验。使用R程序进行统计分析[21.].
结果
表格1结果显示,7名对照组和8名COPD患者的年龄、性别和身高匹配良好,而对照组体重较重。所有COPD患者都曾吸烟,而对照组中有3人从未吸烟。
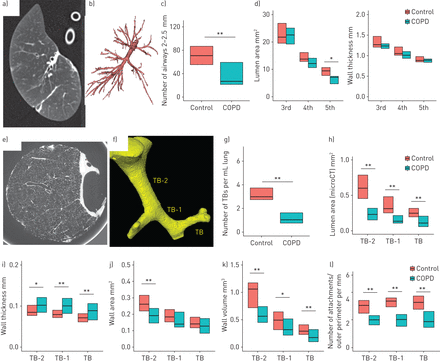
图1一个b显示用阿波罗软件重建气道树的多层螺旋ct标本扫描图。表2.显示COPD患者的总肺体积和标本MDCT扫描的肺气肿变化明显大于对照样本。COPD患者气道总数量、气道壁面积和管腔面积较对照组均呈下降趋势,直径2-2.5 mm气道分支数量(图1 c)和第五代气道腔区(图1 d)。图1 d也显示COPD与对照组第三代、第四代和第五代气道壁厚无差异。
样品多排计算机断层摄影(MDCT)和呼吸道的微计算机断层扫描(微CT)分析。一个)MDCT扫描,从该气道树分割(b)中。c) MDCT measurements show the number of airway branches 2–2.5 mm in diameter and luminal area of the fifth-generation airways (sub-subsegmental) are decreased in chronic obstructive pulmonary disease (COPD) compared with control lungs while d) wall thickness does not differ. e) MicroCT scan, from which the lumen of terminal (TB), preterminal (TB-1), and pre-preterminal (TB-2) bronchioles were segmented (f). MicroCT measurements show that g) the number of terminal bronchioles and h) the luminal areas of TB, TB-1, and TB-2 are decreased in COPD compared with control lungs. These measurements also show increases in i) the wall thickness of TB, TB-1 and TB-2 and j) the wall area of TB-2 and k) decreases in the wall volume and l) the number of alveolar attachments per outer perimeter of TB, TB-1 and TB-2 in COPD. *: p<0.05; **: p<0.01.
图1 e和f示出了如何显微CT扫描被用来确定终端支气管和跟踪从TB回TB-1和TB-2。表3将来自7个对照肺的38个样本与来自8个移植肺的40个样本的microCT数据进行比较图E1显示这些样本在肺内的位置分布在对照组和COPD肺之间没有差异。在慢性阻塞性肺病患者中,每毫升肺的末端细支气管数量以及结核、结核-1和结核-2的管腔面积和肺泡附着体减少(表3,图1 g和h)。TB-2、TB-1和TB的壁厚(图1我)在COPD增加而不在壁面积的增加(图1 j)在这些气道,而壁体积(图1 k)及由外周长调整的牙槽附着体数目(图1 l)降低。
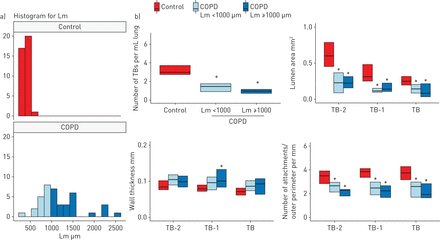
图2A显示了来自对照和慢性阻塞性肺病患者样本的Lm分布。图2B.shows that the number of terminal bronchioles, lumen area and number of alveolar attachments to TB-2, TB-1, and TB were decreased in samples with mild emphysema (Lm <1000 µm) in the COPD compared with control lungs.补充图E2LAA% (MDCT)、Lm、终末细支气管数量、管腔面积或肺泡附着体数量(microCT)在有和无吸烟史的对照组之间无差异。
多排计算机断层扫描和控制和慢性阻塞性肺病(COPD)肺气肿的不同级别的样品之间的微计算机断层扫描进行比较。a)一个直方图平均线性截距(LM)中控制和COPD。To compare mild emphysematous regions of the COPD lungs with controls, COPD samples were divided into those with Lm <1000 µm (n=16) and Lm ≥1000 µm (n=24). b) The number of terminal bronchioles (TBs) per mL of lung, the mean lumen area, and the number of alveolar attachments per length of outer perimeter of TB, TB-1 and TB-2 were decreased in both groups of COPD samples compared to controls. *: p<0.05与控制。
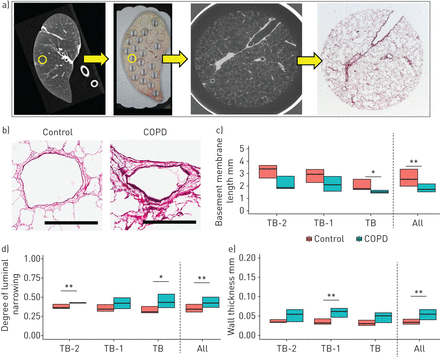
图3A显示与相应肺切片照片相匹配的标本多层螺旋ct扫描,其中圆圈区域表示取样用于微ct和组织学。图3B.示出了代表在对照和慢性阻塞性肺病的肺TB-1的横截面。与控制肺部,这成为统计显著结核病相比,该循环被切断气道的组织学分析显示,基底膜在COPD周边呈下降趋势(图3 c)。与此相反,有走向更大的管腔变窄的趋势(图3 d)和壁厚(图3 e),而肺结核-1在统计学上有显著意义。
在组织学上具有微计算机断层摄影(微CT)扫描合并的小气道的结构的评估。a)一种多排的一个例子计算与相应的肺切片的照片相匹配的样本(左面板)的断层摄影扫描在其上圆形区域表示随后用于显微CT和组织学的区域。这允许使用相同的气道的组织学显微CT的比较。通过显微CT图像匹配的组织切片,这种技术使能终端(TB)的识别,preterminal(TB-1),和预preterminal(TB-2)在组织学上的细支气管。b)中的代表性横截面TB-1在对照和慢性阻塞性肺病(COPD)。比例尺表示0.5 mm。相对圆形的细支气管的组织学测量(9个TB,11 TB-1,而在控制5 TB-2和8个TB,11 TB-1,以及五个TB-2在COPD)c)中基底膜长度,d)气道的程度变窄和e)的壁厚。气道变窄的程度计算为;1-(测量管腔面积)/(计算出的由基底膜在假想封闭区域最大程度地扩张气道)。 “All” on thex轴表示数据组合所有圆形细支气管包括结核病,TB-1和TB-2时(在控制N = 25和n = COPD 24)。*:P <0.05;**:P <0.01。
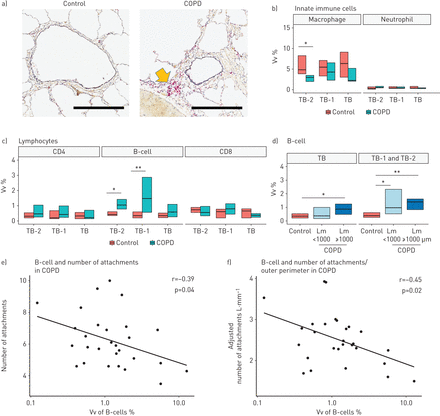
图4A在对照组和COPD中显示TB-1具有代表性的CD79a染色。来自所有圆形和非圆形气道免疫化学染色的数据显示,COPD中CD68抗体染色的巨噬细胞在TB-2中减少(图4 b), TB-1和TB-2中CD79a抗体染色的b细胞增多(图4一和c)。图4d在COPD肺中Lm <1000µm和Lm≥1000µm的样本中,TB-1和TB-2中b细胞数量增加。此外,COPD中b细胞对TB-1和TB-2的浸润增加与肺泡附着/气道数量减少相关(图4 e)中并用(由外周调节肺泡附件的数量图4 f)具有相同的气道,但不具有壁厚或管腔面积(补充表E2)。
免疫组化和微计算机断层成像联合分析评估小气道免疫细胞浸润和结构改变。a) CD79a抗体(b细胞标记物,以黄色箭头表示)在对照组和慢性阻塞性肺疾病(COPD)晚期前细支气管(TB-1)中具有代表性的免疫组化。比例尺表示0.5 mm。TB和TB-2表示终末和前-终末细支气管。b和c)使用所有圆形和非圆形细支气管的免疫细胞占用的气道壁体积分数(Vv)(对照组为15-16 TB、15-17 TB-1和9-10 TB-2, COPD为17-18 TB、15-16 TB-1和13 TB-2)。d)与对照组(n=24)相比,COPD样本中平均线性截距(Lm) <1000µm (n=14)和Lm≥1000µm (n=15)的TB1和TB-2壁的b细胞浸润明显增加。TB-1和TB-2壁上b细胞的Vv分别与e)每条气道的肺泡附着数量(r=−0.39,p=0.04)和f)每mm外周长的肺泡附着数量(r=−0.45,p=0.02)的关系。*: p<0.05; **: p<0.01。
讨论
In this study, the combined use of MDCT and microCT provides new information about the lung's “quiet” zone in COPD by showing that both the numbers of airways 2–2.5 mm in diameter identifiable on MDCT scans and the terminal bronchioles on microCT scans are decreased, and the lumens of the fifth-generation airways and the pre-preterminal, preterminal and terminal bronchioles (TB-2, TB-1 and TB) are narrowed in COPD. These data suggest that the disease in the lung's “quiet zone” extends from airways 2–2.5 mm in diameter to the terminal bronchioles. Furthermore, the combination of microCT and histology allowed us, for the first time, to show that increased B-cell infiltration into the walls of TB-1 and TB-2 in COPD is associated with destruction of alveolar attachments to these airways.
本报告的主要优点是,它是基于技术的进步[16.],允许细支气管使用显微CT准确地定位,然后进行组织学处理。这使得有可能研究相对于炎性免疫细胞浸润的组织重塑和破坏到终端和细支气管preterminal(即。TB, TB-1和TB-2)由microCT定义。因此,目前的数据扩展了许多关于COPD小气道疾病的组织学报告[10.- - - - - -12.,14.]通过显示壁增厚和TB-1的管腔变窄并且增加的B细胞浸润到TB-1和TB-2是与肺泡附件的损失相关联。
小气道和实质b细胞浸润增多已被认为是慢性阻塞性肺病的主要组织学特征[10.,22.- - - - - -24.],和基因表达分析提示肺气肿破坏细胞和B细胞相关的免疫途径[之间的关联25.,26.].然而,尽管小气道通常被定义为直径小于2毫米的细支气管,包括相对较大的细支气管(直径1-2毫米)以及末端前和末端细支气管(直径0.5-0.7毫米),但没有研究检查特定一代小气道的b细胞浸润。此外,虽然终末和终末前细支气管的异常是COPD的重要病理病变[14.,15.],通过该增加B细胞浸润有助于这些气道结构变化不被理解的机制。因此,显示出增加的B细胞数量之间的关联本发明的结果和在TB-1和TB-2降低肺泡附件COPD肺的基本上延伸以前的研究结果,并且建议的持久B细胞介导的免疫响应会导致破坏肺泡的附件,并最终促进肺气肿的进展。
值得注意的是,即使在轻度肺气肿(Lm <1000µm)的样本中,COPD肺的终末细支气管数量减少、管腔狭窄、肺泡附件数量减少和b细胞浸润增加也存在。这表明小气道的这些病理改变可能在严重的肺气肿破坏建立之前就发生了。
微ct数据显示TB和TB-1的细支气管长度减少,但TB-2没有。我们假设气道的缩短是由弹性纤维断裂引起的气道树轴向收缩的结果,这些弹性纤维从气管延伸到最外围的细支气管和肺泡。27.,28.].结果还表明,TB、TB-1和TB-2的壁厚增加,但壁面积和体积没有增加。壁厚和面积之间的这种差异与我们最近关于末前细支气管结构的报告一致[15.],并且可以通过在腔区域中的更大的减少比在总面积进行说明(即。壁和管腔面积)。此外,观察到在COPD中所有这几代小气道的壁体积和肺泡附着的数量都减少,支持了这样的假设,即终末和终末前细支气管以及周围肺泡组织的破坏是COPD的一个主要病理特征[8,10.,11.,14.,15.].
基底膜或内腔的周边已用于气道大小来估计,因为此长度是不太可能受组织处理(如肺膨胀度)或平滑肌收缩的程度[影响10.,20.].在本研究中,我们发现,末端细支气管的基底膜的长度是在COPD比对照肺短。这是由B中的上次报告一致oskenet al。[11.],观察到谁在COPD膜细支气管的内周长的减少。基于表示管腔变窄的程度越大在COPD比对照的结果,我们推测,除了基底膜,气道过度折叠的缩短由于异常修复过程中形成和瘢痕组织的收缩过程占了COPD管腔面积的减少。The MDCT measurements confirmed the reduced numbers of 2–2.5 mm diameter airways while the wall areas of the fifth-generation airways tended to be smaller in the COPD lungs (p=0.06). These reductions in airway count and wall area in COPD are consistent with recent MDCT reports on total airway counts [17.]及气道的尺寸[29.,30.].因为气道树是基于区域生长方法分割,分割处理将在窄点即使当管腔周边到该窄点保持开放[终止17.].The present finding of luminal narrowing of the fifth-generation airways without wall thickening leads us to speculate that the reduced number of 2–2.5 mm diameter airways reflects luminal narrowing of these airways in COPD.
Explanted lungs were inflated with a positive pressure of 30 cmH2O实现完全充气,然后放气并保持恒定压力(10 cmH2O) 而冻结固体。我们选了10个 cmH2O as the static pressure because 30 cmH2O压力可能导致过度膨胀和空气漏入间质,而且因为从30到10 cmH肺容量只会减少相对较小(约10%)2O位于压力-体积曲线的通缩边缘[31.,32.].
需要指出本研究的一些局限性。本研究仅提供了经肺移植治疗的晚期COPD患者的气道信息。轻、中度COPD小气道病理可能与终末期COPD不同。由于潜在的治疗干预主要针对的是轻至中度COPD患者,因此未来应该对这一人群通过手术获得的肺组织进行气道病理研究。第二个局限性是,尽管本研究检测了两代末梢细支气管近端(对照组的直径为0.88±0.20 mm),但由于样本芯的大小有限,更多的近端细支气管(直径1-2 mm)无法识别。最后,虽然采用多层螺旋CT扫描对切除的冷冻肺测量LAA%,但尚不清楚移植和冷冻肺的过程是否对CT密度有影响。由于解释过程中肺血容量丢失,这可能导致肺密度降低,LAA%增加。
In conclusion, this study shows that small airways disease extends from 2 mm diameter airways to the terminal bronchioles in COPD. Further, the combination of microCT with histology provides important new information associating the infiltration of B-cells with the destruction of alveolar attachments to the outer wall of the preterminal bronchioles, which we postulate represents the site of the spread of this destructive process from the airway lumen and wall into the alveolar tissue.
补充材料
披露
致谢
作者的贡献如下:获取数据,分析和解释信息:N. Tanabe, D.M. Vasilescu, M. Kirby, H.O. Coxson, S.E. Verleden, B.M. Vanaudenaerde和D. Kinose。参与研究的概念、假设描述和设计:N.田边,D.M. Vasilescu, H.O. Coxson, Y. Nakano, P.D. Paré和J.C. Hogg。撰写文章或在投稿前参与修改:N.塔纳部,D.M. Vasilescu, M. Kirby, H.O. Coxson, P.D. Paré和J.C. Hogg。所有作者都通过了手稿的最终版本。
脚注
本文提供了补充材料www.qdcxjkg.com.
支持声明:美国国家卫生研究所(R01 HL122438),加拿大卫生研究所(加拿大胸部成像网络),Grifols和Respivert公司的研究人员发起的合同。本文的资金信息已存入CrossRef Resder注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com.
- 已收到2017年6月22日。
- 接受2017年11月30日。
- 版权所有©ERS 2018