摘要
越来越多的证据表明肺动脉高压的炎症成分。然而,由于标记物特异性的复杂性和组织不可接近性,肺中多种炎症细胞群的最终特征具有挑战性。我们使用无偏计算流式细胞术方法描绘特发性肺动脉高压(IPAH)和健康供肺的炎症情况。
采用主成分分析明确区分供体和IPAH样本,以减少单细胞流式细胞术分析获得的多维数据。在IPAH肺中,主要是CD45+细胞类型从中性粒细胞转变为CD3+T细胞,CD4增加+,CD8+和γΔt-小区子集。另外,多移激活的古典霉菌衍生的树突细胞(CD14-HLA-DR.+CD11C.+CD1A.+ /−)和非经典浆细胞样树突状细胞(pDCs;CD14-CD11C.-CD123+HLA-DR.+),以及肥大细胞和嗜碱性细胞,在IPAH样本中更丰富。我们首次描述了IPAH中两种细胞类型的存在和调节,γδ t细胞和pDCs,它们连接先天免疫和适应性免疫。
利用我们的高通量流式细胞学具有多维数据集分析,我们揭示了多个炎症细胞之间的交互式相互作用是其综合网络的重要组成部分。该疾病中γδT细胞和PDC的鉴定可能在IPAH,自身免疫和炎症之间提供缺失的联系。
摘要
计算流式细胞术详细说明了肺动脉高压患者复杂的炎症细胞景观http://ow.ly/rjFZ30g1tew
介绍
肺动脉高压(PH)的特点是严重的血管重塑,导致肺血管阻力增加。越来越多的证据表明炎症成分在疾病发展中起着重要作用。在PH中,已观察到重塑动脉内和周围炎性细胞数量升高,其中血管周围区域的浸润细胞数量与内膜和中膜重塑相关[1].尽管PH与免疫系统的pH和失调之间的透明链接[2仍然缺乏肺部肺部免疫和炎症细胞的系统分析。
据报道,肥大细胞和B-和T淋巴细胞在具有不同形式的pH的患者中增加[3.- - - - - -7].募集的炎症细胞可以释放某些不仅直接改变血管微环境的介质,而且还招募额外的循环炎症细胞,这反过来进一步恶化疾病进展。几种细胞因子和趋化因子的表达,例如CCl2,CCl5或Cx3Cl1 / reachine,肺部和pH患者的重组血管增加[8- - - - - -10.].此外,炎症细胞是其他介质的重要来源,例如危险分子(HMGB1)和蛋白酶(胰蛋白酶),其在当地生产时会导致肺平平滑肌细胞增殖增加[7,11.].
迄今为止,对人肺内炎症细胞的分析主要依赖于免疫组化或形态学特征[1,4,9,12.]. 然而,由于标记物特异性的复杂性,仅使用单个标记物对几个炎症人群进行决定性分类是一个挑战。流式细胞术提供了一种更复杂的方法来彻底识别和量化不同的免疫细胞群。这项技术在人体血液或灌洗液样本的细胞特征分析中已得到很好的应用,但最近只有少数研究表明其在分析整个组织样本中的有用性[13.- - - - - -15.].我们采用了一种基于无偏性流式细胞术的方法,对大组特征明确的特发性肺动脉高压(IPAH)患者和健康的非利用供体肺组织中的肺和肺动脉中的多个炎症细胞群进行免疫表型分析。这是第一个进行如此广泛的分析,最终证明IPAH发病机制中的炎症成分的研究。
材料与方法
提供了对方法的详细描述在线补充材料.
肺组织
来自iPAH患者(n = 16)和对照(n = 15)的肺组织是从维也纳医科大学(维也纳,奥地利)的胸外科划分。由于尺寸减少的肺移植而未植入,已收获的非植物供体肺组织,但由于对照,而不是植入的肺部[16.,17.].所有的肺都被冲洗了通过用Perfadex(XVivo灌注,瑞典)进行抗灌和逆行灌注,以除去任何残留的血液。没有任何炎症病症如肺炎,肺结核或具有胸腔积液的感染的迹象。协议和组织使用由制度伦理委员会(976/2010)批准。
组织制备和流式细胞术
在新鲜外部外植体肺部随机(外周或垂直)拍摄两个独立的样品(〜400mg),并以致盲的方式使用标准化方案处理。肺动脉被隔离,如图所示在线补充图S1; 简单地说,根据动脉的解剖位置和结构,对其进行识别、切除,然后以与肺样本相同的方式进行处理。制备单细胞悬浮液,并使用四种不同的细胞表面标记组合进行染色,详情见联机补充表S1和S2并记录在LSRII流量仪(BD Biosciences,Vienna,奥地利)。然后对成对的肺样品的结果平均,并且呈现为CD45百分比的数据+细胞或每毫克组织的细胞数。
Biocomputational分析
用于生物信息学分析(www.rstudio.com)和r(www.r-project.org)被使用了。Prcomp用于根据CD45百分比的对数优势比计算主成分+细胞;前两个主组件是使用ggplot2包绘制的。细胞数量/组织重量或CD45百分比的对数比值比的热图+使用pheatmap包绘制细胞。基于t分布随机邻域嵌入(t-SNE)的非线性降维[18.]在FlowJo(亚什兰,OR,美国)表演。
Immunofluorescent染色
如前所述,对石蜡包埋的肺切片进行免疫荧光染色[19.].使用激光扫描共聚焦显微镜(LSM 510 Meta; Zeiss,Gottingen,Germany)获得共聚焦图像。
统计
统计学分析在R中进行。使用Shapiro-Wilk正常性测试测试每组进行分发。使用Wilcoxon等级测试测定统计显着性;图中指示p值。散点图显示Boxplot叠加层,配有中位数和狭窄的范围。
结果
流仪结果
在这项研究中,我们使用多参数流式细胞术结合生物信息学分析来描述整体炎症概况(图1)在IPAH(n = 16)的患者的肺部中,并将其与健康供体的肺(n = 15)进行比较。描述了患者和捐赠者的人口统计和临床特征表1.显示IPAH中显示古典血管重塑的肺形态的代表性图像在线补充图S2.
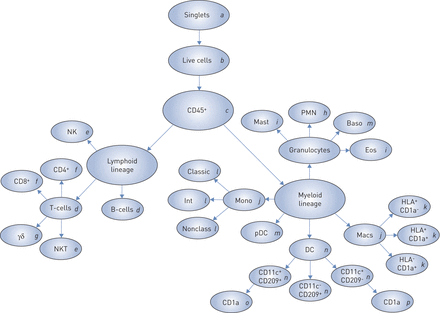
在流式细胞分析中鉴定的分析细胞群的示意图表示。所有造血衍生CD45的等级组织+淋巴和骨髓谱系的细胞。NK:天然杀伤细胞;NKT:天然杀伤T细胞;PMN:多素核性嗜嗜中性粒细胞;Baso:嗜碱性粒细胞;EOS:嗜酸性粒细胞;单核:单核细胞;INT:中间单核细胞;非殖民:非繁拟单核细胞;DC:树突细胞; pDC: plasmacytoid DC; Macs: macrophages. Italic letters (p)表示常见的细胞群,如图2.
21个不同的细胞群被分析并分成1)淋巴系,包括B细胞和t细胞,t细胞亚群和自然杀伤(NK)细胞,2)髓系,包括单核细胞,巨噬细胞,肥大细胞,中性粒细胞和树突状细胞(DCs)等。利用CD1a和HLA-DR(人白细胞抗原-抗原D相关)标记物测定树突状细胞和巨噬细胞的激活状态。用于描述细胞种群的多种细胞表面标记和综合门控策略的详细描述见在线补充表S2和图2,分别。由于采用多面板方法,我们首先进行相关性分析,以确定在不同面板中确定的细胞类型的结果如何变化(在线补充图S3).面板之间观察到强烈的相关性,这证明了我们分析的稳健性,并使个人值能够平均值,从而允许我们产生用于随后分析的细胞群的最大可能覆盖。类似地,从两个独立样品获得的流式细胞术结果的比较显示出高再现性(在线补充图S4).
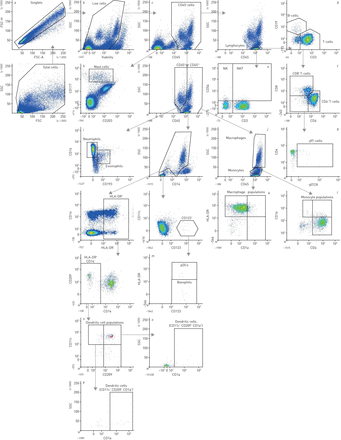
流式细胞术分析中使用的门控策略概述。分析的群体首先浇注除去细胞团块和碎片,通过活力排除除去死细胞。使用CD45阳性选择所有白细胞,然后分为单独的细胞群,如图所示。FSC-H:前向散射高;FSC-A:前进散射区;SSC:侧面散射;HLA-DR:人白细胞抗原 - 抗原D相关;PDCS:血浆骨质特性细胞;NK:天然杀伤细胞;NKT:天然杀伤T细胞。 Boxes and italic lettering (p)表示常见的细胞群,如图1.
炎症性概况的全局变化
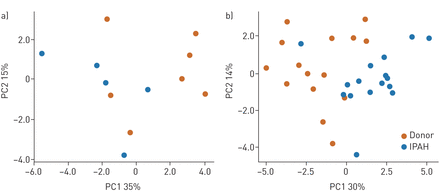
接下来,我们试图确定IPAH和健康控制肺是否显示出明显的免疫细胞签名。为此,我们利用了计算流式细胞术的最新发展[20.[执行主成分分析(PCA),尺寸减少完整的数据集,同时最大化捐助者和IPAH样品之间的差异。仅使用完整的数据集仅使用肺部,从而分析了总共七个供体和五个IPAH肺的所有21个细胞种群,并良好地分离了供体和IPAH样品(图3A).然后,我们通过从全局分析中省略限制的三个细胞群(嗜酸性粒细胞,NK,NKT细胞)来增强PCA的力量。该程序最大化了分析的肺和群体的数量,并在组之间进行了卓越的歧视(图3B.). 供体和IPAH之间这三个细胞群的相对水平没有观察到差异(在线补充图S5). 对最终数据集(包括31个肺和18个细胞群)进行了深入分析。
流式细胞术数据的主成分分析图将特发性肺动脉高压(IPAH)与对照样本分离。使用手工门控流式细胞术获得的子集分析数据的对数比值比,用于构建主成分分析的相似矩阵。描述了前两个主成分(PC)各自的百分比变化。双变量降维图a) 12个肺(7个供体/ 5个IPAH),包括21个细胞群;b) 31个肺(15个供体/16个IPAH)和18个细胞群。
CD45的细胞分布+IPAH患者和供体的肺部细胞
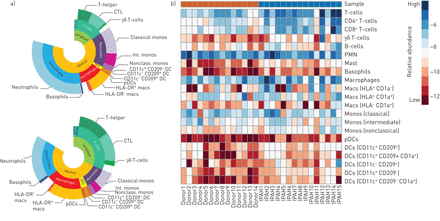
在对照样本中,约占所有CD45的64%+细胞来自髓系,主要是粒细胞(32%)和单核细胞(17%);约15%的淋巴细胞,主要是t细胞(14%),CD4含量几乎相等+和CD8+T细胞。小群体包括B细胞,嗜碱性粒细胞,DC,γδT细胞和肥大细胞(图4A).在IPAH肺中,免疫细胞分布明显,支持PCA图中可见的清晰聚类。骨髓细胞的强优势降低到52%,而淋巴细胞来源的细胞富集到31%。因此,IPAH肺中最大的单个细胞分类转变为t细胞(29%),这与粒细胞群体(19%)和骨髓源性单核细胞群体(11%)的明显相对减少相对应。此外,还观察到几个小群体的相对丰度较高,包括树突状细胞和肥大细胞(图4A).在使用的标志物中,不能将约21%的对照样品中的细胞和16%的IPAH中的细胞进行鉴定。
炎症性概况的全局变化。a)Sunburst地块显示来自特发性肺动脉高血压患者的供体肺和肺部的所有细胞群的平均分布;b)热图表示呈现患者对患者的患者对数单个组织数据衍生自细胞数的对数量的可变性,用于18个单独的细胞群。CTL:细胞毒性CD8+T淋巴细胞;中性粒细胞:多形核中性粒细胞;巨噬细胞;单核细胞:单核细胞;Int:中级;非经典的:非经典的;树突状细胞;PDC:浆细胞样DC。
使用Heatmap表示,我们检查了CD45百分比的分布方式+细胞(在线补充图S6)和绝对的数字(图4B.)在每个病人中各不相同。在每一组中,观察到相对均匀的模式,而在IPAH和供体样本之间,发现了明确的差异,突出表现为IPAH患者中t细胞和DC人群的富集(图4B.).采用欧氏距离计算对样本进行排序,IPAH与供体样本聚类良好(在线补充图S7).
肺样本中单个细胞类型的调节
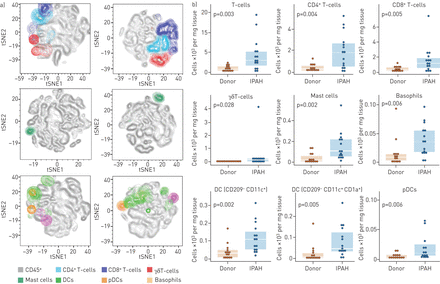
从全球差异到单个细胞类型的变化,我们分析了18个细胞群图4B.单独。在分析细胞数量时,IPAH与供体肺之间有10个细胞群差异丰富(图5).这些人群(如在图2)被绘制在t-SNE复合图上,这显示了大多数人群明显的歧视和本地化(图5a).T-SNE图突出了通过考虑所有原始尺寸的相似性获得的新的双相矩阵的不同细胞簇之间的关系。通过增加的T细胞数来证明IPAH肺中的改变的炎症状态(CD4+和CD8+T细胞),肥大细胞,嗜碱性粒细胞和DC。此外,我们鉴定了γδT细胞的升高,迄今为止尚未在pH中报告的群体。在骨髓源性CD11C中+DC组,均为CD209+和CD209-亚群增加,包括CD1a+激活的DCS(图5b和在线补充图S7).注意,直流覆盖在图5a与供体相比,在IPAH样品中显示出更具分散的群体。这可以从IPAH肺部调节和激活的多种DC种群产生。此外,在iPAH肺部增加了非胶质树突细胞PDC。在CD19绝对丰富的情况下没有观察到任何变化+b细胞、巨噬细胞亚群(HLA-DR和CD1a表达不同)、CD11c-CD209.+DC、单核细胞亚群或中性粒细胞(在线补充图S8).接近CD45百分比的检查+细胞揭示了大多数细胞类型中的类似调节(在线补充图S9).然而,一些群体,如中性粒细胞和单核细胞,减少了,这可能是由于t细胞群体的强烈增加(在线补充图S9).
t-随机邻邦嵌入(t-SNE)可视化和调节细胞群在肺样本。a)下采样和连接CD45的t-SNE复合维数图+源自具有覆盖的流式细胞术数据的细胞,具有覆盖的手动门控细胞群。b)通过流式细胞术鉴定的特发性肺动脉高血压和供体肺之间的受管制细胞群差异丰富。DCS:树突细胞;PDCS:血浆曲线细胞细胞。箱线图显示中位数和四分位数间的范围。
分离肺动脉炎症谱的调节
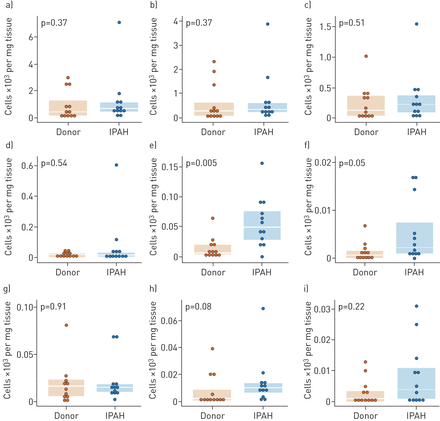
我们检查了这种细胞调节是否仅限于包含多个室的肺组织,如小肺动脉,或者是否可以在较大的肺动脉中发现。事实上,即使在这些大容器中(第三到第四代;在线补充图S1),我们观察到类似的趋势,肥大细胞和嗜碱性粒细胞数量增加;然而,有几种细胞类型低于统计学意义(图6).此外,我们观察了增加了丰富的活化巨噬细胞(CD1a+HLA+)和DCs (CD11+CD209.+CD1A.+)和单核细胞群(在线补充图S10).
孤立肺动脉中的细胞群体丰富。通过流式细胞术在第三和第四代肺动脉中测量多个细胞群(如图所示的肺匀浆样品)。a)t细胞;b)CD4+t细胞;c) CD8+t细胞;d)γδt细胞;e)肥大细胞;f)嗜碱性粒细胞;g)树突细胞(CD209-CD11C.+);h)树突状细胞(CD209-CD11C.+CD1A.+);I)浆细胞样树突状细胞。IPAH:特发性肺动脉高压。箱线图显示中位数和四分位数间的范围。
pDCs和γδ t细胞的定位
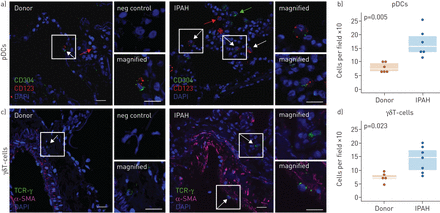
由于pdc和γδ t细胞都是以前没有在PH中检测过的细胞类型,我们另外进行了多色免疫荧光染色来确认和显示它们在肺组织中的存在。髓(CD123+CD304+), IPAH患者的肺中患病率高于供者,且主要局限于靠近血管的肺泡间隙(图7ab)。可以在供体和IPAH患者的肺部中检测γΔT细胞,并且在后者的频率近距离接近频率(图7c和d)。
肺中血浆骨质树突细胞(PDC)和γδT细胞的存在和定位。对特发性肺动脉高压(IPAH)和供体肺组织的免疫荧光染色和对A,B)CD123(RED)和CD304(绿色)的特性肺组织进行检测PDC(CD123+CD304+)和c,d) TCRγ(绿色)检测γδ t细胞。平滑肌肌动蛋白(SMA)染色为紫色;核染色通过DAPI(蓝色)。较小的面板代表放大的区域,就像在较大的面板中显示的那样。白色箭头表示感兴趣的细胞,红色和绿色箭头表示单个阳性细胞。阴性对照:在没有一抗的情况下进行染色。规模酒吧= 20µm。
循环pDC水平
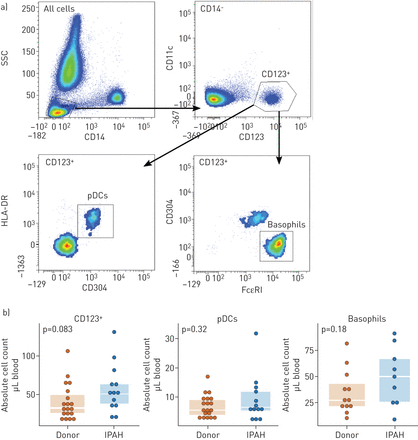
最后,我们研究了在IPAH肺中观察到的pDC增加是否也可以在循环中检测到。给出了门诊PAH组和对照组的特点在线补充表S3.总CD123分析+CD11C.-细胞或PDC(CD123+CD11C.-CD304+HLR-DR+)没有透露任何重大增加。同样,其他CD123+人口、嗜碱粒细胞(CD123+CD11C.-CD304-FceRi+),没有升高(图8).这些结果表明,这些人群在肺动脉高压患者的肺中选择性增加。
特发性肺动脉高压(IPAH)患者外周血浆细胞样树突状细胞(pDC)数量不升高。a)流式细胞术定量循环pDCs (CD14)的门控策略-CD11C.-CD123+CD304+HLR-DR+)和嗜碱性粒细胞(CD14-CD11C.-CD123+CD304-FceRi+)在外周血中。b)量化总CD11c的散点图和盒子叠加-CD123+细胞,pdc和嗜碱性细胞。箱线图显示中位数和四分位数间的范围。
讨论
在这项研究中,我们创建了迄今为止IPAH肺内免疫细胞群最全面的图像。使用无监督和无偏见的方法,我们评估了21种不同的炎症细胞群的存在和丰度,从而不仅详细描述了健康对照组肺部的炎症景观,而且还详细描述了IPAH患者的炎症景观。以往的研究主要依靠传统的评分或免疫组化分析来检测PH患者肺部炎症细胞的存在[1,4- - - - - -6,12.,21.].尽管这些技术具有一些优势,例如快速识别建筑和结构扰动的能力,但它们受到同时可以分析的细胞群数量的限制。相反,流式细胞术允许使用大量分化标记同时分析多个独立的细胞群,包括亚群及其激活状态的多维描述。使用这种方法和伴随的生物信息学分析,我们描述了1)健康肺部免疫表型的详细图像;2) IPAH免疫细胞信号改变;3) IPAH免疫失衡的新调控细胞群。
在IPAH患者中,我们不仅观察到细胞分布的变化(因此是不同的轮廓),而且增加了丰富的炎症细胞。由于我们的分析仅限于IPAH和控制样本,我们无法确定此配置文件是否特定于IPAH,或者可以与其他病理条件共享。未来的研究应与其他患者群体进行比较,例如Eisenmenger的综合症。然而,即使在这些患者中,也不能排除炎症组分,因为免疫应答也可能参与对增加的流动和/或压力的反应。这是通过使用大鼠pH大鼠的研究表明由于Supracoronary主动脉束后的左心疾病的研究。在这里,肥快细胞及其介质对于肺血管重塑和pHOP发育是重要的[22.].
因为血管重塑发生在大血管和小肺动脉中[16.],我们采用了另一种创新方法,并分析了孤立的较大肺动脉(>500)的炎症特征 µm)。事实上,即使在这些肺动脉中,也观察到炎症状况的变化,这为在更大的重塑血管中存在炎症细胞(包括肥大细胞、活化的巨噬细胞和DC)提供了确凿的证据。在离体肺动脉中存在活化的巨噬细胞支持其参与PH的长期前提[23.,24.].
从全球炎症图片转向IPAH中改变的特定细胞类型,在我们的多维流式细胞术表征中,我们观察到增加的肥大细胞和淋巴细胞等,其中支持以前的报告[3.- - - - - -7,12.,25并证明了我们方法的有效性。然而,在我们的肺部样本中,之前报道的PH值改变的少数人群并没有改变,例如b细胞或所有巨噬细胞[4,24.].pH族群,使用的标记或使用酶消化可能有助于这些差异。不幸的是,我们的分析面板无法区分肺泡和间质巨噬细胞,这需要许多附加标记,包括CD169以进行准确识别[13.].未来的研究可以利用新细胞标记物的持续发展,以具体分析这些细胞类型。
类似于肥大细胞,嗜碱性粒细胞(在我们的IMAH队列中也增加)是典型的先天效应细胞,可以释放出诸如白细胞介素(IL)-6,IL-13或白三烯B4的过多的介质,这些介导剂包括在pH发病机制中[26- - - - - -29],这反过来可以激活和招募T细胞[30.]. 与此一致,我们观察到多种T细胞亚群,即CD4的丰度显著增加+,CD8+和γδ t细胞在IPAH患者中的作用[25].有趣的是,我们之前已经发现IPAH中循环淋巴细胞数量减少,这表明活跃的肺募集[31].在这项研究中,我们首次描述了IPAH中γδ t细胞的增加。γδ t细胞作为先天(例如NK细胞和巨噬细胞)与适应性免疫(例如B细胞和CD4+t细胞)反应32].在皮肤中,γΔT细胞在组织稳态和伤口愈合中具有重要作用[33]通过释放先前显示的胰岛素样生长因子-1,以增强平滑肌细胞增殖[34].
负责T细胞活化的关键细胞类型是DCS,其在本地衍生自两个不同的谱系,髓样DC(CD11C)+和/或CD209+(DC-SIGN)和PDC(CD123+CD11C.-).使用只有一个标记的DCS的结论性鉴定非常具有挑战性;因此,我们另外使用HLA-DR(主要组织相容性复合体II类)积极性和CD14-消极,以鉴定CD209+和CD11C.+DCS。我们观察到增加丰富的髓样DC,包括CD209-IPAH患者肺和肺动脉中的树突状细胞,从而扩展了以前的观察[5,12.].此外,我们还观察到,在IPAH样本中,活化的DCs和巨噬细胞的数量和复杂性增加,如CD1a(一种跨膜糖蛋白,在脂质和糖脂抗原的呈递中起重要作用)的阳性所示,这可以进一步增强t细胞的活化。树突状细胞和t细胞的调节表明PH发病机制中有很强的适应性免疫成分。
据报道pH有权拥有自身免疫功能[5,35],并可在多种自身免疫性疾病,如系统性红斑狼疮或系统性硬化症中发生[36,37].类似于γδT细胞,PDC在自身免疫调节中具有关键作用,并且处于先天和自适应免疫的十字路口[38].我们在这里展示了IPAH患者肺部的第一次升高的PDC数量。与W.类似盎et al。[39[我们观察到外周血中的PDC数量没有变化,这可能表明肺部具体变化或可能是由于外植入和门诊团体之间的疾病严重程度(纽约心脏协会III-IV之间的差异与II-III分别)。PDC是抗病毒型最重要的生产者 - I干扰素[40],这与PH的发病机制有关[41].因此,PDC可能代表pH与自身免疫性和病毒感染之间的关联之间的缺失链接[42].或者,PDC也可以诱导调节或抗炎反应[43].在动物模型中,调节免疫反应,例如,通过已经显示调节性T细胞强烈保护pH表型[44].因此,可以想到的是,IPAH肺中的增加的PDC可以代表对持续炎症过程的机制。
在对照和IPAH样本中炎症细胞的存在强调了研究免疫反应如何从生理反应转变为不适应反应的重要性。我们可以推测,多个变化累积,直到一个分子/细胞成为引起重构级联的吸管。此外,全球概况(特定的组成、分布和相互作用)可能对疾病进展很重要,而不仅仅是某一特定细胞类型的丰度增加。综上所述,我们的数据支持VOelkel.et al。[45].
可能有几个因素会影响观察到的炎症细胞谱,例如这些患者的BMPR2状态是未知的,所以我们不能评论这个突变可能产生的影响。PH药物也可能改变炎症信号,例如,前列腺素已被证明影响核因子-κB信号[46],而磷酸二酯酶-5抑制剂可提高cGMP和一氧化氮水平,从而起到消炎作用[47].然而,缺乏这些药物在pH患者中抗炎作用的临床证据。最后,我们的分析仅限于移植的末期肺部。需要进行未来的研究来解决IPAH中免疫细胞的机械效应。沿着这些线,在几种小鼠模型研究中,已经显示出免疫细胞及其分泌的介质引起肺动脉重塑和增加的右心室压力[29,48,49].
我们使用流式细胞术分析IPAH患者肺部的炎症细胞群是一种新颖的方法,并强调了通过同时分析多个细胞群可以获得的丰富信息。随着越来越多的研究小组将这些技术纳入他们对炎症人群的分析,这将进一步提高肺动脉高压炎症状况的分辨率,甚至可能根据患者的炎症状态对患者进行分层。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑的,而是由作者提供的。
图S1。肺动脉隔离程序。由于它们靠近Airways(§)而在立体显微镜下鉴定了肺动脉(*)。通过逐渐去除肺组织暴露动脉,直至可见〜1-2cm的动脉。然后除去动脉,包括侧分支,并转发至细胞分离。秤条表示1厘米。ERJ-01214-2017图1
图S2。捐赠者和IPAH样品中的肺形态。来自外植入肺样品的部分的代表性图像(n = 4)。还示出了含有肺血管的放大区域。ERJ-01214-2017_图_S2
图S3。不同流式细胞术盘中测量的细胞群的相关图。a)CD45 +细胞,B)PMN:多晶核中性粒细胞,C)CD3 + T细胞,D)MAC:巨噬细胞和e)肥大细胞。每个相关性显示源自Spearman等级相关的P值和Rho(R)估计。ERJ-01214-2017\u图\u S3
图S4。配对肺样本中单个细胞群的相关性分析。用斯皮尔曼秩相关法比较了两个独立肺的细胞群。P值和rho (r)估计由斯皮尔曼的秩相关显示。ERJ-01214-2017_图_S4
图S5。从全球主要成分分析中排除的细胞群体丰富。由流式细胞术分析的IPAH和供体肺中细胞群的散点图和盒子覆盖物。NK,天然杀伤细胞;NKT,天然杀伤T细胞。箱线图显示中位数和四分位数间的范围。ERJ-01214-2017_图_S5
图S6。CD45+细胞群患者间的差异性。热图表示患者对患者的对数比值比变异性,该比值比来自18个个体细胞群的CD45+百分比数据。蓝色表示丰度最高,红色表示单个细胞类型丰度最低。多形核中性粒细胞,中性粒细胞,mac,巨噬细胞;单一,单核细胞;直流,树突细胞;pDC,血浆直流;gdγδ。ERJ-01214-2017_图_S6
图S7。个体IPAH和供体样本的欧氏聚类。热图表示使用欧几里德聚类的对数比值比,该比值比来自21个单个细胞群体每mg组织数据的细胞数量。蓝色表示丰度最高,红色表示单个细胞类型丰度最低。单一,单核细胞;DC树突状细胞,Macs,巨噬细胞;CTL,细胞毒性T细胞;gdγδ;PMN,多晶核中性粒细胞。ERJ-01214-2017_图_S7
图S8。肺样本中剩余细胞群的丰度。丰富的细胞群不包括在图4采用流式细胞仪分析IPAH和供肺。直流,树突细胞;多形核中性粒细胞,中性粒细胞。箱形图显示中位数和四分位范围,组间差异采用Wilcoxon秩和检验。ERJ-01214-2017_图_S8
图S9。肺样品中CD45 +细胞的相对比例。多种细胞群在IPAH和供体肺中的相对比例。直流,树突细胞;PDC;血浆骨质细胞骨质细胞;多形核中性粒细胞,中性粒细胞。箱形图显示中位数和四分位范围,组间差异采用Wilcoxon秩和检验。ERJ-01214-2017图9
图S10。离体肺动脉细胞群丰度。剩余的细胞群不包括在图5在IPAH和供体样本中采用流式细胞仪分析。直流,树突细胞;多形核中性粒细胞,中性粒细胞。箱形图显示中位数和四分位范围,组间差异采用Wilcoxon秩和检验。erj - 01214 - 2017 - _figure_s10
披露的信息
补充材料
诉市中心erj - 01214 - 2017 - _foris
G夸皮斯泽夫斯卡erj - 01214 - 2017 - _kwapiszewska
A. Olschewski.ERJ-01214-2017_OLSCHEWSKI_A.
h . OlschewskiERJ-01214-2017_OLSCHEWSKI_H.
致谢
我们要感谢Sabrina Reinisch,Nina Treitler,Lisa Oberreitor和Eva Grasmann(Ludwig Boltzmann肺血管研究所,Graz,奥地利)为他们的优秀技术援助和Jochen Wilhelm(Giessen和Marburg Lung Center,Giessen,Germand)借助计算分析的指导。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
支持声明:该研究部分得到了奥地利科学基金(FWF) (P278488-B23)和奥地利国家银行Jubilee基金会(grant 16187)的支持,授予G. Kwapiszewska。本文的资金信息已存入CrossRef Resder注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com.
- 已收到2017年6月19日。
- 接受2017年10月15日。
- 版权所有©ers 2018
本文是开放获取的,并根据知识共享188滚球软件署名许可证4.0的条款分发。