摘要
哮喘的特征在于异质临床表型。我们的目的是通过分析来自104个中度至严重的哮喘受试者和16个非惊厥受试者来确定哮喘的分子表型。
在筛选嗜酸性粒细胞相关性和非嗜酸性粒细胞相关性痰炎差异表达基因后,我们对508个差异表达基因进行无偏层次聚类,并对特定基因集进行基因集变异分析。
我们定义了三种转录组相关簇(TACs): TAC1(以免疫受体为特征)IL33R那CCR3.和TSLPR)、TAC2(以干扰素-、肿瘤坏死因子-α-和炎症小体相关基因为特征)和TAC3(以代谢途径、泛素化和线粒体功能基因为特征)。TAC1对白细胞介素-13/ t辅助细胞2型(Th2)和先天淋巴样细胞2型的基因标记富集程度最高。TAC1痰嗜酸性粒细胞增多和呼出一氧化氮含量最高,局限于口服糖皮质激素依赖、频繁发作和严重气流阻塞的严重哮喘。TAC2显示痰中性粒细胞、血清c反应蛋白水平和湿疹患病率最高。TAC3正常至中度高痰嗜酸性粒细胞,1 s内强迫呼气量保存较好。TAC1和TAC2的基因-蛋白共表达网络扩展了这一分子分类。
我们定义了一种th2高嗜酸性表型TAC1,以及两种非th2表型TAC2和TAC3,分别以炎症小体相关和代谢/线粒体途径为特征。
摘要
痰细胞转录组基因的聚类定义了一种Th2相关表型和两种非Th2相关表型http://ow.ly/UEkA3069ZYL
介绍
严重哮喘被定义为对哮喘治疗部分或完全无反应的哮喘[1]。严重哮喘的炎症机制涉及多个细胞室,具有多种疾病驱动机制。由气道上皮组织协调的CD4 t辅助细胞2型(Th2)介导途径已被认为是过敏性哮喘的驱动力[2那3.]。诱导痰中嗜酸性粒细胞计数被用作这一途径的替代生物标志物[4.]。然而,嗜酸性粒细胞(EOS)哮喘也可以通过涉及先天淋巴细胞型2(ILC2)的非TH2机制下划线[5.那6.]。非eos哮喘(如嗜中性哮喘)的驱动机制与先天免疫反应的改变和Th17细胞的激活有关[7.那8.]。来自嗜中性哮喘患者的痰液或血细胞的基因表达分析报告了与病原体识别,中性粒细胞趋化性,蛋白酶活性和炎症组件相关的基因高表达[9.-11]。与粒细胞不足性哮喘相关的疾病驱动因素在很大程度上仍不清楚[12那13]。
仅使用临床特征的聚类并没有产生潜在生物学信息,因为在这些临床聚类之间已经看到了类似的炎症细胞概况[14]。我们进行的关于EOS差异表达基因(DEGS)的无监督聚类与非eos哮喘的分类驱动机制,告知粒细胞炎症的重要性。我们首先定义了一组EOS和非EOS炎症表型痰液中表达的基因。在这些基因上的聚类导致了三个由不同的基因标记集区分的新聚类。我们定义了一种白介素(IL)-13/ th2高的EOS集群和两种非th2表型,分别通过干扰素(IFN)/肿瘤坏死因子(TNF)-α/炎症小体相关、代谢和线粒体途径进行表征。
方法
在线补充材料中提供了对方法的完整描述。
研究设计
我们获得了来自U-BIOPRED队列中104名中度至重度哮喘参与者(在线补充表S1)和16名健康志愿者(HV组)的痰细胞的转录组数据[15]。这项研究得到了招聘中心伦理委员会的批准。所有参与者均给予书面知情同意。
痰“omics”分析
吸入高渗盐水诱导痰液,收集痰塞,从中获得痰细胞和痰上清,如前所述[16]。使用Affymetrix U133 Plus 2.0 (Affymetrix, Santa Clara, CA, USA)微阵列与从痰细胞中提取的RNA进行表达谱分析。使用SOMAscan蛋白质组分析对痰上清进行蛋白质组分析[17.那18.]。
转录组特征的计算分析
数据上传并在传输系统中策划[19.]。我们分析了508只比赛中,在哮喘受试者中的基因表达中的比较,具有高痰嗜酸性粒细胞计数(≥1.5%),在哮喘受试者中,低嗜酸性粒细胞计数(<5%)和HV组(图1一个和B.和在线补充表S1)。原始探测集的强度是日志2通过鲁棒多体射线平均方法转换和标准化[20.]。一种基于回归的方法(R包limma;www.r-project.org)用于分析与兴趣组相关的差异基因,并将批次/技术效应、年龄、性别和口服皮质类固醇给药作为线性模型中的协变量进行调整。采用Benjamini-Hochberg方法的错误发现率对多个检验进行p值调整。
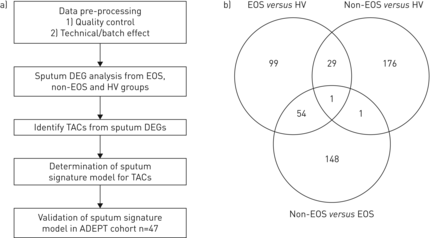
聚类方法。a)鉴定转录组相关聚类(TACs)、确定特征分类器、验证聚类特征和临床特征的工作流程。DEG:差异表达基因;EOS:嗜酸性;内行:个性化治疗的气道疾病内型。b)用维恩图显示的EOS、非EOS和健康志愿者(HV)组比较得出的deg数。
基于欧几里德距离的分层群集用于集群探索。使用缩小质心方法的监督学习算法[21.将]应用到聚类结果中,确定每个聚类的预测特征,并结合学习算法实现特征约简方法,获得便于解释的稀疏模型。共识聚类是一种考虑聚类算法多次运行时的聚类共识的重采样技术,用于确定最优聚类数,方法是找到聚类数k,其中一致矩阵直方图在k聚类处近似双峰分布,在k+1聚类处累积分布函数曲线下面积增加相对较小[22.-24.]。最近缩小质心法[22.使用]作为监督学习算法,以便改进对所识别的转录相关的簇(TACS)的签名。
基因集变化分析总结了签名
基因集变异分析(GSVA)计算样本wise富集分数(ESs) [25.那26.]。我们编译了与哮喘的特定方面相关的九个基因集(在线补充表S4),并且针对每个受试者的每个基因计算ES。ANOVA用于分析组手段之间的ES差异,并应用T检验以比较两种方法之间的差异。
验证研究
痰签名发现预测距离U-BIOPRED每个TAC的被应用到从痰疾病仿形哮喘和慢性阻塞性肺疾病(ADEPT(气道疾病Endotyping用于个性化治疗))队列)的研究中获得的数据转录27.使用GSVA(在线补充表S5)。采用Affymetrix U133微阵列对38例哮喘患者和9例HV组患者的痰标本进行分析。
数据沉积
转录组数据已被沉积在Geo(基因表达式omnibus)数据库中(www.ncbi.nlm.nih.gov地理),登录号为GSE76262。
结果
的转录功能途径分析
我们通过从EOS定义的三组U组(≥1.5%)的三组(≥1.5%)的比较来分析508次患者的亚组与non-EOS, EOS与HV和非EOS与高压(图1一个和b,和网上补充表S1)。网上补充表S2显示了三套度的视角,从现有的公共本体数据库的前10显著途径[28.]。在每个比较组中,大多数的deg富集于与免疫激活和细胞因子产生相关的生物过程或通路,而来自EOS的deg与非EOS呈现富集在一些特定的类别,如半胱氨酸型内肽酶活性的调节(P = 1.19×10-6),图案识别受体信号通路(P = 1.55×10-5),反应IFN-γ(P = 0.001),IPAF炎症组络合物(P = 0.002)和点状受体信号传导途径(P = 0.004)。
三种转录组相关簇的定义
k=2和k=5之间的聚类一致矩阵(图2一个-D)显示簇K = 2簇X = 2的共识指数的累积分布函数曲线近似是双峰分布(图2 e),但k = 3曲线下的区域的增加(图2 f)非常大。
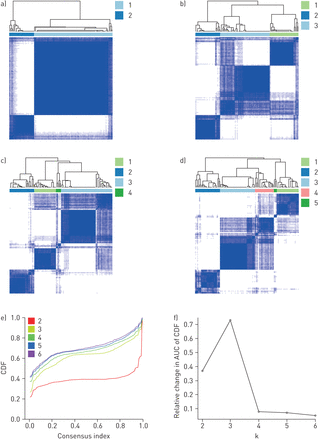
采用一致聚类方法确定最优矩阵数。AUC:曲线下面积;CDF:累积分布函数。最优聚类数的确定方法是找到一个聚类数k,其中一致矩阵直方图近似于k聚类的双峰分布,并且在k+1聚类中CDF的AUC相对较小的增加。a) k=2, b) k=3, c) k=4, d) k=5。e) k=2 - 6时共识指数的CDF曲线,其中k=2近似为双峰分布,f) k=3时AUC增加最大。聚类数k=3是最优选择。
分层群集(图3)和重采样(图2)产生了三个tac。TAC1,具有最高的嗜酸性粒细胞,呼出型一氧化氮(F.伊诺)和血清骨膜素,限定只重度哮喘患者的高口服皮质激素依赖性,急性加重,鼻息肉和严重气流阻塞(表1).收缩的质心算法[21.) (图4和在线补充图S1)定义了20个与多种细胞因子受体和信号转导相关的TAC1基因(il1rl1.那SOCS2那CCR3.那CRLF2.)、巨噬细胞、肥大细胞和嗜酸性粒细胞中发现的酶(PRSS33那CLC那阿洛克15.那TPSB2.那CPA3)和粒细胞和涉及受损诱导的适应性免疫反应的细胞上的细胞粘附分子(CD24) [29.]。TAC2以最高的痰中性粒细胞计数、血清c反应蛋白(CRP)和更高的湿疹患病率为特征,并由与IFN和TNF超家族相关的39个基因定义(IFIT2那TNFSF10那IFIH1那TNFAIP3.那IFITM1那IL18RAP)、介导先天免疫的白细胞表面受体(FPR2.那TREML2那tlr1.),中性粒细胞趋和迁移(CXCR1.那CXCR2.那VNN2.那VNN3.), inflammasomes (CASP4那MEFV那简要),以及模式识别(CLEC4D那CLEC4E).TAC3的痰嗜酸性粒细胞正常至中等水平,1秒内强制呼气量保存较好,严重哮喘发生率最低,口服皮质类固醇依赖性最低。TAC3标记包括17个与葡萄糖和琥珀酸代谢相关的基因(SUCLG2.那TBC1D4)、泛素化(Zyg11b.),线粒体功能(MRPL57那PDCD2),能量消耗(aTP1B1)和endo /溶酶体功能和运输(围巾那TGOLN2那SCOC) (图4).
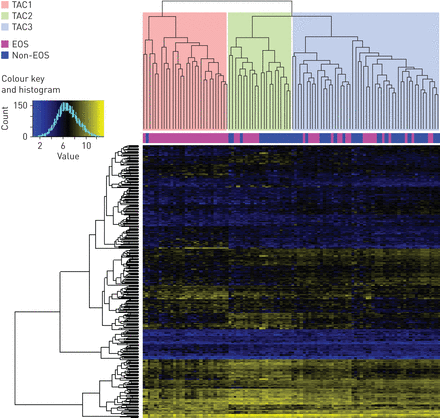
104个哮喘受试者(柱)的分层聚类热插拔,具有508个转录组特征(行)。聚类导致三个转录组相关簇:TAC1,TAC2和TAC3。每个参与者的痰粒细胞状态均在柱树形图下方映射。EOS:嗜酸性粒细胞。
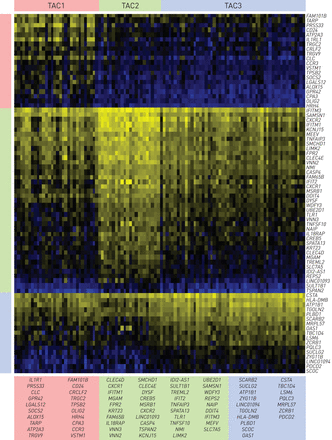
热图显示的基因的最判别各转录相关簇(TAC)用收缩的重心方法获得的签名。列表示104名哮喘患者和行表示76个基因。在每个TAC的对应颜色的基因的签名(TAC1:20个基因; TAC2:39种的基因; TAC3:17点的基因)被示出。
使用GSVA [25.],与哮喘相关的9个特征的富集程度有显著差异(图5),即。IL-13/Th2、ILC1、ILC2、ILC3、Th17的活化、中性粒细胞活化、炎症小体、氧化磷酸化(OXPHOS)和衰老特征。TAC1对IL-13/Th2和ILC2表现出最高的ESs,对Th17、中性粒细胞激活、炎性小体、OXPHOS和衰老信号表现出较低的ESs,而TAC2对ILC1、中性粒细胞激活和炎性小体信号表现出最高的ESs。TAC3对ILC3、Th17、OXPHOS和衰老信号的ESs最高,但对IL-13/Th2、ILC1、中性粒细胞活化和炎症小体信号的ESs较低(图5).
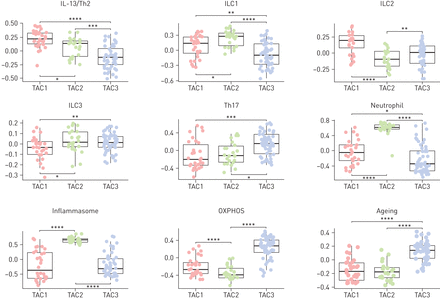
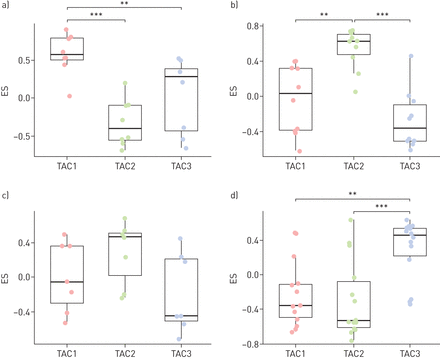
基因集变异分析(GSVA)。在线补充表S4显示了9个不同基因标记在三个转录组相关簇(TAC1、TAC2和TAC3)中的表达得分。IL:白介素;Th:辅助细胞;ILC:先天性淋巴样细胞;OXPHOS:氧化磷酸化。数据以单个数据点的形式呈现,盒须图显示中位数和四分位数范围。*: p < 0.05;* *: p < 0.01;* * *: p < 10-3;* * * *: p < 10-5.
TAC和痰粒细胞炎症
三种TACs均存在EOS炎症,其中96.7%(30例中有29例)TAC1存在高水平的痰嗜酸性粒细胞增多,36.4%(22例中有8例)TAC2存在EOS炎症,40.4%(52例中有21例)TAC3存在EOS炎症。TAC1亚型具有丰富的IL-13/Th2和ILC2特征(p=10)-7和p = 0.01;图6b). TAC2和TAC3主要存在中性粒细胞性炎症(图6和b),以及paucigranulocytic组主要TAC3(图6).在中性粒细胞炎症,嗜中性粒细胞和炎性签名最高的是与TAC2 TAC3(P = 0.01和p <0.02)进行比较。混合炎症组成TAC1和TAC2,具有TAC1例示出了用于IL-13 / Th2细胞富集该混合基团,但TAC2受试者相对富集中性粒细胞和炎性签名(p <0.01和P = 0.002,分别;图6c).这些发现支持混合粒细胞表型在生物学上差异较小的观点[12那13,但取决于每个TAC所确定的病理生物驱动。
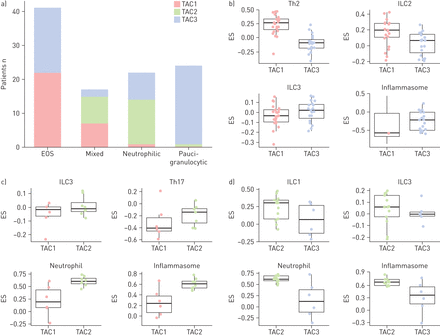
根据粒细胞炎症的转录组相关簇(TACS)的分布。a)嗜酸性粒细胞(EOS)炎症同样地连接到TAC1和TAC3,并主要针对TAC1和TAC2的混合粒细胞(混合)链接。中性粒细胞(Neu)和睡皂组(PAUCI)表型分别与TAC2和TAC3相匹配(Chi平方测试P = 3.2×10-13).b)在以eos为主的表型中,TAC1亚型(n=23)具有较高的t辅助细胞2型(Th2)(富集评分(ES)差异0.33,p=10-7)和先天淋巴样细胞2型(ILC2)的特征(ES差异0.14,p=0.01),而TAC3亚型(n=19)的炎症小体特征较高,但不显著。两个TAC亚型之间的ILC3相似。c)在混合粒细胞表型中,TAC2亚型(n=8)在中性粒细胞(ES差异0.39,p=0.02)和炎症小体(ES差异0.35,p=0.004)标记中轻微富集,但TAC1亚型的ILC3标记不富集。d)在中性粒细胞为主的表型中,TAC2亚型(n=13)在中性粒细胞(ES差异0.47,p=0.001)和炎症小体(ES差异0.37,p=0.011)标记中富集,而ILC1标记无显著差异。数据在b-d)显示为单个数据点,盒须图显示中位数和四分位数范围。
Adept Cohort中TAC签名分析
在ADEPT队列中,中度哮喘患者TAC1特征的ES(在线补充图S2)显著高于轻度哮喘患者(均差- 0.52,p=0.010)或健康对照组(均差- 0.48,p=0.030)。健康对照组、轻、中度和重度哮喘患者的TAC2和TAC3特征(在线补充图S2)相似。当根据粒细胞炎症表型对受试者进行分类时,ADEPT样本重现了U-BIOPRED队列的结果。我们证实了嗜酸性粒细胞占优势的表型,即TAC1和TAC3标记的平均ES均为阳性,但TAC2不阳性(图7).混合粒细胞表型富含TAC1和TAC2签名,但不适用于TAC3(图7).此外,TAC2标记的中性粒细胞优势表型富集,而TAC1或TAC3不富集;TAC3标记的缺粒粒细胞表型富集,而TAC1或TAC2不富集(图7).
根据痰粒细胞性炎症,ADEPT(个性化治疗的气道疾病内分型)队列中转录组相关聚类(TAC)标记的富集一)Eosinophil-predominant:≥1.5%。b) Neutrophil-predominant:≥74%。c)混合粒细胞:嗜酸性粒细胞≥1.5%,中性粒细胞≥74%。d)粒细胞少:嗜酸性粒细胞<1.5%,中性粒细胞<74%。数据以单个数据点的形式呈现,盒须图显示中位数和四分位数范围。*: p < 0.05;* *: p < 0.01;* * *: p < 10-3;* * * *: p < 10-5.
每个TAC相关基因和蛋白质的网络
作为生物过程通常由共表达的基因调节,每个TAC签名仅代表最有特点的基因,所有参与的每个生物过程的基因的子集。因此,我们试图了解所有TAC相关的基因和蛋白在与哮喘相关的生物学过程可能起作用的共表达关系。我们首先过滤基于与每个TAC基因标记的GSVA ES一个中度至高度正相关的单个基因。这产生三套TAC-相关基因,含有153 TAC1相关基因,194 TAC2相关基因和312 TAC3相关基因。对于导致的三套TAC-相关蛋白质的鉴定单个蛋白质,含有91 TAC1相关蛋白98 TAC2相关蛋白和42 TAC3相关蛋白相似的滤波方案。在此之后,每个TAC-相关基因 - 蛋白网络被显示为相关矩阵(在线补充图S3)。我们发现,这三个TAC相关的基因 - 蛋白质网络呈现轻度至中度的平均基因蛋白的相关性(网上补充图S3,蓝框,平均Pearson相关:TAC1 R = 0.292,TAC2 R = 0.416和TAC3 R = 0.403),这表明这三组的TAC相关基因和蛋白质的功能的一致性。
在总可捕量的基因蛋白的关系
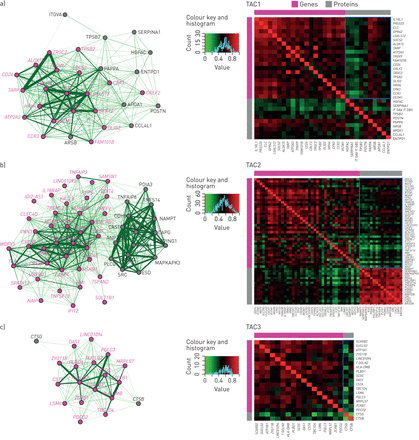
我们使用萎缩质心算法分析了痰中相关蛋白和基因标记的机制含义。我们为TAC1定义了10个蛋白(包括金属蛋白酶(PAPPA)、趋化因子(CCL4L1)和硫酸酯酶(ARSB)),为TAC2定义了16个蛋白(包括蛋白酶体(PSMA1)、磷脂酶(PLCG1)和TNF-α (TNFAIP6)相关的蛋白),为TAC3定义了2个蛋白(组织蛋白酶CTSG和CTSB)(在线补充表S3)。我们使用每个TAC签名建立了三个共表达网络(图8), TAC1 (r=0.49, p<0.001)和TAC2 (r=0.46, p<0.005)网络的平均基因-蛋白相关性显著高于随机基因-蛋白关系(在线补充图S4),说明TAC1和TAC2的基因和蛋白受相似机制的调控。高度coexpressedIL33R/ ARSB (r = 0.78, p = 4.2×10-16),IL33R/ PAPP-A(R = 0.73,P = 2.3×10-13)和CLC/爸爸(r = 0.79, p = 9.7×10-17),以及IFITM3/ PGLYRP1 (r = 0.67, p = 9.0×10-11),IFITM1/ PGLYRP1 (r = 0.63, p = 2.3×10-9)和MEFV/ PLCG1 (r = 0.67, p = 9.0×10-11)。TAC3网络的平均基因-蛋白相关性与随机基因-蛋白关系相似(r=0.40, p=0.566;在线补充图S4),表明TAC3的特征具有更多样化的机制,特别是转录后机制。
基因(品红节点)和蛋白质(灰节点)的每个转录组相关簇(TAC)特征的共表达网络。每对节点之间以一条边(绿线)连接,表示两个节点之间的相互关系为基因-基因、基因-蛋白质或蛋白质-蛋白质关系。网络中只显示>0.5节点对的相互相关性,其中边缘越厚,相互相关性越接近1.0。a) TAC1具有最高的基因-蛋白共表达关系,相关性较高IL33R/ ARSB,IL33R/ pappa和CLC/爸爸。b) TAC2基因与蛋白共表达关系第二高,相关性中等IFITM3/pglyrp1.那IFITM1/pglyrp1.和MEFV/PLCG1.TAC2显示最高的蛋白质 - 蛋白质共表达。c)中TAC3不显示高的基因共表达蛋白尽管是由适度相关特征灶性ATP1B1/ Capeopsin B和TBC1D4/cathepsin B.在TAC3中,蛋白-蛋白关系的相关性较低,因为这两个蛋白彼此分离。
讨论
我们已经描述了三种新的严重哮喘的TACs,来自使用层次聚类的痰转录组学的半偏倚分析。TAC1含有更丰富的IL-13/Th2和ILC2信号,并与血液和痰嗜酸性粒细胞增多有关,反映了以肥大细胞和嗜酸性粒细胞激活和TSLP、IL-33、IL-3和CCL11 (CCR3)受体上调为特征的严重哮喘。TAC2以炎症小体为主,伴有IFN和TNF超家族上调和DAMPs(损伤相关分子模式)的高表达,主要与中性粒细胞炎症和最高CRP水平有关,与TAC1中发现的严重程度较低的慢性气流阻塞有关。TAC3的分子标记突出了代谢、泛素化酶和线粒体能量代谢基因,线粒体氧化应激(OXPHOS)和与粒细胞不足和轻度EOS炎症相关的衰老基因标记的表达得分最高。与TAC1相比,TAC3的特点是最低的口服皮质类固醇使用量,轻微的气流阻塞和较少的急性发作频率。因此,基于痰细胞的分子表型得出了三个不同的临床群集。
对于TAC1和TAC2的基因签名与相应的蛋白质签名高度相交,表明两种分类中的每种分类中的每种分类中的相似水平,并提供了基因和/或蛋白质生物标志物和针对严重潜在新疗法的目标哮喘。高度共识IL33R/ ARSB,IL33R/ pappa和CLC/ PAPP-A中TAC1发现强调IL-33R和嗜酸性粒细胞活化标记物,这是在符合警报素IL-33能够加剧嗜酸性粒细胞介导的气道炎症通过基于的Th2细胞因子IL-5和IL的释放之间的链路-3 [30.]。在TAC2表型,高度共表达IFITM3/ PGLYRP1,IFITM1/ PGLYRP1和MEFV/PLCG1反映宿主对病毒和细菌的先天防御反应[31.那32.]。
这种高度共表达的关系在TAC3的基因-蛋白特征中没有发现,这表明它可能是由更复杂的调节因素驱动的,如翻译后修饰和改变的代谢酶活性,而不是经典的细胞激活机制。由巨噬细胞和粒细胞组成的痰细胞位于环境和肺上皮细胞层之间的界面,这些TACs可能反映了这种在TAC2中与炎症小体激活显著的相互作用,如前所述[33.]。最后,这些特征仅在一个单独的较小的哮喘队列(ADEPT)中得到部分验证,因此扩大了这些特征的适用性。
为了试图了解这些炎症表型的生物学基础,我们检查了与痰炎症表型相关三种TAC的分布。嗜酸性粒细胞 - 主要(TAC1或TAC3),中性粒细胞依赖性(TAC2或TAC3)和混合粒细胞 - 优势(TAC1或TAC2)表型分为两个主要的生物分类,而幼儿基因细胞 - 占优势(TAC3)表型仅代表一个TAC,即。TAC3。这项研究的主要发现是,至少两个不同的转录签名用痰嗜酸粒细胞增多有关。嗜酸性粒细胞为主型TAC1有IL-13 / Th2和ILC2签名的更高的表达,而嗜酸性粒细胞相关TAC3是炎性签名更高,表明TAC1的向Th2介导的过敏性哮喘和ILC2介导的EOS哮喘的相似性。这也被一些基因(反射例如IL33R那TSLPR)。[34.那35.在TAC1签名中名列前茅。
TAC1由高水平的血嗜酸性粒细胞和血清骨膜蛋白分化,而不是由高水平的血嗜酸性粒细胞和血清骨膜蛋白分化F.伊诺.我们没有发现与传统Th2细胞因子IL-4、IL-5和IL-13的相关性,但TAC1确实与从IL-13刺激的上皮细胞中获得的特征相关。然而,这种信号富集只是TAC1表型的一个组成部分。虽然TAC1是唯一的EOS,这并不奇怪,因为我们对来自EOS的deg与非EOS和健康受试者进行了聚类分析,但在所有三种TACs中都发现了不同程度的EOS炎症。这可能是由于这些信号是由痰细胞中巨噬细胞来源的基因驱动的,而不是单纯的嗜酸性粒细胞。
与TAC1嗜酸性粒细胞增多的患者相比,TAC3组以嗜酸性粒细胞为主的哮喘患者炎症小体特征更丰富。这与我们对泛素化酶基因的发现是一致的,泛素化酶基因是炎症小体组装所必需的[36.]。此外,炎症途径的激活可以导致抑制IL-33相关的EOS炎症[37.]。TAC3信号中编码多种代谢酶的基因集也与最近的一项研究相呼应,该研究将NLRP3炎性小体激活与小鼠肥胖相关哮喘模型中脂肪酸和胆固醇代谢失调联系在一起[38.]。
混合粒的表型中的表型TAC2有嗜中性粒细胞和炎性签名的更大的富集,而TAC1受试者混合粒哮喘有对IL-13 / Th2细胞签名的更高表达的趋势。这表明,TAC2是由嗜中性粒细胞驱动机制为主[39.]。相比之下,TAC1显示了IL-13/Th2的主导特征,EOS成分较高。然而,混合粒细胞TAC1显示了更高的Th2签名表达,这表明其EOS组分相对于中性组分占主导地位,在生物学上与主要的EOS表型相似。混合粒细胞表型的生物学特性被认为是不太稳定的过渡性表型[12那13]。我们的研究支持混合粒细胞表型在恶性上截然不同的视野,而是依赖于由中性粒细胞或嗜酸性粒细胞确定的生物学。
TAC3被定义为与线粒体氧化应激和衰老基因相关,这是一个新的定义,也是一个相当有趣的定义,因为线粒体对衰老过程的各个方面的潜在贡献,包括细胞衰老和慢性炎症[40]。有报道称,严重哮喘患者的气道平滑肌细胞线粒体功能障碍,有氧化磷酸化的证据[41.]但是线粒体氧化应激和老化签名如何驱动哮喘,几乎没有炎症的证据(睡皂细胞炎症和低血清CRP)尚不清楚。进一步研究检查其他细胞类型的作用(例如巨噬细胞和上皮细胞)可能有助于确定这些机制。
总之,我们的方法提供了一种新的框架,对表型哮喘和对特定治疗的更精确的靶向[42.]。需要进一步的工作来验证这里展示的非th2途径的生物学特性。由于不能完全通过测量痰粒细胞炎症来预测这些TACs的分层,并且不是所有的受试者都能产生痰,因此需要一个即时的、最好是基于血液的这些TACs的生物标志物。
补充材料
披露
补充材料
贝聿铭爱德考克ERJ-02135-2016_ADCOCK.
F. Baribaud.ERJ-02135-2016_Baribaud.
K.F.钟erj - 02135 - 2016 - _chung
j . Corfielderj - 02135 - 2016 - _corfield
r .也有erj - 02135 - 2016 - _djukanovic
M. Loza.ERJ-02135-2016_LOZA.
R. Lutt.erj - 02135 - 2016 - _lutter
P.J.斯德克已erj - 02135 - 2016 - _sterk
致谢
U型BIOPRED联盟项目组成员:U.霍达(气道疾病,国立心肺研究所,英国伦敦帝国学院和生物医学研究所,生物医学研究所,皇家布朗普顿和哈尔菲尔德NHS信托,英国伦敦),C Rossios(航空公司病,国家心肺研究所,英国伦敦帝国学院和生物医学研究所,生物医学研究所,皇家布朗普顿和哈尔菲尔德NHS信托,英国伦敦),E。贝尔(医学院,阿姆斯特丹大学,阿姆斯特丹,荷兰),N。饶(Janssen的R&d,High Wycombe的,UK),D.迈尔斯(呼吸治疗区域单位,葛兰素史克,斯托克利公园,UK),C.康普顿(愉医药,葛兰素史克公司,斯托克利公园,UK),M.范格斯特(阿斯利康R&d,默恩达尔,瑞典),P豪沃思(医学院,南安普敦大学,英国南安普敦和NIHR南安普敦呼吸生物医学研究单位,大学医院南安普敦,南安普敦,英国),G·罗伯茨(医学院,南安普敦大学,南安普敦,英国和NIHR南安普敦呼吸生物医学研究单位,大学医院南安普敦,南安普敦,英国),D Lefaudeux(欧洲系统生物学研究所和医学,CNRS-ENS-UCBL,Üniversite电里昂,里昂,法国),B。德Meulder(欧洲我nstitute for Systems Biology and Medicine, CNRS-ENS-UCBL, Université de Lyon, Lyon, France), A.T. Bansal (Acclarogen, Cambridge, UK), R. Knowles (Knowles Consulting, Stevenage Bioscience Catalyst, Stevenage, UK), D. Erzen (Boehringer Ingelheim Pharma, Ingelheim am Rhein, Germany), S. Wagers (BioSci Consulting, Maasmechelen, Belgium), N. Krug (Immunology, Allergology and Clinical Inhalation, Fraunhofer Institute for Toxicology and Experimental Medicine, Hannover, Germany), T. Higenbottam (Allergy Therapeutics, Worthing, UK), J. Matthews (Genentech, South San Francisco, CA, USA), V. Erpenbeek (Translational Medicine – Respiratory Profiling, Novartis Institutes for BioMedical Research, Basel, Switzerland), L. Carayannopoulos (Merck, Kenilworth, NJ, USA), A. Roberts (U-BIOPRED Patient Input Platform, European Lung Foundation, Sheffield, UK), D. Supple (U-BIOPRED Patient Input Platform, European Lung Foundation, Sheffield, UK), P. deBoer (U-BIOPRED Patient Input Platform, European Lung Foundation, Sheffield, UK), M. Caruso (Dept of Clinical and Experimental Medicine Hospital University, University of Catania, Catania, Italy), P. Chanez (Département des Maladies Respiratoires, Laboratoire d'immunologie, Aix Marseille Université, Marseille, France), S-E. Dahlen (The Centre for Allergy Research, The Institute of Environmental Medicine, Karolinska Institute, Stockholm, Sweden), I. Horváth (Dept of Pulmonology, Semmelweis University, Budapest, Hungary), N. Krug (Fraunhofer Institute for Toxicology and Experimental Medicine, Hannover, Germany), J. Musial (Dept of Medicine, Jagiellonian University Medical College, Krakow, Poland), T. Sandström (Dept of Medicine, Respiratory and Allergy Unit, University Hospital, Umeå, Sweden).
我们感谢每一个临床中心为参会的招聘和评估的所有成员。
作者贡献:R. Djukanovic, P.J. Sterk, C. Auffray, I.M. Adcock和K.F. Chung发起并设计了该研究项目。C-H.S。手稿由郭怡广、I.M. Adcock和钟嘉丰撰写。M. Loza, S. Pavlidis, F. Baribaud, A. Rowe, I.M. Adcock和C-H.S。Kuo分析了U-BIOPRED痰样本和ADEPT数据的转录组和蛋白质组学数据。R. Lutter和J. Corfield负责痰液、样品的分析和质量控制。I. Pandis, A. Sousa, J. Corfield和K.F. Chung从招募、临床和组学数据收集方面管理U-BIOPRED队列。I. Pandis, A. Sousa, J. Corfield和Y. Guo策划并将数据上传到tranSMART。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
支持声明:U-BIOPRED财团收到资金从欧盟和欧洲制药工业协会联合会作为创新药物计划联合企业资助项目(115010)代表U-BIOPRED研究小组从U-BIOPRED输入病人输入平台和病人的代表道德委员会和安全管理委员会。C-H.S。由台湾桃园长庚医学基金会资助,由林口长庚纪念医院胸科科部资助。该项目还得到了英国皇家布朗普顿和哈里菲尔德国民保健制度基金会信托和伦敦帝国理工学院的国家健康研究所呼吸系统疾病生物医学研究单位的支持。钟启芳(K.F. Chung)是英国国家健康研究所的高级研究员。本文的资金信息已存入开放式资助服务员注册表.
利益冲突:可以在本文中找到披露www.qdcxjkg.com.
- 收到了2016年11月1日。
- 接受2016年11月3日。
- 版权©2017人队