摘要
我们分析了鼻咽液(NPF)中鼻病毒(RV)对I型和III型干扰素(IFN)反应的影响(如。干扰素α和干扰素-λ)及其信号转导,在基线和疾病恶化期间,在患有和没有哮喘的学龄前儿童队列中。
在纳入全欧洲研究PreDicta时和出现症状时,收集NPF并分析RV局部定植。外周血单个核细胞(pmcs)受到挑战在体外有没有房车。RNA通过实时荧光定量PCR和基因阵列分析。ELISA检测血清ifn和c反应蛋白。
我们发现哮喘儿童的pmcs感染了在体外RV1b血清型上调MYD88,IRF1,STAT1而且STAT2信使rna,而MYD88,IRF1,STAT1而且IRF9以对照组儿童为主。此外,在NPF中与RV检测相关的疾病加重的症状就诊中,IFN-α的产生增加,而在哮喘儿童中,基线时RV已经诱导了IFN-λ的分泌。
在与RV相关的哮喘加重期间,哮喘儿童可以诱导IFN-α分泌,表明对反复呼吸道病毒感染的高度活跃的免疫反应。
摘要
儿童与鼻病毒相关的哮喘加重可诱导PBMCs中的IFN-α和STAT1/STAT2http://ow.ly/o14r303MW32
简介
病毒感染,特别是小rna病毒科成员鼻病毒(RV),在哮喘发展、儿童哮喘加重和气道重塑中发挥重要作用[1- - - - - -4].RV进入细胞通过低密度脂蛋白受体家族成员或细胞间粘附分子1(在线补充图S1) [2,5].在细胞内,单链病毒RNA被toll样受体TLR7, TLR8,尤其是TLR3检测[5].骨髓分化主要反应蛋白(MyD88)依赖通路最终导致干扰素(IFN)调节因子IRF7、IRF3和NF-κB的磷酸化和激活。活化的IRF7、IRF3和NF-κB转运至细胞核并引发抗病毒免疫应答[1,6].
具有抗病毒活性的一大组药物是干扰素家族。根据结构特征、受体用途和生物活性,干扰素可分为三种不同类型[7].I型和III型干扰素主要负责人类的抗病毒活动[1,7].虽然I型IFN包含13种IFN-α,但每种IFN-β、IFN-ε、IFN-κ和IFN-ω都只有一种。在哮喘中,I型ifn被描述为下调[6]并且已有研究表明,用聚乙二醇形式的IFN-α治疗可有效消除免疫抑制患者的持续性RV [8].此外,III型IFN反应也被证明在哮喘加重期间受损[9].
I型ifn的受体由两条跨膜糖蛋白链组成,称为IFNAR1和IFNAR2。几种ifn调控的信号元件和级联已被发现[10,11].虽然大多数细胞类型表达I型和II型IFN受体,但III型IFN受体主要存在于上皮来源的细胞上,包括髓系细胞,如树突状细胞和巨噬细胞[10,12].
受体的胞浆内结构域为Janus激酶1 (Jak1)和酪氨酸激酶2 (Tyk2)提供结合位点。配体的结合激活了Jak1和Tyk2的自体和反式酪氨酸磷酸化,以及它们磷酸化的主要目标,即。信号换能器及转录激活因子(STAT)蛋白STAT1及STAT2 [10,11,13].与IRF9一起,磷酸化的STAT1和STAT2形成所谓的ifn刺激基因因子3 (ISGF3)复合体。随后,这种异源三聚体复合物转运到细胞核,检测特定的DNA基序,称为ifn刺激反应元件,并促进ifn刺激基因的转录[10,11,13].
负调控因子,如细胞因子信号1抑制因子(SOCS1),通过直接抑制激酶活性来限制抗病毒反应的规模和持续时间通过与IFNAR1-Tyk2复合物结合[10,14].
尽管III型IFN(也称为IFN-λ1(或白介素(IL)-29)、IFN-λ2(或IL- 28a)和IFN-λ3(或IL- 28b)与I型IFN操作的受体复合物不同,但它们激活类似的抗病毒信号,导致不同的STAT蛋白磷酸化[7].
因为有必要更好地了解和管理哮喘,特别是儿童哮喘[15由于哮喘通常开始于儿童早期,我们重点研究了4-6岁的学龄前儿童。在儿童中,唯一与哮喘加重显著相关的病毒类型是rv [5];因此,在本研究中,我们询问了在与RV相关的疾病加重期间,RV感染如何调节儿童哮喘的I型和III型ifn。
材料与方法
人类研究预测
我们的调查是全欧洲研究PreDicta(感染后免疫重编程及其与呼吸道过敏性疾病持久性和慢性的关系)的一部分。这项多中心前瞻性队列研究在欧洲主要文化和气候地区的五个不同中心进行。分子肺气科与弗里德里希-亚历山大儿童医院(Universität Erlangen-Nürnberg,德国埃尔兰根)儿科和青少年医学部合作,是这些研究中心之一。
受试者招募和研究的时间表在网上补充材料和其他地方有详细描述[16].报告了儿童的一些临床情况表1最近出版了[16- - - - - -19].
该研究得到了Universitätsklinikum Friedrich-Alexander Universität Erlangen-Nürnberg (Re-No 4435)伦理委员会的批准。获得所有参与者父母/监护人的知情同意。该研究已在德国临床试验注册(www.germanctr.de: DRKS00004914)。
关于样品回收和后续分析的详细信息在在线补充材料中给出。
统计分析
采用非参数双尾Mann-Whitney检验(Prism version 6 for Windows;GraphPad, La Jolla, CA, USA)。
结果
本研究分析了儿童队列的临床数据
本研究分析的所有受试者都是4至6岁的学龄前儿童。所有健康儿童都没有接受任何治疗,而哮喘儿童则使用类固醇、非类固醇药物(如。支气管扩张剂或抗组胺药)或两者的组合。在Erlangen的PreDicta队列的临床和病毒学数据之前已经描述过,并将在准备中的手稿中集体报告[16- - - - - -18].表1而且2概述加入PreDicta研究时Erlangen队列的重要临床数据。
房车诱导STAT1/STAT2在哮喘儿童的PBMCs和IRF9控制的孩子,然而IRF1两组都上调了吗
我们知道,在细胞RV感染后,IFN-α和IFN-λ都从各种细胞中分泌出来,如。浆细胞样树突状细胞,以及这些细胞因子在t细胞中诱导STAT1信号传导(在线补充图S1) [4,7,11].
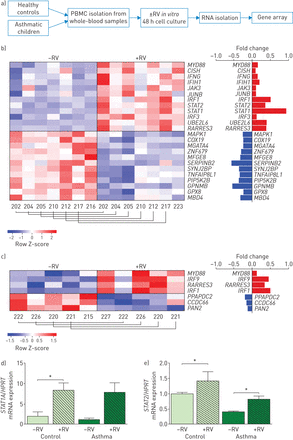
因此,我们想要研究在pbmc中上调的基因在体外暴露于RV中,随后细胞培养48小时,使用RNA基因阵列(图1一个).为了证明RV在对照组和哮喘pmcs细胞培养中挑战细胞,注意到与RV孵育在体外导致了MYD88表达式(图1 bc).此外,我们确定STAT1而且STAT2两个候选基因在哮喘儿童的rv挑战pmcs中上调(图1 b在线补充图S2)。定量实时荧光定量PCR (qPCR)证实了这些数据的准确性STAT1A同种型(20.),STAT2在哮喘患儿中RV分别上调7倍和2倍(图1 de).药物,特别是类固醇,似乎不是这些类固醇治疗的哮喘儿童中STAT1/STAT2上调的原因,因为类固醇对STAT1亚型A和B有相反的作用(在线补充图S2)。此外,对照组儿童表现出上调IRF9(图1 c),而两组分析均显示上调IRF1,一种抗病毒转录因子(图1 bc) RV暴露后,通过基因阵列评估。综上所述,这些数据支持了在对照组和哮喘儿童感染RV的pbmc中IFN上调的下游基因的存在。
哮喘儿童暴露于鼻病毒(RV)的外周血单个核细胞(pmcs)在体外显示调节MYD88而且STAT1A / STAT248小时后。a) pmcs RNA阵列的实验设计,在RV1b血清型存在或不存在的情况下孵育1小时,然后再培养48小时。b, c)暴露于(+RV)或未暴露于(-RV) RV的b)哮喘患儿和c)对照患儿外周血单核细胞分离mRNA的热图。调控基因的差异表达分析显示(log2average +RV/average -RV)。n哮喘n = 7,控制= 5。d, e) d)的实时定量PCRSTAT1A和e)STAT2来自对照组和哮喘儿童的pbmc中的mRNA用于阵列。n控制,RV-negative=5 (-RV), n控制,RV-positive=5 (+RV), n哮喘, RV-negative=3 (-RV), n哮喘、RV-positive= 5 (+ RV)。数据以平均值+表示扫描电镜.*: p≤0.05。
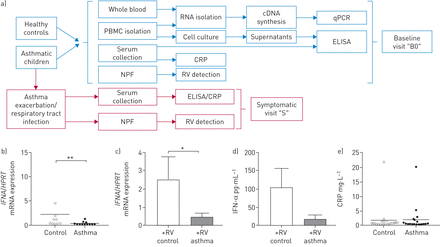
有缺陷的IFNA哮喘学龄前儿童招募时在上呼吸道检测到鼻病毒(RV)时的mRNA,而c反应蛋白(CRP)未升高。a) PreDicta研究的实验设计。PBMC:外周血单个核细胞;NPF:鼻咽液;qPCR:实时定量PCR。b)相对IFNAqPCR检测pmcs中mRNA的表达。n控制n = 10日哮喘= 12。c)根据RV检测对b)结果进行细分在活的有机体内在NPF。n控制, RV-positive=9 (+RV), n哮喘, RV-positive= 7 (+ RV)。d) ELISA法测定RV感染患儿血清中干扰素(IFN -α)水平在活的有机体内在NPF。n控制,RV-positive=10 (+RV), n哮喘, RV-positive= 11 (+ RV)。e)基线血清CRP值。n控制n = 19日哮喘= 19。数据以b, e)单个数据点和平均值或c, d)平均值+表示扫描电镜.*: p≤0.05;* *: p≤0.01。
的监管IFNA学龄前哮喘患儿呼吸道病毒感染及外周血淋巴细胞mRNA表达IFNA基因分析
接下来,STAT1/STAT2的上游,IFNA用qPCR方法分析了上述组群中有哮喘和无哮喘的学龄前儿童分离的和未接触的PBMCs中的mRNA水平(图2一个).在这里,我们发现有统计学意义上的下降IFNA哮喘患儿mRNA表达与对照组比较(图2 b).突变筛选分析在这些队列中没有显示任何基因改变IFNA基因(在线补充表S2)。
我们接下来假设,环境因素如RV可能会以不同的方式调节哮喘儿童血细胞中IFN-α的表达。
为了解决这一问题,我们在这些儿童的鼻咽中寻找RV的存在,这可能导致气道感染,这一特征在学龄前儿童中尤其明显。平均而言,基线时RV RNA检测在健康儿童和哮喘儿童之间无显著差异(表1).
调查IFNApbmc mRNA表达及RV RNA检测在活的有机体内在鼻咽液(NPF)中显示了健康和哮喘受试者之间的另一个区别。在健康儿童中,RV检出在活的有机体内NPF的增加与IFNA与哮喘患儿NPF中RV检测阳性相比,哮喘患儿pmcs中mRNA的表达(图2 c).血清中的蛋白质水平也检测到这种情况,尽管没有观察到统计学意义(图2 d).综上所述,哮喘患者有在活的有机体内RV检测未见上调IFNA水平与rv阳性对照患者相同。此外,在PBMCs治疗在体外对于类固醇,我们没有发现任何显著的影响IFNAmRNA表达(在线补充图S3)。
综上所述,这些发现表明,当呼吸道中存在RV时,哮喘儿童血液中的抗病毒免疫反应会受损。此外,在这些患者中,我们没有发现IFN-α调节与药物或过敏状态之间的任何关系(表3而且4).
对照组和哮喘患儿招募时的c反应蛋白水平
在NPF中检测到或没有检测到鼻咽RV RNA的哮喘儿童和对照组儿童中,我们发现c反应蛋白(CRP)的水平,c反应蛋白是一种在炎症和感染期间产生的半衰期为19小时的蛋白质[21],对照组和哮喘患儿在招募时血清中无差异(图2 e),尽管与对照组儿童相比,哮喘儿童在冬季被优先招募(在线补充图S4)。
RV或其他呼吸道病毒在NPF上的作用STAT1 / SOCS1在哮喘患者中
为了更好地分析IFN-α在哮喘患者中的调节,我们随后对5个CpG岛的甲基化状态进行了分析IFNAR1而且SOCS1基因,这也没有显示出健康和哮喘儿童甲基化的任何差异(在线补充图S5和表S3)。一致地,我们找不到任何规则SOCS1qPCR后的mRNA水平(补充图S6)。
当我们看STAT1IFN-α受体下游的mRNA表达,看看我们是否能发现受损的IFN信号,STAT1在RV检测阳性的哮喘患儿中,全血表达未见增加在活的有机体内(网上补充图S7)。接下来,我们分析了类固醇是否会影响STAT1,发现情况并非如此;相反,类固醇会减少STAT1mRNA表达(在线补充图S7)。
研究发现NPF中RV RNA检测与哮喘儿童血液中IFN-λ诱导相关
由于STAT1/STAT2位于不同IFN家族成员的下游,包括IFN-λ(一种强抗病毒因子),我们接下来检测了血清中的III型IFN。我们发现,与基线时RV阴性哮喘儿童相比,哮喘儿童和鼻咽道检测到RV的儿童血清中IFN-λ蛋白显著增加(图3).对照组的孩子也有同样的倾向。
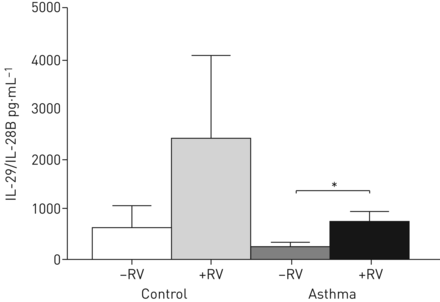
检测到鼻病毒(RV)在活的有机体内哮喘患者血清中干扰素(IFN)-λ(白细胞介素(IL)-29/IL- 28b)水平上调的相关性:ELISA法和RV法测定血清中IFN-λ含量在活的有机体内在鼻咽液中n控制, RV-negative=4 (-RV), n控制, RV-positive=14 (+RV), n哮喘, RV-negative=7 (-RV), n哮喘, RV-positive= 12 (+ RV)。数据以平均值+表示扫描电镜.*: p≤0.05。
哮喘儿童NPF中RV和其他呼吸道病毒感染的急性哮喘加重与诱导IFN-α分泌有关
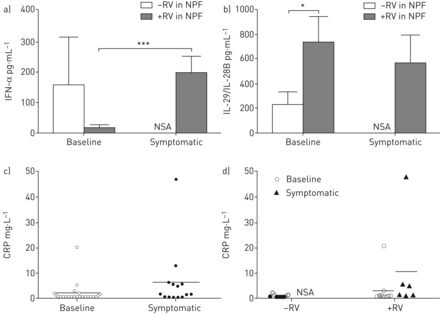
上述结果表明,在NPF中检测到RV的哮喘儿童与基线时RV定殖的健康儿童相比,血清中IFN-α水平降低。有趣的是,在哮喘发作或感染后,当哮喘儿童在症状出现后48小时内被要求到医院进行检查时(有症状的访问“S”;图2一个),与招募来访时RV阳性儿童相比,NPF中RV存在时血清中IFN-α浓度升高(图4一).血清IFN-λ浓度未发现因急性哮喘加重而改变(图4 b),并在基线时维持上调。哮喘患儿血清CRP水平的差异分析显示,在有症状的就诊时,CRP值有升高的趋势,进一步的调查提供了证据,表明在RV检测和/或感染后,CRP值甚至更高(图4 cd).这些结果表明,在NPF中检测到RV的哮喘儿童,在稳态条件下IFN-α的产生和/或释放似乎受损。然而,这种观察似乎与时间有关;哮喘儿童在急性感染期间能够显著上调IFN-α的产生,而IFN-λ在这一过程中没有进一步调控。我们还将该分析扩展到PreDicta的另外三个队列,并观察到哮喘儿童中IFN-α的整体诱导,在儿童医院有症状就诊期间分析了这些儿童的血清,当时他们的血清CRP显著升高,与呼吸道病毒感染有关(在线补充图S9)。根据Erlangen的队列研究,IL-29/IL-28B血清水平无显著差异(在线补充图S9)。
哮喘患儿哮喘加重和/或鼻病毒(RV)检测与血清中干扰素(IFN)-α表达增加有关。a)哮喘患儿招募时和症状就诊时血清中IFN-α和b) IFN-λ(白细胞介素(IL)-29/IL- 28b)水平,采用ELISA法测定。NPF:鼻咽液;国安局:没有样本。一)n基线, RV-negative=7 (-RV), n基线, RV-positive=11 (+RV), n有症状的, RV-negative=0 (-RV), n有症状的房车,积极的= 5 (+ RV);b) n基线房车,负=7 (-RV), n基线, RV-positive=12 (+RV), n有症状的, RV-negative=0 (-RV), n有症状的, RV-positive= 6 (+ RV)。c, d)招募时和症状就诊时哮喘儿童血清中c反应蛋白(CRP)水平测定。c) n基线n = 19日有症状的= 14;d) n基线, RV-negative=7 (-RV), n基线, RV-positive=10 (+RV), n有症状的, RV-negative=0 (-RV), n有症状的, RV-positive= 6 (+ RV)。数据以a, b) mean+表示扫描电镜或者c, d)个体数据点和平均值。*: p≤0.05;* * *: p≤0.001。
讨论
既往研究显示哮喘患者支气管肺泡灌洗液和支气管上皮细胞中RV IFN反应存在缺陷[6,22].在这项研究中,我们支持并扩展了先前描述的哮喘成人患者I型IFN产生缺陷的概念[6]给学龄前儿童。我们发现减少了IFNA与招募时健康儿童相比,哮喘儿童的血细胞水平。此外,我们发现RV RNA在上呼吸道的检测与诱导有关IFNA对照儿童与哮喘学龄前儿童血细胞mRNA表达的比较。
IFN-α被认为是pmcs对呼吸道病毒的先天反应中产生的主要IFN [23],尤其是浆细胞样树突状细胞[13].在这项研究中,我们发现哮喘儿童在某些情况下上调I型ifn的能力似乎也得到了保留。我们发现哮喘儿童在与RV相关的疾病加重发作后48小时内到医院就诊时,血清中IFN-α蛋白水平显著上调,这表明哮喘患者I型IFN生产不足是短暂的,可以在急性感染中克服。有趣的是,在我们的队列中,有症状就诊的哮喘儿童的RV或其他呼吸道病毒检测均呈阳性,这表明这些儿童的疾病恶化与呼吸道病毒检测完全相关。此外,我们关于儿童哮喘发作期间IFN-α增加的假设得到了PreDicta研究中对不同儿童队列的观察扩展的支持。这也符合我们的分析IFNA1而且IFNA13甲基化分析,表明在表观遗传学上没有差异IFNAR1而且SOCS1哮喘患儿和对照组患儿之间。然而,哮喘患者IFN-α缺乏的确切机制以及急性感染患者克服这种缺乏的能力仍然未知。一种可能与呼吸道病毒检测的时间点有关。有可能在有症状访视期间,哮喘儿童与基线访视相比更接近右心室感染。这也由有症状就诊时较高的CRP水平所支持。IFN-α动力学显示,该细胞因子在病毒感染后10小时内下降[24].此外,在过去,已经开发了几种改善RV感染治疗的方法,包括对持续性RV感染的成人使用IFN-α。这项试验显示出有希望的结果[8].然而,使用IFN-α治疗也有一些缺点。虽然它已被证明能迅速清除RV RNA [8],但似乎只能适度减轻症状,患者还会出现严重的副作用,包括流感样疾病、恶心和头痛[1,5,25].
我们对IFN-α的时间依赖性调节的假设得到了进一步的支持,我们的观察扩展到PreDicta研究的其他队列(即。雅典,Łódź和图尔库)。在本分析中,我们观察到一种可变性,这种可变性可能归因于不同的混杂因素,如特异反应性、花粉季节的取样、细菌并发症的抗生素或其他口服药物,甚至疾病活动性[6,26].然而,使用类固醇治疗没有观察到影响IFNA信使rna表达。这与皮质类固醇已被证明对患有rv相关的首次喘息的儿童具有临床益处的发现相一致[27,28].这方面的进一步研究正在进行中。
此外,在与RV相关的哮喘急性加重期间,观察III型IFN,如IFN-λ,我们发现它在血清中诱导,尽管观察到CRP和IFN-α的增加。这可能与IFN-λ的延迟动力学相一致。
与它们的抗病毒活性一致,病毒感染的细胞通常诱导I型和III型ifn。其中一个原因可能是I型和III型IFN基因中常见的上游调控元件,如NF-κB、IRF3和IRF7 [7].然而,I型和III型ifn的转录调控并不完全相同。此外,使用中和抗体的研究表明,I型和III型受体系统在应对病毒感染时的激活是独立的[7],但不同的干扰素组确实相互作用。例如,IFN-α可能能够上调IFN-λ通过增加toll样受体和IRF7基因的表达[7].由于IFN-λ的产生与症状的严重程度呈负相关[9], III型IFN被认为对哮喘有保护作用[5].需要进一步的研究来更好地了解哮喘和健康儿童RV感染后IFN通路的相互作用。我们的在体外基因阵列数据表明,对照组和哮喘患儿的基因上调幅度都显著更高IRF1,而哮喘儿童上调STAT1A而且STAT2组件、控制子优先激活STAT1A而且IRF9感染RV的外周血单核细胞中IFN的下游。因此,由于STAT1A/STAT2位于IFN-α/IFN-λ的下游,这两种类型的IFN在儿童哮喘RV加重期间没有缺陷似乎是合理的。这种差异调节的确切机制有待进一步研究。
关于临床情况,我们已经知道病毒和细菌的存在会影响免疫系统,并增加慢性肺部疾病恶化的风险[1- - - - - -4,29].此外,右心室感染不仅在哮喘的发展中发挥重要作用[1,2,25],但它们是唯一与儿童哮喘加重显著相关的病毒类型[1,3.,5,23].此外,已知RV在鼻接种后可到达、穿透并复制于下气道,从而降低气道炎症,长期有助于气道重塑[1,30.].在本研究中,我们特别关注NPF中RV的检测及其对学龄前儿童免疫反应的影响。这些结果也与特应性哮喘患者没有更大的右心室感染风险,但感染更频繁,症状更严重的事实相一致[31].
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充材料erj - 00969 - 2016 - _supplementary_material
补充图S1erj - 00969 - 2016 - _figure_s1
补充图S2erj - 00969 - 2016 - _figure_s2
补充图S3erj - 00969 - 2016 - _figure_s3
补充图S4erj - 00969 - 2016 - _figure_s4
补充图S5erj - 00969 - 2016 - _figure_s5
补充图S6erj - 00969 - 2016 - _figure_s6
补充图S7erj - 00969 - 2016 - _figure_s7
补充图S8erj - 00969 - 2016 - _figure_s8
补充图S9erj - 00969 - 2016 - _figure_s9
披露的信息
确认
作者感谢所有参加我们在欧洲范围内开展的PreDicta研究的儿童及其父母/监护人。此外,作者感谢S. Trump, C. Holzinger, S. Mousset和A. Maier(分子肺病学部门,Friedrich-Alexander-Universität Erlangen-Nürnberg, Universitätsklinikum Erlangen, Erlangen,德国)和E. Muschiol, I. Jawa和L. Schramm(儿科和青少年医学部,Universitätsklinikum Erlangen, Erlangen,德国)的技术支持。此外,作者感谢M. Wölfel、C. Reinhardt、A. Neubert和W. Rascher(儿科和青少年医学系,Universitätsklinikum Erlangen, Erlangen, Germany)在PreDicta UKER wp1研究中的帮助。我们也感谢A. Eberwein在人类遗传学研究所(Friedrich-Alexander-Universität Erlangen-Nürnberg, Universitätsklinikum Erlangen, Erlangen, Germany)对测序的帮助,以及R. Schneider-Stock和I. Mons(实验肿瘤病理学系,Friedrich-Alexander Universität Erlangen-Nürnberg, Erlangen, Germany)为我们介绍了通过磷酸测序进行甲基化分析。此外,我们感谢R. Stergiou和S. Taka(希腊雅典国立大学和Kapodistrian大学的过敏和临床免疫部门)提供了RV1b。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:目前的工作是为了满足A. Bergauer获得“医学博士”学位的要求。这项研究得到了教育和欧洲文化基金会的支持。本文的资助信息已存入公开出资人注册处.
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2016年5月13日。
- 接受2016年8月24日。
- 版权所有©ERS 2017